高三一轮原创化学精品学案:40羧酸 酯 氨基酸 蛋白质 (含答案)
- 格式:doc
- 大小:402.00 KB
- 文档页数:9

高三化学一轮复习:羧酸酯学案复习目标:1.认识羧酸和酯的组成和结构特点;3.掌握乙酸的酸性和酯化反应等化学性质,理解酯化反应的概念;4.掌握酯水解反应的机理,并了解酯化反应和酯的水解是一对可逆反应。
知识梳理:一、乙酸1.结构:分子式:___;结构式:_____;结构简式:_____。
官能团是_____。
2.物理性质:乙酸俗称,它是一种无色气味的体,易挥发,熔、沸点较,其熔点为16.6℃时,因此当温度低于16.6℃时,乙酸就凝成像冰一样的晶体,故无水乙酸又称。
它易溶于水和乙醚等溶剂。
⒊化学性质:⑴酸性:电离方程式:写出有关反应的离子方程式:A:与大理石反应:B:与小苏打溶液反应:C:设计一个简单的一次性完成的实验装置,验证乙酸、碳酸和苯酚溶液的酸性强弱。
⑵酯化反应:CH3COOH+C2H5OH CH3COO C2H5+H2O①试剂加入顺序:②加热目的:③饱和Na2CO3的作用:④现象:⑤注意事项:A、化学原理:浓硫酸起催化脱水作用。
B、装置:液-液反应装置。
用烧瓶或试管。
试管倾斜成45°(使试管受热面积大)。
弯导管起冷凝回流作用。
导气管不能伸入饱和Na2CO3溶液中(防止Na2CO3溶液倒流入反应装置中)。
C、饱和Na2CO3溶液的作用。
①.乙酸乙酯在饱和Na2CO3溶液中的溶解度较小,减小溶解,利于分层。
②挥发出的乙酸与Na2CO3反应,除掉乙酸;挥发出的乙醇被Na2CO3溶液吸收。
避免乙酸特殊气味干扰乙酸乙酯的气味。
二、羧酸⑴定义:由烃基或H与羧基相连的一类化合物,官能团为—COOH⑵分类:C原子数目:低级,高级脂肪酸脂肪酸烃基种类烃基的饱和情况:饱和,不饱和芳香酸羧酸一元羧酸羧基数目多元羧酸⑶饱和一元羧酸:C n H 2n O 2①酸C n H 2n O 2的同分异构体的数目:看R -COOH 中-R 的异构体数目②与C 数相同的饱和一元酯异构⑷物性:①熔沸点:随n ↑而升高②溶解性:随n ↑而减小(低级脂肪酸易溶,高级脂肪酸不溶)(5)甲酸:俗称蚁酸,结构式 结构简式 ,所以甲酸即具有酸的性质又具有醛的性质。

2020高考化学一轮复习学案(必修2)羧酸氨基酸蛋白质(二)学案〔二〕知识点11.天然蛋白质水解得到的氨基酸均为氨基酸,写出其结构通式:2.举出几种常见的氨基酸3.写出氨基酸解离的示意图:氨基酸的等电点是指:等电点时,氨基酸的溶解度,利用这性质能够4.写丙氨酸和甘氨酸反应的方程式〔生成二肽的可能产物都写〕5.肽的官能团的结构简式:典题解悟.例1.当含有以下结构片段的蛋白质在胃中水解时,不可能生成的氨基酸是解析:蛋白质水解时,是肽键中的 键断裂,然后 一侧连-OH一侧加-H ,该蛋白质片断水解后得到的氨基酸是A 、B 、C答案:D变形题:1..以下物质水解时,最难断裂的化学键是提示:酯、肽、卤化烃能水解,答案:B2.以下高聚物不是由两种单体缩聚而成的是ABC D提示:.A 、B 是加聚的产物 C 是 和HCHO 的缩聚产物D 是乙氨酸和苯丙氨的缩聚产物. 答案:AB 知识点2.1.蛋白质分子中通常含有 个以上的肽键,相对分子质量一样在上。
2.是构成蛋白质的物质基础,顺序决定了蛋白质的专门功能。
3.酶的特点:-NH - OH4.举出生活中常见的蛋白质:5.举例讲明蛋白质的要紧性质:〔1〕盐析:〔2〕变性:〔3〕颜色反应:〔4〕灼烧:典题解悟:例2.2004年诺贝尔化学奖授予美国和以色列的三位科学家,以表彰他们在蛋白质降解的研究中取得的成果。
以下关于蛋白质的讲法中不正确的选项是.......A.蛋白质属于天然有机高分子化合物,没有蛋白质就没有生命B.HCHO溶液或(NH4)2SO4溶液均能使蛋白质变性C.某些蛋白质跟浓硝酸作用会变黄D.能够采纳多次盐析或多次渗析的方法分离、提纯蛋白质解析: A蛋白质是生命运动的基础 B.HCHO使蛋白质变性, (NH4)2SO4溶液使蛋白质渗析C.蛋白质是显色反应 D.蛋白质溶液是胶体,能够渗析答案:B变形题:1、能使蛋白质从溶液中析出,而又不破坏蛋白质活性的方法是A、加饱和硫酸铵溶液B、加医用消毒酒精C、加入硫酸铜溶液D、加入福尔马林溶液提示: 1.重金属盐例如CuSO4,某些有机物例如HCHO一定浓度后酒精等能够使蛋白质变性,Na2SO4(NH4)2SO4溶液能够使蛋白质盐析。

羧酸氨基酸和蛋白质第二课时【学案导学】1.氨基酸是氨基取代了羧酸分子中烃基上的氢原子形成的。
天然蛋白质水解的最终产物都是。
简述α-氨基酸的鉴别。
2.氨基酸的两性:写出氨基酸两性离子在酸碱性不同时的解离关系式。
当调节溶液的pH为某一特定值时,可以使溶液中阴、阳离子的相等,为零,此时溶液的pH称为该氨基酸的。
达到此点时,氨基酸在水中的最小。
可以根据此来。
3.氨基酸形成二肽的断键原理:羧基断键,氨基断键。
以甘氨酸和丙氨酸为例,写出形成二肽的方程式。
4.酶是一类,是一种高效。
酶催化的主要特点是(1)需要;(2)具有高度的;(3)。
【课时测控15】1.下列说法正确的是()A.蔗糖、淀粉、蛋白质、油脂都属于高分子化合物B.蛋白质水解的最终产物是多种氨基酸C.蛋白质溶液中分别加入NaCl溶液、CuSO4溶液,其过程均是不可逆的D.蛋白质既与盐酸反应又与氢氧化钠溶液反应2.下列现象中不属于蛋白质变性的是()A.打针时用酒精消毒B.用福尔马林泡制标本C.用Cu(OH)2悬浊液防治农作物的病虫害D.蛋白质溶于水3.下列关于酶的叙述中不正确的是()A.酶是一种氨基酸,具有两性特点B.酶是一种蛋白质C.酶是生物体内代谢的催化剂D.酶催化反应切忌高温条件下进行4.为了鉴别某白色纺织品的成分是蚕丝还是“人造丝”,可选用的方法是()A.滴加浓硝酸B.灼烧C.滴加酒精 D.滴加NaCl溶液5.在下列反应中生成或断裂的不是C—N键的是()A.浓H2SO4和浓HNO3混合液和苯作用(温度为60℃)B.由棉花制得纤维素硝酸酯C.蛋白质水解生成多种α——氨基酸D.苯酚与浓H2SO4和浓HNO3混合溶液作用6.向淀粉中加入少量稀H2SO4,并加热使之发生水解。
为测定水解的程度,所需下列试剂中的()①NaOH溶液②银氨溶液③新制Cu(OH)2溶液④碘水⑤BaCl2溶液A.①⑤B.②④C.①③④D.②③④7.若1 mol有机物A在稀酸作用下水解生成2 mol B,下列物质中符合题意的物质可能是()①蔗糖②麦芽糖③葡萄糖④淀粉8.下列叙述中,正确的是()A.能发生酯化反应的酸,一定是羧酸B.油脂水解后得到的醇是丙三醇C.天然蛋白质水解的最后产物是多种氨基酸D.淀粉、纤维素、油脂都是高分子化合物9.下列关于蛋白质的叙述中,不正确的是()A.蛋白质溶液中加入饱和硫酸铵溶液,蛋白质析出,虽再加水,也不溶解B.重金属盐能使蛋白质凝结,所以误食重金属盐会中毒C.浓硝酸溅在皮肤上呈黄色是由于浓硝酸和蛋白质发生了颜色反应D.蛋白质溶液中的蛋白质能透过半透膜【课后提高】1.当含下列结构片段的蛋白质在胃中水解时,不可能生成的氨基酸是()2.某共价化合物含碳、氢、氮三种元素,分子内有4个氮原子,且4个氮原子排列成内空的四面体(如白磷结构),每两个氮原子间都有一个碳原子.已知分子内无C——C键和C =C键则该化合物的化学式为()A.C6H8N4B.C6H12N4C.C6H10N4D.C4H8N43.血液中有一种含铜的呈蓝色的蛋白质分子,其式量约为151000.已知该分子中铜的质分数0.34%,则平均每个铜蓝蛋白质分子中的铜原子数为()A.8B.6C.4D.24.血红蛋白质分子中含有0.34%的铁元素,若它的每个分子中含有1个铁原子,则这种血红蛋白质的相对分子质量为____.5.某有机化合物化学式为C3H7O2N,①若它能和酸或碱反应生成盐,且分子结构含有甲基,则它的结构简式为_____________.②若它是一种不溶于水的中性物质,分子结构中既有甲基又有丙基,则它的结构简式为______________________.6.一分子氨基酸中的羧基与一另分子氨基酸中的氨基之间脱去水的物质叫二肽.(1)试写出氨基乙酸和丙氨酸形式二肽的结构简式___________.(2)已知赖氨酸分子中含有一个羧基和两个氮原子,含氮质量分数为19.18%,其化学式为________.若又知其一个氨基在α-碳原子上,另一个在直链分子末端碳原子上,分子中无烃基支链,它的结构简式是______.7.棉花纤维素式量为174960,每个分子中含有_________个葡萄糖单元.当纤维素与浓H2SO4浓HNO3的混合物反应后产物中含氮8.12%,每个葡萄糖单元中发生硝化反应的羟基数是____个8.化学式为C7H7NO2的有机物A、B、C、D、E、F分子中均含有苯环.(1)A、B、C三种有机物既能溶于强酸又能溶于强碱,则A、B、C的结构简式为:A________B、________C、________(2)D、E、F既不溶于强酸又不溶于强碱,则D、E、F的结构简式为:D__________、E_______、F________.。


【本讲教育信息】一、教学内容:高考复习《化学选修5》第五章官能团与有机化学反应烃的衍生物第四节羧酸氨基酸和蛋白质1、羧酸的典型代表物的组成、结构特点及其与其它烃的衍生物之间的关系。
2、氨基酸的组成、结构特点及主要化学性质,氨基酸与人体健康的关系。
3、蛋白质的组成、结构和性质。
二、教学目的:1、了解羧酸的典型代表物的组成、结构特点及其与其它烃的衍生物之间的关系。
2、了解氨基酸的组成、结构特点和主要化学性质,氨基酸与人体健康的关系。
3、了解蛋白质的组成、结构和性质。
4、了解化学学科在生命科学发展中所起的重要作用。
三、重点和难点:1、羧酸的典型代表物的组成、结构特点、主要化学性质及其与其它烃的衍生物之间的关系。
2、氨基酸的组成、结构特点和主要化学性质。
3、蛋白质的结构、组成和性质。
四、考点分析:本节内容在高考中的主要考查点是:1、羧酸及其典型代表物的组成、结构和性质。
2、羧酸与其它烃的衍生物之间的关系。
3、氨基酸的组成、结构和性质。
4、蛋白质的结构、组成和性质。
五、知识要点:1、羧酸是由_________(或氢原子)和_________相连组成的有机化合物。
根据分子中_________种类的不同,如果分子中_________和_________相连的羧酸我们称为脂肪酸;如果分子中_________直接连接在_________的羧酸我们称为芳香酸。
根据分子中_________的不同,我们把羧酸分为一元羧酸、二元羧酸等。
2、甲酸结构简式为_________,是有_________气味的无色液体,有腐蚀性,能与_________、_________、_________、甘油等互溶,由于甲酸中含有_________和_________两个官能团,因此既具有羧酸的性质,又具有醛类的性质,可以做工业上的_________,医用_________等。
乙二酸的结构简式为_________,俗称_________,属于_________元羧酸,是_________色的透明_________,分子中通常含有两分子结晶水,能溶于水或乙醇。

《第四节羧酸氨基酸和蛋白质》课后作业答案与解析1,该有机化合物中含有羧基和羟基,而且四个碳原子不出现支链,羟基在碳链的一端(能成五元环,脱水产物只有一种)2,1个迷迭香酸分子中含有2个苯环和一个碳碳双键,最多能和7个氢气分子发生加成反应;迷迭香酸中含有羧基、酯基、酚羟基,故可以发生酯化反应、水解反应、取代反应(酚羟基的邻对位上的氢原子可以被取代);1 mol迷迭香酸含有4 mol酚羟基、1 mol羧基、1 mol酯基,故1 mol迷迭香酸最多能和含6 mol NaOH的水溶液完全反应。
3项两者互为同分异构体;B项两者均为不含碳碳双键的一元羧酸,互为同系物;C项前者为甲酸,后者可能为丙酸,也可能为乙酸甲酯等物质,故C项两者可能互为同系物;D项,一个为一元羧酸,一个为二元羧酸,二者既不是同系物,又不是同分异构体。
45,莽草酸中含羧基、醇羟基和碳碳双键,鞣酸中含有羧基、酚羟基。
由各官能团性质可知A正确。
应特别注意鞣酸分子中含苯环,苯环中并不存在典型的碳碳双键。
答案:A6、答案:D7、解析:因为酯化反应是可逆的,不能完全进行到底,A错,B、C、D均正确。
答案:A8、解析:因1 mol酯完全水解可得到1 mol羧酸和2 mol乙醇,即C 18H26O5+2H2O根据原子守恒,得C x H y O z为C14H18O5,所以选A。
答案:A9、解析:α-氨基酸指氨基在羧基的α位上,即,A正确。
半胱氨酸中既含有碱性基团—NH2,又有酸性基团—COOH,B正确。
HS—CH2—CH2—COONH4是半胱氨酸的铵盐,与NaOH溶液反应有NH3生成,C正确。
两分子半胱氨酸,脱水形成的二肽结构简式为,D不正确。
答案:D10、解析:根据结构简式可知三者的分子式相同,均为C8H8O2,因此三者互为同分异构体。
三者在结构上的最大区别在于甲分子中含有酚羟基,可以用FeCl3溶液鉴别出来;乙分子中存在羧基,向其中加入Na2CO3或NaHCO3溶液能够产生气泡;丙分子中含有醛基,与银氨溶液共热可以发生银镜反应。

羧酸 酯 氨基酸 蛋白质 编号40组别_________姓名___________【学习目标】 1、扎实掌握羧酸、酯、氨基酸、蛋白质的主要化学性质及它们的联系。
2、通过小组合作探究官能团和性质的关系3、以极度的热情投入学习, 体验成功的快乐【使用说明】 先认真阅读课本, 然后完成学案, 下课收齐。
下节课先修改10分钟, 针对存在问题重点讨论8分钟, 学生展示并点评, 教师适当拓展总结, 最后学科班长做好评价。
【能力点拨】1、通过对羧酸和酯性质的研究, 进一步形成由结构分析性质的能力 2、进一步培养学生细致规范的使用化学用语的能力。
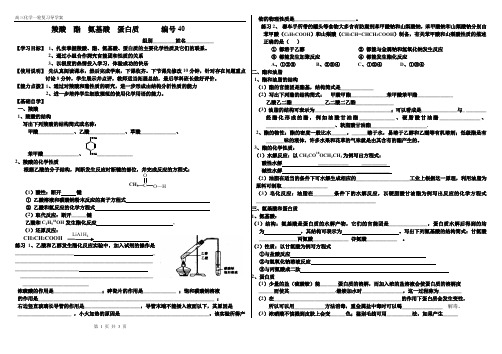
【基础自学】 一、羧酸 1、羧酸的结构写出下列羧酸的结构简式或名称:甲酸______________、乙酸______________、草酸______________、苯甲酸______________、COOHCOOH ______________2、羧酸的化学性质根据乙酸的分子结构, 判断发生反应时断键的部位, 并完成反应的方程式:CH 3(1)酸性:断开 键① 乙酸溶液和碳酸钠粉末反应的离子方程式 ② 乙酸和氨反应的化学方程式 (2)取代反应:断开______键乙酸和C 2H 518OH 发生酯化反应 , (3)还原反应:CH 3CH 2COOHC OO —HLiAl H 4练习1、乙酸和乙醇发生酯化反应实验中, 加入试剂的操作是_______________________ _ _____________________________________________________________________________________________________________________________________________________________浓硫酸的作用是___________________;碎瓷片的作用是_____________ ;饱和碳酸钠溶液的作用是_____________________________________________________________________ ;右边竖直玻璃长导管的作用是______________________, 导管末端不能插入液面以下, 其原因是_____________________ , 小火加热的原因是___________________________________, 该实验所得产物的物理性质是________________________。
高三化学一轮复习导学案羧酸 酯 氨基酸 蛋白质 编号40组别_________姓名___________ 【学习目标】 1、扎实掌握羧酸、酯、氨基酸、蛋白质的主要化学性质及它们的联系。
2、通过小组合作探究官能团和性质的关系3、以极度的热情投入学习,体验成功的快乐【使用说明】 先认真阅读课本,然后完成学案,下课收齐。
下节课先修改10分钟,针对存在问题重点讨论8分钟,学生展示并点评,教师适当拓展总结,最后学科班长做好评价。
【能力点拨】1、通过对羧酸和酯性质的研究,进一步形成由结构分析性质的能力 2、进一步培养学生细致规范的使用化学用语的能力。
【基础自学】 一、羧酸 1、羧酸的结构写出下列羧酸的结构简式或名称:甲酸______________、乙酸______________、草酸______________、苯甲酸______________、COOHCOOH ______________2、羧酸的化学性质根据乙酸的分子结构,判断发生反应时断键的部位,并完成反应的方程式:CH 3 (1)酸性:断开 键① 乙酸溶液和碳酸钠粉末反应的离子方程式 ② 乙酸和氨反应的化学方程式 (2)取代反应:断开______键乙酸和C 2H 518OH 发生酯化反应 , (3)还原反应:CH 3CH 2COOH 练习1、乙酸和乙醇发生酯化反应实验中,加入试剂的操作是_______________________ _ _______________________________________________________________________________ ______________________________________________________________________________浓硫酸的作用是___________________;碎瓷片的作用是_____________ ;饱和碳酸钠溶液 的作用是_____________________________________________________________________ ; 右边竖直玻璃长导管的作用是______________________,导管末端不能插入液面以下,其原因是_____________________ ,小火加热的原因是___________________________________,该实验所得产物的物理性质是________________________。

高三化学一轮复习 2.4 羧酸、氨基酸蛋白质学案【考纲要求】了解羧酸、酯的典型代表物的组成和结构特点以及它们的相互联系。
【课前预习案】一、酯1、酯的官能团名称和结构简式:,饱和酯的通式,可见,碳原子数....相同的饱和一元脂肪酸和酯是同分异构体..................。
2、低级酯的物理性质:有香味的液体,不溶于水易溶于有机溶剂,密度一般比水小。
3、酯的化学性质(1)酯在酸性条件下不完全水解,写出反应通式:(2)在碱性条件下水解趋于完全,写出反应通式:(3)油脂在碱性条件下水解反应称为皂化反应,写出硬脂酸(C17H35COOH)甘油酯皂化反应的方程式:[思考]①如何证明油脂的皂化反应已经彻底?②甲酸酯(HCOOR)具有什么化学性质?例1、有一种有机物的结构简式如右图:下列有关它的性质的叙述,正确的是()①有弱酸性,能与氢氧化钠反应②不能发生水解反应③能发生水解反应,水解后生成两种物质④它能发生水解反应,水解后只生成一种物质A.只有① B.只有①② C.只有①③ D.只有①④二、氨基酸1、氨基酸的结构:氨基酸是羧酸分子里烃基上的氢原子被氨基(-NH2)取代后的生成物。
氨基酸的命名是以羧酸为母体,氨基为取代基,碳原子的编号通常把离羧酸最近的碳原子称为α碳原子,α-氨基酸的分子结构可表示为:R-CH(NH2)-COOH。
氨基酸的官能团为,天然氨基酸都是α—氨基酸。
常见氨基酸有:甘氨酸,丙氨酸,苯丙氨酸。
2、氨基酸性质(1)、两性其中-COOH使氨基酸表现弱酸性,-NH2使氨基酸表现弱碱性,所以氨基酸为两性化合物。
既能与酸反应,又能与碱反应。
写出下列反应的化学方程式:①甘氨酸与盐酸反应,②丙氨酸与氢氧化钠溶液反应。
【思考】既能与酸又能与碱反应的物质有哪些?(2)成肽反应例2、(双选)下列物质中,既能与盐酸反应又能与氢氧化钠溶液反应的是( )A.氨基乙酸 B.碳酸氢钾 C.硫酸氢钾 D.苯酚钠二、肽1、核心官能团名称,表示为,形成:一个氨基酸分子的与另一个氨基酸分子的脱去一分子形成的。

2020高考化学一轮复习9.4分类突破(3)羧酸、酯、基本营养物质学案(含解析)第4课时分类突破3羧酸、酯、基本营养物质知识点一羧酸的结构与性质1.羧酸的定义由烃基与羧基相连构成的有机化合物。
官能团为COOH,饱和一元羧酸分子的通式为CnH2nO2n≥1。
2.羧酸的分类按烃基种类脂肪酸乙酸、硬脂酸C17H35COOH 芳香酸苯甲酸按羧基个数一元羧酸甲酸HCOOH、乙酸、硬脂酸二元羧酸乙二酸HOOCCOOH 多元羧酸3.甲酸和乙酸的分子组成和结构物质分子式结构简式官能团甲酸CH2O2 HCOOH COOH和CHO 乙酸C2H4O2 CH3COOH COOH 4.羧酸的化学性质羧酸的性质取决于羧基,反应时的主要断键位置如图1酸的通性乙酸是一种弱酸,其酸性比碳酸强,在水溶液中的电离方程式为-+H+。
乙酸分别与Na2CO3和NaHCO3反应的化学方程式Na2CO3+2CH3COOH→2CH3COONa+H2O+CO2↑,NaHCO3+CH3COOH→CH3COONa+H2O+CO2↑。
2酯化反应CH3COOH和CH3CHOH发生酯化反应的化学方程式为CH3COOH+CH3CHOHCH3CO18OCH2CH3+H2O。
3注意事项①能与NaHCO3反应产生CO2气体的有机物中一定含有羧基,且1 mol COOH与NaHCO3反应产生1 mol CO2。
②甲酸的结构为,分子中既含COOH,又含CHO,因此,甲酸既有羧酸的性质,又有醛的性质。
③草酸乙二酸草酸HOOCCOOH的酸性强于甲酸,具有强的还原性,可使酸性KMnO4溶液褪色;草酸在浓H2SO4作用下分解可用于制取COH2C2O4CO2↑+CO↑+H2O。
[对点训练] 1.2019·济宁一模有机物M的结构简式如图所示,与氢气发生加成反应得到物质甲,下列有关说法错误的是A.有机物M含有2种官能团B.有机物M的分子式为C4H6O2 C.有机物M能发生取代反应、加聚反应D.甲的只含有一种官能团的链状同分异构体有6种解析选D 含有碳碳双键和羧基,A正确;分子式为C4H6O2,B正确;含有羧基,可与醇发生酯化反应取代反应,含碳碳双键,可发生加聚反应,C正确;满足题给条件的同分异构体有以下5种,酸CH3CH2CH2COOH。

羧酸酯氨基酸蛋白質編號40組別_________姓名___________【學習目標】1、扎實掌握羧酸、酯、氨基酸、蛋白質的主要化學性質及它們的聯繫。
2、通過小組合作探究官能團和性質的關係3、以極度的熱情投入學習,體驗成功的快樂【使用說明】先認真閱讀課本,然後完成學案,下課收齊。
下節課先修改10分鐘,針對存在問題重點討論8分鐘,學生展示並點評,教師適當拓展總結,最後學科班長做好評價。
【能力點撥】1、通過對羧酸和酯性質的研究,進一步形成由結構分析性質的能力2、進一步培養學生細緻規範的使用化學用語的能力。
【基礎自學】一、羧酸1、羧酸的結構寫出下列羧酸的結構簡式或名稱:甲酸______________、乙酸______________、草酸______________、苯甲酸______________、COOHCOOH______________2、羧酸的化學性質根據乙酸的分子結構,判斷發生反應時斷鍵的部位,並完成反應的方程式:CH3(1)酸性:斷開鍵① 乙酸溶液和碳酸鈉粉末反應的離子方程式COO—H② 乙酸和氨反應的化學方程式(2)取代反應:斷開______鍵乙酸和C2H518OH發生酯化反應,(3)還原反應:LiAl H4CH3CH2COOH練習1、乙酸和乙醇發生酯化反應實驗中,加入試劑的操作是_______________________ ______________________________________________________________________________________________________________________________________________________________濃硫酸的作用是___________________;碎瓷片的作用是_____________ ;飽和碳酸鈉溶液的作用是_____________________________________________________________________ ;右邊豎直玻璃長導管的作用是______________________,導管末端不能插入液面以下,其原因是_____________________ ,小火加熱的原因是___________________________________,該實驗所得產物的物理性質是________________________。

2018山东科技版化学高考第一轮复习——羧酸、氨基酸和蛋白质(习题+解析)只要总体积一定,完全燃烧消耗的氧气的物质的量也一定的是( )①乙醇和乙醚 ②丙醛和丙炔 ③甲烷和甲酸甲酯④125H C 和86H C ⑤丙酮和丙二醇(283O H C ) ⑥甘氨酸和硝基乙烷A 、只有①②③④B 、只有②④⑥C 、除①外D 、只有②③⑤5、下式表示蛋白质分子结构的一部分: 它的水解产物可能是A 、④⑤⑥B 、①②④C 、②③⑦D 、②④⑦6、分子式为277NO H C 的有机物A 、B 、C 、D 、E 、F 六种分子中均含有苯环。
(1)A 、B 、C 三种有机物既能溶于强酸又能溶于强碱,写出A 、B 、C 的结构简式:A 为__________;B 为__________;C 为__________。
(2)D 、E 、F 既不溶于强酸又不溶于强碱,写出D 、E 、F 的结构简式:D 为__________;E 为__________;F 为__________。
7、丙氨酸在强酸性溶液里以阳离子存在,在强碱性溶液中以阴离子存在,在pH=6时以两性离子存在。
丙氨酸在水溶液中存在下列关系:(1)滴加少量盐酸,浓度__________。
(2)滴加少量NaOH溶液,浓度___________。
,有机物B的8、有机物A的分子式为NOCH327,这两种有机物分子中都有一个分子式为NHOC392与碳原子连接的甲基,它们都能与NaOH溶液反应,也能与盐酸反应。
(1)有机物A、B的结构式为:A______________,B______________。
(2)A、B分别与NaOH反应的化学方程式为:_______________________________________ _________________,_______________________________________ _________________。

第3节羧酸氨基酸和蛋白质考试评价解读1.能描述说明、分析解释羧酸及其衍生物、生命中的基础有机化学物质的重要反应,能书写相应的化学方程式。
2.能辨识蛋白质结构中的肽键,能说明蛋白质的基本结构特点,能判断氨基酸的缩合产物、多肽的水解产物。
3.能基于官能团、价键类型、特点及反应规律分析和推断含有羧基、酯基和氨基、肽键等有机化合物的化学性质,并根据有关信息书写相应的反应式。
核心素养达成宏观辨识与微观探析能从官能团角度认识羧酸及其衍生物、氨基酸和蛋白质的组成、结构、性质和变化,并能从宏观与微观相结合的视角分析与解决实际问题。
证据推理与模型认知具有证据意识,对氨基酸和蛋白质的组成、结构及其变化提出可能的假设,解释现象的本质和规律。
羧酸及其衍生物[以练带忆]1.化学是你,化学是我,化学深入我们的生活。
下列说法错误的是( )A.食用油反复加热会产生稠环芳烃等有害物质B.花生油和鸡蛋清都能发生水解反应C.地沟油与矿物油可通过分别加入足量氢氧化钠溶液共热的方法区分,不分层的是地沟油D.将牛油和烧碱溶液混合加热,充分反应后加入热的饱和食盐水,上层析出甘油D 解析:食用油反复加热,碳链会变成环状,产生稠环芳烃等有害物质,故A项正确;食用花生油属于油脂,是高级脂肪酸甘油酯,可以发生水解反应;鸡蛋清是蛋白质,也可以发生水解反应,故B项正确;地沟油的主要成分属于油脂,加入氢氧化钠溶液共热可以发生水解反应生成可溶于水的高级脂肪酸钠、甘油,不会出现分层现象,而矿物油不溶于氢氧化钠溶液,也不发生反应,会出现分层现象,因此可以用该方法区分二者,故C项正确;将牛油和烧碱溶液混合加热制肥皂,加入热的饱和食盐水后降低了肥皂的溶解度,因此上层析出的是肥皂,而甘油溶解在水溶液中,故D项错误。
2.我国科学家构建了一种有机框架物M,结构如图。
下列说法错误的是( )A.1 mol M可与足量Na2CO3溶液反应生成1.5 mol CO2B.苯环上的一氯代物有3种C.所有碳原子可能均处于同一平面D.1 mol M可与15 mol H2发生加成反应D 解析:根据物质结构可知,在该化合物中含有3个—COOH,由于每2个H+与CO2-3反应产生1 mol CO2气体,所以1 mol M可与足量Na2CO3溶液反应生成1.5 mol CO2,A 正确。

羧酸氨基酸和蛋白质一、选择题(每小题只有一个选项符合题意)1.下列物质中,不能使酸性KMnO4溶液褪色的是()①②CH3CH2OH③④CH3COOH⑤CH2===CH—COOH ⑥A.①③⑤B.①④⑥C.②⑤⑥D.①③④2.新版人民币的发行,引发了人们对有关人民币中化学知识的关注。
下列表述不正确的是()A.制造人民币所用的棉花、优质针叶木等原料的主要成分是纤维素B.用于人民币票面文字等处的油墨中所含有的Fe3O4是一种磁性物质C.某种化学验钞笔中含有碘酒溶液,遇假钞呈现蓝色,其中遇碘变蓝的是淀粉D.防伪荧光油墨由颜料与树脂连接料等制成,树脂与油脂一样,属于高分子化合物3.下列说法正确的是()A.麦芽糖及其水解产物都能与银氨溶液发生反应B.棉、麻、丝、毛完全燃烧都只生成CO2和H2OC.皂化反应后期向反应液中加入饱和食盐水,下层析出高级脂肪酸钠D.甘氨酸和丙氨酸通过缩合反应最多可以得到3 种二肽4.反兴奋剂是体育赛事关注的热点,利尿酸是一种常见的兴奋剂,其分子结构简式如图所示。
下列关于利尿酸的说法正确的是()A.它的分子式是C13H11O4Cl2B.它不能使酸性高锰酸钾溶液褪色C.它不能与饱和碳酸钠溶液反应放出CO2D.它能发生取代反应、加成反应和酯化反应5.肉桂酸异戊酯是一种香料,其结构简式如图所示。
下列有关肉桂酸异戊酯的叙述正确的是()A.不能使酸性KMnO4溶液褪色B.能与新制的碱性Cu(OH)2悬浊液共热生成砖红色沉淀C.能与FeCl3溶液反应显紫色D.能与热的浓硝酸和浓硫酸混合液反应6.药物麻黄碱和牛磺酸的结构简式如图所示。
下列有关麻黄碱、牛磺酸的叙述正确的是()A.分子式分别为C10H16ON、C2H7NO2SB.均能发生取代反应,麻黄碱还能发生加成反应C.均能与金属钠及氢氧化钠溶液反应D.牛磺酸与HSCH2CH(NH2)COOH(半胱氨酸)互为同系物7.(2021·泰安模拟)Z是合成某药物的中间体,其合成原理如下:下列说法正确的是()A.用NaHCO3溶液可以鉴别X和ZB.X、Y、Z都能发生取代反应C.X分子所有碳原子可能共平面D.与X具有相同官能团的同分异构体还有5种二、不定项选择题(每小题有一个或两个选项符合题意)8.化合物Z是合成平喘药沙丁胺醇的中间体,可通过下列路线制得:下列说法正确的是()A.X分子中所有原子在同一平面上B.Y与足量H2的加成产物分子中有4个手性碳原子C.可用FeCl3溶液鉴别Y和ZD.1 mol Z最多能与4 mol NaOH反应9.阿斯巴甜(结构简式如图)具有清爽的甜味,甜度约为蔗糖的200倍。

2020高考化学一轮复习学案(必修2)羧酸氨基酸和蛋白质(一)知识再现:知识点1.1.羧酸官能团的名称和结构式分不是 和2.羧酸的命名:〔1〕选的碳链作主链,称某酸 〔2〕从给主链碳编号。
〔3〕在某酸名称前加写出完整名称 CH 3-CH-CH 2-CH 2-COOH 名称CH 3-CH-CH 22-CH 3名称酸 举例3.分类:依照烃基种类分:羧酸酸 举例举例酸 举例 4.羧酸类物质溶于水的规律特点:CH 3COOHC 2H 5CH 3-CH-CH 2-CH-COOHCH 3CH 3羧酸较相近相对分子质量的醇的沸点 〔高或低〕,其缘故是典题解悟:例1:以下讲法中,正确的选项是 [ ]A .羧酸的通式为C n H 2n O 2B .羧酸在常温下均为液态,没有气态C .烃基和羧基直截了当相连的化合物一定是羧酸D .在饱和链状一元羧酸中,甲酸沸点最低解析: A .饱和一元羧酸的通式为C n H 2n O 2B .羧酸没有气态的,但有固态的例苯甲酸草酸等C .这是羧酸的定义D .同类有机物中碳原子数越少,一样溶沸点越低。
答案:CD变形题:1.以下各有机物,互为同系物的是A.醋酸与硬脂酸B.丙烯酸(CH 2==CHCOOH)与油酸C.甲酸与苯甲酸D.甲醇与乙二醇 提示:①把握芳香族化合物,同系物的定义和实质②把握一样物质类不的物理性质变化规律 答案:AB2. 芬必得〞要紧成分的结构简式:它属于A.芳香族化合物B.苯甲酸的同系物C.易溶于的化合物D.易升华的物质提示:同系物在分子组成上相差(CH2)n,从结构上看,官能团的种类、个数、烃基的种类都要相同,从这两个角度都解决此题答案:AB变形题:3. 丁基共有4种,不必试写,赶忙可推断分子式C5H10O2的羧酸的同分异构体的数目是[ ]A.3种B.4种C.5种D.6种提示:丁基连上羧基即为C5H10O2的羧酸答案:B知识点2:羧酸的化学性质:羧酸分子中易断的键是1.酸性:写出由乙酸制取乙酰胺的方程式2.羟基取代:写出由乙酸制取乙酸乙酯的化学方程式:写出由乙酸制取乙酸酐的化学方程式制备乙酸乙酯时,能够采取哪些方法提高乙酸乙酯的产量3.а-H的取代:写出由乙酸制取氯乙酸的方程式:4.用酸将CH3COOH还原为例1:在国际环境咨询题中,使用由聚苯乙烯材料做成的各种制品,由于难以分解、处理苦恼而带来〝白色污染〞。

高考化学一轮总复习教师用书:氨基酸和蛋白质必备知识·梳理夯实知识梳理1.氨基酸的结构与性质(1)组成与结构羧酸分子中烃基的氢原子被氨基取代后的产物。
蛋白质水解后得到的几乎都是α-氨基酸,其通式为,官能团为—NH2和—COOH 。
(2)化学性质①两性氨基酸分子中既含有羧基,又含有氨基,故氨基酸是两性化合物,能与酸、碱反应生成盐。
例如,甘氨酸(HOOCCH2NH2)与HCl、NaOH反应的化学方程式分别为。
②成肽反应两个氨基酸分子(可以相同,也可以不同)在一定条件下,通过氨基与羧基间缩合脱去水,形成含有肽键()的化合物,发生成肽反应。
由两个氨基酸分子缩合后形成的含有肽键的化合物称为二肽,反应通式如下:二肽还可以继续与其他氨基酸分子缩合生成三肽、四肽、五肽,以至生成长链的多肽,多肽的结构表示如下:多肽常呈链状,因此也叫肽链,肽链能盘曲、折叠,还可以相互结合,形成蛋白质。
2.蛋白质的结构与性质(1)组成与结构①蛋白质含有C、H、O、N、S等元素。
②蛋白质是由氨基酸通过缩聚反应生成的,蛋白质属于天然有机高分子。
(2)化学性质(3)蛋白质盐析与变性的比较盐析变性内涵加入无机盐溶液使蛋白质的溶解度降低而析出一定条件下,使蛋白质失去原有生理活性条件较浓的轻金属盐或铵盐溶液,如(NH4)2SO4、Na2SO4溶液等加热、紫外线、X射线、重金属盐、强酸、强碱、甲醛等特点可逆,蛋白质仍保持原有活性不可逆,蛋白质已失去原有活性应用分离、提纯蛋白质消毒、灭菌,给果树施用波尔多液,保存动物标本等(1)酶是一种由细胞产生的、对生物体内的化学反应具有催化作用的有机化合物,其中绝大多数是蛋白质,具有蛋白质的性质。
(2)酶是一种生物催化剂,催化作用具有以下特点:①条件温和,一般在接近体温和中性的条件下进行;②具有高度的专一性;③具有高效催化作用。
4.核酸的结构与性质(1)核酸的形成核酸是由核苷酸聚合而形成的高分子化合物,属于生物大分子。

2024年高考化学氨基酸和蛋白质历年真题精解在2024年的高考中,化学科目的考试中涉及了氨基酸和蛋白质的相关知识点。
本文将对这些知识点进行详细的解析,通过历年真题的精选,帮助考生们更好地理解和掌握这些内容。
第一部分:氨基酸的基本概念和分类氨基酸是构成蛋白质的基本单位,它由氨基(NH2)、羧基(COOH)、一个氢原子和一个侧链基团(R)组成。
根据氨基酸的侧链基团的性质,可以将氨基酸分为20种常见氨基酸。
这些氨基酸在蛋白质中按照一定的顺序连接在一起,形成不同的多肽链,进而组成功能各异的蛋白质。
第二部分:氨基酸的性质和功能不同的氨基酸具有不同的性质和功能。
下面列举了几个常见的例子:1. 起酸碱作用:某些氨基酸在溶液中可以释放出H+离子,起酸性作用,例如谷氨酸和天冬氨酸;而另一些氨基酸则可以接受H+离子,起碱性作用,例如赖氨酸和精氨酸。
2. 光学性质:氨基酸的α碳上有一个手性的位点,因此大多数天然氨基酸可以存在两种立体异构体,分别为D型和L型。
其中,绝大部分天然氨基酸都是L型的。
3. 编码遗传信息:氨基酸在蛋白质合成中扮演着重要的角色。
核糖核酸(RNA)通过三个碱基的密码子来编码氨基酸的序列,进而决定蛋白质的结构和功能。
第三部分:蛋白质的结构和功能蛋白质是生物体内功能最多样化的大分子化合物,具有极其复杂的结构。
根据其结构层次的不同,可以将蛋白质分为四个级别:一级结构、二级结构、三级结构和四级结构。
1. 一级结构:指氨基酸通过肽键的形成与连接顺序。
2. 二级结构:指蛋白质中由氢键形成的α螺旋和β折叠等空间结构。
3. 三级结构:指蛋白质链进一步折叠成特定的空间结构。
4. 四级结构:指由多个蛋白质链相互作用形成的复杂蛋白质结构。
不同的结构赋予蛋白质不同的功能,例如,酶是一种特殊的蛋白质,能够催化生物体内的各种化学反应。
第四部分:历年真题的精解以下是几个历年高考真题中与氨基酸和蛋白质相关的题目及解析:1. 题目:某种蛋白质由600个氨基酸组成,其中脯氨酸(Pro)的含量占总氨基酸的5%,试回答以下问题:(1) 脯氨酸在该蛋白质中的个数是多少?(2) 其他氨基酸的数量是多少?解析:(1) 脯氨酸占总氨基酸的5%,可以得出脯氨酸的个数为600* 5% = 30个;(2) 其他氨基酸的数量为600 - 30 = 570个。
羧酸 酯 氨基酸 蛋白质 编号40组别_________姓名___________【学习目标】 1、扎实掌握羧酸、酯、氨基酸、蛋白质的主要化学性质及它们的联系。
2、通过小组合作探究官能团和性质的关系3、以极度的热情投入学习,体验成功的快乐【使用说明】 先认真阅读课本,然后完成学案,下课收齐。
下节课先修改10分钟,针对存在问题重点讨论8分钟,学生展示并点评,教师适当拓展总结,最后学科班长做好评价。
【能力点拨】1、通过对羧酸和酯性质的研究,进一步形成由结构分析性质的能力 2、进一步培养学生细致规范的使用化学用语的能力。
【基础自学】 一、羧酸 1、羧酸的结构写出下列羧酸的结构简式或名称:甲酸______________、乙酸______________、草酸______________、苯甲酸______________、COOH______________2、羧酸的化学性质根据乙酸的分子结构,判断发生反应时断键的部位,并完成反应的方程式:CH 3 (1)酸性:断开 键① 乙酸溶液和碳酸钠粉末反应的离子方程式 ② 乙酸和氨反应的化学方程式 (2)取代反应:断开______键乙酸和C 2H 518OH 发生酯化反应 , (3)还原反应:CH 3CH 2COOHC OO —H LiAl H 4练习1、乙酸和乙醇发生酯化反应实验中,加入试剂的操作是_______________________ _ _____________________________________________________________________________________________________________________________________________________________浓硫酸的作用是___________________;碎瓷片的作用是_____________ ;饱和碳酸钠溶液的作用是_____________________________________________________________________ ;右边竖直玻璃长导管的作用是______________________,导管末端不能插入液面以下,其原因是_____________________ ,小火加热的原因是___________________________________,该实验所得产物的物理性质是________________________。
练习2、赛车手所带的罐头等食物大多含有防腐剂苯甲酸钠和山梨酸钠,苯甲酸钠和山梨酸钠分别由苯甲酸(C6H5COOH)和山梨酸(CH3CH=CHCH2COOH)制备,有关苯甲酸和山梨酸性质的描述正确的是()①都溶于乙醇②都能与金属钠和氢氧化钠发生反应③都能发生加聚反应④都能发生酯化反应A、①②③B、②③④C、①②④D、①③④二、酯和油脂1、酯和油脂的结构(1)酯的官能团是酯基,结构简式是_____________(2)写出下列酯的结构简式:甲酸甲酯______________苯甲酸苯甲酯______________ 乙酸乙二酯_____________乙二酸二乙酯_______________(3)油脂的结构可表示为______________________________;可以看成是______________与_ ________经酯化形成的酯,例如油酸甘油酯______________、硬脂酸甘油酯________________、___________________________、软脂酸甘油酯______________________.2、酯的物性:酯的密度一般比水______,______溶于水,易溶于乙醇和乙醚等有机溶剂;低级酯是有_______味的液体,许多水果和花草的气味就是由其含有的酯产生的。
3、酯的化学性质:(1)水解反应:以CH3CO18OCH2CH3为例写出方程式:酸性水解____________ __________碱性水解_____________(2)油脂在适当的条件下可水解生成相应的_____________________工业上根据这一原理,利用油脂为原料可制取__________________(3)皂化反应:油脂在________条件下的水解反应,以硬脂酸甘油酯为例写出反应的化学方程式_______________________________________________三、氨基酸和蛋白质1、氨基酸:(1)结构:氨基酸是蛋白质的水解产物,它们的官能团是_______________,蛋白质水解后得到的均为,其结构可表示为。
写出下列氨基酸的结构简式:甘氨酸_______________丙氨酸______________ 谷氨酸____________ 。
(2)性质:以甘氨酸为例写方程式①与盐酸反应②与氢氧化钠溶液反应③与丙氨酸成二肽2、蛋白质(1)少量的盐(硫酸铵)能_______蛋白质的溶解,而加入浓的盐溶液会使蛋白质的溶解度______而使其__________________,继续加水时________________,这一过程称为_________(2)在__________________________________________________的作用下蛋白质会发生变性,所以可以用____________方法消毒,重金属盐中毒时可以喝________________ 解毒。
(3)浓硝酸不慎溅到皮肤上会变______色;鉴别毛线可用__________法,如果产生__________________________,说明是真毛线。
(4)酶从本质上说是一类,其催化的主要特点是。
练习3、下列有关蛋白质的叙述正确的是()A、蛋白质溶液中,加入浓的硫酸铵溶液有沉淀析出,加水后沉淀不溶解B、蛋白质水解的最后产物是氨基酸C、蛋白质的分子能透过半透膜D、蛋白质都能跟浓硝酸作用呈黄色【合作探究、讨论展示】Array1、某有机物结构简式如右图,1mol此物质与足量的氢氧化钠溶液充分反应,消耗碱的量是()A、2molB、4molC、5molD、6mol2、有机物A(C8H16O2该条件的A的同分异构体有)A(C8H16O2)A、1种B、2种C、3种D、4种3、下列既能与NaOH溶液又能与盐酸反应的有()①Al(OH)3 ② NaHCO3③CH3COOCH3④苯丙氨酸⑤甘氨酰丙氨酸⑥碳酸铵A、3种B、4种C、5种D、6种【能力提升】1、能使蛋白质变性的物质是()①硫酸钾②甲醛③氯酸钾④硝酸汞⑤氯化铵⑥氢氧化钠A、②④⑥B、①③⑤C、①②③D、④⑤⑥2、某有机物与过量的钠反应得到V A L气体A,另取等量的该有机物与适量的碳酸钠完全反应得V B L气体B,同温同压下,V A与V B的关系一定是()A、V A=V BB、V A≥V BC、V A<V BD、无法确定3、化合物A最早发现于酸牛奶中,它是人体内糖代谢的中间体,可由马铃薯、玉米淀粉等发酵制得,A 的钙盐是人们喜爱的补钙剂之一。
A在某种催化剂的存在下进行氧化,其产物不能发生银镜反应。
在浓硫酸存在下,A可发生如下图所示的反应:写出下列方程式并注明反应类型:(1)A→B:______________________________________________________()(2) A→D:_______________________________________________________()(3) A→E:_______________________________________________________()(4) A→F:_______________________________________________________()★★4。
下图中A、B、C、D、E、F、G 均为有机化合物。
根据上图回答问题:(1)D 的化学名称是__________________。
(2)反应③的化学方程式是___________ ____。
(3)B的分子式是__________________。
A的结构简式是__________________。
反应①的反应类型是__________________。
(4)符合下列 3 个条件的 B 的同分异构体的数目有 ______________个。
i )含有邻二取代苯环结构、ii )与 B 有相同的官能团、iii )不与 FeCl 3 溶液发生显色反应。
写出其中任意一个同分异构体的结构简式______(5)G 是重要的工业原料,用化学方程式表示 G 的一种重要的工业用途_____ ______。
(6) D 生成J 的化学方程式_________________________________D 能氧化为W ,W 能发生银镜反应,W 与新制Cu(OH)2反应的化学方程式为__编号40一、羧酸1、—COOH (2)HCOOH CH 3COOH HOOC —COOH COOHCOOH对苯二甲酸2、(1)O —H①2CH 3COOH+CO 32—→2CH 3COO —+CO 2↑+H 2O②CH 3COOH+NH 3→CH 3COONH 4(2)C —O CH 3COOH+C 2H 518OH CH 3CO 18OC 2H 5+H 2O (3) CH 3CH 2CH 2OH【练习1】先向试管中加入一定量的乙醇和乙酸的混合物,然后一边摇动试管一边加入浓硫酸。
(或者先向试管中加入一定量的乙醇和,然后一边摇动试管一边加入浓硫酸,最后加入乙酸), 催化剂、吸水剂 防止液体爆沸 吸收乙酸,溶解乙醇,降低乙酸乙酯在水中的溶解度导气冷凝 防止倒吸 减少乙酸和乙醇的挥发,提高酯的产率和纯度。
无色有香味的油状液体,密度比水小,难溶于水 【练习2】C 二、酯和油脂CO O —R1、(1) (2)HCOOCH 3 (3)甘油 高级脂肪酸2、小 难 芳香气3、(1)CH 3CO 18OC 2H 5+H 2OCH 3COOH+C2H 518OHCH 3CO 18OC 2H 5+NaOH CH 3COONa+C 2H518OH(2)高级脂肪酸和甘油 甘油 (3)碱性 三、氨基酸和蛋白质1、(1)氨基和羧基 α—氨基酸2、(1)促进 降低 从溶液中析出 仍能溶解 盐析(2)紫外线照射,加热或加入有机化合物、酸、碱、重金属盐(如铜盐、铅盐、汞盐等)稀硫酸△高温 豆浆(牛奶) (3)黄 灼烧 特殊的气味(4)蛋白质 ①条件温和, ②具有高度的专一性 ③具有高效催化作用。
【练习3】B【合作探究】1.C 2.B 3、C 【能力提升】1、A 2、B 3、 (1) (2) (3) (4)4、(1)乙醇 (2)(3)C 9H 10O 3 水解反应 中和反应 (4)3(5) 制聚氯乙烯塑料 (6)酯化反应酯化反应 消去反应酯化反应。