枸杞子中食用红色素的提取及稳定性研究
- 格式:pdf
- 大小:94.32 KB
- 文档页数:3

枸杞色素的提取及纯化技术冯作山1 陈计峦2 孙高峰1 张春兰11(新疆农业大学食品学院,乌鲁木齐,830052)2(中国农业大学食品科学与营养工程学院,北京,100083)摘 要 以制汁、制酒后的枸杞残渣为原料,通过有机溶剂进行提取,得到枸杞色素粗提品。
试验结果表明,最佳提取溶剂乙酸乙酯,55e 下提取1h,提取3次可得最大提取率619%。
用氧化镁柱层析对粗品进行纯化,用石油醚能有效洗脱粗品中的脂溶性杂质,再用石油醚-丙酮(体积比10B 1)为洗脱液可有效洗脱得到类胡萝卜素,采用薄层色谱法(T LC 法)、高效液相法(H PLC 法)测定,B -胡萝卜素、类胡萝卜素的纯度可达78%。
关键词 枸杞,色素,提取,纯化第一作者:博士研究生,教授。
收稿时间:2004-08-15,改回时间:2004-10-25枸杞子(Lycium Chinese),茄科,是我国药食两用植物,也是传统名贵的中药材,具有补肾养肝、润肺明目之功效[1~4]。
新疆具有独特的土壤和气候条件,枸杞质量具有汁多肉厚、色泽红艳、多糖含量高等特点,目前产量已居全国之首。
仅新疆精河县托里乡种植面积已达8200km 2,年产量近6000t 。
枸杞已成为新疆红色产业开发项目之一[5]。
但目前从事枸杞产品开发的企业大多均以枸杞粗加工为主,仅针对黑果枸杞作了少量研究[6,7]。
为了大力发展新疆红色资源,提高枸杞子的综合利用价值,使资源优势转化为生产优势,本研究以制汁后的枸杞残渣为原料,对枸杞色素的最佳提取工艺及其纯化的方法进行了研究,为进一步开发新疆特色的枸杞资源提供科学依据。
1 材料与方法111 原 料新疆枸杞残渣,由新疆长生酿造有限责任公司提供。
112 试剂及仪器甲醇、乙酸乙酯、石油醚、丙酮、无水乙醚、氯仿、无水乙醇、硫酸、无水硫酸钠、NaOH (均为分析纯)。
薄层色谱硅胶板(青岛海洋化工厂)、氧化镁、层析硅胶、B -胡萝卜素(M erck,全反式)。
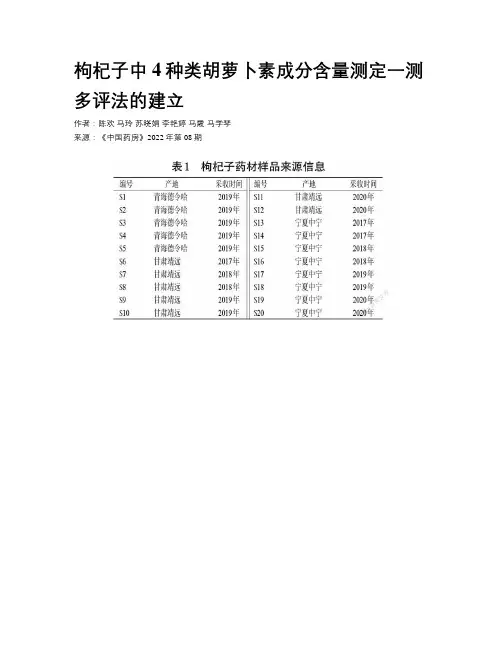
枸杞子中4种类胡萝卜素成分含量测定一测多评法的建立作者:陈欢马玲苏晓娟李艳婷马霞马学琴来源:《中国药房》2022年第08期中圖分类号 R917 文献标志码 A 文章编号 1001-0408(2022)08-0957-05DOI 10.6039/j.issn.1001-0408.2022.08.09摘要目的建立同时测定枸杞子中玉米黄质、β-胡萝卜素、β-隐黄素棕榈酸酯、玉米黄素双棕榈酸酯含量的方法。
方法枸杞子药材经正己烷-无水乙醇-丙酮-甲苯(10 ∶ 6 ∶ 7 ∶ 7,V/V/V/V)超声提取后,采用高效液相色谱法进行测定。
以YMC C30为色谱柱,以甲醇-乙腈-水(81 ∶ 14 ∶ 5,V/V/V)为流动相A、二氯甲烷为流动相B进行梯度洗脱,柱温为20 ℃,流速为1.0 mL/min,检测波长为450 nm,进样量为20 μL。
以玉米黄质为参照物,计算β-胡萝卜素、β-隐黄素棕榈酸酯、玉米黄素双棕榈酸酯的相对校正因子,再以此计算上述成分的含量,并与外标法测定结果进行比较。
结果玉米黄质、β-胡萝卜素、β-隐黄素棕榈酸酯、玉米黄素双棕榈酸酯检测质量浓度的线性范围分别为0.119 4~2.983 8、0.121 7~1.521 6、0.285 9~5.718 8、8.460 5~211.513 3 μg/mL(R2均大于0.999);精密度、重复性、稳定性(16 h)试验的RSD均小于4%;平均加样回收率分别为103.34%、107.37%、105.64%、96.16%(RSD关键词枸杞子;高效液相色谱法;一测多评法;玉米黄质;β-胡萝卜素;β-隐黄素棕榈酸酯;玉米黄素双棕榈酸酯Establishment of quantitative analysis of multi-components by singer marker for content determination of 4 carotenoids in Lycium barbarumCHEN Huan1,2,MA Ling1,SU Xiaojuan3,LI Yanting3,MA Xia1,MA Xueqin3(1. Ningxia Hui Autonomous Region Institute of Drug Control,Yinchuan 750002,China;2. Ningxia Key Laboratory of Drug Creation and Generic Drug Research, Yinchuan 750004,China;3. College of Pharmacy,Ningxia Medical University,Yinchuan 750004,China)ABSTRACT OBJECTIVE To establish a method for simultaneous determination of zeaxanthin,β-carotene,β-cryptoxanthin palmitate and zeaxanthin dipalmitate in Lycium barbarum. METHODS L. barbarum was extracted with n-hexane-anhydrous ethanol-acetone-toluene (10 ∶6 ∶7 ∶ 7, V/V/V/V) by ultrasonic method. High performance liquid chromatography (HPLC) method was adopted. The determination was performed on YMC C30 column with mobile phase A consisted of methanol-acetonitrile-water (81 ∶ 14 ∶ 5, V/V/V) and mobile phase B consisted of dichloromethane (gradient elution) at the flow rate of 1.0 mL/min. The column temperature was set at 20 ℃. The detection wavelength was set at 450 nm, and sample size was 20 μL. Using zeaxanthin as control, the relative correction factors (RCFs)of β-carotene,β-cryptoxanthin palmitate and zeaxanthin dipalmitate were calculated, and then the content of each component was calculated according to RCFs and compared with the results of external standard method(ESM). RESULTS The linear range of zeaxanthin,β-carotene,β-cryptoxanthin palmitate and zeaxanthin dipalmitate were 0.119 4-2.983 8, 0.121 7-1.521 6, 0.285 9-5.718 8,8.460 5-211.513 3 μg/mL(all R2>0.999). RSDs of precision, repeatability and stability(16 h)tests were all less than 4%. The average recoveries were 103.34%, 107.37%, 105.64%, 96.16%(RSDKEYWORDS Lycium barbarum; HPLC; QAMS; zeaxanthin; β-carotene; β-cryptoxanthin palmitate; zeaxanthin dipalmitate类胡萝卜素是中药枸杞子所含的主要色素,也是其重要的活性成分之一,具有提高人体免疫功能、抗肿瘤、抗氧化、护肝、保护视力等作用[1-5]。

枸杞食用色素的提取及稳定性研究冯文婕【摘要】采用有机溶剂浸提法提取宁夏枸杞中的食用色素.实验表明, 以乙醇为提取溶剂, 枸杞食用色素制备的影响因素主次分别为提取温度>乙醇浓度>提取时间>料液比.最佳提取工艺为: 以无水乙醇为提取剂, 料液比1:9, 45 ℃提取1.5 h, 此时枸杞色素的提取率最大.同时研究了枸杞色素的稳定性, 研究表明: 枸杞色素耐光性、耐高温性好, 在酸性介质、还原剂以及常用食品添加剂存在的条件下也有较好的稳定性.【期刊名称】《广州化工》【年(卷),期】2018(046)024【总页数】3页(P32-34)【关键词】枸杞;食用色素;提取;稳定性【作者】冯文婕【作者单位】浙江经贸职业技术学院,浙江杭州 310018【正文语种】中文【中图分类】TS201.2枸杞为茄科植物,俗称“红宝”,其根、叶、花、果都能入药,具有较高的营养价值,同时也是我国重要的经济资源,主要分布在宁夏、青海、新疆、河北、内蒙古和山西等地,其中以宁夏枸杞质量最优[1-2]。
枸杞不仅具有增强免疫力、抗肿瘤、防衰老,还能增加造血功能和抗脂肪肝等作用[3]。
枸杞食用色素是存在于枸杞浆果中的总呈色物质,主要是脂溶性胡萝卜素类化合物,具有天然食用色素的生理和药理活性,枸杞食用色素呈橘红色(略带黄色),可以用做天然着色剂,也可用于食品和化妆品的着色。
目前,国内外对于枸杞色素的提取主要使用石油醚作为提取剂[4-5],而本文选用无水乙醇作为提取剂,用正交设计法提取枸杞红色素的最佳条件,并研究了枸杞色素的稳定性与温度、光照、pH、金属离子等因素的关系,确定枸杞红色素在实际应用和操作中应该注意的事项,为进一步开发枸杞色素的用途提供科学依据。
1 实验1.1 材料与仪器宁夏枸杞干果(市售)。
SPS202F型电子天平;T6型紫外、可见分光光度仪;pHS-25B型酸度计。
1.2 实验方法1.2.1 枸杞色素提取的正交试验枸杞干果粉碎,准确称取2.0 g的枸杞干粉4份,用乙醇溶液浸提。


枸杞及其制品中枸杞红素的测定1范围本方法规定了枸杞红素的测定方法,液相色谱法。
本方法适用于枸杞及其制品中枸杞红素的测定。
2原理枸杞红素为玉米黄素二棕榈酸酯,试样经乙酸乙酯、正己烷、无水乙醇等有机溶剂提取后,定容、离心、过滤,经反向色谱柱分离,外标法定量。
3试剂与材料除非另有说明,本方法所用试剂均为分析纯,水为GB/T 6682规定的一级。
3.1试剂3.1.1甲醇(CH 3OH):色谱纯。
3.1.2二氯甲烷(CH 2C l2):色谱纯。
3.1.3乙腈(CH 3CN):色谱纯。
3.1.4乙酸乙酯(CH 3COOC 2H 5)。
3.1.5无水乙醇(C 2H 6O)。
3.1.6正己烷(C 6H 14)。
3.1.7石英砂:60-80目。
3.2试剂配制3.2.1提取溶剂:正己烷:乙酸乙酯:甲醇=1:1:1(v/v/v )。
3.2.2萃取溶剂:正己烷:无水乙醇=3:1(v/v )。
3.3标准品3.3.1玉米黄素二棕榈酸酯(别名酸浆素C 72H 116O 4,CAS 号:144-67-2):纯度≥95%,或经国家认证并授予标准物质证书的标准物质。
3.4流动相3.4.1流动相A:甲醇:乙腈:水=81:14:5。
3.4.2流动相B:二氯甲烷。
3.5标准溶液配制3.5.1玉米黄素二棕榈酸酯标准储备液(1mg/ml):玉米黄素称取枸杞红素标准品0.005g(精准至0.00001g),溶解于流动相A:流动相B=1:1(v/v)溶液中并定容至5mL。
于-20℃以下避光储存。
3.5.2玉米黄素二棕榈酸酯标准工作液:准确吸取储备液,并用流动相A:流动相B=1:1进行稀释,并定容至10ml刻度线。
制成5ug/ml,10ug/ml,25ug/ml,50ug/ml,100ug/ml,标准工作液,现配现用。
4仪器和设备4.1液相色谱分析仪,配紫外检测器。
4.2离心机;转速≥3000r/min。
4.3分析天平;感量0.0001g和0.00001g5操作方法5.1试样的制备枸杞样品粉碎混匀,使用四分法缩取有代表性的试样,密封避光保存;枸杞提取物样品混合均匀,取有代表性的试样,密封避光保存。



枸杞皮渣中类胡萝卜素的提取及稳定性研究枸杞皮渣中类胡萝卜素的提取及稳定性研究摘要:植物中的类胡萝卜素具有丰富的营养价值和药用功能,而枸杞皮渣是一种丰富的类胡萝卜素来源。
本研究旨在探究在提取枸杞皮渣中类胡萝卜素的最佳工艺,并研究其稳定性,为其应用于食品和药品工业提供科学依据。
通过酶解、溶剂提取和净化析出等步骤,成功提取到了枸杞皮渣中的类胡萝卜素。
同时,通过稳定性研究验证了其适用性。
关键词:枸杞皮渣;类胡萝卜素;提取;稳定性引言类胡萝卜素是一类色素化合物,广泛存在于植物组织中,具有抗氧化、抗肿瘤、抗衰老、保护视力等多种生物活性。
枸杞皮渣是枸杞加工过程中剩余的废弃物,含有丰富的类胡萝卜素,但其利用率却相对较低。
因此,本研究旨在提取枸杞皮渣中的类胡萝卜素,并研究其稳定性,为其在食品和药品工业中的应用提供科学基础。
材料与方法1. 枸杞皮渣的制备:将新鲜枸杞果实收获后,进行果肉与种子的分离,然后将果皮晒干至含水量低于10%,并研磨成粉末。
2. 酶解提取类胡萝卜素:将10g枸杞皮渣粉末加入50mL 0.6% NaOH溶液中,于60°C水浴中酶解2小时,反应结束后通过离心分离上清液。
3. 溶剂提取:将上清液与1:1的醇和石油醚混合,振荡抽提20分钟,再通过离心分离,得到石油醚相。
4. 净化析出:将石油醚相置于旋转蒸发器中,待溶剂大部分挥发后,加入正己烷研磨均匀,形成含有类胡萝卜素的油状物质。
5. 稳定性研究:将提取出的类胡萝卜素溶于不同溶剂(如甲醇、乙醇、二甲基亚砜等),在不同温度和时间下进行测定。
结果与讨论经过酶解和溶剂提取的提取液中成功检测到了类胡萝卜素的吸收峰,且其浓度与提取液中的类胡萝卜素含量呈正相关关系。
通过净化析出,获得了高纯度的类胡萝卜素油状物质。
稳定性研究结果显示,在室温下保存72小时内,类胡萝卜素的含量基本保持稳定,但随着时间和温度的增加,其含量逐渐下降。
结论本研究成功提取了枸杞皮渣中的类胡萝卜素,并通过稳定性研究验证了其适用性。

枸杞色素的提取工艺研究[摘要] 利用有机溶剂浸提枸杞中的色素,通过正交设计试验确定了提取枸杞色素的最佳工艺条件。
结果表明,枸杞色素提取的最佳工艺条件为温度60℃,时间60min,料液比1:6。
该条件下浸提率为95.7%,提取效果较好。
[关键词] 枸杞子;色素;提取工艺食用天然色素不仅没有毒性,有的还有一定的营养,甚至一定的药理作用。
目前人们使用的食用色素有天然食用色素和合成食用色素两大类。
天然色素来自天然产物,主要由植物组织中提取,也包括来自动物和微生物的一些色素。
枸杞为茄科枸杞属植物的果实,它在祖国的传统医学中具有重要的地位,其药用价值备受历代医家的推崇[1]。
本文采用正交试验设计,选择枸杞色素提取的优化工艺,旨在为枸杞色素的提取及开发提供参考。
一、材料与方法1.材料枸杞果实为晒干的宁夏枸杞。
取成熟、无虫害的果实放在通风处凉干,去核取皮,粉碎,80目筛过筛获得枸杞细粉。
2.仪器与设备仪器:uv-2000紫外可见分光光度计(莱伯泰科有限公司);dhg-9140a电热恒温鼓风干燥箱(上海一恒科技有限公司);恒温水浴锅。
试剂:甲醇、95%乙醇、正丁醇和乙酸乙酯均为分析纯,水为二次水。
3.试验方法(1)色素测定方法将约0.2g枸杞粉末用95%的乙醇溶解,在50℃下恒温水浴,浸提3次,过滤,合并滤液,用95%乙醇定容至50ml容量瓶中。
用95%的乙醇作对照,在紫外分光光度计上从波长200nm开始至380nm,每递增2nm测其吸光度,以波长为横坐标,以吸光度为纵坐标绘制曲线,确定枸杞色素最大吸收波长。
(2)浸提率的计算称取约1g枸杞用95%的乙醇充分浸提,至提取液无色为止,合并滤液,量其体积,吸取提取液用相应的溶剂稀释,在最大吸收波长下测吸光度值。
把此测定值作为完全提取的测量值,其他条件下的测定值与之相比,得到该条件下的浸提率。
(3)提取溶剂的选择[3]分别称取约0.5g干燥枸杞粉末4份于100ml的提取瓶中,分别加入甲醇、95%乙醇、正丁醇、乙酸乙酯各20ml。

枸杞天然色素的提取与检测一、实验目的及意义本实验只对药用栽培植物枸杞类胡萝卜素进行提取。
枸杞中含有很多对人体有益的天然色素。
如核黄素、番茄红素、玉米黄色素、胡萝卜素等。
尤其是β-胡萝卜素,β-胡萝卜素是维生素A的前体物质,用于治疗因缺乏维生素A引起的各种疾病。
国家已将其归类为营养强化剂,可防止人体维生素缺乏症【1,2】。
枸杞色素是存在于枸杞浆果中各种呈色物质的总称,主要是由类胡萝卜素和其他一些有色物质组成。
枸杞色素是枸杞的主要功能因子之一,对枸杞色素的提取、特性及功能的研究是枸杞深加工的重要课题【2-4】。
类胡萝卜素可以降低发生癌症的危险,其中对β-胡萝卜素的研究一直是人们研究的焦点【5】,大量的流行病学研究显示摄入相对较多富含类胡萝h素食物的个体,其肺癌发生危险度较低【6】。
二、色素结构特征和性质类胡萝卜素,主要结构是共轭多烯烃,两头或一头环构化,有多种同分异构体及其衍生物,类胡萝卜素分子中含有四个异戊二烯单位,中间两个尾尾相连,两端的两个首尾相连,形成一个链状的共轭结构,链的两端可连接不同的基团。
类胡萝卜素是脂溶性色素,属于色烯类色素。
易溶于石油醚,难于甲醇和乙醇,不溶于水,以β-胡萝卜素为代表【2】。
类胡萝卜素的双键结构使得它们具有高度的不稳定性:对光、氧、热和活性界面特别敏感,酸性或碱性条件下对某些类胡萝h素也会有影响【7】刘咏、罗建平在90℃下采用85%乙醇提取枸杞色素,该色素为水溶性色素,耐光性、耐高温性好,在酸性介质、还原剂以及常用食品添加剂等条件下有较好的稳定性【8】。
三、试验材料枸杞四、试验试剂石油醚、丙酮、无水硫酸钠、乙酸乙酯、甲醇、氢氧化钠、无水乙醚五、仪器与设备电子天平、恒温水浴锅、可见分光光度计、电热烘干箱、高效液相色谱仪六、实验方法和步骤1)最佳浸提条件的确定张延明等从生产实际和成本考虑,最终确定枸杞类胡萝卜素的提取条件为:浸提温度45οC、料液比l:40、浸提时间120min、浸提次数3次。
![枸杞子中酸浆果红素的鉴定及其稳定性研究[1]](https://uimg.taocdn.com/9371e2056c85ec3a87c2c54c.webp)
韩山师范学院生物技术专业实验论文枸杞红色素的提取及性质鉴定指导老师:杨永利职称:教授答辩组成员莫东宗 2011235110巫季俞 2011235117何青枚 2011235118吴瑾 2011235127张培杰 2011235118肖漫萍 2011235132张文浩 2011235144完成时间:2012年6月5日星期二摘要:本实验通过改变单一变量确定了枸杞红色的最佳提取条件,并分析了枸杞红色素的稳定性。
结果表明最佳提取条件为40℃下采用无水乙醇浸取,料液比为1:10,提取时间为2.5h ;关键词:枸杞红色素 提取 性质鉴定前言:枸杞红色素是存在于枸杞浆果中各种呈色物质的总称,现代药物学研究表明,枸杞红色素是枸杞中的重要生物活性成份之一,主要包括类胡萝素和少量叶黄素及其它有色物质。
枸杞子色素为暗红色,略带黄色的粉末状或极易松散的块状,稍有正常的枸杞味。
乙醚提取液为黄色,水(PH>7)或乙醇的提取液则黄中透红。
易溶于乙醚,溶于碱性水溶液、乙醇、不溶于丙酮、酸性水溶液。
低于45℃时色素稳定,高于70℃时色素极为不稳定。
色素对光敏感。
枸杞色素本身安全无毒,安全性能好,可用于维生素A 的前体、预防癌症、通过抗氧化作用以减少自由基对细胞遗传物质和细胞膜的损伤、提高免疫力及减弱放疗和化疗对机体的毒副作用。
1. 材料与试剂1.1实验材料:市售枸杞1.2实验试剂:0.1mol/L 氢氧化钠溶液;85%乙醇;5%盐酸;5%氢氧化钠;甲醇;无水乙醇;乙醚;0.1mol/L 碳酸钠;0.1mol/L 碳酸氢钠;丙酮、乙酸乙酯、三氯甲烷、石油醚、蒸馏水1.3实验仪器:干燥箱;电热恒温水浴锅;722分光光度计;粉碎机2.实验方法2.1最佳提取剂的确定称取0.5g 枸杞粉末,分别用无水乙醇、丙酮、乙酸乙酯、三氯甲烷、石油醚、蒸馏水各50ml 浸提2h ,抽滤,取1ml 滤液稀释至10ml ,在350~600nm 波长段扫描,测定其吸光度,记录曲线,进行对比,选取最佳提取溶剂。
枸杞子黄色素的提取及其性质的研究枸杞子是一种珍贵的药材,具有抗衰老、抗氧化、增进免疫力、抗疲劳和抗病毒等多种功效。
其中,枸杞子黄色素是对枸杞子的研究热点,它也是枸杞子的重要成分。
它是一类具有生物活性的芳香族多肽,能够起到抗氧化、调节免疫、保护心脑血管及抗炎等功效。
研究表明,枸杞子黄色素是丰富的天然资源,它们能够活化机体,促进机体健康。
枸杞子黄色素的化学结构是羟氨基苯甲酰对苯二酰亚胺(HAPA)。
枸杞子黄色素的生物活性主要体现在其特殊的放射性氢排斥现象,以及它的单肽键结热力学稳定性和较强的抗氧化能力上,可以防止脂质的氧化。
此外,枸杞子黄色素的稳定性也非常强,它不易被溶解,即使暴露在空气中也不会显著降解。
枸杞子黄色素的提取是枸杞子应用及研究的一个重要环节。
传统提取技术包括浓缩、离子交换、溶剂萃取等,其中浓缩是目前枸杞子黄色素提取方法中最简单、最实用的,也是最常用的方法,它可以有效提高提取率。
溶剂萃取法利用不同溶剂对枸杞子黄色素的溶解性差异,将枸杞子黄色素从枸杞子中萃取出来,提高枸杞子黄色素的提取率。
枸杞子黄色素的性质研究是分析枸杞子黄色素的功能及其在抗氧化方面的作用等重要研究内容。
据研究,枸杞子黄色素能够抑制自由基的形成,降低脂质的氧化,减少细胞损害;此外,它还能通过促进神经鞘脂的合成和细胞活性,加强机体的抗氧化能力及抗疾病能力,促进机体的健康状态。
在实际应用中,枸杞子黄色素可用于抗衰老、抗氧化、增进免疫力、抗疲劳和抗病毒等药物的研究。
例如,研究人员已经研制出了一种新型的抗衰老药,它是通过提高枸杞子黄色素的含量来抑制自由基的形成,从而达到延缓衰老的目的。
此外,枸杞子黄色素还用于抗病毒药物的研发,它可以促进机体免疫力,预防病毒感染。
总之,枸杞子黄色素的提取及其性质的研究具有重要的理论和实践意义。
通过完善枸杞子黄色素的提取工艺,对在药物中进行有效应用,有助于开发出更有效、安全和绿色的新型药物。
同时,还要进一步研究枸杞子黄色素的性质和功效,以促进枸杞子和枸杞子中的其他成分在药学、医学和保健领域的应用及研究。
第38卷第8期西南师范大学学报(自然科学版)2013年8月V o l.38N o.8J o u r n a l o f S o u t h w e s t C h i n aN o r m a lU n i v e r s i t y(N a t u r a l S c i e n c eE d i t i o n)A u g.2013文章编号:10005471(2013)08010806响应面优化枸杞色素提取工艺及稳定性研究①王孝荣,罗佳丽,潘年龙,王雪莹,蒋和体西南大学食品科学学院,重庆400716摘要:以宁夏枸杞为原料,通过B o x-B e h n k e n试验设计研究提取时间㊁料液比及浸提温度对枸杞素浸提效果的影响,建立各影响因素的回归方程,并通过响应面分析法优化,得到了枸杞色素的最佳浸提条件:料液比为1ʒ9㊁温度为38ħ㊁时间为2.5h.进一步研究光照㊁温度㊁酸㊁碱㊁金属离子对枸杞色素稳定性的影响.结果表明:对日光不稳定,避光保存较稳定;在高温下不稳定;在碱性环境中较稳定;对金属离子如F e3+,F e2+,C u2+等不稳定,而K+,N a+对其影响较小.关键词:枸杞色素;响应面法;提取;稳定性中图分类号:T S255.1文献标志码:A枸杞(W o l f b e r r y F r u i t),属茄科,是我国药食兼用性的植物之一[1],具有滋肝补肾㊁润肺明目等功效[2].相关研究表明,枸杞色素是存在于枸杞浆果中各种呈色物质的总称,主要由类胡萝卜素组成[3-4].类胡萝卜素是国际公认的具有生理活性的功能性抗氧化剂,单线态氧的有效淬灭剂,能清除羟基自由基,在细胞中与细胞膜中的脂类相结合,有效抑制脂类氧化[5-6],而且在抗癌㊁抑制心脏病的发生等方面也有一定功能价值[7-9].同时,枸杞色素不仅是安全的天然着色剂,而且还是食品的营养强化剂[10-11].目前,从枸杞中提取色素方法有热水提取法㊁醇提法㊁有机溶剂萃取法㊁超声法等[12-14],但应用响应面法优化枸杞色素提取方面还鲜见报道.本实验不仅使用响应面法对枸杞色素浸提条件进行全面的优化,而且还研究了光㊁热㊁酸㊁碱㊁金属离子等因素对枸杞色素稳定性的影响,以期对枸杞中浸提枸杞色素的生产工艺㊁选择适宜的贮藏条件等提供理论依据和参考.1材料与方法1.1材料与试剂枸杞,产地宁夏,实验室冷藏.无水乙醇㊁丙酮㊁石油醚㊁乙醚㊁乙酸乙酯㊁氯化钠㊁氯化铝㊁氯化钾㊁氯化锌㊁氯化铜㊁氯化铁㊁氯化亚铁㊁氯化钙(均为分析纯).1.2仪器与设备U V-2450紫外可见分光光度计:苏州普今生物科技有限公司;R E-52A旋转蒸发仪:上海亚荣生化仪器厂;F A2004A电子天平:上海精天电子仪器厂;D Z F-6020真空干燥箱:上海精宏实验设备有限公司;H R2027粉碎机:飞利浦电子香港有限公司.1.3方法①收稿日期:20110607Copyright©博看网. All Rights Reserved.作者简介:王孝荣(1987),男,重庆人,硕士研究生,主要从事现代食品加工理论与技术方面的研究.通信作者:蒋和体,教授,博士.1.3.1 枸杞色素浸提工艺流程枸杞ң粉碎后过40目筛ң枸杞粉ң浸提ң抽滤ң上清液ң真空浓缩ң真空干燥(40ħ)ң枸杞色素成品.1.3.2 枸杞色素最大吸收波长的测定称取枸杞色素干粉2m g ,乙醚为溶剂,溶解并定容至25m L ,以乙醚为空白对照,用紫外可见分光光度计400~500n m 全波段内扫描,观测其最大吸收峰.1.3.3 浸提溶剂的选择准确称取6份枸杞干粉1.0000g ,取无水乙醇㊁乙醚㊁丙酮㊁乙酸乙酯ʒ乙醚(V /V=1/1)㊁石油醚㊁乙酸乙酯各10m L ,在30ħ下浸提2.5h 后抽滤,以相应浸提剂为参比,在最大吸收波长下测吸光度.1.3.4 浸提液配比的选择准确称取5份枸杞干粉1.0000g ,乙酸乙酯:乙醚混合液的配比分别为1ʒ9,2ʒ8,3ʒ7,4ʒ6,5ʒ5,总体积为10m L ,在30ħ下浸提2.5h 后抽滤,在最大吸收波长测吸光度.1.3.5 单因素浸提条件的选择准确称取枸杞干粉1.0000g ,以乙酸乙酯ʒ乙醚(V /V =2ʒ8)为浸提液10m L ,在10,20,30,35,40,45ħ下浸提2.5h 后抽滤,在最大吸收波长测吸光度.准确称取枸杞干粉1.0000g ,以乙酸乙酯ʒ乙醚(V /V =2ʒ8)为浸提液10m L ,在30ħ条件下浸提0.5,1,2,2.5,3,3.5h 后抽滤,在最大吸收波长测吸光度.准确称取枸杞干粉1.0000g ,取4,6,8,10,12m L 的乙酸乙酯ʒ乙醚(V /V =2ʒ8)为浸提液,在30ħ条件下浸提2.5h 后抽滤,在最大吸收波长测吸光度.1.3.6 枸杞色素提取响应面法优化分析[15]本试验采用D e s i g n -E x p e r t 软件,利用中心组合试验设计原理设计响应面试验.根据单因素试验结果,选取提取温度㊁提取时间及液料比3个因素作为试验因素,以枸杞色素吸光度为响应值设计试验,试验因素及水平见表1.表1 响应面试验因素与水平因 素水 平液料比/(m L ㊃g-1)8910时间/h22.53温度/ħ3035401.3.7 枸杞色素的稳定性取枸杞色素1g ,乙醚溶解并定容至250m L .将枸杞色素溶液分别置于日光㊁室内光和避光条件下保存1,3,6,8,10h ;置于25,40,55,70,85ħ下保存1,2,3,4h ;分别配制0.2%,0.4%的H C l 和N a O H 溶液,以1%的添加量添加到枸杞色素溶液中,室温避光保存1,2,3,4,5h ;在枸杞色素溶液中以0.01m o l /L的添加量分别加入A l 3+,K +,Z n 2+,F e 3+,F e 2+,C u 2+,C a 2+,N a +,室温避光保存5,10,15,20h .以相应不加枸杞色素的溶液为空白对照,测定吸光度的变化情况,计算保存率[16].色素保存率(%)=(测定吸光值/初始吸光值)ˑ100%2 结果与分析2.1 枸杞色素最大吸收波长由图1可知,枸杞色素提取液的紫外可见光谱为类胡萝卜素的特征吸收,主峰在450n m 有最大吸收峰,两个肩峰在425和476显示出类胡萝卜素的特征吸收.2.2 不同溶剂的浸提效果由表2可知,乙酸乙酯与乙醚混合溶剂浸提的效果优于其它溶剂,乙醚㊁石油醚浸提效果次之.这与理论上枸杞色素中包括非极性的胡萝卜素和极性较大的叶黄素有关,用单一溶剂浸提效果不理想,故选择乙酸乙酯与乙醚的混合液浸提枸杞色素.表2 不同溶剂的浸提效果211西南师范大学学报(自然科学版) h t t p ://x b b jb .s w u .c n 第38卷Copyright ©博看网. All Rights Reserved.图1 最大吸收波长的测定溶剂无水乙醇乙醚丙酮乙酸乙酯ʒ乙醚石油醚乙酸乙酯吸光度/A1.3711.9031.7421.9131.8961.8442.3 浸提液配比的浸提效果由表3可知,乙酸乙酯ʒ乙醚配比2ʒ8时,对色素的浸提效果最佳.配比小于2ʒ8时,溶剂极性较小,反之极性较大.枸杞中胡萝卜素的含量多,乙醚对该色素提取效果较好,增大乙醚含量有利于胡萝卜素的溶出,但枸杞色素中还含有叶黄素,乙酸乙酯对其浸提效果较好,故确定乙酸乙酯与乙醚配比为2ʒ8.表3 浸提液配比的浸提效果1ʒ92ʒ83ʒ74ʒ65ʒ51.9201.9291.9191.9121.909图2 温度对浸提效果的影响2.4 单因素实验结果2.4.1 温度对浸提效果的影响由图2可知,随着浸提温度的升高,溶剂的渗透性增强,有利于枸杞色素的溶出,但浸提温度由30ħ升高至45ħ,色素浸出液的吸光度(色素浸出率)增加缓慢,同时较高温度不利于枸杞色素的稳定性,故选择30~40ħ作为浸提温度.2.4.2 时间对浸提效果的影响由图3可知,随着浸提时间的延长,浸出液中色素含量随浸提时间延长而增加,但浸提时间在2h 之后色素浸出液的吸光度增加缓慢,同时为了避免长时间加热对色素的破坏,故浸提时间控制在2~3h 内为宜.2.4.3 料液比对浸提效果的影响由图4可知,随着料液比的增大,色素浸出液的吸光度也会随之增加,在1ʒ8之后逐渐趋于平衡状态.主要是原因当料液比达1ʒ8时,溶剂对枸杞色素的溶解基本上达到饱和,继续增加溶剂用量不能显著提高枸杞色素含量,从经济角度考虑,选择料液比在1ʒ8~1ʒ10之间为宜.图3时间对浸提效果的影响图4 料液比对浸提效果的影响2.5 响应面分析2.5.1 响应面分析优化试验设计及方差分析根据B o x -b e h n k e n 的中心组合试验设计原理,在单因素实验结果的基础上,进行响应面分析试验,试验设计与试验结果见表4.从表5可知,以吸光度为响应值时,模型P <0.0001,表明该二次方程模型显著.同时失拟项P =0.0513>0.05,失拟项不显著,表示单因素试验结果可以和数学模型拟合良好,即可以使用数学模型推测311第8期 王孝荣,等:响应面优化枸杞色素提取工艺及稳定性研究Copyright ©博看网. All Rights Reserved.试验结果.回归系数显著性检验表明,在所各取的因素水平范围内,对枸杞色素浸提效果的影响排序依次为温度㊁时间和料液比.表4 响应面分析方案与试验结果实验号因 素液料比X 1时间X 2/h 温度X 3/ħ吸光度/A 192.5351.904293.0301.6223102.5401.942482.5301.691583.0351.795692.0301.5357103.0351.818892.5351.889992.5351.9041092.5351.90711102.0351.7561282.5401.84513102.5301.6051492.5351.9351593.0401.8611682.0351.6091792.0401.829表5 方差分析表项目平方和自由度均方F 值P 值显著性模型0.27090.03031.73<0.0001**X 14.095ˑ10-314.095ˑ10-34.350.0753X 20.01710.01717.900.0039*X 30.13010.130139.36<0.0001**X 1X 23.844ˑ10-313.844ˑ10-34.090.0829X 1X 38.372ˑ10-318.372ˑ10-38.900.0204*X 2X 37.563ˑ10-317.563ˑ10-30.800.3997X 120.01110.01112.180.0101*X 220.05210.05255.310.0008**X 320.03010.03032.270.0513**失拟项5.461ˑ10-335.461ˑ10-36.480.0513注:*.差异显著,P <0.05;**.差异极显著,P <0.01.2.5.2 拟合模型的建立利用D e s i g n -E x p e r t 软件对表数据进行整理分析,确立如下回归预测模型:Y (A )=-9.57820+0.79607X 1+3.06525X 2+0.19472X 3-0.062000X 1X 2+9.15000ˑ10-3X 1X 3-5.50000ˑ10-3X 2X 3-0.052150X 12-0.44460X 22-3.39600ˑ10-3X 322.5.3 响应面分析从图5可以看出,温度对枸杞色素浸提的影响最大,浸提温度与料液比之间的交互作用对枸杞色素浸提有显著影响.通过软件分析,得到枸杞色素的最佳提取条件为温度37.86ħ㊁提取时间2.58h ㊁液料比8.91m L /g,在此条件下吸光度预测为1.952A b s .对响应面分析法优化的提取工艺条件进行适当调整:温度38ħ㊁提取时间2.5h ㊁液料比9m L /g,在411西南师范大学学报(自然科学版) h t t p ://x b b jb .s w u .c n 第38卷Copyright ©博看网. All Rights Reserved.此条件下进行3次验证实验,其浸提液吸光度平均值为1.947A b s,响应面的实验值与回归方程预测值吻合良好.图5 因素间交互作用对枸杞色素浸提效果的影响2.6 枸杞色素的稳定性2.6.1 光照及温度对枸杞色素稳定性的影响由图6可知,日光对枸杞色素有明显的破坏作用,而室内光及避光保存对枸杞色素的影响相对较小,原因可能是光照加速了枸杞色素的氧化,生产环氧化物,所以应尽量避光保存.由图7可知,温度在50ħ内枸杞色素较稳定,但随着温度的升高,其保存率降低.可能的原因是高温使枸杞色素降解速度加快,而且由于加热时间较长,色素结构被破坏,吸光度下降.图6 光照对枸杞色素稳定性的影响图7 温度对枸杞色素稳定性的影响2.6.2 酸㊁碱对枸杞色素稳定性的影响由图8可知,在酸性环境下,室温避光保存5h 后保存率大幅下降,并随H C l 浓度的增大而降低.在碱性环境下,保存率降幅不大,说明碱性环境对枸杞色素的稳定性影响相对较小.2.6.3 金属离子对枸杞色素稳定性的影响由图9可知,F e 3+对枸杞色素的破坏作用最强,F e 2+,C u 2+其次;Z n 2+,A l 3+,C a 2+对枸杞色素也有影响;K +,N a+对枸杞色素的影响不大,可能的原因是一些金属离子起到催化剂作用,加速枸杞色素的降解.所以应避免枸杞色素直接与重金属如常见的铁器㊁铜器等接触.图8 酸㊁碱对枸杞色素稳定性的影响图9 金属离子对枸杞色素稳定性的影响511第8期 王孝荣,等:响应面优化枸杞色素提取工艺及稳定性研究Copyright ©博看网. All Rights Reserved.3 结 论本研究在单因素试验结果的基础上,通过响应面法优化,得到了枸杞色素的最佳浸提工艺条件为:温度38ħ㊁提取时间2.5h ㊁液料比9m L /g.对枸杞色素的稳定性研究表明:对日光不稳定,避光保存较稳定;在高温下不稳定;在碱性环境中较稳定;对金属离子如F e 3+,F e 2+,C u 2+等不稳定,而K +,N a+对其影响较小.参考文献:[1]苏宇静,贺海明,孙兆军.中国枸杞资源及其在食品工业中的应用现状和开发前景[J ].食品科学,2002,23(8):292-294.[2] 钱彦丛,宇文萍.枸杞子的化学成分及药理研究新进展[J ].中医药学报,2000(4):33-35.[3] 彭光华,李 忠,张声华.薄层色谱法分离鉴定枸杞子中的类胡萝卜素[J ].营养学报,1998,20(1):76-78.[4] 何 进,阎淳泰,梁运祥.枸杞果实化学成分研究概况[J ].中国野生植物资源,1997(1):8-11.[5] J A S W I R I ,K O B A Y A S H IM ,K O Y AMAT ,e t a l .A n t i o x i d a n t B e h a v i o u r o f C a r o t e n o i d sH i g h l y A c c u m u l a t e d i nH e pG 2C e l l s [J ].F o o dC h e m i s t r y,2012,132(2):865-872.[6] 赵 萍,吴灿军,赵 瑛,等.枸杞色素总抗氧化能力的研究[J ].食品与发酵工业,2012,36(3):60-64.[7] Z HA N G X ,Z HA O W ,HUL ,e t a l .C a r o t e n o i d s I n h i b i t P r o l i f e r a t i o n a n dR e g u l a t eE x p r e s s i o n o f P e r o x i s o m eP r o l i f e r a -t o r s -A c t i v a t e dR e c e p t o rG a mm a (P P A R γ)i nK 562C a n c e rC e l l s [J ].A r c h i v e so fB i o c h e m i s t r y a n dB i o p h y s i c s ,2011,512(1):96-106.[8] S A T OM IY ,N I S H I N O H.I m p l i c a t i o n o fM i t o g e n -A c t i v a t e dP r o t e i nK i n a s e i n t h e I n d u c t i o n o fG 1C e l l C y c l eA r r e s t a n d G a d d 45E x p r e s s i o nB y t h eC a r o t e n o i dF u c o x a n t h i n i n H u m a nC a n c e rC e l l s [J ].B i o c h i m i c ae tB i o p h y s i c aA c t a -G e n e r a l S u b j e c t s ,2009,1790(4):260-266.[9] P A L A C E VP ,K HA P E RN ,Q I N Q ,e t a l .A n t i o x i d a n t P o t e n t i a l s o fV i t a m i nAa n dC a r o t e n o i d s a n dT h e i rR e l e v a n c e t oH e a r tD i s e a s e [J ].F r e eR a d i c a l B i o l o g y a n d M e d i c i n e ,1999,26(5-6):746-761.[10]S A N T I P A N I C HWO N G R ,S U P HA N T HA R I K A M.C a r o t e n o i d sa sC o l o r a n t s i nR e d u c e d -F a tM a y o n n a i s eC o n t a i n i n g S p e n tB r e w e r sY e a s t β-G l u c a na s aF a tR e p l a c e r [J ].F o o dH y d r o c o l l o i d s ,2007,21(4):565-574.[11]V A I S MA N N ,HA E N E N G R M ,Z A R U K Y ,e t a l .E n t e r a l F e e d i n g En r i c h e dw i t hC a r o t e n o i d sN o r m a l i z e s t h e C a r o t e n o i d S t a t u s a n dR e d u c e sO x i d a t i v e S t r e s s i nL o n g -T e r m E n t e r a l l y F e dP a t i e n t s [J ].C l i n i c a lN u t r i t i o n ,2006,25(6):897-905.[12]吴灿军,赵 萍,王 雅.天然色素及枸杞色素的提取和抗氧化作用的研究进展[J ].陕西农业科学,2012(1):103-107.[13]孙 奎.柴达木盆地黑果枸杞色素最佳提取工艺研究[J ].湖北农业科学,2011,50(11):2318-2320.[14]史高峰,李 娜,陈学福.枸杞中色素的超声辅助提取工艺研究[J ].食品工业科技,2010,31(10):276-279.[15]赵 翾,李红良,张惠妹.响应面法优化火麻仁黄酮提取工艺[J ].食品科学,2011,32(2):127-131.[16]邱伟芬,汪海峰.天然番茄红素在不同环境条件下的稳定性研究[J ].食品科学,2004,25(2):56-60.O nO p t i m i z a t i o no fE x t r a c t i o no fP i g m e n tU s i n g R e s po n s e S u r f a c e M e t h o d a n dS t a b i l i t y o fP i g m e n t i n W o l f b e r r y Fr u i t s WA N G X i a o -r o n g , L U OJ i a -l i ,P A N N i a n -l o n g , WA N G X u e -y i n g , J I A N G H e -t i C o l l e g eo f F o o dS c i e n c e ,S o u t h w e s t U n i v e r s i t y ,C h o n g q i n g 400716,C h i n a A b s t r a c t :T h e c o n d i t i o n s e x t r a c t i o n t i m e ,r a t i o so f l i q u i d t os o l i da n d t e m p e r a t u r eh a v eb e e n i n v e s t i ga t e d t ou n d e r s t a n d t h e i r e f f e c t s o n t h e p i g m e n t e x t r a c t i o n i nw o l fb e r r y f r u i t f r o m N i n g x i a .B o x -B e h n k e nm a t r i x d e s i g nh a sb e e nu s e d t oe s t a b l i s ha q u a d r a t ic r e g r e s s i o n m ode l ,a n dr e s p o n s es u rf a c ea n a l ys i s c a r r i e do u t f o r o p t i m i z a t i o n p u r p o s e .T h eo pt i m u me x t r a c t i o nc o n d i t i o n sh a v eb e e nd e t e r m i n e da s f o l l o w s :r a t i o so f l i q u i d t o s o l i d i s1ʒ9;t e m p e r a t u r e ,38ħ;a n de x t r a c t i o nt i m e ,2.5h .T h es t a b i l i t y o f p i gm e n t f r o m w o l f b e r r y f r u i t sh a s b e e n s t u d i e d i n t h i s r e s e a r c h .T h e r e s u l t s s h o wt h a t h i g h t e m p e r a t u r e a f f e c t s t h e s t a -b i l i t y o f p i g m e n t .I na d d i t i o n ,t h e y a r e s e n s i t i v e t o s u n l i gh t .H o w e v e r ,i t i s n o t s o s e n s i t i v e t od a r k n e s s .P i g m e n t a r em o r e s t a b l e i na l k a l i n e c o n d i t i o nc o m p a r e d t oa c i dc o n d i t i o n ;T h e s t a b i l i t y o f p i g m e n t i s r e -611西南师范大学学报(自然科学版) h t t p ://x b b jb .s w u .c n 第38卷Copyright ©博看网. All Rights Reserved.d u ce dw h e nF e 3+,F e 2+,C u 2+,i s r e s p e c t i v e l y ad de dt o i t sm e d i u m w h e r e a so t h e rm e t a l i o n sK +,N a +h a v en o s u c he f f e c t o n t h e i r s t a b i l i t y.K e y wo r d s :W o l f b e r r y C o l o r ;r e s p o n s e s u r f a c e a n a l y s i s ;e x t r a c t i o n ;s t a b i l i t y 责任编辑 汤振金711第8期 王孝荣,等:响应面优化枸杞色素提取工艺及稳定性研究Copyright ©博看网. All Rights Reserved.。
包装与食品机械2000年第18卷第2期摘要:应用超临界CO2萃取分离技术,以枸杞油作为载体,从枸杞色素中分离萃取β-胡萝卜素,对其理化指标进行了检测分析,为从枸杞色素中提取β-胡萝卜素作为制药原料奠定基础。
关键词:超临界CO2萃取枸杞油载体枸杞色素β-胡萝卜素中图分类号:T S22414文献标识码:A文章编号:1005-1295(2000)02-0018-04Su p ercritical CO2Extraction ofβ-carotene from L y cium Pi g ment Abstract:β-carotene is isolated from l y cium p i g m ent b y su p ercritical CO2extraction usin g l y cium oil as the carrier and the p h y sicochem ical p ro p erties are tested,thus la y in g a foundation for extraction ofβ-carotene from l y cium p i g2 m ent.β-carotene is a raw m aterial for p harm ac y.K e y w ords:su p ercritical extraction;carrier l y cium oil;l y cium p i g m ent;β-carotene.1前言现代药理学研究一般认为宁夏枸杞中的生物活性成分可归纳三个主要方面:①枸杞色素中丰富的类胡萝卜素(Carotehoids);②甜菜碱(Betaine),在生物体内起甲基供应体的作用,能促进脂质代谢,具有抗脂肪肝的作用。
③枸杞多糖( L y cium Barbaram P ol y saccharides,LBP),是一种非特异性的免疫增强剂,能提高机体免疫功能,增强抗病能力,从而达到抗衰老、抗癌、抗放射线、抗肝炎以及抗爱滋病等作用。
枸杞子中红色素的提取及稳定性
伍明;王杰;等
【期刊名称】《中国食品添加剂》
【年(卷),期】1997(000)001
【摘要】本文对比了枸杞子中提取红色素的回流法,索氏提取法和液泛提取法,
并研究了红色素的稳定性。
试验结果表明,液泛提取法优于其他两法。
红色素耐热,酸和碱,并在铜,钙离子存在下稳定。
故此技术将会得到广泛应用。
【总页数】3页(P12-14)
【作者】伍明;王杰;等
【作者单位】中南民族学院化学系,武汉430074;浙江大学化工系
【正文语种】中文
【中图分类】TQ611
【相关文献】
1.枸杞子中食用红色素的提取及稳定性研究 [J], 刘咏;罗建平
2.球面对称设计法研究纤维素酶对枸杞子中枸杞总糖提取率的影响 [J], 徐艳;原振江
3.枸杞子中红色素的提取及稳定性 [J], 伍明;王杰
4.一株黑枸杞内生真菌红色素提取工艺及其稳定性分析 [J], 韦冠宇;杨小朵;李松澄;郑敬晖;蓝秋菊;刘俊林
5.枸杞红色素的提取及稳定性的探讨 [J], 惠贤民
因版权原因,仅展示原文概要,查看原文内容请购买。