06第六章 空气动力计算-2010年
- 格式:ppt
- 大小:2.20 MB
- 文档页数:66
车辆空气动力学与车身造型空气动力学(Aerodynamics)是研究物体在与周围空气作相对运动时两者之间相互作用力的关系及运动规律的科学,它属于流体力学的一个重要分支。
长期以来,空气动力学成果的应用多侧重于航空及气象领域,特别是在航空领域内这门科学取得了巨大的进展,给汽车或路面车辆的空气动力学(Automotive Aerodynamics-Road Vehicle Aerodynamics)研究提供了借鉴。
然而进一步的深入研究表明,汽车或车辆的空气动力学问题从理论到实际两方面都与航空等问题有本质的区别,汽车空气动力学已逐步发展成为了空气动力学的一个独立分支,在方程式赛车领域更是得到了极大的应用。
下面就谈谈赛车中空气动力学的应用。
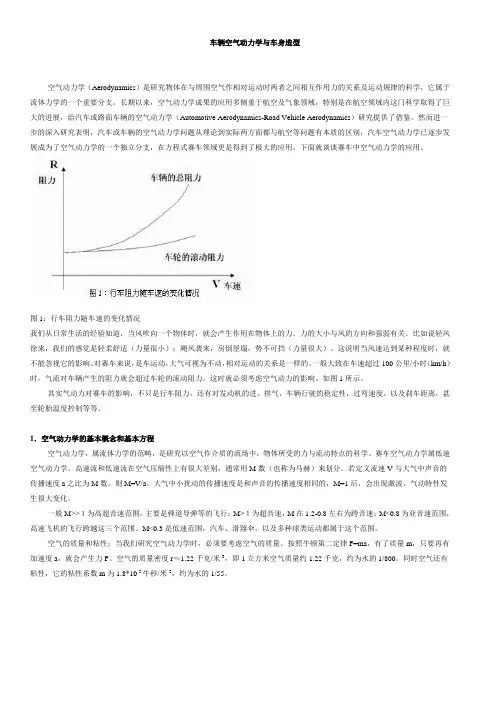
图1:行车阻力随车速的变化情况我们从日常生活的经验知道,当风吹向一个物体时,就会产生作用在物体上的力。
力的大小与风的方向和强弱有关。
比如说轻风徐来,我们的感觉是轻柔舒适(力量很小);飓风袭来,房倒屋塌,势不可挡(力量很大)。
这说明当风速达到某种程度时,就不能忽视它的影响。
对赛车来说,是车运动,大气可视为不动,相对运动的关系是一样的。
一般大致在车速超过100公里/小时(km/h)时,气流对车辆产生的阻力就会超过车轮的滚动阻力。
这时就必须考虑空气动力的影响。
如图1所示。
其实气动力对赛车的影响,不只是行车阻力,还有对发动机的进、排气,车辆行驶的稳定性,过弯速度,以及刹车距离,甚至轮胎温度控制等等。
1.空气动力学的基本概念和基本方程空气动力学,属流体力学的范畴,是研究以空气作介质的流场中,物体所受的力与流动特点的科学。
赛车空气动力学属低速空气动力学。
高速流和低速流在空气压缩性上有很大差别,通常用M数(也称为马赫)来划分。
若定义流速V与大气中声音的传播速度a之比为M数,则M=V/a。
大气中小扰动的传播速度是和声音的传播速度相同的,M=1后,会出现激波,气动特性发生很大变化。
一般M>>1为高超音速范围,主要是弹道导弹等的飞行;M>1为超音速,M在1.2-0.8左右为跨音速;M<0.8为亚音速范围,高速飞机的飞行跨越这三个范围。
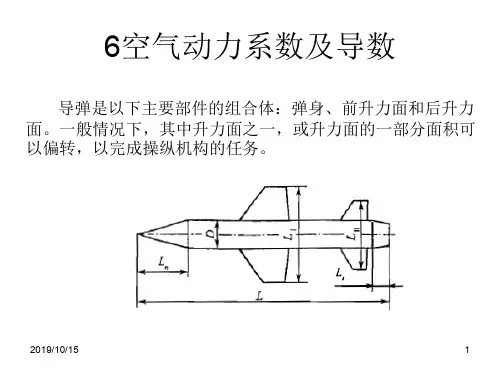





空气动力学基础前六章总结第一章空气动力学一些引述1、空气动力学涉及到的物理量的定义及相应的单位①压强:是作用在单位面积上的正压力,该力是由于气体分子在单位时间内对面发生冲击(或穿过该面)而发生的动量变化,具有点属性。
p = lim i dF ,dAr 0IdA丿单位:Pa, kPa, MPa 一个标准大气压:101kPa②密度:定义为单位体积内的质量,具有点属性。
— lim dm,dv > 0dv单位:kg/tf 空气密度:1.225Kg/卅③温度:反应平均分子动能,在高速空气动力学中有重要作用。
单位:C④流速:当一个非常小的流体微元通过空间某任意一点的速度。
单位:m/s⑤剪切应力:.二卩:黏性系数dy⑥动压:4比="2空;2、空气动力及力矩的定义、来源及计算方法空气动力及力矩的来源只有两个:①物体表面的压力分布②物体表面的剪应力分布。
气动力的描述有两种坐标系:风轴系(L,D )和体轴系(A,N)。
力矩与所选的点有关系,抬头为正,低头为负。
L = N cos : - Asin :,D = Ns i n A c o s3、气动力系数的定义及其作用气动力系数是比空气动力及力矩更基本且反映本质的无量纲系数,在三维中I的力系数与二维中有差别,^口:升力系数C L=丄(3D),q =丄(2D)q(S q^cc_L Q _D Q _N Q _A CC L, C D , C N, C A, C MqSq ::Sq :Sq ::S二维:S=C (1)=C4、 压力中心的定义压力中心,作用翼剖面上的空气动力,可简化为作用于弦上某参考点的升力 L,阻力D 或法向力N ,轴向力A 及绕该点的力矩M 。
如果绕参考点的力矩为零, 则该点称为压力中心,显然压力中心就是总空气动力的作用点,气动力矩为005、 什么是量纲分析,为什么要进行量纲分析,其理论依据,具体方法在等式中,等号左边和等号右边各项的的量纲应相同, 某些物理变量可以用 一些基本量(质量,长度,时间等)来表达,据此有了量纲分析法,量纲分析可 以减少方程独立变量个数,其理论依据是白金汉n 定理。

空气动力学是力学的一个分支,它主要研究物体在同气体作相对运动情况下的受力特性、气体流动规律和伴随发生的物理化学变化。
空气动力学重点研究飞行器的飞行原理,是航空航天技术最重要的理论基础之一。
气体流动在不同的速度范围呈现不同的特点。
空气动力学的发展经历了低速、高速和新变革三个时期。
它是在流体力学的基础上,随着航空工业和喷气推进技术的发展而成长起来的一个学科。
空气动力学 - 简介相关书籍空气动力学是研究空气和其他气体的运动以及它们与物体相对运动时相互作用的科学,简称为气动力学。
空气动力学重点研究飞行器的飞行原理,是航空航天技术最重要的理论基础之一。
在任何一种飞行器的设计中,必须解决两方面的气动问题:一是在确定新飞行器所要求的性能后,寻找满足要求的外形和气动措施;一是在确定飞行器外形和其他条件后,预测飞行器的气动特性,为飞行器性能计算和结构、控制系统的设计提供依据。
这些在飞行速度接近到超过声速(又称音速)时更为重要。
20世纪以来,飞机和航天器的外形不断改进,性能不断提高,都是与空气动力学的发展分不开的。
亚音速飞机为获得高升阻比采用大展弦比机翼;跨音速飞机为了减小波阻采用后掠机翼,机翼和机身的布置满足面积律;超音速飞机为了利用旋涡升力采用细长机翼(见机翼空气动力特性);高超音速再入飞行器为了减少气动加热采用钝的前缘形状,这些都是在航空航天技术中成功地应用空气动力学研究成果的典型例子。
除此以外,空气动力学在气象、交通、建筑、能源、化工、环境保护、自动控制等领域都得到广泛的应用。
空气动力学 - 学科分支空气动力学空气动力学是流体力学的一个分支。
气体流动在气体流动在不同的速度范围呈现不同的特点。
飞行器的飞行马赫数大于0.3时,就必须考虑空气压缩性。
当飞行速度接近音速时,在飞行器的绕流中会出现局部的超音速区,在其后形成激波,使迎面阻力剧增。
当飞行速度超过音速几倍时,由于高速气流的温度升高,气体内部发生种种物理化学变化,这时必须同时考虑气体的热力现象和动力现象,研究这些现象的学科就是空气动力学的一个分支气动热力学。

第六章 气体动理论6-1 一束分子垂直射向真空室的一平板,设分子束的定向速度为v ,单位体积分子数为n ,分子的质量为m ,求分子与平板碰撞产生的压强.分析 器壁单位面积所受的正压力称为气体的压强.由于压强是大量气体分子与器壁碰撞产生的平均效果,所以推导压强公式时,应计算器壁单位面积在单位时间内受到气体分子碰撞的平均冲力.解 以面积为S 的平板面为底面,取长度等于分子束定向速度v 的柱体如图6-1所示,单位时间内与平板碰撞的分子都在此柱体内.柱体内的分子数为nSv .每个分子与平板碰撞时,作用在平板上的冲力为2mv ,单位时间内平板所受到的冲力为v v nS m F ⋅=2根据压强的定义,分子与平板碰撞产生的压强为22v nm SFp ==6-2 一球形容器,直径为2R ,内盛理想气体,分子数密度为n ,每个分子的质量为m ,(1)若某分子速率为v i ,与器壁法向成θ角射向器壁进行完全弹性碰撞,问该分子在连续两次碰撞间运动了多长的距离?(2)该分子每秒钟撞击容器多少次?(3)每一次给予器壁的冲量是多大?(4)由上结果导出气体的压强公式.分析 任一时刻容器中气体分子的速率各不相同,运动方向也不相同,由于压强是大量气体分子与器壁碰撞产生的平均效果,气体压强公式的推导过程为:首先任意选取某一速率和运动方向的分子,计算单位时间内它与器壁碰撞给予器壁的冲力,再对容器中所有分子统计求和.v图6-1解 (1)如图6-2所示,速率为v i 的分子以θ角与器壁碰撞,因入射角与反射角都相同,连续两次碰撞间运动的距离都是同样的弦长,为θcos 2R AB =(2)该分子每秒钟撞击容器次数为θcos 2R AB ii v v =(3)每一次撞击给予器壁的冲量为θcos 2i m v(4)该分子每秒钟给予器壁的冲力为Rm R m i i i 2cos 2cos 2v v v =θθ由于结果与该分子的运动方向无关,只与速率有关,因此可得容器中所有分子每秒钟给予器壁的冲量为21212222221v v v v v v v RmN N N R m R m R m R m R m R m N i i N i i N i ===+++++∑∑== 其中n R N 334π=.根据压强的定义,分子与器壁碰撞产生的压强为W n m n nm R R m Np 3221323142222=⎪⎭⎫ ⎝⎛===v v vπ 其中W 为分子的平均平动动能.6-3 容积为10 L 的容器内有1 mol CO 2气体,其方均根速率为1440 km/h ,求CO 2气体的压强(CO 2的摩尔质量为31044-⨯kg/mol ).分析 在常温常压下可以将气体视为理想气体,理想气体压强公式中引入了统计平均量----方均根速率2v 和分子数密度n ,1 mol 的气体中分子数为阿伏图6-2伽德罗常量N A ,根据这些关系可求出压强.解 容积为V 的容器中有1 mol CO 2气体,则分子总数为N A ,摩尔质量为M ,则分子数密度为V N A ,分子质量为A N M,因此由气体压强公式得22A A 2313131v v v VM N M V N nm p ===代入数字得Pa 102.35Pa 3600101440101010443131523332⨯=⎪⎪⎭⎫ ⎝⎛⨯⨯⨯⨯⨯==--v V M p 6-4 在实验室中能够获得的最佳真空相当于大约Pa 10013.19-⨯,试问在室温(273K )下在这样的“真空”中每立方厘米内有多少个分子?分析 引入玻尔兹曼常量k 和分子数密度n 后,理想气体状态方程可以表示为nkT p =.解 由理想气体状态方程nkT p =得3-113-239m 1069.2m 2731038.110013.1⨯=⨯⨯⨯==--kT p n 6-5 已知气体密度为1 kg/m 3,压强为Pa 10013.15⨯,(1)求气体分子的方均根速率;(2)设气体为氧,求温度.分析 气体密度ρ是单位体积中气体的质量,因此与分子数密度n 和分子质量m 的关系为nm =ρ.解 压强公式可写为 223131v v ρ==nm p(1)分子的方均根速率m/s 551m/s 110013.13352=⨯⨯==ρpv(2)氧的摩尔质量M =31032-⨯kg/mol ,由定义MRT32=v ,则 K 390K 31.8310325513322=⨯⨯⨯==-R M T v6-6 体积为10-3 m 3,压强为Pa 10013.15⨯的气体,所有分子的平均平动动能的总和是多少?分析 气体动理论的能量公式给出了微观量气体分子的平均平动动能和宏观量气体温度之间的关系.分子的平均平动动能是大量分子的统计平均值,是每个分子平均占有的平动动能量值.解 由气体动理论的能量公式,分子的平均平动动能为kT m 23212=v 容器中分子数nV N =,又由压强公式nkT p =,可得容器中所有分子的平均平动动能的总和为J152J 1010013.123232321352=⨯⨯⨯===-pV kT nV m Nv6-7 一容器内贮有氧气,其压强为Pa 10013.15⨯=p ,温度T =C 27︒,求(1)单位体积内的分子数;(2)氧气的密度;(3)氧分子的质量;(4)分子间的平均距离;(5)分子的平均平动动能;(6)若容器是边长为0.30 m 的立方体,当一个分子下降的高度等于容壁的边长时,其重力势能改变多少?并将重力势能的改变与其平均平动动能相比较.分析 常温和常压下,氧气可视为理想气体.从宏观的角度,可以认为气体是空间均匀分布的,因此分子间的平均距离的立方就是每个分子平均占有的体积.通过本题的计算,可以得到气体动理论中常用到的物理量的量级概念.解 (1) 由理想气体的状态方程nkT p =,可得单位体积内的分子数为3-253-235m 1045.2m 3001038.110013.1⨯=⨯⨯⨯==-kT p n (2) 利用理想气体的状态方程RT MmpV =,氧气的密度为 3335kg/m 3.1kg/m 30031.8103210013.1=⨯⨯⨯⨯===-RT pM V m ρ(3) 氧分子的质量为kg 105.3kg 1045.23.126-25⨯=⨯==nm ρ(4) 分子平均占有的空间开方等于分子间的平均距离m 10443m 1045.21193253.n d -⨯=⨯== (5) 分子的平均平动动能J 10.216J 3001038.123232121-232⨯=⨯⨯⨯==-kT m v(6) 一个氧分子下降的高度等于容壁的边长时,其重力势能改变为J 101.56J 30.08.9103.5-2526⨯=⨯⨯⨯=-mgh与分子平均平动动能相比较,有4252121098.31056.11021.621⨯=⨯⨯=--mgh m v 6-8 在什么温度时,气体分子的平均平动动能等于一个电子由静止通过1 V 电位差的加速作用所得到的动能(即1eV 的能量).解 根据题意,气体分子的平均平动动能J 10260.1eV 12321192-⨯===kT m v 则 K 7739K 1038.1310602.122319=⨯⨯⨯⨯=--T 6-9 1 mol 氢气,在温度C 27︒时,求(1)具有若干平动动能;(2)具有若干转动动能;(3)温度每升高C 1︒时增加的总动能是多少?分析 氢气是双原子分子气体,如果作为刚性分子看待,就具有3个平动自由度和2个转动自由度,根据能量按自由度均分原则可以求出平均平动动能和平均转动动能.解 (1) 1 mol 氢气的平动动能为J 10.743J 30031.82323233A⨯=⨯⨯==RT kT N(2) 1 mol 氢气的转动动能为J 10.492J 30031.8223A⨯=⨯==RT kT N(3) 温度每升高C 1︒,1 mol 氢气增加的总动能为J 8.02J 131.8252525A=⨯⨯=∆=∆T R T k N 6-10 1 mol 单原子理想气体和1 mol 双原子理想气体,温度升高C 1︒时,其内能各增加多少?1 g 氧气和1 g 氢气温度升高C 1︒时,其内能各增加多少?分析 一定量理想气体的内能T R iM m E ∆=2,对于单原子理想气体3=i ,对于双原子理想气体5=i ,对于1 mol 理想气体1=Mm.氧气和氢气都是双原子气体,氧气的摩尔质量kg/mol 10323-⨯=M .解 1 mol 单原子理想气体温度升高C 1︒,内能增量为J 5.12J 131.8232=⨯⨯=∆T R i1 mol 双原子理想气体温度升高C 1︒,内能增量为J 8.02J 131.8252=⨯⨯=∆T R i1 g 氧气温度升高C 1︒,内能增量为J 65.0J 131.8251032101233=⨯⨯⨯⨯⨯=∆--T R i M m 1 g 氢气温度升高C 1︒,内能增量为J 4.01J 131.825102101233=⨯⨯⨯⨯⨯=∆⋅--T R i M m 6-11 计算:(1)氧分子在C 0︒时的平均平动动能和平均转动动能;(2)在此温度下,4 g 氧的内能.分析 氧气是双原子分子气体,如果作为刚性分子看待,就具有3个平动自由度和2个转动自由度,5=i .解 (1) 氧分子在C 0︒时的平均平动动能为J 10.655J 2731038.1232321-23⨯=⨯⨯⨯=-kT 平均转动动能为J 10.773J 2731038.12221-23⨯=⨯⨯==-kT kT(2) 4 g 氧在C 0︒时的内能为J 709J 27331.8251032104233=⨯⨯⨯⨯⨯=⋅--RT i M m 6-12 有40个粒子速率分布如下表所示 (其中速率单位为m/s):速率区间100以下100~200 200~300 300~400 400~500 500~600 600~700 700~800 800~900 900以上粒子数 1 4 6 8 6 5 4 3 2 1若以各区间的中值速率标志处于该区间内的粒子速率值,试求这40个粒子的平均速率v 、方均根速率2v 和最概然速率p v ,并计算出p v 所在区间的粒子数占总粒子数的百分率.分析 为了更深入地理解麦克斯韦速率分布律以及气体动理论中引入的平均速率v 、方均根速率2v 和最概然速率p v 的统计意义,有必要通过实际例子,经过计算,体验速率分布规律和统计方法.解 这40个粒子分成了10个速率区间,若取1000 m/s 为粒子速率在900 m/s 以上的速率区间的中值速率,则根据定义,其平均速率v 为m/s448.75 m/s )1100028503750465055506450 835062504150150(4011101=⨯+⨯+⨯+⨯+⨯+⨯+⨯+⨯+⨯+⨯⨯==∑=i i i N N v v 方均根速率2v 为m/s 499.9 m/s )]1100028503750465055506450 835062504150150(401[121222222222210122=⨯+⨯+⨯+⨯+⨯+⨯+⨯+⨯+⨯+⨯⨯==∑=i i i N Nv v 最概然速率m/s 350p =v .p v 所在区间的粒子数占总粒子数的百分率为%20%100408p =⨯=∆NN 6-13上题所给分布情况,若以200m/s 为间隔作重新统计,列出分布情况表,计算出相应的v 、2v 和p v ,以及p v 所在区间的粒子数占总粒子数的百分率,并与上题结果进行比较.分析 通过本题和上题计算结果可以看出,在某一速率区间中的分子数和所计算的三种速率不但与速率区间位置有关,还与速率区间的宽度有关.只有当所统计的分子总数足够大,划分的速率区间足够小时,才可能获得处于平衡状态的气体分子速率的一个确定的分布函数,三种速率也才有确定值.解 以200m/s 为间隔对上题粒子速率作重新统计,速率分布情况为(其中速率单位为m/s):速率区间 200以下 200~400 400~600 600~800 800以上 粒子数 5 14 11 7 3这40个粒子分成了5个速率区间,若取900 m/s 为粒子速率在800 m/s 以上的速率区间的中值速率,则根据定义,其平均速率v 为m/s445 m/s)3900770011500143005100(401151=⨯+⨯+⨯+⨯+⨯⨯==∑=i i i N N v v 方均根速率2v 为498m/sm/s )]39007700 11500143005100(401[121222225122=⨯+⨯+⨯+⨯+⨯⨯==∑=i i iN Nvv最概然速率m/s 300p =v .p v 所在区间的粒子数占总粒子数的百分率为%35%1004014p =⨯=∆NN 6-14 N 个假想的气体分子,速率分布如图6-14所示.(1)用N 和v 0表示出a 的值;(2)求最概然速率p v ;(3)以v 0为间隔等分为三个速率区间求各区间中分子数占总分子数的百分率.分析 速率分布函数)(v f 表示气体分子速率在v 值附近单位速率区间内的分子数占总分子数的百分率.本题给出了一个特殊的分布情况,通过计算,理解速率分布函数和最概然速率的物理意义,以及各速率区间中分子数占总分子数的百分率的计算方法.解 (1) 由图6-14可见,分布函数与气体分子总数N 的乘积曲线下的总面积应等于气体分子总数N ,即000302322121d )(0v v v v v v a a a f N =⋅+==⎰则 032v Na =Nf (v )a0 v 0 2 v 0 3 v 0 v图6-14(2) 最概然速率 0p v v =(3) 以v 0为间隔等分为三个速率区间,分子数占总分子数的百分率分别为%3.3331211d )(10010==⋅==⎰v v v v a N f N N N %5021431d )(10220==⋅==⎰v v v v v a N f N N N %7.1661411d )(103230==⋅==⎰v v v v v a N f NN N *6-15在速率区间1v ~2v 内麦克斯韦速率分布曲线下的面积等于分布在此区间内的分子数的百分率.应用(6-17)式和麦克斯韦速率分布函数表示式(6-18)式,求在速率区间v p ~1.01v p 内的气体分子数占总分子数的比率.分析 麦克斯韦速率分布律表明,由速率分布函数)(v f 可得气体分子速率在v ~v v ∆+速率区间内的分子数占分子总数的百分率为v v ∆=∆)(f NN. 解 麦克斯韦速率分布函数22232e24)(v v v kT m kT m f -⎪⎭⎫ ⎝⎛=ππ,因mkT2p =v ,则分布函数可写为1p 2p223p2p22p2e4e4)(----==v v v v v v v v v v ππππf 速率区间v p ~1.01v p 内的气体分子数占总分子数的比率为%83.001.01e 4e4e 4)(1p 2p223p 2p22p2=⨯⨯⨯=∆=∆=∆=∆----πππv v v v v v v v v v v v v f N N *6-16应用平均速率表示式(6-20)*式、麦克斯韦速率分布函数表示式(6-18)式以及积分公式bb 21d e23=-∞⎰v v v 求v 的值.分析 这里采用的是数学中加权求某量值的平均值的方法,权重就是麦克斯韦速率分布函数)(v f .如果要计算方均根速率2v ,可先求速率平方的平均值,只需将积分式中的v 改为2v ,即v v)v v d 022⎰∞=f(,再将积分结果开方.解 麦克斯韦速率分布函数表示式(6-18)式和平均速率表示式(6-20)*式给出v v v v)v v v d e24d 0322302⎰⎰∞-∞⎪⎭⎫⎝⎛==kTm kT m f(ππ利用积分公式bb 21d e 23=-∞⎰v v v 得 mkTkT m kT m f(πππ822124d 2230=⎪⎭⎫ ⎝⎛⎪⎭⎫⎝⎛==⎰∞v v)v v *6-17 试由麦克斯韦速率分布律推出相应的平动动能分布律,并求出最概然能量E p ,它是否就等于2p 21v m .分析 要找出分子按平动动能的分布规律,即求出分布在平动动能区间E k ~E k +d E k 中的分子数占总分子数的百分率.解 速率为v 的分子的平动动能为E k = 221v m ,则v v d d k m E =,麦克斯韦速率分布律可改写为kk k k 232212232223d )(d e12 d e 2112 d e 24d )(d k 22E E f E E kT m m kT kT m f N N kTE kT m kT m =⎪⎭⎫ ⎝⎛=⋅⎪⎭⎫ ⎝⎛⋅⎪⎭⎫ ⎝⎛=⎪⎭⎫ ⎝⎛==---ππππv v v v v v v v v即分子按平动动能分布律,其中分布函数kTE E kT E f k e12)(k 23k -⎪⎭⎫⎝⎛=π参考最概然速率的定义,令0d )(d kk =E E f ,由上式得最概然动能 kT E 21k p =因m kT 2p =v ,则 k p 2p 221E kT m ==v 6-18 飞机起飞前机舱中的压强计指示为Pa 10013.15⨯,温度为C 27︒.起飞后压强计指示为Pa 1010.84⨯,温度仍为C 27︒.试计算飞机此时距地面的高度.解 根据玻尔兹曼分子数密度按高度分布公式kT mgh n n /0e -=和压强公式nkT p =,在高度1h 和2h 的压强分别为1p 和2p ,则有kT h h mg p p /)(2121e --=得m 100.2m 1010.810013.1ln 8.9102930031.8 ln ln 3453212112⨯=⨯⨯⨯⨯⨯⨯==+=-p p Mg RTp p mg kT h h6-19 设地球大气是等温的,温度为C 17︒,海平面上的气压为Pa 100.150⨯=p ,已知某地的海拔高度为h = 2000 m ,空气的摩尔质量kg/m ol 10293-⨯=M ,求该地的气压值.解 根据玻尔兹曼分子数密度按高度分布公式kT mgh n n /0e -=和理想气体状态方程nkT p =,在高度h 处的压强p 为Pa 107.90Pa e100.1e 429031.820008.910295/03⨯=⨯⨯==⨯⨯⨯⨯---RT Mgh p p6-20 在某一粒子加速器中,质子在Pa 10333.14-⨯的压强和273 K 的温度的真空室内沿圆形轨道运动.(1)估计在此压强下每立方厘米内的气体分子数;(2)如果分子有效直径为2.0×10-8 cm .则在此条件下气体分子的平均自由程为多大?分析 由理想气体状态方程nkT p =可得压强和分子数密度的关系,并由此可计算平均自由程.解 (1) 由理想气体状态方程可得3103163234cm 1054.3m 1054.3m 2731038.110333.1----⨯=⨯=⨯⨯⨯==-kT p n (2) 由定义,平均自由程为cm 101.59m )102(1054.32121428102⨯=⨯⨯⨯⨯⨯==-ππλnd6-21设电子管内温度为300 K ,如果要管内分子的平均自由程大于10 cm时,则应将它抽到多大压强?(分子有效直径约为3.0×10-8 cm ).分析 由平均自由程定义和理想气体状态方程可建立压强与平均自由程以及温度之间的关系.解 由平均自由程定义221ndπλ=和理想气体状态方程nkT p =,得Pa 0.1035Pa 1.0)103(23001038.12210232=⨯⨯⨯⨯⨯==--πλπd kT p6-22 计算:(1)在标准状态下,一个氮分子在1 s 内与其它分子的平均碰撞次数;(2)容积为4 L 的容器,贮有标准状况下的氮气,求1 s 内氮分子间的总碰撞次数.(氮分子的有效直径为3.76×10-8 cm .)解 (1) 因平均速率MRTπ8=v ,标准状态下22.4 L 中的分子数为A N ,则平均碰撞次数1-91-32321033-A 22s 1067.7 s 104.2210023.6)1076.3(102827331.816 1022.4162⨯=⨯⨯⨯⨯⨯⨯⨯⨯=⨯==---πππN d M RT n d Z v(2) 4 L 氮的分子数N =A 4.224N ,分子间的总碰撞次数为1321923s 10125.4s 1067.710023.64.2242121-⨯=⨯⨯⨯⨯⨯=-Z N 6-23 假设氦气分子的有效直径为10-10 m ,压强为Pa 10013.15⨯,温度为300 K ,(1)计算氦气分子的平均自由程λ和飞行一个平均自由程所需要的时间τ;(2)如果有一个带基本电荷的氦离子在垂直于电场的方向上运动,电场强度为104 V/m ,试计算氦离子在电场中飞行τ时间内沿电场方向移动的距离s 及s 与λ的比值;(3)气体分子热运动的平均速率与氦离子在电场方向的平均速率的比值;(4)气体分子热运动的平均平动动能与氦离子在电场中飞行一个λ远的距离所获得的能量和它们的比值.解 (1) 由平均自由程定义221ndπλ=和理想气体状态方程nkT p =,得m 1029m 10013.1)10(23001038.1275210232-.pd kT ⨯=⨯⨯⨯⨯⨯==--ππλ 平均速率 m/s 1260m/s 10430031.8883=⨯⨯⨯⨯==-ππM RT v 则 s 107.3s 1260102.910-7⨯=⨯==-v λτ (2) 氦离子质量为A N M m =,沿电场方向受到的电场力为eE ,加速度meE a =,在τ时间内沿电场方向移动的距离为m 106.4m 1042103.710023.610106.1 2218-310234192A 2⨯=⨯⨯⨯⨯⨯⨯⨯⨯===---M eEN a s ττ 14.4104.6102.987=⨯⨯=--s λ(3) 氦离子沿电场方向的平均速率为m/s 87.7m/s 103.7104.6108E =⨯⨯==--τsv 14.4E==s λv v(4) 氦气分子平均平动动能为J 106.21J 3001038.1232321-23⨯=⨯⨯⨯=-kT 氦离子在电场中飞行一个λ远的距离所获得的能量为J 101.472J 102.910106.1-217419⨯=⨯⨯⨯⨯=--λeE二者之比为 22.410472.11021.62121=⨯⨯-- *6-24用范德瓦耳斯方程计算压强为Pa 10013.18⨯,体积为0.050 L 的1 mol氧气的温度,如果用理想气体状态方程计算,将引起怎样的相对误差?已知氧的范德瓦耳斯常数为:225/mol L Pa 10378.1⋅⨯=a ;L/mol 0318.0=b .解 由范德瓦耳斯方程得K 342.6K 10)0318.0050.0(050.010378.110013.131.81 )(13258020=⨯-⨯⎪⎪⎭⎫ ⎝⎛⨯+⨯⨯=-⎪⎪⎭⎫⎝⎛+=-b V V a p R T由理想气体状态方程得K .5609K 31.810050.010013.138=⨯⨯⨯==-R pV T相对误差为%7878.06.3426.3425.609==-*6-25在C 27︒时,2 mol 氮气的体积为0.1 L ,分别用范德瓦耳斯方程及理想气体状态方程计算其压强,并比较结果.已知氮气224/mol L Pa 1039.8⋅⨯=a ,L/mol 1005.32-⨯=b .解 范德瓦耳斯方程)(222RT M m b V V a M m p =-⎪⎪⎭⎫ ⎝⎛+,得Pa 109.43Pa 101039.82Pa 1005.321030031.82 782254222⨯=⨯⨯-⨯⨯-⨯⨯=--=----V a M m bMm V RTM m p 由理想气体状态方程得Pa 104.99Pa 1030031.8274⨯=⨯⨯==-V RT M m p 结果表明由理想气体状态方程计算出的压强小于由范德瓦耳斯方程的计算值.*6-26实验测知C 0︒时氧的粘滞系数1.92×10-4 s)g/(cm ⋅,试用它来求标准状态下氧分子的平均自由程和分子的有效直径.解 粘滞系数 v λρη31= 其中密度Vm=ρ.又由理想气体状态方程 RT Mm pV =平均速率MRTπ8=v ,联立可得m109.49 m 1032827331.810013.11092.138338-355⨯=⨯⨯⨯⨯⨯⨯⨯⨯===--ππηρηλM RT p v 分子的有效直径为m 102.97m 1049.910013.122731038.1 210-8523⨯=⨯⨯⨯⨯⨯⨯⨯==--πλπp kT d*6-27实验测知氮气C 0︒时热传导系数为23.7×10-3 W/(m ·K),定体摩尔热容为20.9 J/(mol ·K),试由此计算氮分子的有效直径.解 热传导系数 λρκv MC mV,31=其中密度A N nM =ρ,平均速率MRTπ8=v ,平均自由程221nd πλ=,则2Am V,132dM RT N C ππκ=m 102.23m 1102827331.810023.6107.2339.202 13210-4343233434Am V,⨯=⨯⨯⋅⨯⨯⨯⨯⨯=⋅=--ππκM RT N C d。

空气动力学的力量计算公式空气动力学是研究物体在空气中受到的力和运动的学科。
在空气动力学中,力的计算是至关重要的,因为它可以帮助我们理解物体在空气中的运动规律。
在本文中,我们将讨论空气动力学的力量计算公式,以及这些公式的应用。
空气动力学的力量计算公式可以分为两类,气动力和阻力。
气动力是指物体在空气中受到的推力或拉力,而阻力则是物体在空气中受到的阻碍运动的力。
下面我们将分别介绍这两种力的计算公式。
首先是气动力的计算公式。
气动力的大小取决于物体的形状、速度和空气的密度。
一般来说,气动力可以通过以下公式进行计算:F = 0.5 ρ v^2 A Cd。
其中,F表示气动力的大小,ρ表示空气的密度,v表示物体的速度,A表示物体的横截面积,Cd表示物体的阻力系数。
这个公式告诉我们,气动力与空气密度、速度的平方和物体的横截面积成正比,与物体的阻力系数成反比。
这个公式在飞行器设计和空气动力学研究中有着广泛的应用。
接下来是阻力的计算公式。
阻力的大小取决于物体的形状、速度和空气的密度。
一般来说,阻力可以通过以下公式进行计算:D = 0.5 ρ v^2 A Cd。
其中,D表示阻力的大小,ρ表示空气的密度,v表示物体的速度,A表示物体的横截面积,Cd表示物体的阻力系数。
这个公式与气动力的计算公式非常相似,只是它们的物理意义不同。
阻力的大小与空气密度、速度的平方和物体的横截面积成正比,与物体的阻力系数成反比。
以上是空气动力学的力量计算公式,它们可以帮助我们理解物体在空气中受到的力和运动规律。
这些公式在飞行器设计、汽车设计和建筑结构设计等领域都有着重要的应用。
通过对这些公式的研究和应用,我们可以更好地理解物体在空气中的运动规律,从而设计出更加高效和安全的产品。
除了以上介绍的气动力和阻力的计算公式,空气动力学还涉及到其他一些力的计算公式,比如升力的计算公式和升阻比的计算公式。
这些公式在飞行器设计和空气动力学研究中也有着重要的应用。

第六章 气体动理论6-1 一容积为10L 的真空系统已被抽成1.0×10-5 mmHg 的真空,初态温度为20℃。
为了提高其真空度,将它放在300℃的烘箱内烘烤,使器壁释放出所吸附的气体,如果烘烤后压强为1.0×10-2 mmHg ,问器壁原来吸附了多少个气体分子?解:由式nkT p =,有3202352/1068.15731038.1760/10013.1100.1m kT p n 个⨯≈⨯⨯⨯⨯⨯==-- 因而器壁原来吸附的气体分子数为个183201068.110101068.1⨯=⨯⨯⨯==∆-nV N6-2 一容器内储有氧气,其压强为1.01⨯105 Pa ,温度为27℃,求:(l )气体分子的数密度;(2)氧气的密度;(3)分子的平均平动动能;(4)分子间的平均距离。
(设分子间等距排列)分析:在题中压强和温度的条件下,氧气可视为理想气体。
因此,可由理想气体的物态方程、密度的定义以及分子的平均平动动能与温度的关系等求解。
又因可将分子看成是均匀等距排列的,故每个分子占有的体积为30d V =,由数密度的含意可知d n V ,10=即可求出。
解:(l )单位体积分子数325m 1044.2-⨯==kT p n(2)氧气的密度3m kg 30.1-⋅===RT pM V m ρ(3)氧气分子的平均平动动能J 1021.62321k -⨯==kT ε(4)氧气分子的平均距离m1045.3193-⨯==n d6-3 本题图中I 、II 两条曲线是两种不同气体(氢气和氧气)在同一温度下的麦克斯韦分子速率分布曲线。
试由图中数据求:(1)氢气分子和氧气分子的最概然速率;(2)两种气体所处的温度。
分析:由M RT v /2p =可知,在相同温度下,由于不同气体的摩尔质量不同,它们的最概然速率p v 也就不同。
因22O H M M <,故氢气比氧气的p v 要大,由此可判定图中曲线II 所标13p s m 100.2-⋅⨯=v 应是对应于氢气分子的最概然速率。
测试
1、 解释方程p dT dp C Q dt dt α-=各项的物理意义
2、
什么是θ、e θ、ωθ,用图示说明(Ema 图) 3、
什么是对流不稳定,它与条件性不稳定有何不同,对流不稳定发生的关键因子是什么 4、
写出涡度方程并解释各项的物理意义,若应用在辐散层,忽略扭转项,其物理意义是什么 5、
写出Rossby 波相速位移公式及其物理意义(设基本气流为西风,重点讨论不同波长的移动状况) 6、
等熵坐标系中的位势涡度表达式,说明它在天气运动分析中的作用 7、
什么是Hadley 环流和Walker 环流,为什么它们是辐散环流 8、
说明大气和地表之间的交换过程及其对天气过程的重要性(从动量、能量、水汽(潜热)交换方面分析) 9、
在气候变暖的条件下,分析台风不能变得更强的原因 10、
为什么准地转坐标模式不以预报天气系统的移动和发展 11、 判断ω和t φ∂∂,即未来天气系统的发生发展。
空气的动力粘滞系数引言:空气是地球上最常见的物质之一,对于人类来说,离开空气我们无法生存。
在我们日常生活中,我们经常会感受到空气的存在,比如我们呼吸时的感觉、风的吹拂、飞机在空中飞行等等。
但是,你是否了解空气的动力粘滞系数呢?本文将对空气的动力粘滞系数进行解析,带你了解空气的神秘之处。
一、空气的动力粘滞系数是什么?动力粘滞系数是描述流体内部粘滞阻力大小的物理量,它与流体的粘性有关。
对于气体来说,空气作为一种常见的气体,在动力粘滞系数的研究中也有其特殊之处。
二、空气动力粘滞系数的计算方法由于本文要求不得包含数学公式或计算公式,因此在此不对计算方法进行详细介绍。
但是,我们可以通过一些实验和模型来估算空气的动力粘滞系数,比如通过测量空气在管道中的流速和压力差等参数来计算。
三、空气动力粘滞系数的影响因素空气动力粘滞系数受多种因素影响,下面我们将介绍其中的一些主要因素:1. 温度:空气的动力粘滞系数随着温度的升高而增大。
这是因为温度升高会使空气分子的平均速度增加,从而增加了分子之间的碰撞频率和力量。
2. 压力:空气的动力粘滞系数随着压力的增加而减小。
这是因为在高压下,空气分子之间的碰撞会变得更加频繁,从而增加了分子之间的相互作用力,减小了动力粘滞系数。
3. 空气成分:空气中的成分对动力粘滞系数也会有一定的影响。
不同成分的气体具有不同的分子大小和形状,从而影响了分子之间的相互作用力,进而影响了动力粘滞系数的大小。
四、空气动力粘滞系数的应用空气的动力粘滞系数在工程领域有着广泛的应用,下面我们将介绍其中的一些应用场景:1. 管道输送:在液体或气体通过管道输送的过程中,空气的动力粘滞系数决定了流体在管道中的阻力大小,对于管道输送的设计和优化具有重要意义。
2. 飞行器设计:在飞行器设计中,了解空气的动力粘滞系数可以帮助工程师更好地估算空气对飞行器的阻力大小,从而指导飞行器的设计和改进。
3. 空气动力学研究:在空气动力学研究中,空气的动力粘滞系数是一个重要的参数,可以帮助研究人员了解气体流动的特性和动力学行为。