2018届高考化学总复习第6章化学反应与能量第一节化学能
- 格式:ppt
- 大小:5.64 MB
- 文档页数:103


第1讲化学能与热能[考纲要求] 1.了解化学反应中能量转化的原因,能说出常见的能量转化形式。
2.了解化学能与热能的相互转化,了解吸热反应、放热反应、反应热等概念。
3.了解热化学方程式的含义,能用盖斯定律进行有关反应热的简单计算。
4.了解能源是人类生存和社会发展的重要基础,了解化学在解决能源危机中的重要作用。
考点一焓变与反应热1.化学反应中的能量变化(1)化学反应中的两大变化:物质变化和能量变化。
(2)化学反应中的两大守恒:质量守恒和能量守恒。
(3)化学反应中的能量转化形式:热能、光能、电能等。
通常主要表现为热量的变化。
2.焓变、反应热(1)定义:在恒压条件下进行的反应的热效应。
(2)符号:ΔH。
(3)单位:kJ·mol-1或kJ/mol。
3.吸热反应和放热反应(1)从反应物和生成物的总能量相对大小的角度分析,如图所示。
(2)从反应热的量化参数——键能的角度分析(3)常见放热反应①可燃物的燃烧;②酸碱中和反应;③大多数化合反应;④金属跟酸的置换反应;⑤物质的缓慢氧化。
(4)常见吸热反应①大多数分解反应;②盐的水解和弱电解质的电离;③Ba(OH)2·8H2O与NH4Cl反应;④碳和水蒸气、C和CO2的反应。
深度思考1.同质量的硫粉在空气中燃烧和在纯氧中燃烧,哪一个放出的热量多,为什么?答案在空气中燃烧放出的热量多,因在纯氧中燃烧火焰明亮,转化成的光能多,故放出的热量少。
2.判断正误,正确的划“√”,错误的划“×”(1)放热反应不需要加热就能反应,吸热反应不加热就不能反应( )(2)物质发生化学变化都伴有能量的变化( )(3)伴有能量变化的物质变化都是化学变化( )(4)吸热反应在任何条件都不能发生( )(5)Na转化为Na+时,吸收的能量就是该过程的反应热( )(6)水蒸气变为液态水时放出的能量就是该变化的反应热( )答案(1)×(2)√(3)×(4)×(5)×(6)×解析(5)(6)是物理变化过程,其能量变化不能称为反应热。

高考化学一轮总复习:第六章化学反应与能量目录第1节化学能与热能第2节原电池化学电源第3节电解池金属的腐蚀与防护第1节化学能与热能1.已知热化学方程式:2SO2(g)+O2(g)2SO3(g) ΔH=-Q kJ·mol-1(Q>0)。
下列说法正确的是( )A.相同条件下,2 mol SO2(g)和1 mol O2(g)所具有的能量小于2 mol SO3(g)所具有的能量B.将2 mol SO2(g)和1 mol O2(g)置于一密闭容器中充分反应后,放出热量为Q kJC.若使用催化剂,该反应的|ΔH|减小D.如将一定量SO2(g)和O2(g)置于某密闭容器中充分反应后放热Q kJ,则此过程中有2 mol SO2(g)被氧化答案 D2.一定条件下,在水溶液中1 mol Cl-、ClOx-(x=1,2,3,4)的能量(kJ)的相对大小如图所示,下列有关说法正确的是( )A.e是ClO3-B.b→a+c反应的活化能为60 kJ·mol-1C.a、b、c、d、e中c最稳定D.b→a+d反应的热化学方程式为3ClO-(aq)===ClO3-(aq)+2Cl-(aq) ΔH =-116 kJ·mol-1答案 D解析A项,e中Cl元素化合价为+7价,而ClO3-中Cl元素化合价为+5价,错误;B项,b→a+c反应的活化能为40 kJ·mol-1,错误;C项,a、b、c、d、e中a能量最低,所以最稳定,错误;D项,b→a+d,根据转移电子守恒得该反应方程式为3ClO-===ClO3-+2Cl-,反应热=64 kJ·mol-1+2×0 kJ·mol-1-3×60 kJ·mol-1=-116 kJ·mol-1,所以该热化学方程式为3ClO-(aq)===ClO3-(aq)+2Cl-(aq) ΔH=-116 kJ·mol-1,正确。
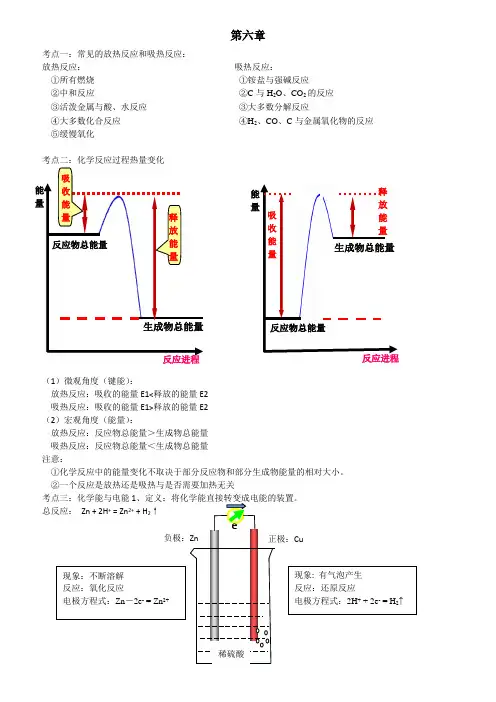
第六章考点一:常见的放热反应和吸热反应:放热反应: 吸热反应:①所有燃烧 ①铵盐与强碱反应②中和反应 ②C 与H 2O 、CO 2的反应 ③活泼金属与酸、水反应 ③大多数分解反应④大多数化合反应 ④H 2、CO 、C 与金属氧化物的反应 ⑤缓慢氧化考点二:化学反应过程热量变化(1)微观角度(键能):放热反应:吸收的能量E1<释放的能量E2 吸热反应:吸收的能量E1>释放的能量E2 (2)宏观角度(能量):放热反应:反应物总能量>生成物总能量 吸热反应:反应物总能量<生成物总能量 注意:①化学反应中的能量变化不取决于部分反应物和部分生成物能量的相对大小。
②一个反应是放热还是吸热与是否需要加热无关总反应: Zn + 2H + = Zn 2+ + H 2↑e - 反应物总能量生成物总能量 能量 反应进程 吸收能量 能量释放能量反应进程反应物总能量生成物总能量吸收能量释放能量稀硫酸负极:Zn 正极:Cu 现象:不断溶解 反应:氧化反应 电极方程式:Zn -2e - = Zn 2+ 现象: 有气泡产生 反应:还原反应 电极方程式:2H + + 2e - = H 2↑外电路:电子由负极经导线流向正极内电路:阳离子→正极;阴离子→负极2.形成原电池的条件(两极一液一回路):①两个活泼性不同的电极(金属与金属或金属与碳棒)②电解质溶液③形成闭合回路,自发进行的氧化还原反应3.氢氧燃料电池:(1)酸性燃料电池:负极:2H2-4e-= 4H+ 正极:O2 +4e- + 4H+= 2H2O(2)碱性燃料电池:负极:2H2 + 4OH- - 4e- = 4H2O 正极:O2 + 2H2O + 4e- = 4OH-总反应:2H2 + O2 =2H2O4.甲烷燃料电池:(电解质为KOH)负极:CH4+10OH--8e-=CO32-+7H2O 正极:2O2+4H2O+8e-=8OH-总反应:CH4+2O2+2KOH=K2CO3+3H2O练习:1.下列关于能量变化的说法,正确的是()A.等质量的红磷和白磷完全燃烧生成P2O5(s)放出的热量相同B.2Na+2H2O===2NaOH+H2,该反应生成物的总能量高于反应物的总能量C.放热反应中,反应物的总能量大于生成物的总能量D.有化学键断裂的是吸热过程,并且一定发生了化学变化2.下列反应既属于氧化还原反应,又是放热反应的是()A.铝与盐酸反应B.NaOH和HCl反应C.Ba(OH)2·8H2O与NH4Cl的反应D.CaCO3受热分解为CaO和CO23.下列变化过程,属于放热反应的是:()①NaOH固体溶于水②炸药爆炸③食物因氧化而腐败④铝热反应⑤酸碱中和反应⑥煅烧石灰石制生石灰⑦盐酸溶液中插入打磨过的铝片A.②③④⑤⑦B.①②④⑤C.②③④⑤D.①②③⑥⑦4.已知拆开1mol H–H键,1mol N≡N键分别需要吸收的能量为436kJ 、946kJ;形成1mol N–H键,会放出能量391kJ,在反应N2 + 3H22NH3中,每生成2mol NH3,()A.放出92 kJ热量B.吸收92 kJ热量C.放出209kJ热量D.吸收209kJ热量5.反应M+Z→Q(ΔH>0)分两步进行:①M+Z→X(ΔH<0),②X→Q(ΔH>0)。


第六章化学反应与能量电化学基础第一讲化学反应的热效应一、选择题(本题共7个小题,每题6分,共42分,每个小题只有一个选项符合题意) 1.下列关于能量的变化及反应热的说法中正确的是 ( )。
A.任何化学反应都有反应热B.有些化学键断裂时吸收能量,有些化学键断裂时放出能量C.新化学键的形成不一定放出能量D.有热量变化的反应一定有化学键的断裂与形成答案 A2.(2012·哈尔滨模拟)已知化学反应A2(g)+B2(g)===2AB(g)的能量变化如图所示,判断下列叙述中正确的是 ( )。
A.每生成2分子AB吸收b kJ热量B.该反应热ΔH=+(a-b)kJ·mol-1C.该反应中反应物的总能量高于生成物的总能量D.断裂1 mol A—A和1 mol B—B键,放出a kJ能量解析由图示可知生成物总能量高于反应物总能量,C错;1 mol A2(g)与 1 mol B2(g)反应生成2 mol AB(g)吸收(a-b)kJ热量,A错,B正确;化学键断裂吸收能量,D错。
答案 B3.向足量H2SO4溶液中加入100 mL 0.4 mol·L-1 Ba(OH)2溶液,放出的热量是5.12 kJ。
如果向足量Ba(OH)2溶液中加入100 mL 0.4 mol·L-1盐酸时,放出的热量为2.2 kJ。
则Na2SO4溶液与BaCl2溶液反应的热化学方程式为 ( )。
A.Ba2+(aq)+SO2-4(aq)===BaSO4(s)ΔH=-2.92 kJ·mol-1B.Ba2+(aq)+SO2-4(aq)===BaSO4(s)ΔH=-18 kJ·mol-1C.Ba2+(aq)+SO2-4(aq)===BaSO4(s)ΔH=-73 kJ·mol-1D.Ba2+(aq)+SO2-4(aq)===BaSO4(s)ΔH=-0.72 kJ·mol-1解析这道题要求学生自己写出正确的热化学方程式,根据目标反应利用盖斯定律进行计算。

第二章化学反应与能量活动一自主学习化学键与化学反应中能量变化的关系一、化学能与热能的相互转化分子或化合物的原子之间是通过化学键相结合的,化学反应的实质就是反应物分子内化学键断裂和生成物中化学键形成的过程。
化学键的断裂和形成总是和能量的变化紧密联系的。
当物质发生反应时,断开(反应物的)化学键要吸收能量,形成(生成物的)化学键要放出能量。
因此,化学反应中能量变化的主要原因:反应物分子内化学键的断裂和生成物分子内化学键的形成。
1、键能大小关系(微观):断键吸收的总能量>成键释放的总能量:化学反应吸收能量,该反应为吸热反应;断键吸收的总能量<成键释放的总能量:化学反应释放能量,该反应为放热反应。
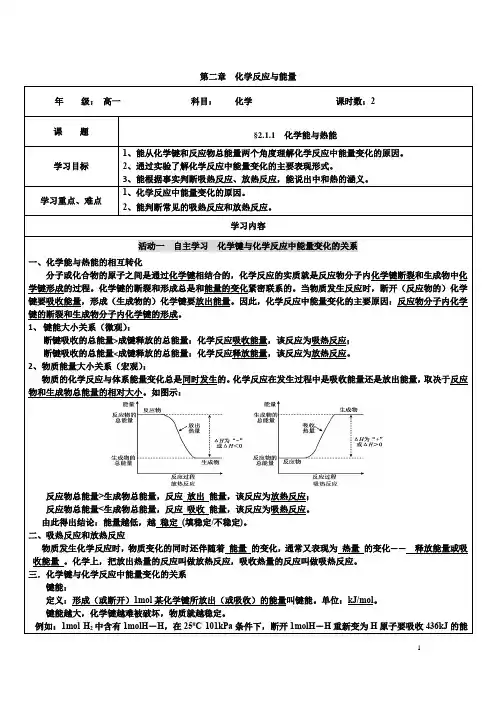
2、物质能量大小关系(宏观):物质的化学反应与体系能量变化总是同时发生的。
化学反应在发生过程中是吸收能量还是放出能量,取决于反应物和生成物总能量的相对大小。
如图示:反应物总能量>生成物总能量,反应放出能量,该反应为放热反应;反应物总能量<生成物总能量,反应吸收能量,该反应为吸热反应。
由此得出结论:能量越低,越稳定(填稳定/不稳定)。
二、吸热反应和放热反应物质发生化学反应时,物质变化的同时还伴随着能量的变化,通常又表现为热量的变化—— 释放能量或吸收能量。
化学上,把放出热量的反应叫做放热反应,吸收热量的反应叫做吸热反应。
三.化学键与化学反应中能量变化的关系键能:定义:形成(或断开)1mol某化学键所放出(或吸收)的能量叫键能。
单位:kJ/mol。
键能越大,化学键越难被破坏,物质就越稳定。
例如:1mol H2中含有1molH-H,在250C 101kPa条件下,断开1molH-H重新变为H原子要吸收436kJ的能13、下列说法中不正确的是()A.化学反应中能量的变化只能表现为热量变化B.化学反应在发生物质变化的同时还伴随着能量的变化,这是化学反应的一大特征C.化学能是能量的一种形式,它可以转化为其它形式的能量,如热能、电能等D.放热反应不需要加热即可发生E.吸热反应必须加热才能发生F.需要加热条件的化学反应都是吸热反应G.任何化学反应都伴随有能量的变化H.反应物的总能量高于生成物的总能量时,发生放热反应I.反应物的总能量低于生成物的总能量时,发生吸热反应J.需要持续加热才能进行的反应一般都是是吸热反应14、下列反应中既属于氧化还原反应又属于放热反应的是()A.氢氧化钾与硫酸的反应B.锌与盐酸反应放出氢气C.镁条在空气中燃烧D.Ba(OH)2•8H2O与NH4Cl反应15、对于放热反应2H2+O22H2O,下列说法正确的是()A.产物H2O 所具有的总能量高于反应物H2和O2所具有的总能量B.反应物H2和O2具有的能量相等C.断开2molH—H键和1molO—O键吸收的总能量小于形成4molO—H键所放出能量D.该反应中,化学能只有转变为热能16、如图所示,把试管小心地放入盛有(20℃)碳酸饮料的烧杯中,试管中开始放入适量饱和CuSO4溶液,再用滴管滴加5mL浓硫酸于试管中,试回答下列问题:(1)实验中观察到的现象是________________。