英语四级怎么准备,90%的人都不知道
- 格式:docx
- 大小:14.74 KB
- 文档页数:3

化学试题可能用到的相对原子质量:H1C12N14O16Cl35.5Cu64一、选择题:本题共14小题,每小题3分,共42分。
在每小题给出的四个选项中,只有一项是符合题目要求的。
1.近年来,我国新能源产业得到了蓬勃发展,下列说法错误的是A.理想的新能源应具有资源丰富、可再生、对环境无污染等特点B.氢氧燃料电池具有能量转化率高、清洁等优点C.锂离子电池放电时锂离子从负极脱嵌,充电时锂离子从正极脱嵌D.太阳能电池是一种将化学能转化为电能的装置【答案】D【解析】【详解】A.理想的新能源应具有可再生、无污染等特点,故A正确;B.氢氧燃料电池利用原电池将化学能转化为电能,对氢气与氧气反应的能量进行利用,减小了直接燃烧的热量散失,产物无污染,故具有能量转化率高、清洁等优点,B正确;C.脱嵌是锂从电极材料中出来的过程,放电时,负极材料产生锂离子,则锂离子在负极脱嵌,则充电时,锂离子在阳极脱嵌,C正确;D.太阳能电池是一种将太阳能能转化为电能的装置,D错误;本题选D。
2.下列化学用语表述错误的是A.NaOH的电子式:B.异丙基的结构简式:C.NaCl溶液中的水合离子:D.2Cl分子中σ键的形成:【答案】C【解析】【详解】A.NaOH由Na+和OH-构成,电子式为:,故A正确;B.异丙基的结构简式:,故B正确;C.Na+离子半径比Cl-小,水分子电荷情况如图,Cl-带负电荷,水分子在Cl-周围时,呈正电性的H朝向Cl-,水分子在Na+周围时,呈负电性的O朝向Na+,NaCl溶液中的水合离子应为:、,故C错误;D.2Cl分子中的共价键是由2个氯原子各提供1个未成对电子的3p原子轨道重叠形成的p-pσ键,形成过程为:,故D正确;故选C。
A.AB.BC.CD.D【答案】B【解析】【详解】A.被水蒸气轻微烫伤,先用冷水冲洗一段时间,再涂上烫伤药膏,故A正确;-的NaHCO3溶液,故B错误;B.稀释浓硫酸时,酸溅到皮肤上,先用大量的水冲洗,再涂上35%C .苯酚有毒,对皮肤有腐蚀性,常温下苯酚在水中溶解性不大,但易溶于乙醇,苯酚不慎沾到手上,先用乙醇冲洗,再用水冲洗,故C 正确;D .酒精灯打翻着火时,用湿抹布盖灭,湿抹布可以隔绝氧气,也可以降温,故D 正确;故选B 。

钇90含量
钇90含量是指钇元素(Y)中的钇90同位素(^90Y)的含量。
钇90是一种放射性同位素,具有较长的半衰期(约28.8小时)。
它主要用于医学上的放射性治疗,特别是放射性肿瘤治疗。
在治疗过程中,钇90放射性粒子可以直接破坏肿瘤细胞,达到治疗的目的。
钇90通常以放射性粒子的形式通过注射或放置在患处进行治疗。
钇90含量的测定和控制对于放射性治疗的安全和有效非常重要。
高纯度的钇90样品可以通过核反应得到,而其他钇同位素则可以通过分离和提纯过程进行去除。
钇90含量的计量通常以百分比或者放射性活度来表示。
具体的含量要根据实际需要和治疗目的进行确定。

化学用语练习一、写出下列元素符号:氦:____ 氢_____ 氖_____ 氟______ 氯_____ 硫____ 氧___ 磷___ 氮____ 硫____碳___镁____ 钠_____ 铝_____锰_ 汞___ 钙_____ 金___ 钡___ 铂____ 锌___铁____ 碘____ 氩___ 硅____ 钾__ 银____ 铜____二、写出下列离子符号:钾离子_____钠离子____ 氢离子_____镁离子_____钙离子_____银离子_____氯离子_____ 锌离子_____氧离子______铜离子_____铁离子_____亚铁离子_____钡离子______氟离子_____硫离子_____铵根离子______ 硫酸根离子_______硝酸根离子________碳酸根离子______铝离子_____氢氧根离子_______三、化学式的书写氮气______氢气______氧气______氯气______臭氧______水______过氧化氢_______二氧化碳_____ 二氧化硫_______二氧化锰_________四氧化三铁________五氧化二磷________氧化汞________汞__ 铜____铁______锌______氦气______氖气_____ 氯化钠______氯化钾_______氯酸钾________高锰酸钾____________锰酸钾__________碳____ 一氧化碳_____氧化铝________氯化氢______碳酸钙___ 氢氧化钙_______氧化铜_______三氧化硫_____碘化钾______硝酸钠______硝酸铵__________二氧化氮_________一氧化氮_____氨气_____ 氯化银______硝酸______ 硫酸_______碳酸钠_________ 硫酸铜________硫酸亚铁__________氧化镁________ 氢氧化钠_________ 氧化钙________四、物质的组成与构成1.二氧化碳是由__________________组成的,是由_____________构成的,二氧化碳分子是由________________构成的。

1氢H(qīng)欧阳歌谷(2021.02.01)2氦He(hài)3锂Li(lǐ)4铍Be(pí)5硼B(péng)6碳C(tàn)7氮N(dàn)8氧O(yǎng)9氟F(fú)10氖Ne(nǎi)11钠Na(nà)12镁Mg(měi)13铝Al(lǚ)14硅Si(guī)15磷P(lín)16硫S(liú)17氯Cl(lǜ)18氩Ar(yà)19钾K(jiǎ)20钙Cs(gài)21钪Sc(kàng)22钛Ti(tài)23钒V(fán)24铬Cr(gè)25锰Mn(měng) 26铁FE(tiě) 27钴Co(gǔ)28镍Ni(niè)29铜Cu(tóng) 30锌ZN(xīn) 31镓Ga(jiā) 32锗Ge(zhě) 33砷As(shēn) 34硒Se(xī)35溴Br(xiù)36氪Kr(kè)37铷Rb(rú)38锶Sr(sī)39钇Y(yǐ)40锆Zr(gào)41铌Nb(ní)42钼MO(mù) 43锝Tc(dé)44钌Ru(liǎo)45铑Rh(lǎo) 46钯Pd(bǎ) 47银Ag(yín) 48镉Cd(gé) 49铟In(yīn) 50锡Sn(xī) 51锑Sb(tī)52碲Te(dì)53碘I(diǎn) 54氙Xe(xiān) 55铯Cs(sè) 56钡Bs(bèi) 镧系57镧La(lán) 58铈Ca(shì) 59镨Pr(pǔ)60钕Nd(nǚ) 61钷Pm(pǒ) 62钐Sm(shān) 63铕Eu(yǒu) 64钆Gd(gá) 65铽Tb(tè) 66镝Dy(dī)67钬Ho(huǒ) 68铒Er(ěr)69铥Tm(diū) 70镱Yb(yì) 71镥Lu(lǔ) 72铪Hf(hā)73钽Ta(tǎn) 74钨W(wū) 75铼Re(lái) 76锇Os(é)77铱Ir(yī)78铂Pt(bó)79金Au(jīn) 80汞Hg(gǒng) 81铊Tl(tā)82铅Pb(qiān) 83铋Bi(bì)84钋Po(pō) 85砹At(ài)86氡Rn(dōng) 87钫Fr(fāng) 88镭Ra(léi)89锕Ac(ā)90钍Th(tǔ)91镤Pa(pú)92铀U(yóu)93镎Np(ná)94钚Pu(bù)95镅Am(méi) 96锔Cm(jú)97锫Bk(péi)98锎Cf(kāi)99锿Es(āi)100镄Fm(fèi) 101钔Md(mén) 102锘No(nuò) 103铹Lr(láo) 104钅卢Rf(lú) 105钅杜Db(dù) 106钅喜Sg(xǐ) 107钅波Bh(bō) 108钅黑Hs(hēi) 109钅麦Mt(mài) 110钅达Ds(dá) 111钅仑Rg(lún)112Uub Cn113Uut114Uuq115Uup116Uuh117Uus118UuoH He Li Be B (氢氦锂铍硼)C N O F Ne (碳氮氧氟氖)Na Mg Al Si P (钠镁铝硅磷)S Cl Ar K Ca (硫氯氩钾钙)侵害从前,有一个富裕人家,用鲤鱼皮捧碳,煮熟鸡蛋供养着有福气的奶妈,这家有个很美丽的女儿,叫桂林,不过她有两颗绿色的大门牙(哇,太恐怖了吧),后来只能嫁给了一个叫康太的反革命。

八年级化学方程式的专项练习姓名:班级:一、写出下列反应的化学方程式:1、镁在空气中燃烧:______________________ _____2、铁在氧气中燃烧:____________________ _______3、铜在空气中受热:______________ _____________4、铝在空气中燃烧:_________________ __________5、氢气中空气中燃烧:__________ _______________6、红磷在空气中燃烧:_______________ ___ ______7、硫粉在空气中燃烧:__________________ _______8、碳在氧气中充分燃烧:______________________ _ _9、铁生锈:____________________________________10、葡萄糖缓慢氧化(呼吸作用):___________________________ _____11、水在直流电的作用下分解:_______________________________________________12、澄清石灰水通入二氧化碳:_______________________________________________13、氢氧化钠溶液和硫酸铜溶液反应:_________________________________________14、利用过氧化氢和二氧化锰的混合物制氧气:_________________________________15、加热氯酸钾:___________________________________________________________16、加热高锰酸钾:_________________________________________________________二、配平下列化学方程式:(一) 最小公倍数法:(找出式子两边的化学式中同种原子的个数最多的原子,然后求最小公倍数,得原子个数。

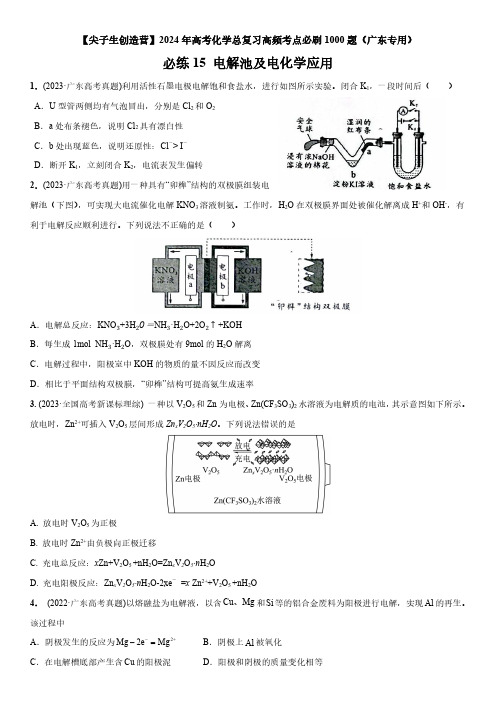
【尖子生创造营】2024年高考化学总复习高频考点必刷1000题(广东专用)必练15电解池及电化学应用1.(2023·广东高考真题)利用活性石墨电极电解饱和食盐水,进行如图所示实验。
闭合K 1,一段时间后()A .U 型管两侧均有气泡冒出,分别是Cl 2和O 2B .a 处布条褪色,说明Cl 2具有漂白性C .b 处出现蓝色,说明还原性:Cl ->I -D .断开K 1,立刻闭合K 2,电流表发生偏转2.(2023·广东高考真题)用一种具有“卯榫”结构的双极膜组装电解池(下图),可实现大电流催化电解KNO 3溶液制氨。
工作时,H 2O 在双极膜界面处被催化解离成H +和OH -,有利于电解反应顺利进行。
下列说法不正确的是()A .电解总反应:KNO 3+3H 2=NH 3·H 2O+2O 2↑+KOHB .每生成1mol NH 3·H 2O ,双极膜处有9mol 的H 2O 解离C .电解过程中,阳极室中KOH 的物质的量不因反应而改变D .相比于平面结构双极膜,“卯榫”结构可提高氨生成速率3.(2023·全国高考新课标理综)一种以V 2O 5和Zn 为电极、Zn(CF 3SO 3)2水溶液为电解质的电池,其示意图如下所示。
放电时,Zn 2+可插入V 2O 5层间形成Zn x V 2O 5·nH 2O 。
下列说法错误的是A.放电时V 2O 5为正极B.放电时Zn 2+由负极向正极迁移C.充电总反应:x Zn+V 2O 5+nH 2O=Zn x V 2O 5·n H 2OD.充电阳极反应:Zn x V 2O 5·n H 2O-2xe -=x Zn 2++V 2O 5+nH 2O4.(2022·广东高考真题)以熔融盐为电解液,以含Cu Mg 、和Si 等的铝合金废料为阳极进行电解,实现Al 的再生。
该过程中A .阴极发生的反应为2+Mg 2e Mg --=B .阴极上Al 被氧化C .在电解槽底部产生含Cu 的阳极泥D .阳极和阴极的质量变化相等5.(2022·广东高考真题)科学家基于Cl 2易溶于CCl 4的性质,发展了一种无需离子交换膜的新型氯流电池,可作储能设备(如图)。

一、选择题1.化学与生活密切相关。
下列叙述正确的是A.漂白粉与盐酸可混合使用以提高消毒效果 B.温室气体是形成酸雨的主要物质C.棉花、麻和蚕丝均为碳水化合物 D.干冰可用在舞台上制造“云雾”【答案】D 【解析】【详解】A .漂白粉的有效成分次氯酸钙与盐酸混合,会发生氧化还原反应生成有毒的氯气,两者不能混合使用,A 错误;B .温室气体主要是指二氧化碳,二氧化碳不是形成酸雨的主要物质,形成酸雨的主要物质是硫氧化物、氮氧化物等,B 错误;C .棉花、麻来源于植物,主要成分均是纤维素,为碳水化合物,但蚕丝来源于动物,主要成分是蛋白质,蛋白质不是碳水化合物,C 错误;D .干冰是固态的二氧化碳,干冰升华时,吸收大量的热,使周围温度降低,大量的水蒸气凝结成了小液滴,形成“云雾”效果,D 正确;答案选D 。
2.辅酶10Q 具有预防动脉硬化的功效,其结构简式如下。
下列有关辅酶10Q 的说法正确的是A.分子式为60904C H O B.分子中含有14个甲基C.分子中的四个氧原子不在同一平面D.可发生加成反应,不能发生取代反应【答案】B 【解析】【详解】A .由该物质的结构简式可知,其分子式为C 59H 90O 4,A 错误;B .由该物质的结构简式可知,键线式端点代表甲基,10个重复基团的最后一个连接H 原子的碳是甲基,故分子中含有1+1+1+10+1=14个甲基,B 正确;C .双键碳以及与其相连的四个原子共面,羰基碳采取sp 2杂化,羰基碳原子和与其相连的氧原子及另外两个原子共面,因此分子中的四个氧原子在同一平面上,C 错误;D.分子中有碳碳双键,能发生加成反应,分子中含有甲基,能发生取代反应,D错误;答案选B。
3.能正确表示下列反应的离子方程式为A.硫化钠溶液和硝酸混合:S2-+2H+=H2S↑B.明矾溶液与过量氨水湿合:Al3++4NH3+2H2O=AlO2-+4NH4+C.硅酸钠溶液中通入二氧化碳:SiO23-+CO2+H2O=HSiO3-+HCO3-D.将等物质的量浓度的Ba(OH)2和NH4HSO4溶液以体积比1∶2混合:Ba2++2OH-+2H++SO24-=BaSO4↓+2H2O【答案】D【解析】【详解】A.硝酸具有强氧化性,可以将S2-氧化为S单质,自身根据其浓度大小还原为NO或NO2,反应的离子方程式为4H++2NO3-+S2-=S↓+2NO2↑+2H2O(浓)或8H++2NO3-+3S2-=3S↓+2NO+4H2O(稀),A错误;B.明矾在水中可以电离出Al3+,可以与氨水中电离出的OH-发生反应生成Al(OH)3,但由于氨水的碱性较弱,生成的Al(OH)3不能继续与弱碱发生反应,故反应的离子方程式为Al3++3NH3·H2O=Al(OH)3↓+3NH4+,B错误;C.硅酸的酸性小于碳酸,向硅酸钠溶液中通入二氧化碳时,生成硅酸沉淀,二氧化碳则根据其通入的量的多少反应为碳酸根或碳酸氢根,反应的离子方程式为SiO23-+H2O+CO2=H2SiO3↓+CO23-(CO2少量)或SiO23-+2H2O+2CO2=H2SiO3↓+2HCO3-(CO2过量),C错误;D.将等物质的量浓度的Ba(OH)2与NH4HSO4溶液以体积比1:2混合,Ba(OH)2电离出的OH-与NH4HSO4电离出的H+反应生成水,Ba(OH)2电离出的Ba2+与NH4HSO4电离出的SO24-反应生成BaSO4沉淀,反应的离子方程为为Ba2++2OH-+2H++SO24-=BaSO4↓+2H2O,D正确;故答案选D。

浙教版科学九年级上册“期末提分”高频考点过关(三十一)酸碱盐(6)1.已知:CaCO3+CO2+H2O═Ca(HCO3)2,且Ca(HCO3)2易溶于水。
按如图进行实验,下列图象正确的是()2.氢氧化铯是一种可溶性碱,其分子式是CsOH,则下列叙述中正确的是()A. CsOH溶液能使紫色的石蕊变成红色B. CsOH在水中的电离方程式为:CsOH = Cs2++2OH-C. CsOH溶液能使无色的酚酞试液变红色D. CsOH与硫酸反应生成的盐的分子式为CsSO43.对下列实验过程的评价,不正确的是()A. 某固体加入稀盐酸,产生无色气体,该固体可能含有CO32-B. 某无色溶液滴入酚酞试液显红色,该溶液一定是碱性溶液C. 某溶液中滴加BaCl2溶液产生不溶于稀HNO3的白色沉淀,该溶液中不一定含有SO42-D. 验证烧碱部分变质,先加少量氯化钡溶液产生白色沉淀,再加无色酚酞溶液呈红色4.如图所示已平衡的天平两端放着两个分别盛有浓盐酸和浓硫酸的敞口烧杯,过一段时间后,天平会()A. 左端下沉B. 右端下沉C. 仍平衡D. 无法判断5.小刚同学用如图所示装置进行“粒子不断运动”的研究,一段时间后,可观察到无色酚酞试液变红,则物质X是()A. 浓氨水B. 浓盐酸C. 浓硫酸D. 浓食盐水6.如图“五环旗”的上面3个环代表一种液体,下面2个环各代表一种酸碱指示剂,两环相交部分表示指示剂跟有关液体混合后显示的颜色,如图表示相交部分显示的颜色,其中显示颜色不正确的是()A. 红色B. 蓝色C. 红色D. 蓝色7.下列检测某溶液pH的操作正确的是()A. 将pH试纸投入待测液,对照标准比色卡读数B. 用干燥、洁净的玻璃棒蘸取少量待测液,沾在置于洁净表而皿的pH试纸上,根据试纸呈现颜色,对照标准比色卡读数C. 用玻璃棒蘸取待测液沾在用蒸馏水润湿的pH试纸上。
对照标准比色卡读数D. 用蒸馏水冲洗玻璃棒,蘸取待测液沾在pH试纸上,对照标准比色卡读数8.根据下列各组提供的试剂,判断不能发生反应的一组是()A. Na2SO4溶液和Ba(NO3)2溶液B. NaOH溶液和稀硫酸C. KNO3溶液和CaCl2溶液D. Na2CO3溶液和稀盐酸9.下列反应属于酸碱反应的是()A. Cu(OH)2+2HNO3=Cu(NO3)2+2H2OB. CO2+H2O=H2CO3C. 2KMnO4=ΔK2MnO4+MnO2+O2↑D. HCl+AgNO3= AgCl↓+HNO310.一些物质在常温下的近似pH如下表:下列有关上述四种物质的说法中正确的是()A. 只有葡萄汁显酸性B. 只有血浆显碱性C. 正常雨水显中性D. 胃酸过多的人应多饮用葡萄汁11.下列各组物质的溶液,不用其他试剂,只用观察和组内物质的溶液相互混合的方法,就能将它们一一鉴别出来的是()①NaCl、BaCl2、CuSO4、NaOH、NH4NO3②Ba(NO3)2、NaCl、Na2SO4、H2SO4、HCl③NaOH、FeCl3、MgSO4、BaCl2、KCl ④AgNO3、HCl、K2CO3、NaCl、BaCl2A. ①②④B. ①②③C. ①③④D. ②④12.下列实验,其现象足以说明结论的是()13.向一定质量的稀硫酸中逐滴加入氢氧化钡溶液,直至过量。

初三化学中考化学复习:计算题单元测试提优卷试题(1)一、选择题1.将某赤铁矿石样品10g 放入盛有适量稀盐酸的烧杯中,恰好完全反应,反应后烧杯中物质的总质量为114.5g ,过滤后将固体洗涤、干燥,称其质量为2g 。
(杂质不溶于水也不反应)求:⑴赤铁矿石样品中氧化铁的质量分数; ⑵稀盐酸的溶质质量分数.答案:(1)80%(2)10.5% 【解析】 【分析】 【详解】(1)赤铁矿石样品中氧化铁的质量为10g−2g=8g 赤铁矿石样品中氧化铁的质量分数为×100%=80% 答:赤铁矿石样品中氧化铁的质量分解析:(1)80%(2)10.5% 【解析】 【分析】 【详解】(1)赤铁矿石样品中氧化铁的质量为10g−2g=8g 赤铁矿石样品中氧化铁的质量分数为8g10g×100%=80% 答:赤铁矿石样品中氧化铁的质量分数为80%。
(2)解:设参加反应的稀盐酸中的溶质质量为y2332Fe O 6HCl 2FeCl +=+160216H O98g y160:219=8g :y y =10.95g稀盐酸的溶质质量分数为10.95g114.5g-10g×100%≈10.5%答:稀盐酸的溶质质量分数为10.5%。
2.请你参与配制一定溶质质量分数的氢氧化钠溶液,并进行有关计算。
(1)要将100g 40%的氢氧化钠溶液稀释成10%的稀溶液,需加水_____________g 。
(2)量取水时若仰视读数,会使得到的稀氢氧化钠溶液质量分数____________。
(填“偏大”“偏小”或“不变”)(3)将一定质量的CO 2通入200g10%的氢氧化钠溶液中,最多能生成的碳酸钠的质量是____g 。
答案:偏小 26.5【解析】(1)根据溶液配制过程中,溶质的质量保持不变解答;(2)根据用量筒读数时,要使视线与液体凹液面的最低处保持水平,仰视或俯视都会造成读数不准确解答;(3)根据反应的化学方程式解析:偏小 26.5【解析】(1)根据溶液配制过程中,溶质的质量保持不变解答;(2)根据用量筒读数时,要使视线与液体凹液面的最低处保持水平,仰视或俯视都会造成读数不准确解答;(3)根据反应的化学方程式计算解答。

更多免费资料请接见:教育百科一般化学三基试题库pthxⅠ名词解说pthxⅠ-1 波函数能级:pthxⅠ-2 原子轨道:pthxⅠ-3 电子云:pthxⅠ-4 障蔽效应:pthxⅠ-5 障蔽常数:pthxⅠ-6 简并轨道:pthxⅠ-7 电离能:pthxⅠ-8 电子亲和能:pthxⅠ-9 电负性:pthxⅠ-10 离子键:pthxⅠ-11 共价键:pthxⅠ-12 杂化:pthxⅠ-13 杂化轨道:pthxⅠ-14 极化:pthxⅠ-15 取向力:pthxⅠ-16 引诱力:pthxⅠ-17 色散力:pthxⅠ-18 范德华力:pthxⅠ-19 蒸气压pthxⅠ-20 沸腾:pthxⅠ-21 沸点:pthxⅠ-22 物质的量浓度:pthxⅠ-23 质量摩尔浓度:pthxⅠ-24 摩尔分数:pthxⅠ-25 质量分数:pthxⅠ-26 稀溶液的通性:pthxⅠ-27 浸透压:pthxⅠ-28 活度:pthxⅠ-29 胶体分别系:pthxⅠ-30 Tyndall现象:pthxⅠ-31 Brown运动:pthxⅠ-32 电泳:pthxⅠ-33 聚沉:pthxⅠ-34 表面活性剂:pthxⅠ-35 乳浊液:pthxⅠ-36 反响速率:pthxⅠ-37 均匀速率和刹时速率:pthxⅠ-38 基元反响:pthxⅠ-39 决速步骤:pthxⅠ-40 反响机理:pthxⅠ-41 速率方程:pthxⅠ-42 质量作用定律:pthxⅠ-43 反响级数:pthxⅠ-44 活化分子:pthxⅠ-45 活化能:pthxⅠ-46 催化剂:pthxⅠ-47 状态和状态函数:pthxⅠ-48 过程和门路:pthxⅠ-49 热力学第必定律:pthxⅠ-50 热和功:pthxⅠ-51 热化学:pthxⅠ-52 化学反响的反响热:pthxⅠ-53 热力学能:pthxⅠ-54 焓:pthxⅠ-55 盖斯定律:pthxⅠ-56 可逆反响:pthxⅠ-57 化学均衡:pthxⅠ-58 化学均衡定律:pthxⅠ-59 吕·查德里原理:pthxⅠ-60 共轭酸碱对:pthxⅠ-61 稀释定律:pthxⅠ-62 同离子效应:pthxⅠ-63 盐效应:pthxⅠ-64 缓冲溶液:pthxⅠ-65 缓冲溶液的缓冲容量:pthxⅠ-66 积淀溶解均衡:pthxⅠ-67 溶度积常数:pthxⅠ-68 溶解度:pthxⅠ-69 分步积淀:pthxⅠ-70 积淀的转变:pthxⅠ-71 氧化复原反响:pthxⅠ-72 自氧化复原反响:pthxⅠ-73 歧化反响:pthxⅠ-74 氧化数:pthxⅠ-75 氧化复原电对:pthxⅠ-76 原电池:pthxⅠ-77 电极反响:pthxⅠ-78 原电池的电动势:pthxⅠ-79 标准氢电极:pthxⅠ-80 标准电极电势:pthxⅠ-81 标准电势图:pthxⅠ-82 配位化合物:pthxⅠ-83 配位体:pthxⅠ-84 配位原子:pthxⅠ-85 配位数:pthxⅠ-86 单齿配体和多齿配体:pthxⅠ-87 螯合物:pthxⅠ-88 外轨型配合物:pthxⅠ-89 内轨型配合物:pthxⅠ-90 高自旋配合物:pthxⅠ-91 低自旋配合物:pthxⅡ简答题pthxⅡ-1 请指出4个量子数的取值范围和意义?pthxⅡ-2 量子力学中原子轨道的观点与波尔理论中的有什么不一样?pthxⅡ-3 基态原子核外电子排布原理是什么?pthxⅡ-4 阐述原子构造与周期表的关系。

第一章 习题一、填空题1.稀溶液的依数性包括 蒸气压下降 , 沸点升高 , 凝固点降低 , 渗透现象 。
2.引起溶胶聚沉的诸多因素中,最重要的是 电解质的聚沉作用 。
3.在15℃和97 kPa 压力下,15 g 氮气所占有的体积为 13 升。
4.在20℃和97 kPa 压力下,0.842 g 某气体的体积是0.400 L ,这气体的摩尔质量是 52.89 g •mol -1 。
5.试比较下列溶液的沸点:0.1 mol •L -1蔗糖水溶液 < 0.1 mol •L -1NaCl 水溶液 < 0.1 mol •L -1Na 2SO 4水溶液。
6.试比较下列溶液的凝固点:0.1 mol •L -1蔗糖水溶液 = 0.1 mol •L -1甲醇水溶液 = 0.1 mol •L -1苯甲醇水溶液。
7.试比较下列溶液的渗透压:0.1 mol •L -1蔗糖水溶液 < 0.1 mol •L -1NaCl 水溶液 < 0.1 mol •L -1Na 2SO 4水溶液。
二、选择题1.下列溶液性质中哪一种不是依数性? ( D ) A. 凝固点 B. 沸点 C. 渗透压 D. 颜色2.在容易聚沉的溶胶中加入适量的大分子物质溶液,以使溶胶的稳定性大大增加,这叫做什么作用? ( B )A. 敏化作用B. 保护作用C. 加聚作用D. 聚沉作用3.等体积:0.1 mol •L -1KI 和:0.1 mol •L -1AgNO 3溶液混合制成的AgI 溶胶,下列电解质中,聚沉能力最强的是 ( C )A. Na 2SO 4B. MgSO 4C. FeCl 3D. K 3[Fe(CN)6]4.溶胶的基本特征之一是 ( D ) A. 热力学上和动力学上皆稳定的系统 B. 热力学上和动力学上皆不稳定的系统 C. 热力学上稳定而动力学上不稳定的系统 D. 热力学上不稳定和动力学上稳定的系统5.25℃时,0.01mol•kg -1的糖水的渗透压为∏1,而0.01mol•kg -1的尿素水溶液的渗透压为∏2,则 ( C )A. ∏1<∏2B. ∏1>∏2C. ∏1=∏2D. 无法确定6.当AgNO 3的稀溶液与KI 的稀溶液作用时,若 AgNO 3过量时,此溶胶( B ) A. 不带电 B. 带正电 C. 带负电 D. 无法确定7.加入下列哪一种溶液,能使As 2S 3胶体溶液凝聚最快 ( A ) A. Al 2(SO 4)2 B. CaCl 2 C. Na 3PO 4 D. MgCl 28.当不挥发性溶质溶于溶剂形成稀溶液后,则 ( A ) A. 溶剂蒸气压降低 B. 溶液的蒸气压升高C. 溶液的蒸气压不变D. 溶液的蒸气压可能升高也可能降低 三、是非题1.真实气体在低温高压下可以近似地看作理想气体。

江苏省南通市如皋磨头中学2021年高一化学下学期期末试卷含解析一、单选题(本大题共15个小题,每小题4分。
在每小题给出的四个选项中,只有一项符合题目要求,共60分。
)1. 锎(25298Cf)是医学上常用作治疗恶性肿瘤的中子源,1mg锎(25298Cf)每秒约放出2.34×109个中子。
下列有关锎元素的说法错误的是A.25298Cf原子中,中子数为154 B.25298Cf原子中,质子数为98C.25298Cf原子中,电子数为98 D.锎元素的相对原子质量为252参考答案:D略2. 下列氢化物中最稳定的是()A. PH3B. SiH4C. HClD. HF参考答案:D略3. 短周期元素甲、乙、丙、丁的原子序数依次增大,甲和乙形成的气态化合物的水溶液呈碱性,乙位于第VA族,甲与丙同主族,丁原子最外层电子数和电子层数相等,则正确的是()A.原子半径:丙>丁>乙 B.单质的还原性:丁>丙>甲C.甲、乙、丙的氧化物均为共价化合物D.乙、丙、丁的最高价氧化物对应的水化物能相互反应参考答案:AD略4. 下列叙述中正确的是()A.在元素周期表中,零族元素的单质在常温下全部都是气体B.同周期元素,ⅦA族的原子半径最大C.ⅥA族元素的原子,其半径越大,越容易失去电子D.所有主族元素的原子形成单原子离子时的最高化合价数都和它的族序数相等参考答案:C随着相对原子质量的增大,稀有气体单质可以是液态或固体。
同周期元素自左向右原子半径是增大的,所以同周期元素中第IA族的原子半径最大。
同主族元素自上而下原子半径逐渐增大,原子核对外层电子的吸引力逐渐减弱,所以金属性逐渐增强,非金属性逐渐减弱。
F元素没有正价,O元素没有最高化合价,所以选项D是错误的。
5. 一定条件下,可逆反应2A B+3C,在下列四种状态中,处于平衡状态的是() 选项正反应速率逆反应速率A v A=2 mol·L-1·min-1v B=2 mol·L-1·min-1B v A=2 mol·L-1·min-1v C=2 mol·L-1·min-1C v A=1 mol·L-1·min-1v B=2 mol·L-1·min-1D v A=1 mol·L-1·min-1v C=1.5 mol·L-1·min-1参考答案:D化学反应到达平衡时,同一物质的正逆反应速率相等;A.A物质的正反应速率υA=2mol/(l·min),逆反应速率υB=2mol/(l·min),则逆反应速率υA=4mol/(l·min),A的正逆反应速率不相等,所以该反应未达到平衡状态,故A错误;B.同一反应中,各物质的反应速率之比等于计量数之比,A物质的正反应速率是2mol/(L·min),C的逆反应速率为2mol/(L·min),A的逆反应速率为mol/(L°·min),所以A的正逆反应速率不等,故B 错误;C.同一反应中,各物质的反应速率之比等于计量数之比,A物质的正反应速率是1 mol/(L·min),B的逆反应速率为2mol/(L·min),A的逆反应速率为4mol/(L·min),所以A的正逆反应速率不等,故C错误;D.同一反应中,各物质的反应速率之比等于计量数之比,A物质的正反应速率是 1 mol/(L·min),C的逆反应速率为1.5mol/(L·min),A的逆反应速率为1mol/(L·min),所以A的正逆反应速率相等,故D正确;故选D。

ka kh kb kw化学表达式
ka, kh, kb, 和kw 是化学常数,它们通常用于描述酸碱反应和溶解度等化学过程中离子的活性程度。
ka代表酸解离常数,它是描述弱酸溶液中酸性离子解离的程度的常数。
它的值越大,说明酸解离得越强,溶液的酸性就越强。
例如,苯甲酸的ka值为6.4×10^-5,说明它是弱酸。
kh代表碱解离常数,它是描述弱碱溶液中碱性离子解离的程度的常数。
与ka类似,kh的值越大,说明碱解离得越强,溶液的碱性就越强。
kb代表碱解离常数,它与kh非常相似,区别在于kh是针对弱碱的,而kb是针对弱酸的。
它描述的是弱酸溶液中碱性离子解离的程度。
kw代表水的离子积常数,它描述了水分子自离子化产生的氢离子(H+)和氢氧根离子(OH-)的浓度乘积。
在常温常压下,Kw的值为1.0×10^-14。
这个常数在酸碱反应中非常重要,因为它可以用于计算溶液中氢离子和氢氧根离子的浓度。

“KH”计算公式可能指的是水族箱水的碳酸盐硬度(KH),这是衡量水抵抗pH 值变化能力的指标。
高KH 值表明水具有较大的缓冲pH 值变化的能力,而低KH 值则表明水容易发生快速的pH 值波动。
计算KH 的公式不是标准的,可能取决于所用测试套件的类型和测量单位。
但是,一个常用的公式是:
KH (dKH) = (滴定体积(ml) * 0.02) / 测试水的体积(L)
在此公式中,滴定体积(以毫升为单位)是将给定体积的水的pH 值降低0.3 个单位所需的酸量。
测试的水量(以升为单位)是水族箱中的水量。
结果以碳酸盐硬度(dKH) 表示。
请务必注意,此公式只是一个估计值,可能并不适用于所有测试套件或水样。
为获得更准确的结果,建议遵循测试套件制造商提供的说明。
英语四级怎么准备,90%的人都不知道
英语四级考试每年都会有两次,分别是在每年的6月和12月份进行,在难度上来说总的是高于高考英语难度的,要是基础好的话,那多练些真题轻松过是没有问题的,要是基础不好的话那就还得下一番功夫,今天就给大家一下英语四级怎么准备的一些建议和方法吧!
1.文章中记忆单词,更容易
对于单词复习了这么久,还总是记不住,只能说明你的复习方法效率稍微有点差。
你可能还没有消化掉你所学到的词汇记忆法,因此不能很好的掌握单词。
其实方法没有好不好,只有适不适合自己。
我基础不好,当时用的是真替语境学习单词的方法。
都没有买其它的书,用的是巨微英语《四级真题/逐句精解》这本真题资料,个人觉得死记硬背太痛苦了。
这本书比较适合我的原因在于它解析详细,我可以一边用它学习单词,一边练习提升我的阅读能力。
我大概每天花费在单词上的时间和精力有一个小时,建议大家不要花费太多时间,不然不划算。
2.考前30天,如何选择练习题
时间充足,有余力的人可以去看看美剧什么的,适当调节的同时还能锻炼你的听力。
像星火和华研附带有的模拟题,预测题就不要做了,最好是进行真题的训练,真题为主,注意好时间的分配。
选择至少近四年的真题,好好安排每天练习的数量和时间,争取把真题都吃透练烂。
我为了提升自己的阅读水平,还买了一本大学英
语四级真题·汇编王,书中大约有18套历年真题资料,可以拿来好好的进行练习。
每天练习一套真题,遇到不会的题目,可以查阅巨微英语土豪金送的满分并大大总结的小册子,从而让自己的阅读水平大步提升。
考前大家可以适当的练习真题,找找考试的感觉,对错不重要,注意分配时间,速度和过程中的自我调节。
3.做阅读题主意用彩色的笔标注
建议大家完整做完一套真题后,就是用彩色笔在原文中标记出答案出处,然后大家需要注意这几个问题:
●看下每个题目都固定在那一段落出题,且是段落的那个位置。
●近几年都会考什么题型的题
●每个题型所对应的解题方法是什么
●原文结构是否明白,中心是否突出
●作者用的写作手法是什么
●文章还有没有难词或难句子
下面是英语四级怎么准备的5点小建议:
1.单词学习真的很重要,单词的学习方法有很多,比如说下载APP记单词,比较好用的有百词斩、拓词、知米等等,可以方便自己随时学习。
2.语法知识要快速掌握,就不要买语法书了,学习来是多么的枯燥无味。
我个人感觉利用真题语境法学习是很不错的,高效且不会很
无趣。
3.听力复习还是要多听的,其次就是多练。
多听的方式多了去了,比如说下载真题听力(可以去“零元课”网站),多听听BBC/VOA,还有多看美剧/美国电影,或者说多听英文歌曲……
4.阅读主要是多练习。
建议每天练习一篇,复习的时候严格按照时间做题(巨微英语土豪金),然后对照答案,书中送的小册子可以顺便研究学习做题技巧。
5.写作的复习很简单,我觉得只要背模板就好。
或者说可以学习范文的思路。
再就是多多积累素材哦!一般的方法是在做阅读的时候积累,或者说你也可以在读外刊或报纸时积累啦!。