高一化学气体摩尔体积知识点梳理及专项训练
- 格式:doc
- 大小:502.38 KB
- 文档页数:16

第2课时气体摩尔体积基础过关练题组一影响气体体积的因素1.(2021江苏常州第一中学高一上期中)气体的体积主要由以下什么因素决定( )①气体分子的直径②气体物质的量的多少③气体分子间的平均距离④气体分子的相对分子质量A.①②B.①③C.②③D.②④2.(2021江苏无锡江阴四校高一上期中)相同物质的量的不同气体,若其体积不相同,则主要原因是( )A.粒子质量不同B.粒子大小不同C.粒子间距离不同D.粒子的数目不同题组二气体摩尔体积3.(2020广东云浮高一上期末)标准状况下,下列物质中体积最大的是( )A.44.8 L H2OB.3.01×1023个CO2C.0.6 mol CH4D.6 g H24.(2021山西祁县中学高一上月考)下列物质中所含分子物质的量最大的是( )A.88 g CO2B.3.01×1023个硫酸分子C.3.5 mol H2D.标准状况下33.6 L SO2题组三气体的体积与物质的量、微粒数目及质量之间的相互换算5.等质量的CH4和NH3相比较,下列结论错误的是( )A.它们的分子个数之比为17∶16B.它们的原子个数之比为17∶16C.它们的氢原子个数之比为17∶12D.同温同压下两种气体的体积之比是17∶166.相等物质的量的一氧化碳和二氧化碳相比较,下列有关叙述中正确的是 ( )①它们所含的分子数目之比为1∶1②它们所含的氧原子数目之比为1∶2③它们的体积之比为1∶1④它们所含的碳原子数目之比为1∶1⑤它们所含的电子数目之比为7∶11A.①④⑤B.②③⑤C.①②④⑤D.①②③④⑤7.(2021湖北武汉高一上期中)如图表示1 g O2和1 g X气体在相同容积的密闭容器中压强(p)与温度(T)的关系,则X气体可能是( )A.C2H4B.CO2C.HClD.SO2题组四阿伏加德罗定律及其应用8.(2020河南许昌第三高级中学高一上期末)三个相同的恒温恒容密闭容器中分别盛有等质量的H2、CH4、O2。

高一化学气体摩尔体积知识点
嘿,同学们!今天咱就来聊聊高一化学超级重要的气体摩尔体积这个知识点呀!比如说咱平常吹气球,那气球能吹多大,和气体摩尔体积可大有关系呢!
你想啊,气体摩尔体积就好像是气体们的一个“小团体标准”。
咱可以把气体想象成一群调皮的小精灵,它们到处乱跑,占的空间也不太一样。
但有了气体摩尔体积,咱就有个统一的标准来衡量它们啦。
就好比不同的小精灵都有了自己的“帮会规则”一样!比如,在标准状况下,1 摩尔任何气体所占的体积都约是升呢。
你说神奇不神奇?
咱再想想看哦,为啥同样是 1 摩尔的氧气和 1 摩尔的氢气,它们体积差不多呢?这就是气体摩尔体积在起作用呀!这就像是不同班级的同学,都要遵守学校的统一规定一样。
所以呀,大家一定要好好理解这个知识点,它可是在好多化学问题里都超级重要的呢!咱得把这个“小精灵帮会规则”搞得清清楚楚的,才能在化学的世界里畅游无阻呀!结论就是:气体摩尔体积是高一化学中超关键的知识点,一定要掌握好哟!。


第二节 气体摩尔体积知识归纳知识归纳学法建议1.“有比较才会有鉴别”,比较物质在气、液、固三种不同物态下的体积影响因素中的主要矛盾,主要影响因素有三条:(1)粒子数的多少;(2)粒子本身的大小;(3)粒子与粒子之间的平均距离。
2.固体或液体粒子之间的距离相对于粒子本身的大小小到可以忽略;气体粒子间距离在通常情况下为其本身直径的10倍,气体体积主要取决于气体粒子间平均距离,而气体粒子间平均距离取决于其所在温度、压强。
3.气体摩尔体积为温度与压强的函数。
温度、压强一定,气体摩尔体积的数值即定。
例如在0℃、1.01×105Pa 下,V m =22.4 L/mol 。
4.阿伏加德罗定律的核心为分子间距离与粒子数或分子数、温度、压强的关系;阿伏加德罗定律还表现为不同的数学表达式,这不过是不同的数学转换而已,如下式:21212121ρρ===M M n n V V (T 、P 不变) 潜能开发[例1]下列叙述中,不正确的是 ( )A.在标准状况下,1 molH 2O 体积约是22.4 LB.在标准状况下,0.5mol H 2、0.5 mol N 2组成的混合气体的体积约为22.41。
C.在非标准状况下,1mol 任何气体的体积不可能约为22.4LD.在同温同压下,气体分子间平均距离几乎相等思路分析气体体积大小相关量为气体物质的量(粒子个数)、粒子间平均距离(温度、压强),相对来说,粒子本身的大小则是影响气体体积的次要因素。
气体摩尔体积址个严密定义,必须明确其内容才能正确无误地运用。
气体摩尔体积:(1)气体、非液体、非固体但可以是混合气体;(2)标准状况(STP);(3)气体体积标况近似值;(4)约22.4L/mol 。
在此基础上涉及有关气体体积的计算则显得有据可依。
[答案] AC思维诊断学生因对气体摩尔体积概念的理解不全面而错选。
气体摩尔体积是个从属于物质的量、阿伏加德罗常数的概念。
但又是一个相对独立而完整的概念。

气体摩尔体积概念巩固一.摩尔体积1. 定义:符号:单位:数学表达式:适用范围:物质的体积,指一定量的物质在一定条件下所占据空间的大小。
从微观的角度去分析,物质的体积的大小决定因素有:①物质的体积的大小②③由上述可知气体的摩尔体积只与和。
理解上述概念,注意以下要点:(1)标准状况:指0℃、1.01×105 Pa的状态。
(2)“单位物质的量的气体”即“1mol任何气体”。
(3)1mol任何气体的体积在标准状况下都约为22.4L,在非标准状况下,其体积也可能为22.4L,可能不为22.4L。
(一). 选择题:1. 下列物质在常温、常压下,各取0.1mol,其体积最大的是()A. 原子半径为0.152nm的金属锂B. 原子半径为0.227nm的金属钾C. 原子半径为0.158nm的硫原子D. 原子半径为0.128nm的金属铜2. 决定一定量气体的体积大小和主要因素是()A. 气体分子的大小B. 气体分子的相对分子质量C. 气体分子间的平均距离D. 气体分子的数目3. 标准状况下,若两种气体所占的体积不同,其原因是()A. 气体性质不同B. 气体分子的大小不同C. 气体分子间平均距离不同D. 气体的物质的量不同(二). 判断正误:1. 温度为0℃,压强为505kPa时,CO2的气体摩尔体积为22.4L/mol ()2. 标准状况下,一定量的任何气体体积都约为22.4L ()3. 标准状况下,1molH2O的体积约为22.4L()4. 当温度高于0℃时,1mol任何气体体积都大于22.4L()5. 相同条件下,1molCO 和1molCO 2所含分子数相同,体积也相同()(三)、有关气体摩尔体积的计算:例题1:在标准状况下,3.2gSO 2的体积是多少?例题2:在标准状况下,测得0.88g 某气体的体积为448mL.计算此气体的相对分子质量。
例题3:标况下,2.24LH 2与2L 氧气反应生成多少mol 水?2、阿伏加德罗定律及其应用阿伏加德罗定律:同温同压下:212121N N =n n =V V ②、推论:同温同压下:212121Mr Mr =M M =ρρ 同温同体积下:212121N N =n n =P P Ⅰ、气体休的密度和相对密度: 标况下:1-L •g 4.22Mr =mol•.4L 22M =)(ρ气体 A 气体对B 气体的相对密度:)B (M )A (M =)B (ρ)A (ρ=)B (D Ⅱ、摩尔质量M (或平均摩尔质量M —)M=22.4L ·mol -1×ρ,•••+)B (n +)A (n •••+)B (M •)B (n +)A (M •)A (n =M — M —=M(A)ф(A)+M(B)ф(B)+···ф为体积分数。

第一章从实验学化学第二节化学计量在实验中的应用第2课时气体摩尔体积易错点一气体摩尔体积1.下列叙述中正确的是A.一定温度、压强下,气体体积由其分子的大小决定B.一定温度、压强下,气体体积由其物质的量的多少决定C.气体摩尔体积是指1 mol任何气体所占的体积为22.4 LD.不同的气体,若体积不等,则它们所含的分子数一定不等【答案】B【解析】决定气体体积大小的主要因素是气体分子数目的多少和气体分子间的距离。
一定温度、压强下,气体体积之比等于其物质的量之比,故A项错误,B项正确;说明某气体的摩尔体积时必须指明所处状况,C项错误;不同的气体,若体积不等,但在不同的特定温度和压强下,它们所含的分子数也可能相等,D项错误。
2.下列叙述中,正确的是A.摩尔是国际单位制七个基本物理量之一B.在标况下,1 mol任何物质的体积都约是22.4 LC.25℃和101 kPa的条件下,气体的摩尔体积大于22.4 L/molD.22.4 L气体所含的分子数一定大于11.2 L气体所含的分子数【答案】C【解析】A.摩尔是物质的量的单位,物质的量是国际单位制七个基本物理量之一,故A错误;B.在标况下,1 mol气体物质的体积约是22.4 L,固体和液体的体积不是22.4 L,故B错误;C、气体摩尔体积是1 mol气体在一定温度和压强下的体积,单位为L/mol,25 ℃和101 kPa的条件下,气体的摩尔体积大于22.4 L/mol,故C正确;D.未注明温度和压强,气体摩尔体积不确定,不能计算气体的物质的量,也不能判断气体分子数目的关系,故D错误;故选C。
3.下列说法正确的是①标准状况下,6.02×1023个分子所占的体积约是22.4 L②0.5 mol H2所占体积为11.2 L③标准状况下,1 mol H2O的体积为22.4 L④常温常压下,28 g CO与N2的混合气体所含的原子数为2N A⑤各种气体的气体摩尔体积都约为22.4 L·mol−1⑥标准状况下,体积相同的气体的分子数相同A.①③⑤B.④⑥C.③④⑥D.①④⑥【答案】B【解析】①标准状况下,6.02×1023个分子为1 mol,但该物质不一定是气体,故占有的体积不一定是22.4 L,故①错误;②氢气所处的状态不一定是标准化状况,气体摩尔体积不一定是22.4 L/mol,0.5 mol H2所占体积不一定为11.2 L,故②错误;③标准化状况下,水是液体,1 mol水的体积远大于22.4 L,故③错误;④28 g CO与N2的混合气体为1 mol,二者都是双原子分子,所含的原子数为2N A,故④正确;⑤影响气体摩尔体积的因素有温度、压强,气体所处的状态不确定,各气体的气体摩尔体积不一定是22.4 L/mol,故⑤错误;⑥同温同压下,体积相同,含有的分子数目相同,故⑥正确;故选B。

3—2 气体摩尔体积自助式复习板块知识在线1.决定物质体积大小的因素有:①;②;③。
(1)固体、液体的体积主要取决于和 。
(2)气体分子间有着较大的距离,在一定温度、压强下,各种气体分子间的 几乎是相等的,因此,在一定温度、压强下,气体体积的大小只随 的多少而变化。
答案:①粒子的大小②粒子间的距离③粒子数目的多少(1)粒子的大小粒子的数目(2)平均距离气体分子数2.气体摩尔体积(1) 叫气体摩尔体积,其符号是,单位是。
(2)计算公式。
(3)标准状况下气体摩尔体积:。
①标准状况:温度,压强 。
②V m=22.4 L·mol-1③V=22.4 L·mol-1·n(气体)理解此概念必须注意五个要点:①必须是气体物质,不适用固体、液体;②物质的量为1 mol;③必须是标准状况;④体积约是22.4 L;⑤可以是混合气体。
答案:(1)单位物质的量的气体所占据的体积V m L·mol-1(2) V=V·nm(3)在标准状况下,1 mol任何气体所占据的体积都约为22.4 L①0 ℃ 1.01×105 Pa3.阿伏加德罗定律(1)当温度和压强一定时,气体分子间平均距离一定,一定物质的量的气体的体积一定。
所以在相同温度和压强下, ,这就是阿伏加德罗定律。
(2)阿伏加德罗定律的推论:①同温同压下,不同气体的体积(V1、V2)之比等于其分子数(N1、N2)之比或物质的量(n1、n2)之比,即;②同温同压下,不同气体的密度(ρ1、ρ2)之比等于其摩尔质量(M1、M2)之比,即;③同温同体积下,气体的物质的量(n1、n2)之比等于其压强(p1、p2)之比,即;④同温同压下,质量相同的气体的体积(V1、V2)之比等于其摩尔质量(M1、M2)的反比,即;⑤同温同压下,同体积的任何气体的质量(m1、m2)之比等于其摩尔质量(M1、M2)之比,即。
答案:(1)相同体积的任何气体具有相同的分子数探究归纳要点1阿伏加德罗定律及其推论的应用【例1】(2004上海高考,20)下列两种气体的分子数一定相等的是( )A.质量相等、密度不等的N 2和C 2H 4B.等体积等密度的CO 和C 2H 4C.等温等体积的O 2和N 2D.等压等体积的N 2和CO 2解析:根据阿伏加德罗定律,212121n n V V N N ==,由于N 2、C 2H 4、CO 的相对分子质量相等,所以质量相等,则物质的量相等,分子数相等,A 、B 正确;但C 中气体压强未知,不能判断,C 错误;D 中气体温度未知,D 错误。

高一化学气体摩尔体积【本讲主要内容】气体摩尔体积【知识掌握】 【知识点精析】一. 决定物质体积的因素:1. 物质体积取决于三个因素⎪⎩⎪⎨⎧微粒间的平均距离微粒本身大小微粒数目2. 影响物质体积的因素:温度、压强(改变微粒的平均间距)3. 液体、固体的体积:主要由微粒本身大小决定4. 气体的体积:主要由微粒间的平均距离决定(分子间距>>分子直径)二. 摩尔体积:1. 摩尔体积:单位物质的量的物质占有的体积。
即每摩尔物质占有的体积。
2. 决定摩尔体积的因素⎩⎨⎧微粒间的平均距离微粒本身大小影响因素:温度和压强(改变分子间距)3. 固态和液态物质的摩尔体积:主要由微粒本身大小决定。
因此不同的固体或液体物质在同一条件下摩尔体积不同。
4. 气体的摩尔体积:单位物质的量的气体所占有的体积,即每摩尔气体物质占有的体积。
用V m 表示单位:()131--⋅⋅molmmolL①由于气体分子间距远大于分子直径,气体摩尔体积主要由气体分子间距决定。
②分子间距受温度和压强影响,因此必须说明所处的条件。
一般常用的是标准状况下的气体摩尔体积:标况下,任何气体的摩尔体积都约为22.4L/mol 。
注意:①0℃,1个标准大气压(1atm ,含101325Pa )为标准状况,若条件改变,气体摩尔体积相应也改变。
②只适用于气态物质。
③适用于纯净物气体,也适用于互不反应的气态混合物。
原因:在标准状况下,不同气体分子间距是相等的。
三. 阿伏加德罗定律:(“四同”定律)1. 内容:在相同的温度下和压强下,相同体积的气体中含有相同数目的分子。
*注意:(1)只适用于气体物质,因为在相同的温度和压强下,不同气体的分子平均间距是相等的,而分子本身直径因远小于分子的平均间距而忽略不计。
固体和液体中分子的直径大于分子间距,体积大小主要由分子本身大小决定。
(2)阿伏加德罗定律适用于任何温度和压强条件下,而标况下气体的摩尔体积22.4L/mol 只适用于0℃,1atm 时,只是阿伏加德罗定律的一个特定情况。

高一化学气体摩尔体积知识点讲解在高一化学中,我们学习了很多关于气体的知识,其中涉及到摩尔体积的概念与计算方法。
摩尔体积是指在相同条件下,1摩尔气体所占有的体积。
本文将为大家详细介绍气体摩尔体积的概念、计算方法以及与其他气体性质的关系。
一、摩尔体积的概念摩尔体积是指在相同条件下,相同物质的气体具有相同的体积。
根据化学气体的理想气体状态方程PV=nRT(其中P为气体压强,V为气体体积,n为气体物质的摩尔数,R为气体常数,T为气体的绝对温度),当温度、压强和气体物质的数量都相同时,气体的体积也是相同的。
这就是摩尔体积的概念。
二、摩尔体积的计算方法气体摩尔体积的计算方法可以通过气体的摩尔数与体积之间的关系来进行计算。
当已知气体的摩尔数时,可以利用以下公式来计算气体的摩尔体积:摩尔体积(V)= 气体体积(V)/ 气体摩尔数(n)举个例子,假设有1 mol氧气,其体积为22.4 L,那么这1 mol 氧气的摩尔体积就等于22.4 L/mol。
需要注意的是,在计算摩尔体积时要注意单位的换算。
通常情况下,气体的摩尔体积的单位是L/mol,而气体的体积一般使用L 作为单位。
三、摩尔体积与其他气体性质的关系摩尔体积与其他气体性质之间存在一定的关系。
下面我们将介绍摩尔体积与气体温度、压强以及气体状态之间的关系。
1. 摩尔体积与温度的关系:根据热力学理论,摩尔体积与气体的温度成正比。
当温度升高时,气体分子的平均动能增加,分子之间的相互作用力减弱,气体的体积也会增大。
2. 摩尔体积与压强的关系:根据理想气体状态方程PV=nRT可以得出,摩尔体积与气体的压强成反比。
在常温下,当压强增大时,气体分子之间的相互作用力增大,气体分子间的距离减小,从而使得气体的体积减小。
3. 摩尔体积与气体状态的关系:不同气体的摩尔体积在相同条件下是相等的。
这是由于不同气体的摩尔体积与气体状态方程PV=nRT中的气体常数R有关。
根据理想气体状态方程可知,气体常数R与摩尔体积呈正比,因此不同气体的摩尔体积相同。
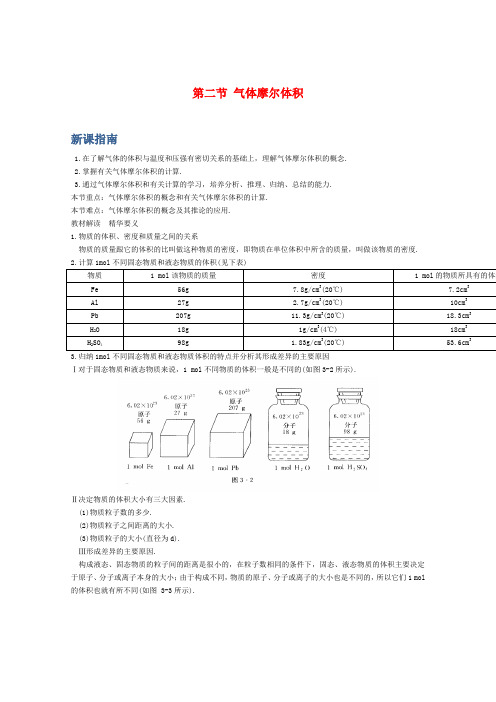
第二节气体摩尔体积新课指南1.在了解气体的体积与温度和压强有密切关系的基础上,理解气体摩尔体积的概念.2.掌握有关气体摩尔体积的计算.3.通过气体摩尔体积和有关计算的学习,培养分析、推理、归纳、总结的能力.本节重点:气体摩尔体积的概念和有关气体摩尔体积的计算.本节难点:气体摩尔体积的概念及其推论的应用.教材解读精华要义1.物质的体积、密度和质量之间的关系物质的质量跟它的体积的比叫做这种物质的密度,即物质在单位体积中所含的质量,叫做该物质的密度.2.计算1mol不同固态物质和液态物质的体积(见下表)物质 1 mol该物质的质量密度 1 mol的物质所具有的体积Fe 56g 7.8g/cm3(20℃) 7.2cm3Al 27g 2.7g/cm3(20℃) 10cm3Pb 207g 11.3g/cm3(20℃) 18.3cm3H2O 18g 1g/cm3(4℃) 18cm3H2SO498g 1.83g/cm3(20℃) 53.6cm33.归纳1mol不同固态物质和液态物质体积的特点并分析其形成差异的主要原因Ⅰ对于固态物质和液态物质来说,1 mol不同物质的体积一般是不同的(如图3-2所示).Ⅱ决定物质的体积大小有三大因素.(1)物质粒子数的多少.(2)物质粒子之间距离的大小.(3)物质粒子的大小(直径为d).Ⅲ形成差异的主要原因.构成液态、固态物质的粒子间的距离是很小的,在粒子数相同的条件下,固态、液态物质的体积主要决定于原子、分子或离子本身的大小;由于构成不同,物质的原子、分子或离子的大小也是不同的,所以它们1 mol的体积也就有所不同(如图 3-3所示).知识详解知识点1 气体摩尔体积(重点、难点)Ⅰ决定气体体积大小的主要因素(1)决定气体所含有的分子数(或气体的物质的量).在一定温度,一定压强下,气体中所含的分子数目(或物质的量)越多,气体的体积就越大.(2)分子的直径和分子之间的距离.一般来说,气体分子的直径约为0.4 nm,而分子之间的距离则约为4 nm,即分子之间的距离约是分子直径的10倍.因此,当分子数目相同时,气体体积的大小主要决定于气体分子之间的距离,而不是分子本身体积的大小(如图3-4所示).思维拓展如图3-5与图3-6所示,讨论气体分子之间的距离受哪些因素的影响?是怎样影响的?点拨受温度和压强的影响。

第二章海水中的重要元素——钠和氯第三节物质的量第2课时气体摩尔体积一、单选题1.设N A为阿伏加德罗常数的值,下述正确的是()A.64g二氧化硫含有原子数为3N AB.O2气体的摩尔质量为36gC.标准状况下,11.2L水含分子数为0.5 N AD.摩尔是国际单位制中七个基本物理量之一【答案】A【解析】A.64g SO2的物质的量为1mol,则含有原子3mol,则原子个数为3N A,A正确;B.O2气体的摩尔质量为36g/mol,B错误;C.标准状况下,水为液体,不能计算其物质的量,C错误;D.摩尔是物质的量的单位,而物质的量才是国际单位制中七个基本物理量之一,D错误;2.下列叙述正确的是()A.1molH2O的质量为18g/molB.CH4的相对分子质量为16C.3.01×1023个SO2分子的体积为11.2LD.标准状况下,1mol任何物质体积均为22.4L【答案】B【解析】A.质量的单位为g,1molH2O的质量为18g,故A错误;B.CH4的相对分子质量为16,故B正确;C. 3.01×1023个SO2分子即0.5mol SO2,但没有指明标况下,无法计算体积,故C错误;D. 标准状况下,1mol气体的体积均为22.4L,故D错误;3.(2020·北京高一期末)关于1molH2O的下列说法中,不正确...的是()A.质量为18g B.含氧原子数约为6.02×1023C.含电子数约为10×6.02×1023D.标准状况下的体积约为22.4L【答案】D 【解析】A. 1molH 2O 的质量为:m=n∙M=1mol×18g/mol=18g ,A 正确;B. 1molH 2O 中含氧原子数目为:23123A ·1mol 6.0210mol 6.0210N n N -==⨯⨯=⨯,B 正确; C. 1molH 2O 中含电子数目为:23123A ·10mol 6.0210mol 10 6.0210N n N -==⨯⨯=⨯⨯,C 正确; D. 标准状况下,H 2O 是液体,不能用m ·V nV=计算,D 错误; 4.(2020·河北深州市中学高一期末)设N A 表示阿伏伽德罗常数的值,下列说法正确..的是( ) A .常温常压下,14g 有N 2与CO 组成的混合气体含有的原子数目为N A 个 B .0.5molO 3与11.2LO 2所含的分子数一定相等 C .标准状况下,22.4 L 四氯化碳的分子数为N AD .用16.25gFeCl 3制备Fe(OH)3胶体,Fe(OH)3胶体粒子数为0.1N A 个 【答案】A 【解析】A. 常温常压下,N 2与CO 的摩尔质量均为28g/mol ,且为双原子分子,则14g 有N 2与CO 组成的混合气体的物质的量为0.5mol ,含有的原子数目为N A 个,符合题意,A 正确;B. 0.5molO 3与标况下的11.2LO 2所含的分子数一定相等,与题意不符,B 错误;C. 标准状况下,四氯化碳为液态,22.4 L 的四氯化碳含有的分子数大于N A ,与题意不符,C 错误;D. 用16.25gFeCl 3制备Fe(OH)3胶体,Fe(OH)3胶体粒子不一定为一个Fe(OH)3,则胶粒数无法确定,与题意不符,D 错误; 答案为A 。

高一化学必修一知识点要点:气体摩尔体积高一化学必修一知识点要点:气体摩尔体积
气体摩尔体积(Vm)
(1)定义:单位物质的量的气体所占的体积叫做气体摩尔体积.
(2)单位:L/mol
2.物质的量=气体的体积/气体摩尔体积n=V/Vm
3.标准状况下, Vm = 22.4 L/mol
化学不像语数英,化学知识相对比较零散,需要学生对课本知识进行归纳总结,建立一个相对完整的知识体系。
不管学生在高二是选择文科还是理科,星火教育网小编希望同学们能够认真学习化学知识,坚持课前预习、课中认真听讲、课后及时复习的良好的学习习惯,努力提高自己的学习效率和质量,争取在每一次考试中都能发挥出自己最佳的水平,取得理想的成绩。
同学们是不是有着聪明的头脑呢?接下来,高一化学必修一知识点要点来供同学们练习从而巩固自己所学过的
知识,大家一定要认真做哦,更多练习高一化学知识点
高一化学必修一知识重点精选:氯离子的检验 17年高一化学必修一知识点:一氧化氮和二氧化氮。

气体摩尔体积一、新课标知识梳理:1、决定物质体积的三因素:(1)微粒(分子)的数目;(2)微粒(分子)本身的大小;(3)微粒与微粒之间的距离。
2、气体摩尔体积定义、使用注意事项:3、体积与气体粒子个数之间的关系:4、阿伏加德罗定律的应用:(1)同温同压下,气体的体积比等于物质的量比。
B A B A n n V V //=(2)同温同容下,气体的压强比等于物质的量比。
B A B A n n P P //=(3)同温同压下,气体的摩尔质量比等于密度比。
B A B A d d M M //=(4)同温同压下,同体积的气体质量比等于摩尔质量比。
B A B A M M m m //=(5)同温同压下,同质量气体的体积比等于摩尔质量的反比。
A B B A M M V V //=二、基础知识释疑:例1.判断正误,并说明理由。
(1)标况下,1 mol 任何物质的体积都约为22.4 L 。
( )(2)1 mol 气体的体积约为22.4 L 。
( )(3)标况下,1 mol O 2和N 2混合气(任意比)的体积约为22.4 L 。
( )(4)22.4 L 气体所含分子数一定大于11.2 L 气体所含的分子数。
( )(5)任何条件下,气体的摩尔体积都是22.4 L 。
( )(6)只有在标况下,气体的摩尔体积才能是22.4 L 。
( )例2.判断下列叙述正确的是A .标准状况下,1mol 任何物质的体积都约为22.4LB .1mol 任何气体所含分子数都相同,体积也都约为22.4LC .在常温常压下1molH 2的体积大于22.4LD .在同温同压下,相同体积的任何气体单质所含原子数目相同例3.如果ag 某气体中含有的分子数为b ,则cg 该气体在标准状况下的体积是A .L acN b A 4.22B .L cN ab A 4.22C .L bN ac A 4.22D .L aN bc A 4.22 例4.按体积比为4:2:3所组成的N 2、O 2、CO 2,混合气体100g 在标准状况下体积为___ L 。
![化学必修一气体摩尔体积知识点及习题-[新课强化练习用]](https://img.taocdn.com/s1/m/b3e06202ff00bed5b9f31d56.png)
气体的摩尔体积知识点①定义:单位物质的量的气体所占的体积,符号V m(提问:为什么液体、固体没有摩尔体积),单位: L/mol②计算公式:n=V/V m (标准状况下:V m=22.4 L/mol)难点一:(1).气体摩尔体积的适用范围气体摩尔体积的适用范围是气态物质,可以是单一气体,也可以是混合气体,如0.2 mol H2与0.8 mol O2的混合气体在标准状况下的体积约为22.4 L。
(2).气体摩尔体积的数值①气体摩尔体积的数值与温度和压强有关②标准状况(0℃,101kPa)下任何气体的气体摩尔体积为22.4 L·mol-1③非标准状况下气体摩尔体积可能是22.4 L·mol-1,也可能不是22.4 L·mol-1。
1 mol 气体的体积若为22.4 L,它所处的状况不一定是标准状况,如气体在273℃和202 kPa时,V m为22.4 L·mol-1。
特别提醒利用22.4 L·mol-1计算或判断时一定要看清气体所处的状况。
常出现的错误:①忽视物质在标准状况下的状态是否为气态,如水在标准状况下为液态,计算该条件下的体积时不能应用22.4 L·mol-1。
②忽视气体所处的状态是否为标准状况,如“常温常压下2 mol O2的体积为44.8 L”的说法是错误的,因常温常压下气体摩尔体积不是22.4 L·mol-1。
1、标准状态下,2mol N2的体积是( )A.44.8L B.22.4L C.11.2L D.2L2、用N A表示阿伏德罗常数,下列叙述正确的是( )A.标准状况下,22.4LH2O含有的分子数为1 N AB.常温常压下,1.06g Na2CO3含有的Na+离子数为0.02 N AC.通常状况下,1 N A个CO2分子占有的体积为22.4LD.在标准状况下,1 N A个SO3分子占有的体积为22.4L3、下列说法正确的是( )A.摩尔是一种国际基本物理量B.标准状况下气体摩尔体积约为22.4LC.1mol氧的质量为16gD.在同温同压下,相同体积的任何气体单质所含分子数相同4、所含分子数相同的一组物质是( )A.1g H2和1g N2B.1mol H2O和1g H2OC.3.2g O2和2.24L的空气(标准状况下)D.44gCO2和6.02×1022个O25、下列说法正确的是()A. 32gO2占有的体积约为22.4LB. 22.4L N2含有N A个氮分子C. 在标准状况下,22.4L水的质量约为18gD. 22g二氧化碳与标准状况下11.2LHCl含有相同的分子数6、在标准状况下,相同质量的下列气体中体积最大的是( )A.O2B.Cl2 C.N2 D.CO27、下列叙述正确的是( )A.同温同压下,相同体积的物质,其物质的量一定相等B.任何条件下,等物质的量的甲烷和一氧化碳所含的分子数一定相等C.1L一氧化碳气体一定比1L氧气的质量小D.一氧化碳气体和氮气,若体积相等,则质量也相等8、下列有关气体体积的叙述中,正确的是( )A.一定温度和压强下,各种气体物质体积的大小由构成气体的分子大小决定B.一定温度和压强下,各种气态物质体积的大小,由构成气体的分子数决定C.不同的气体,若体积不同,则它们所含的分子数也不同D.气体摩尔体积指1mol任何气体所占的体积约为22.4L9、标准状况下,32g某气体的分子数目与22 g CO2的分子数目相同,则该气体的摩尔质量为( )A.32 B.32 g/ mol C.64g/ mol D.6410、N A表示阿伏加德罗常数的值,下列说法中正确的是( )A.常温常压下,0.05 N A个CO2分子所占的体积是1.12LB.氨气的摩尔质量和N A个氨分子的质量在数值上相等C.常温常压下,32g氧气和34 g H2S分子个数比为1:1D.标准状况下, N A个水分子所占的体积为22.4L11、在相同条件下,与0.5mol由N2和CO组成的混合气具有相同的体积的是( )A.1g H2B.10g O2C.11g CO2D.16g CH412、有一种气体的质量是14.2g,体积是4.48升(标准状况),该气体的摩尔质量是( )A.28.4 B.28.4g·mol-1C.71 D.71g·mol-113、下列叙述正确的是( )A.48 g O3气体含有6.02×1023个O3分子B.常温常压下28 g CO与22.4 L O2所含分子数相等C.在标准状况下,1 g氢气含有N A个H2分子D.标准状况下,33.6 L H2O含有9.03×1023个H2O分子14、若N A代表阿伏加德罗常数,下列说法正确的是( )A.1个标准大气压,20℃下11.2LN2含有的分子数为0.5N AB.4℃时9mL水和标准状况下11.2L氮气含有相同的分子数C.同温同压下,N A个NO与N A个N2和O2的混合气体的体积不相等D.0℃、1.01×104Pa时,11.2 L氧气所含的原子数目为N A15、下列叙述正确的是( )A.常温常压下,1mol氮气含有阿伏加德罗常数个氮原子B.一定温度、压强下,气体体积由其物质的量的多少决定C.标准状况下,22.4L H2和11.2L氧气混合,气体的分子总数约为1N A个D.不同的气体,若体积不等,则它们所含的分子数一定不等16、下列各物质所含原子数目,按由大到小顺序排列的是( )①0.5mol NH3②标准状况下22.4L He ③4℃9mL水④0.2mol H3PO4A.①④③② B.④③②① C.②③④① D.①④②③17、同温同压下两个容积相等的贮气瓶,一个装有C2H4,另一个装有C2H2和C2H6的混合气体,两瓶内的气体时一定具有相同的( )A.质量 B.原子总数 C.分子数D.密度二、填空题19、标准状况下,①4 g氢气、②33.6 L甲烷、③6.02×1023个水分子中,含分子数最多的是(填序号,下同)________,含原子数最多的是_________,质量最大的是________ ___,体积最小的是___________。

气体摩尔体积编稿:柏兴增审稿:武小煊【学习目标】1、了解气体摩尔体积的含义。
2、掌握有关气体摩尔体积的计算方法。
【要点梳理】要点一、影响物质体积大小的因素1.影响物质体积大小的因素:从微观来看,影响物质体积大小的因素有三个:微粒个数、微粒大小、微粒间距离。
1 mol任何物质中的粒子数目都是相同的,即约为6.02×1023。
因此,1 mol物质的体积大小主要取决于构成物质的粒子的大小和粒子之间的距离。
2. 影响固体(或液体)物质体积大小的主要因素有两个:微粒个数和微粒自身大小要点诠释:固态或液态物质,粒子之间的距离是非常小的,故1 mol固态或液态物质的体积主要取决于粒子的大小,不同的固态或液态物质,粒子的大小是不相同的,因此,1 mol不同的固态或液态物质的体积是不相同的(见下图)。
固体液体气体3.影响气体物质体积大小的主要因素有两个:微粒个数和微粒间距离。
要点诠释:对于气体来说,粒子之间的距离远大于粒子本身的直径,气体体积与微粒间的距离有关,与粒子本身的直径大小关系不大。
当压强和温度一定时,气体微粒间距离一定,所以当气体分子数一定,则气体体积一定;反之,在压强和温度一定时,相同体积的任何气体分子数相等,这就是常说的阿伏加德罗定律。
如果气体的物质的量为1 mol,则其体积主要取决于气体粒子之间的距离。
而在同温同压下,任何气体粒子之间的平均距离可以看成是相等的,1 mol任何气体都具有相同的体积(见上图)。
要点二、气体摩尔体积1、气体摩尔体积的含义:在一定温度和压强下,单位物质的量的气体所占的体积叫做气体摩尔体积,符号是V m,它的常用单位是L·mol-1和m3·mol-1。
关于物质的量(n)、气体的体积(V)和气体摩尔体积(V m)之间的计算公式为mVVn=。
可变形为V=n·V m与mVnV=。
2、标准状况下气体摩尔体积:在标准状况(指0℃、101 kPa,记作:STP)下,气体摩尔体积约为22.4 L·mol-1。
气体摩尔体积[学习目标定位] 1.知道决定气体体积的主要因素,能叙述阿伏加德罗定律的内容。
2.知道气体摩尔体积的含义,记住标准状况下的气体摩尔体积。
3.能进行气体体积、物质的量、微粒数目之间的换算。
一、决定物质体积大小的因素1.在温度和压强一定时,决定物质体积大小的主要因素:微粒的数目、微粒的大小、微粒间的距离。
2.根据表格中的数据完成下列填空:(1)在温度和压强一定时,任何1 mol固态物质或液态物质所含微粒数目相同。
微粒之间的距离很小,但微粒的大小不同,所以1 mol固态物质或液态物质的体积往往是不同的。
(2)对气态物质来说:通常情况下微粒之间的距离要比微粒本身的直径大很多倍,因此,当微粒数相同时,气态物质体积的大小则主要取决于气体微粒间的距离。
(3)在温度和压强一定时,微粒间的距离近似相等,因此,在相同温度和压强下,任何具有相同微粒数的气体都具有大致相同的体积。
1.物质体积大小的影响因素2.粒子数目相同物质的体积关系1.下列四种因素:①温度和压强②所含微粒数③微粒本身大小④微粒间的距离,其中对气态物质体积有显著影响的是()A.②③④B.②④C.①③④D.①②④答案 D解析气态物质微粒之间的距离要比微粒本身的直径大很多倍,故微粒本身的大小对气态物质体积无显著影响。
2.同温同压下,若两种气体所占体积不同,其主要原因是()A.气体分子的大小不同B.气体分子间平均距离不同C.气体的物质的量不同D.气体的摩尔质量不同答案 C二、气体摩尔体积1.气体摩尔体积是单位物质的量的气体所占的体积,符号是V m,表达式:V m=V n。
常用的单位是L·mol-1。
标准状况下,气体摩尔体积约为22.4 L·mol-1。
2.对于气体摩尔体积的理解,应注意以下几点:(1)气体摩尔体积的适用范围是气态物质。
在标准状况下,1 mol 气体所占的体积约是22.4 L。
(2)气体的体积与温度、压强有关。
相同温度下,单位物质的量的气体压强越小,气体体积越大;相同压强下,单位物质的量的气体温度越高,气体体积越大。
(3)气体摩尔体积不仅适用于纯气体,也适用于混合气体。
如0.3 mol H2与0.7 mol O2的混合气在标准状况下的体积约为22.4 L。
(4)1 mol气体在非标准状况下的体积,可能是22.4 L,也可能不是22.4 L。
3.标准状况下,气体摩尔体积的有关计算①气体的物质的量n=V22.4mol;②气体的摩尔质量M=V m·ρ=22.4ρ g·mol-1;③气体的分子数N=n·N A=V22.4·N A;④气体的质量m=n·M=V22.4·M g。
1.标准状况下的气体摩尔体积2.计算公式n=mM=NN A=V22.4(标准状况)3.下列叙述正确的是()A.1 mol任何气体的体积都为22.4 LB.1 mol任何物质在标准状况下所占的体积都为22.4 LC.只有在标准状况下,气体摩尔体积才约为22.4 L·mol-1D.标准状况下,22.4 L任何气体的物质的量都是1 mol答案 D解析A中没有指明该物质所处的状况,即温度、压强,错误;B中没有指明该物质的状态,错误;C中在非标准状况下,气体的摩尔体积也可能是22.4 L·mol-1,错误;D中是对气体摩尔体积概念的应用,正确。
4.设N A表示阿伏加德罗常数的值,下列叙述中正确的是()A.常温常压下,11.2 L CO2所含的原子数为1.5N AB.常温常压下,48 g O3含有的氧原子数为3N AC.标准状况下,22.4 L H2O所含分子数为N AD.标准状况下,22.4 L H2所含原子数为N A答案 B解析A项,常温、常压下11.2 L CO2的物质的量不是0.5 mol,因此所含原子数不是1.5N A;B项,n(O3)=48 g48 g·mol-1=1 mol,含氧原子数为3N A;C项,标准状况下H2O为液态,不能应用22.4 L·mol-1;D项,n(H2)=22.4 L22.4 L·mol-1=1 mol,含氢原子数为2N A。
方法点拨气体摩尔体积使用时注意事项(1)1个条件:必须指明条件。
非标准状况下,1 mol气体的体积不一定是22.4 L。
(2)1种状态:必须为气态。
如水、酒精、SO3、CCl4等物质在标准状况下不是气体。
(3)1个单位:气体摩尔体积单位是L·mol-1,而不是L。
三、阿伏加德罗定律1.实验探究气体的体积与物质的量的关系(1)下图为电解水的实验装置。
图中A试管中收集到的气体是H2,B试管中收集到的气体是O2,二者的体积之比是2∶1。
(2)物质的量比与气体体积比的关系若有1.8 g H2O电解,产生H2的质量为0.2 g,物质的量为0.1 mol;产生O2的质量为1.6 g,物质的量为0.05 mol;二者物质的量之比为2∶1。
(3)实验结论①在同温同压下,气体的物质的量之比等于体积之比。
②在同温同压下,1 mol的不同气体,其体积相同。
2.判断正误,正确的打“√”,错误的打“×”。
(1)标准状况下,1 mol任何气体的体积都约是22.4 L()(2)同温同压下,1 mol(含有相同的粒子数)任何气体的体积相同()(3)同温同压下,相同体积的任何气体含有相同数目的分子数()(4)标准状况下,16 g氧气与2 g氢气的体积比是1∶2()答案(1)√(2)√(3)√(4)√阿伏加德罗定律(1)阿伏加德罗定律:相同温度相同压强下,相同体积的任何气体都含有相同数目的粒子(分子)。
(2)相同条件下的气体,同体积时,分子数相同;反之,分子数相同时,体积也相同;气体的体积之比等于分子数(或物质的量)之比。
(3)同温同压下,气体的体积之比等于其物质的量之比。
(4)同温同体积时,气体的压强之比等于其物质的量之比。
5.下列叙述正确的是()A.同温同压下,相同体积的物质,其物质的量必然相等B.任何条件下,等物质的量的氧气和一氧化碳所含的分子数必然相等C.1 L一氧化碳气体一定比1 L氧气的质量小D.同温同压下,等体积的物质所含的分子数一定相等答案 B解析 只有气体物质才符合阿伏加德罗定律——在同温同压下,具有相同体积的气体的物质的量相等。
具有相同物质的量的两种由分子构成的物质具有相同的分子数。
因温度、压强不能确定,故1 L CO 和1 L O 2的物质的量大小也不能确定,即二者的质量大小无法比较。
6.如图两瓶体积相等的气体,在同温同压下瓶内气体的关系一定正确的是( )A.原子数相等B.密度相等C.质量相等D.摩尔质量相等答案 A解析 由同温同压可得V m 相同,再由公式n =VV m 可得两瓶内分子的物质的量相同,又都是双原子分子,所以原子的物质的量相同,由原子个数之比等于其物质的量之比可得两瓶内分子所含原子数相同,A 项正确;两瓶内分子的物质的量相等,由m =nM ,M 不一定相等,故m 不一定相等,同时由ρ=mV也可得ρ不一定相等。
1.阿伏加德罗定律可适用于任何气体(纯净的或是互不反应的混合气体),但不适用于液体或固体。
2.同温、同压、同体积、同分子数称为“四同”,四“同”共同存在,相互制约,只要有三个“同”成立,第四个“同”就必定成立,在实际应用中往往是知道三“同”而求导另一“同”。
3.标准状况下气体的摩尔体积是阿伏加德罗定律的特例,与m、N、V之间的换算关系是n=mM=NN A=V22.4 L·mol-1。
1.下列有关气体体积叙述正确的是()A.一定温度、压强下,气体体积由其分子的大小决定B.一定温度、压强下,气体体积由其物质的量的多少决定C.气体摩尔体积是指1 mol任何气体所占的体积约为22.4 LD.不同的气体,若体积不等,则它们所含的分子数一定不等答案 B解析 气体的体积在温度、压强一定时,体积与其物质的量成正比;当分子数目相同时,气体体积的大小主要决定于气体分子之间的距离,而不是分子本身体积的大小,所以A 、D 错误,B 正确;非标准状况下气体摩尔体积不一定为22.4 L·mol -1,C 错误。
2.下列说法正确的是( )A.20 ℃、1.01×105 Pa 时,同体积的O 2和CO 2含有相同数目的分子数B.1 mol 气态物质,当体积为22.4 L 时,该气体一定处于标准状况C.2 mol 任何气体体积都约为44.8 LD.同温同压下,相同体积的任何气体单质所含分子数和原子数都相同答案 A解析 根据阿伏加德罗定律,同温同压下,同体积的任何气体都含有相同数目的分子数,故A 正确,D 错误;B 中,1 mol 气态物质在非标准状况时,体积也有可能等于22.4 L ;C 中缺少标准状况条件。
3.标准状况下,若11.2 L 氧气含有n 个氧原子,则阿伏加德罗常数的数值可表示为 ( )A.4nB.3nC.2nD.n答案 D解析 根据恒等式V 22.4=N N A 可知N A =n ×22.4 L·mol -12×11.2 L=n mol -1。
4.现有m g 某气体,它由双原子分子构成,它的摩尔质量为M g·mol -1。
若阿伏加德罗常数的值用N A 表示,则:(1)该气体的物质的量为 mol 。
(2)该气体所含原子总数为 个。
(3)该气体在标准状况下的体积为 L 。
(4)该气体在标准状况下的密度为 g·L -1。
(5)该气体一个分子的质量为 g 。
答案 (1)m M (2)2mN A M (3)22.4m M (4)M 22.4 (5)M N A解析 (1)由n =m /M 可求。
(2)由物质的量可求得该气体的分子数,进一步可求得原子数。
(3)由V =nV m 可求得该气体在标准状况下的体积。
(4)由质量和已求得的标准状况下的体积可求得密度,也可以由M =V m ·ρ求得密度。
(5)由摩尔质量为M g·mol -1,知每一个分子的质量为M N A g 。
5.同温同压下,同体积的氨气和硫化氢气体(H 2S)的质量比为 ;同质量的氨气和硫化氢气体的体积比为 ,其中含有的氢的原子个数比为 ;若二者氢原子数相等,它们的体积比为 。
答案1∶22∶13∶12∶3解析根据阿伏加德罗定律,同温同压下,同体积的气体物质的量相同。
故氨气和硫化氢气体(H2S)的质量比为17∶34=1∶2;同质量的氨气和硫化氢的物质的量之比为117∶134=2∶1,氢的原子个数比为(2×3)∶(1×2)=3∶1;二者氢原子数相等时,物质的量之比等于13∶12=2∶3,故体积之比为2∶3。