第4章
- 格式:ppt
- 大小:1.91 MB
- 文档页数:94
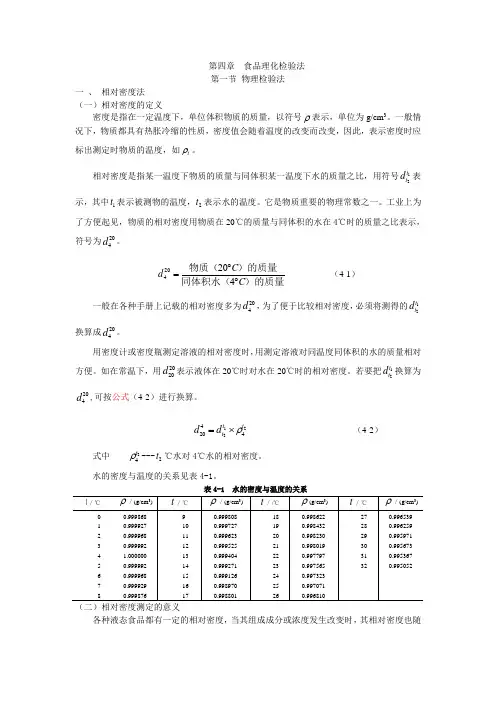
第四章 食品理化检验法第一节 物理检验法 一 、 相对密度法 (一)相对密度的定义密度是指在一定温度下,单位体积物质的质量,以符号ρ表示,单位为g/cm 3。
一般情况下,物质都具有热胀冷缩的性质,密度值会随着温度的改变而改变,因此,表示密度时应 标出测定时物质的温度,如t ρ。
相对密度是指某一温度下物质的质量与同体积某一温度下水的质量之比,用符号12tt d 表示,其中1t 表示被测物的温度,2t 表示水的温度。
它是物质重要的物理常数之一。
工业上为了方便起见,物质的相对密度用物质在20℃的质量与同体积的水在4℃时的质量之比表示,符号为204d 。
204204C d C ︒=︒物质()的质量同体积水()的质量(4-1)一般在各种手册上记载的相对密度多为204d ,为了便于比较相对密度,必须将测得的12tt d 换算成204d 。
用密度计或密度瓶测定溶液的相对密度时,用测定溶液对同温度同体积的水的质量相对方便。
如在常温下,用2020d 表示液体在20℃时对水在20℃时的相对密度。
若要把12tt d 换算为204d ,可按公式(4-2)进行换算。
1224204t tt d d ρ=⨯ (4-2)式中 24tρ---2t ℃水对4℃水的相对密度。
水的密度与温度的关系见表4-1。
表4-1 水的密度与温度的关系(二)相对密度测定的意义各种液态食品都有一定的相对密度,当其组成成分或浓度发生改变时,其相对密度也随着改变,故测定液态食品的相对密度可以检验食品的纯度或浓度。
如蔗糖、酒精等溶液的相对密度随溶液浓度的增加而增高,根据蔗糖溶液的相对密度可直接查出蔗糖的质量分数;根据酒精溶液的相对密度可查出酒精的体积分数。
当某溶液的水分被完全蒸发干燥至恒重时,所得到的剩余物称为干物质或真固形物。
溶液的相对密度与其固形物含量具有一定的关系,故测定溶液相对密度即可求出其固形物含量。
对于某些液态食品(如果汁、番茄酱等),测定其相对密度并通过换算或查经验表,也可确定可溶性固形物或总固形物的含量。

第4章机器人轨迹规划本章在操作臂运动学和动力学的基础上,讨论在关节空间和笛卡尔空间中机器人运动的轨迹规划和轨迹生成方法。
所谓轨迹,是指操作臂在运动过程中的位移、速度和加速度。
而轨迹规划是根据作业任务的要求,计算出预期的运动轨迹。
首先对机器人的任务,运动路径和轨迹进行描述,轨迹规划器可使编程手续简化,只要求用户输入有关路径和轨迹的若干约束和简单描述,而复杂的细节问题则由规划器解决。
例如,用户只需给出手部的目标位姿,让规划器确定到达该目标的路径点、持续时间、运动速度等轨迹参数。
并且,在计算机内部描述所要求的轨迹,即选择习惯规定及合理的软件数据结构。
最后,对内部描述的轨迹、实时计算机器人运动的位移、速度和加速度,生成运动轨迹。
4.1 机器人轨迹规划概述一、机器人轨迹的概念机器人轨迹泛指工业机器人在运动过程中的运动轨迹,即运动点的位移、速度和加速度。
机器人在作业空间要完成给定的任务,其手部运动必须按一定的轨迹(trajectory)进行。
轨迹的生成一般是先给定轨迹上的若干个点,将其经运动学反解映射到关节空间,对关节空间中的相应点建立运动方程,然后按这些运动方程对关节进行插值,从而实现作业空间的运动要求,这一过程通常称为轨迹规划。
工业机器人轨迹规划属于机器人低层规划,基本上不涉及人工智能的问题,本章仅讨论在关节空间或笛卡尔空间中工业机器人运动的轨迹规划和轨迹生成方法。
机器人运动轨迹的描述一般是对其手部位姿的描述,此位姿值可与关节变量相互转换。
控制轨迹也就是按时间控制手部或工具中心走过的空间路径。
二、轨迹规划的一般性问题通常将操作臂的运动看作是工具坐标系{T}相对于工件坐标系{S}的一系列运动。
这种描述方法既适用于各种操作臂,也适用于同一操作臂上装夹的各种工具。
对于移动工作台(例如传送带),这种方法同样适用。
这时,工作坐标{ S }位姿随时间而变化。
例如,图4.1所示将销插入工件孔中的作业可以借助工具坐标系的一系图4.1 机器人将销插入工件孔中的作业描述列位姿P i(i=1,2,…,n)来描述。



第4章:配合物一.配合物的组成(1)配位体:是含有孤电子对的分子或离子,如NH3、Cl-、CN-等。
配位体中直接同中心原子配合的原子,叫做配位原子。
如上例[Cu(NH3)4]2+配离子中,NH3是配位体,其中N原于是配位原子。
配位原子经常是含有孤对电子的原子。
(2)中心离子(或原子):一般是金属离子,特别是过渡金属离子,但也有电中性的原子为配合物的中心原子,如Ni(CO)4、Fe(CO)5中的Ni和Fe都是电中性的原子。
此外,少数高氧化态的非金属元素也能作为中心原子存在,如SiF62-中的Si(Ⅳ)及PF6-中的P(V)等。
(3)配位数:直接同中心离子(或原子)配合的配位原子的数目,叫做该中心离子(或原子)的配位数,一般中心离子的配位数为2、4、6、8(较少见),如在[Pt(NH3)6]C14中,配位数为6,配位原子为NH3分子中的6个氮原子。
(4)配离子的电荷:配离子的电荷数等于中心离子和配位体电荷的代数和。
如[Cu(NH3)4]2+的电荷是+2+(0)×4=+2。
二.配合物的分类配位化合物的范围极广,主要可以分为以下几类:(1)单核配合物这类配合物是指一个中心离子或原子的周围排列着一定数量的配位体。
中心离子或原子与配位体之间通过配位键而形成带有电荷的配离子或中性配合分子。
如[Cu(NH3)4]SO4、K4[Fe(CN)6]等皆属于此类配合物。
(2)螯合物这类配合物是由多齿配位体以两个或两个以上的配位原子同时和一个中心离子配合并形成具有环状结构的配合物。
例如乙二胺H2N-CH2-CH2-NH2和Cu2+形成的如下螯合物:三.配合物的命名配合物的命名与一般无机化合物的命名原则相同。
若配合物的外界是一简单离子的酸根,便叫某化某;若外界酸根是一个复杂阴离子,便叫某酸某(反之,若外界为简单阳离子,内界为配阴离子的配合物也类似这样叫法)。
若配离子的内界有多种配体,须按下列顺序依次命名:简单离子—复杂离子—有机酸根离子;而中性分子配位体的命名次序为:H2O—NH3—有机分子。




