自由基聚合反应的特征教案
- 格式:doc
- 大小:96.50 KB
- 文档页数:2

简述自由基聚合反应和阴离子聚合反应的反应特点自由基聚合反应和阴离子聚合反应是两种不同类型的聚合反应,具有不同的反应特点和反应机制。
自由基聚合反应是一种链式聚合反应,它通过自由基的活性物种进行聚合。
在自由基聚合反应中,单体分子被引发生成自由基,然后自由基之间相互作用,形成聚合物分子。
自由基聚合反应通常具有以下几个特点:1. 反应速率快:自由基聚合反应的速率非常快,通常可以在几秒钟内完成。
这是因为自由基活性物种非常活泼,可以快速地与其他自由基结合形成聚合物。
2. 反应机理简单:自由基聚合反应的机理非常简单,只需要单体分子被引发生成自由基,然后自由基之间相互作用即可完成聚合。
3. 可以控制反应:自由基聚合反应可以通过控制引发剂浓度、反应温度、催化剂种类和浓度等因素来控制反应速率和聚合物分子量。
4. 产物多样性:自由基聚合反应可以生成多种不同类型的聚合物,如线性聚合物、支化聚合物、高聚物晶体等。
相比之下,阴离子聚合反应是一种离子型聚合反应,它通过阴离子活性物种进行聚合。
在阴离子聚合反应中,单体分子被引发生成阴离子,然后阴离子之间相互作用,形成聚合物分子。
阴离子聚合反应通常具有以下几个特点:1. 反应速率较慢:阴离子聚合反应的速率比自由基聚合反应慢,通常需要几分钟或更长时间才能完成。
2. 反应机理复杂:阴离子聚合反应的机理比自由基聚合反应复杂,需要考虑到电荷转移、配位反应等多种因素。
3. 产物纯度高:阴离子聚合反应通常可以生成高纯度的聚合物,因为反应过程中不容易引入其他杂质。
4. 反应介质要求高:阴离子聚合反应需要在酸性或碱性介质中进行,要求反应介质的 pH 值在适宜范围内。
总而言之,自由基聚合反应和阴离子聚合反应具有不同的反应特点和反应机制,分别适用于不同的合成和应用需求。

自由基聚合反应特征自由基聚合反应啊,这可是化学世界里相当神奇的一个过程呢!就好像一场超级热闹的聚会,各种“角色”粉墨登场。
我先来说说自由基聚合反应中的单体吧。
单体就像是聚会里一个个孤独的小客人,它们都有着自己独特的结构。
这些单体大多是含有碳 - 碳双键的小分子,比如我们常见的乙烯、丙烯这些。
它们呀,就等着有个契机来凑到一起,发生点奇妙的变化。
你想啊,这些单体单个看的时候,就像散落在地上的小珠子,普普通通的。
那自由基是怎么来的呢?这就像是聚会上突然出现的小火花,点燃了整个聚会的气氛。
引发剂在一定条件下分解就产生了自由基。
这个引发剂就好比是一个调皮的小捣蛋鬼,在合适的温度或者光照下,“噗”的一下,自己分裂了,产生出自由基。
自由基这东西可活跃啦,就像个精力旺盛的小猴子,到处找东西结合。
自由基一旦产生,就开始寻找那些单体小客人。
当自由基和单体相遇的时候,哇,就像是两块拼图正好凑到了一块儿。
它们结合的方式呢,是自由基进攻单体的双键。
这一结合可不得了,就像多米诺骨牌倒下的第一块,引发了连锁反应。
这个新形成的结构又变成了一个新的自由基,然后它又会去寻找下一个单体。
你看,是不是很神奇?这就像滚雪球一样,越来越大。
在自由基聚合反应里,反应速度那也是很有特点的。
刚开始的时候,反应就像小火苗刚刚燃起,速度不是特别快。
可是随着自由基和单体不断结合,反应就像加了燃料一样,速度蹭蹭地往上涨。
就好比你跑步,刚开始慢悠悠的,跑着跑着,越跑越带劲,速度就越来越快了。
不过呢,这个反应速度也不是一直这么疯狂增长的。
到了后期,因为单体越来越少了,就像聚会上的小客人都差不多凑成对儿了,反应速度就又慢慢降下来了。
这就像一场狂欢,到最后大家都累了,活动也就渐渐平息下来了。
那自由基聚合反应的产物又是什么样的呢?它的产物是聚合物,就像用一个个小珠子串成的长长的链子。
这些聚合物的分子量可不一定是一模一样的哦,它们有大有小,就像一群高矮胖瘦各不相同的小伙伴。
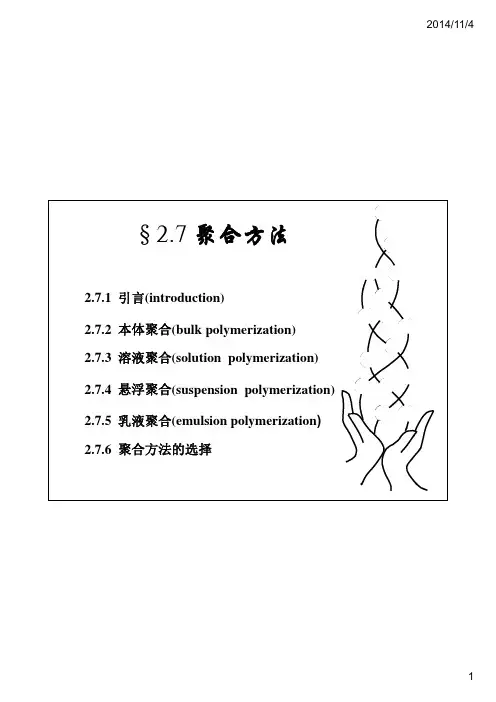
2.7.1 引言(introduction)2.7.2 本体聚合(bulk polymerization)2.7.3 溶液聚合(solution polymerization) 2.7.4 悬浮聚合(suspension polymerization) 2.7.5 (emulsion polymerization.7.5乳液聚合(e u s o po y e o) 2.7.6 聚合方法的选择2.7.1 引言一、聚合工艺引发剂引发剂(催化剂)制备溶、助剂的配制原料制备与精制聚合单体聚单体的精制聚合方法$反应聚合合工艺实施由原料到实施聚合反应分离产物分离$$物产品的一系列工序与流程精制干燥成形产品后处理$2.7.1 引言二、聚合反应与聚合方法由小分子合成聚合物的反应,研究聚合热力学、动力学、机理、历程等(连锁聚合-自由基、阳离聚合反应实施聚合反应的方法,研究物料配比、组成、工艺条件、场所、过程等(连锁聚合-本体、溶液、悬浮、-子、阴离子、配位,逐步聚合-线性、体型)聚合方法乳液,逐步聚合熔融、溶液、界面、固相)连锁聚合:本体聚合Bulk Polymerization溶液聚合Solution Polymerization悬浮聚合Suspension Polymerization乳液聚合Emulsion Polymerization逐步聚合:熔融缩聚Melt Polymerization溶液聚合Solution Polymerization界面缩聚Interfacial Polymerization固相缩聚Sold Polymerization2.7.1 引言三、聚合方法的分类聚合体系和实施方法示例单体-介质体系聚合方法聚合物-单体(或溶剂)体系均相聚合沉淀聚合本体聚合气态苯乙烯乙烯高压聚合氯乙烯均相体系液态固态丙烯酸酯类丙烯腈溶液聚合苯乙烯-苯丙烯酸-水丙烯腈-二甲基甲苯乙烯-甲醇丙烯酸-己烷-酰胺丙烯腈水非均相体系悬浮聚合苯乙烯甲基丙烯酸甲酯氯乙烯乳液聚合苯乙烯、丁二烯氯乙烯2.7.2 本体聚合一、定义bulk polymerization单体本身在不加溶剂以及其它分散剂的条件下,由引发剂或直接由光热等作用下引发的聚合反应二、组成单体+(油溶性)引发剂2.7.2 本体聚合三、特点优点1 组分少,产品纯度高(适于透明材料)2 组分少,成本低(设备少,后处理简单,费用低)3 组分少,生产效率高(只有单体,[M]大,聚合快)4 可以气、液、固三态实现缺点 5 体系粘度大,聚合热不易扩散,易暴聚6 产品不理想,易支化、交联解决办法A 反应进行到一定转化率即将产品分离B 较低温度或光、辐射引发,较低引发剂浓度C 分阶段聚合(PMMA:三段聚合)D 强化传热设备2.7.2 本体聚合四、工业化品种可广泛用于各种链锁聚合、逐步聚合等。

高等有机化学教案之自由基(Radical)第一章:自由基概述1.1 自由基的定义与特性1.2 自由基的产生与检测1.3 自由基的重要反应及应用第二章:自由基的产生与衰变2.1 热引发的自由基反应2.2 光引发的自由基反应2.3 自由基的衰变过程第三章:自由基的加成反应3.1 自由基加成反应的机理3.2 自由基加成反应的类型及特点3.3 自由基加成反应在有机合成中的应用第四章:自由基的消除反应4.1 自由基消除反应的机理4.2 自由基消除反应的类型及特点4.3 自由基消除反应在有机合成中的应用第五章:自由基的聚合反应5.1 自由基聚合反应的机理5.2 自由基聚合反应的类型及特点5.3 自由基聚合反应在材料科学中的应用第六章:自由基反应的调控与应用6.1 自由基反应的调控策略6.2 自由基反应在有机合成中的应用6.3 自由基反应在材料科学中的应用第七章:自由基反应的机理研究7.1 自由基反应的实验研究方法7.2 自由基反应的计算化学研究方法7.3 自由基反应机理的案例分析第八章:自由基反应的动力学8.1 自由基反应的动力学方程8.2 自由基反应速率常数的测定8.3 自由基反应动力学在有机合成中的应用第九章:自由基反应的生物化学应用9.1 自由基在生物体内的与清除9.2 自由基在生物体内的作用及机制9.3 自由基反应在药物设计与生物制药中的应用第十章:自由基反应的环境影响与应用10.1 自由基反应在大气化学中的应用10.2 自由基反应在水处理中的应用10.3 自由基反应在其他环境领域中的应用重点和难点解析重点一:自由基的定义与特性自由基是化学反应中非常重要的一类中间体,具有未成对的电子,具有高度的反应活性。
在有机化学反应中,自由基的、反应及终止过程是理解和掌握有机化学反应机理的关键。
重点二:自由基的产生与检测自由基的产生途径有热引发、光引发等,检测方法包括电子自旋共振(ESR)光谱、气相色谱(GC)等。

高中化学聚合反应概念教案课时安排:1课时教学目标:1.了解聚合反应的基本概念和特点;2.掌握聚合反应的实质和原理;3.理解聚合物的结构和性质。
教学重点:1.聚合反应的定义和分类;2.聚合反应的机理和条件。
教学准备:教师:准备黑板、粉笔、聚合反应的示意图;学生:预习相关内容,提前准备好笔记本和笔。
教学步骤:Step 1:导入(5分钟)教师向学生们提出问题:什么是聚合反应?为什么聚合反应在生活中起着重要作用?带动学生思考和讨论。
Step 2:讲解(15分钟)1.聚合反应的定义和分类:将聚合反应定义为将小分子(单体)通过共价键相连,形成高分子(聚合物)的反应过程。
介绍线性聚合和交联聚合两种基本分类。
2.聚合反应的机理和条件:介绍聚合反应的机理,即重复单元分子间的共价键连接。
讲解聚合反应的条件,如适当的温度、催化剂等条件。
Step 3:实例分析(15分钟)通过举例介绍一些生活中常见的聚合反应,如聚乙烯、聚苯乙烯等。
分析这些聚合反应的机理和特点,帮助学生更好地理解聚合反应的实质。
Step 4:练习与讨论(15分钟)提供一些聚合反应的练习题,让学生在课堂上进行讨论和解答。
帮助学生巩固所学内容,提高解决问题的能力。
Step 5:总结(5分钟)对本节课的重点内容进行总结,并强调学生需要加强的地方。
鼓励学生在课后继续复习和巩固所学的知识。
教学反思:本节课主要介绍了聚合反应的概念和特点,帮助学生理解聚合反应在化学中的重要性。
通过实例分析和练习讨论,让学生更深入地了解聚合反应的机理和条件。
在未来的教学中,可以结合更多实际例子,帮助学生更好地理解和应用聚合反应的知识。


第二章自由基聚合(radical polymerization)【课时安排】2.1 单体的聚合能力2学时2.2 自由基聚合机理4学时2.3 链引发反应3学时2.4 聚合反应动力学2学时2.5 相对分子质量1学时2.6 链转移反应2学时2.7 聚合方法4学时总计18学时【掌握内容】1.单体聚合能力:热力学(△E, △S,T,P);动力学(空间效应-聚合能力,电子效应-聚合类型)2.自由基基元反应每步反应特征,自由基聚合反应特征3.常用引发剂的种类和符号,引发剂分解反应式,表征方法(四个参数),引发剂效率,诱导效应,笼蔽效应,引发剂选择原则4.聚合动力学:聚合初期:三个假设,四个条件,反应级数的变化,影响速率的四因素(M,I,T,P);聚合中后期的反应速率的研究:自动加速现象,凝胶效应,沉淀效应;聚合反应类型5.相对分子质量:动力学链长,聚合度及影响其的四因素(M,I,T,P),6.链转移:类型,聚合度,动力学分析,阻聚与缓聚7.本体,溶液,悬浮,乳液四大聚合方法配方,基本组成,优缺点及主要品种【熟悉内容】1.热、光、辐射聚合。
2.聚合动力学研究方法。
3 自由基聚合的相对分子质量分布。
4 悬浮聚合与乳液聚合所用分散剂种类、聚合过程。
【了解内容】1. 通用单体来源。
2. 自由基聚合进展。
【教学难点】1. 对具体单体聚合热力学与动力学的综合分析2. 终止方式的相对比例及其与体系状态的关系3. 氧化还原类的反应式;笼蔽效应与诱导效应4. 不同条件下反应速率对单体与引发剂浓度的反应级数的推导与分析5. 区别聚合反应速率、动力学链长、平均聚合度的影响因素和变化趋势6. 向不同转移对象的链转移程度的难易分析7. 乳液聚合机理及动力学【教学目标】1. 掌握自由基聚合相关基本概念。
2. 掌握自由基聚合常见单体、引发剂、阻聚剂、聚合方法。
3. 达到如下技能:(1)单体聚合能力的判断与类型的选择(2)引发剂的选择及正确书写引发反应式(3)正确书写任一体系的基元反应式(4)根据动力学方程计算各参数,选择适当方法控制反应进程(5) 根据相对分子质量方程计算各参数,选择适当方法控制产物结构(6)设计聚合工艺,线路与配方2.1 单体的聚合能力【教学内容】2.1.1 聚合热力学一聚合热二聚合熵三聚合温度四小结2.1.2 聚合动力学一连锁聚合种类与活性中心二单体对聚合类型的选择及聚合能力1 取代基对聚合能力的影响(空间效应)2 取代基对聚合类型的选择(电子效应)3 单体共聚能力【授课时间】2学时【教学重点】1影响聚合热的主要因素及其规律2单体对聚合类型的选择及聚合能力【教学难点】1影响聚合热的主要因素及其规律2 对具体单体聚合热力学与动力学的综合分析【教学目标】1 掌握影响聚合热的主要因素及其规律2掌握取代基对单体聚合类型选择及聚合能力的影响规律3 能正确综合分析具体单体的聚合热力学与动力学行为【教学手段】课堂讲授,辅以实例练习【教学过程】聚合能力:化学结构:两个可相互反应官能团常见聚合单体类型两个以上有机官能团单体C=C-X热力学:方向,限度,∆G<0 R-C=O动力学: 聚合方法杂环(O,N,P,S)2.1.1 聚合热力学∆G=∆H-T∆S= ∆E+P∆V-T∆S<0 聚合;=0 达到平衡;>0 解聚一聚合热∆H=∆E+P∆V1 内能变化∆E=∆E f+∆E R+∆E s+∆E’=( E fp - E fm)+( E Rp - E Rm)+( E sp - E sm)+ ∆E’E f------由键能所贡献的内能E R-----由共振效应所贡献的内能E s------由空间张力或位阻效应所贡献的内能∆E’----其它因素引起的内能变化(1) 双键断裂能CH 2=CH 2 -CH 2-CH 2- ∆E f =εm -εp=609.2-2×351.7=-94.2 kJ.mol -1 (实测值∆H=-88.8 kJ.mol -1)(2)共轭效应增强,|—∆H|减小(3)位阻效应增强,|—∆H|减小 (4)氢键与溶剂化作用增强,|—∆H|减小 (5)强电负性取代基的存在使|—∆H|增强(6)需具体综合分析2 压力影响: 压力增大,有利于聚合物进行二 聚合熵 ∆S=-100~-125 kJ.mol -1三 聚合温度1 聚合上限温度∆G=∆H-T ∆S=0→T c =∆H/∆S (不同压力与活度下数值)→T c 有一系列,对应一系列平衡单体浓度→常规定[M] e =1mol/L 时T c 为聚合上限温度→T c =∆H 0/∆S 02 平衡单体浓度eo oM RT S H Tc ]ln[+∆∆= 四 小结增强聚合倾向内因 ∆S 影响不大∆E: 降低共轭效应, 降低位阻效应, 降低氢键与溶剂化作用,增强强电负性取代基 外因 增大压力,降低温度可解释α-甲基苯乙烯(α-MeSt )的聚合现象2.1.2 聚合动力学一 连锁聚合种类与活性中心根据引发活性种与链增长活性中心的不同,链式聚合反应可分为自由基聚合、阳离子聚合、阴离子聚合和配位聚合等二 单体对聚合类型的选择及聚合能力1 取代基对聚合能力的影响(空间效应)(1)单取代能聚合(2)双取代一般可以聚合,但基团太大时难以聚合(3)三、四取代一般不可以聚合,氟取代除外2 取代基对聚合类型的选择(电子效应)(1) 取代基的诱导效应A A 自由基:2A A CH 2CH XA B 阳离子CH =CHX A CH 2H C X离解A +B -δ+B δ-A B 阴离子A CH 2H C X 离解A -B +δ+B δ-带给电子基团的烯类单体易进行阳离子聚合带吸电子基团的烯类单体易进行阴离子聚合与自由基带强给电子基团、强吸电子基团的烯类单体只能分别进行阳离子、阴离子聚合(2) 取代基的共轭效应:流动性大,易诱导极化,可进行多种机理的聚合反应(3) 带不同基团的单体进行几种聚合时的排序 阳离子聚合取代基-X: -NO 2,-CN,-F,-Cl,-COOCH 3,-CONH 2,-OCOR,-CH=CH 2,-C 6H 5,-CH 3,-OR 自由基聚合阴离子聚合3 单体共聚能力:与参与共聚的各种单体均有关2.2 自由基聚合机理【教学内容】2.2.1 自由基2.2.2 自由基聚合的基元反应一 链引发反应(chain initiation )二 链增长反应(chain growth )三 链终止反应(chain termination )四 链转移反应(chain transfer )2.2.3 自由基聚合的反应特征【授课时间】4学时【教学重点】自由基聚合的基元反应;自由基聚合反应特征【教学难点】终止方式的相对比例及其与体系状态的关系【教学目标】1 掌握自由基聚合机理2 掌握自由基聚合反应特征3 能正确写出具体聚合物的基元反应式【教学手段】课堂讲授,配以Flash 动画演示,辅以学生讨论【教学过程】2.2.1 自由基一 分类与产生二 活性1 影响因素:共轭效应大,吸电子诱导效应大,位阻效应强,稳定性强,活性小2 活性顺序三 反应:加成反应,氧化还原反应,偶合反应,脱氢反应,消去反应2.2.2 自由基聚合的基元反应一 链引发反应(chain initiation ) 慢 单体自由基引发剂引发为例二 链增长反应(chain growth ) 快 活性高分子链I 2 Ik I k i I CH 2引发活性种,初级自由基,引发自由基H 2C CHX +CHX M链结构在该步形成:序列结构→头尾为主顺反结构→温度升高有利于顺式结构生成立体结构→无规结构三 链终止反应(chain termination) 速 稳定大分子1 双基终止(均相体系,主要方式) PS,PAN 偶合为主; PMMA 偶合歧化兼有; PVAc 歧化为主问题:k t >>k p , 为何还可得到大分子?2 单基终止四 链转移反应(chain transfer )一定条件下 不同活性的链自由基 2.2.3 自由基聚合的反应特征 1 慢反应,快增长,速终止234 放热反应,低温有利2.3 链引发反应k I CH 2H 2C CH+CH XMCH 2CH CH 2CH 2偶合:CH 2CH CH CH 2歧化:CH 2CH 2CH 2CH 2CH CH X +k k k CH 2+CH S + SCH 2CH 2【教学内容】2.3.1 引发剂类型一 热分解型二 氧化还原类2.3.2 引发剂活性(表征方法)2.3.3 引发剂效率f2.3.4 引发剂的选择【授课时间】2学时【教学重点】典型类型引发剂;引发剂活性表征方法;引发剂效率及影响因素;引发剂的选择原则【教学难点】氧化还原类的反应式;笼蔽效应与诱导效应【教学目标】1 掌握引发剂活性表示方法及其计算方法2掌握引发剂效率、笼蔽效应、诱导效应等基本概念3能正确写出典型引发剂的结构式与引发反应式4 能根据具体要求选择匹配的引发剂【教学手段】课堂讲授,辅以多媒体幻灯图片及实例【教学过程】2.3.1 引发剂类型一 热分解型(Ed=80~140kJ/mol ,中高温使用)1 偶氮类引发剂2 过氧类引发剂(1) 有机过氧类a 烷基过氧化氢(RC-O-O-H):异丙苯过氧化氢(CHP ),叔丁基过氧化氢(t-BHP)b 二烷基过氧化物(R-O-O-R ’):过氧化二异丙苯c 过氧化酯(RCOOCR ’)d 过氧化二酰(RCOOOCOR ’)R 1C R 2N N C R 1R 2R C R N N C R 1R 2对称不对称(X=吸电子取代基)H 3C C CH 3CN N N C CH 3CH 3CN H 3C C CH 3CN 2+ N 2偶氮二异丁腈(AIBN)Ph C O C O Ph 2Ph C O O Ph C O OPh + CO 2过氧化苯甲酰(BPO )e 过氧化二碳酸酯(ROOC-O-O-COOR ’):过氧化二碳酸二异丙酯(IPP)(2) 无机过氧类:S 2O 82─→2 SO 4‧─二 氧化还原类(Ed=40~60kJ/mol ,低温使用)1 水溶性(1) 生成一种R ‧HOOH + Fe 2+→HO ‧+OH ─+Fe 3+S 2O 82─+ Fe 2+ →SO 42─ + SO 4‧─+Fe 3+用量:还原剂<氧化剂,否则Fe 2++‧OH →Fe 3++OH ─白白消耗自由基(2) 生成一种R ‧S 2O 82─+ SO 32─→SO 42─+ SO 4‧─+ SO 3‧─2 油溶性2.3.2 引发剂活性(表征方法)一 分解速率常数kd 越大,引发剂活性越大I k dt I d R d d =-=][二 分解活化能Ed 越小,引发剂活性越大三 半衰期t 1/2越小,引发剂活性越大2/12/][][ln t k I I d o o = 四 残留分率[I]/[I]o 越小,引发剂活性越大2.3.3 引发剂效率f一二 笼蔽效应(Cage Effect)引发剂分解产生的初级自由基,在开始的瞬间被溶剂分子所包围,不能与单体分子接触,无法发生链引发反应。

自由基聚合的基元反应及特点
自由基聚合是一种重要的化学反应,它是由自由基引发的聚合过程。
在这种反应中,自由基起着关键的作用,它们是一种具有未成对电子的分子或原子,非常活跃并且容易参与化学反应。
自由基聚合的基元反应是指一个自由基引发的聚合反应,其中一个自由基引发一个或多个单体分子的聚合。
自由基聚合的基元反应通常包括以下几个步骤:
1. 引发步骤,在这一步骤中,引发剂(通常是一种高能化合物或光引发剂)通过提供能量或引发反应来产生自由基。
2. 传递步骤,在这一步骤中,自由基与单体分子发生反应,形成一个新的自由基和一个共轭双键。
这个新的自由基可以继续引发下一个单体分子的聚合反应。
3. 终止步骤,在这一步骤中,自由基聚合反应会最终停止,通常是由于两个自由基相遇并结合,或者是由于反应物已经用尽。
自由基聚合的基元反应具有以下特点:
1. 高度活泼,自由基是非常活跃的分子或原子,它们容易参与
化学反应并引发聚合反应。
2. 高度选择性,自由基聚合反应通常具有较高的选择性,可以
通过选择合适的引发剂和反应条件来控制聚合的过程和产物的结构。
3. 高度灵活性,由于自由基聚合反应不受限于特定的官能团或
化学键,因此可以用于合成各种类型的高分子材料。
自由基聚合的基元反应在合成聚合物、涂料、胶粘剂等领域具
有广泛的应用,它为我们提供了一种重要的合成工具,可以合成出
具有特定性能和结构的高分子材料。
随着对自由基聚合反应机理的
深入研究和对引发剂的不断改进,相信自由基聚合反应将在未来得
到更广泛的应用和发展。

第四章自由基链式聚合实施方法本章要点:1.自由基链式聚合的实施:通常有本体聚合、溶液聚合、悬浮聚合和乳液聚合,它们有不同的适用场合,有着各自的优缺点;2.本体聚合:为解决散热问题,采用分段聚合;3.溶液聚合:溶剂的选择性是关键;4.悬浮聚合:聚合机理同常规的本体或溶液聚合,分散剂起到关键作用,产物的粒径达到mm级;5.乳液聚合:具有特殊的聚合机理和聚合规律,通过增加乳化剂用量可同时提高聚合速率和产物的分子量;6.大品种高分子:低密度聚乙烯、聚苯乙烯、聚甲基丙烯酸甲酯、聚乙酸乙烯酯和丁苯橡胶等等,宜采取适当方法生产。
本章难点:1.乳液聚合的聚合场所:增溶胶束和乳胶粒为乳液聚合的主要差所;2.乳液聚合的聚合过程:根据聚合速率,乳液聚合分为三个阶段;聚合过程中单体和乳化剂的物料转移由单体液滴、至水相、再至乳胶粒;聚合过程中分散相(胶束、单体液滴和乳胶粒)按一定规律变化;3.乳液聚合动力学:经典的乳液聚合包含许多理想条件。
4.1 聚合方法和聚合体系4.1.1 单体在反应介质中的分散状态本体聚合没有反应介质,溶液聚合中单体以分子状态溶解在反应介质,悬浮聚合中单体以mm级的分散相悬浮于反应介质中,在乳液聚合中单体主要存在于分散相的单体液滴和乳胶粒中。
4.1.2. 按聚合体系的相态单体及其聚合物以分子状态溶解在反应介质中,聚合体系成为一相,此时为均相聚合;反之,单体或/和聚合物不溶于反应介质,聚合体系具有多个相,此时为非均相聚合。
4.1.3. 按单体的物理状态分类分为气相聚合、液相聚合和固相聚合。
4.2 本体聚合4.2.1 本体聚合的组成和特点本体聚合体系由单体、引发剂和少量助剂组成。
除用引发剂进行聚合以外,还可用光和辐照来进行聚合。
本体聚合的聚合速率高,产物纯度大,但是散热和搅拌困难。
4.2.2 本体聚合的适用场合产物纯度高,特别适用于生产板材和型材等透明制品,且所用设备比较简单。
本体聚合反应,也特别适合于实验室研究。

丙烯酸乙酯的自由基聚合反应有何特点丙烯酸乙酯是一种重要的有机化合物,广泛用于塑料、化妆品、涂料、油墨等领域。
其中,丙烯酸乙酯的自由基聚合反应具有重要的理论和应用价值。
本文将探讨丙烯酸乙酯的自由基聚合反应的特点。
一、反应机理自由基聚合是一种以自由基为反应中心的反应机理。
当丙烯酸乙酯在引发剂的作用下形成自由基时,它会与附近的丙烯酸乙酯分子反应,形成另一个自由基。
这个自由基又会与其他分子反应,形成更多的自由基。
这样的反应过程会不断扩散,最终形成大量的高分子物质。
二、引发剂的选择在自由基聚合反应中,引发剂的选择对反应的效果至关重要。
针对丙烯酸乙酯的聚合反应,一般选择过氧化苯甲酰或过氧化二异丙苯作为引发剂。
这些引发剂可以通过热解产生自由基,从而引发聚合反应。
三、特殊反应条件聚合反应需要满足一定的条件,如反应温度、压力、反应物浓度等。
对于丙烯酸乙酯的聚合反应,一般需要在高温下进行。
理论上,温度越高,聚合速度越快。
但是,过高的温度会导致聚合产物的聚合程度过高,从而影响聚合速率。
此外,由于自由基反应具有较强的爆炸性,聚合反应需要在惰性气氛下进行。
四、聚合产物的性能丙烯酸乙酯的自由基聚合反应所形成的聚合产物具有多种优良性能。
首先,聚合物具有良好的透明性和光学性能,可以应用于光学器件等领域。
其次,聚合物具有较高的耐化学性和耐热性,能够耐受各种化学物质的腐蚀和高温环境。
此外,聚合物还具有良好的可加工性和成型性,可以通过注塑、挤出等工艺制成各种形状的产品。
综上所述,丙烯酸乙酯的自由基聚合反应是一种复杂的反应过程,需要在特定的条件下进行。
聚合产物具有多种优良性能,广泛应用于生产和科研领域。
未来,随着聚合技术的不断发展,丙烯酸乙酯的聚合反应仍将有广阔的应用前景。

了解有机化学中的自由基聚合反应反应机制和应用自由基聚合反应是有机化学中非常重要的一种反应类型,它在合成高分子材料、制备聚合物以及药物研发等领域都具有广泛的应用。
本文将深入探讨自由基聚合反应的机理和应用。
一、自由基聚合反应的机制自由基聚合反应是一种通过自由基的自由基反应形成聚合物链的过程。
该反应包括三个关键步骤:起始、传递和终止。
1. 起始自由基聚合反应的起始是通过引入一种起始剂,使之发生自由基解离,生成两个自由基。
常用的起始剂有过氧化物、硝酸酯和过氧硫酸铵等。
起始剂的解离会产生两个自由基,从而引发聚合链的生成。
2. 传递传递是自由基聚合反应的核心步骤,主要是自由基与单体分子之间的反应。
在传递过程中,自由基会与单体发生加成反应,生成一个新的自由基和一个共价键。
新生成的自由基会继续参与到传递反应中,进一步延长聚合链。
3. 终止自由基聚合反应的终止过程会导致聚合链的停止,从而形成聚合物。
终止反应可以分为两种类型:链传递终止和自由基自身的消失。
链传递终止是指两个自由基之间的反应,例如两个聚合链相遇并发生反应。
自由基自身的消失则是指自由基与其他物质发生反应或自由基的自发消失。
二、自由基聚合反应的应用自由基聚合反应的机理和特点使其在许多领域中得到广泛应用。
1. 聚合物合成自由基聚合反应是合成聚合物的主要方法之一。
通过选择不同的单体和起始剂,可以合成出具有不同结构和性能的聚合物。
聚合物的种类包括聚乙烯、聚苯乙烯、聚丙烯等广泛应用的工程塑料。
2. 化学药品合成自由基聚合反应在药物合成过程中也起到重要作用。
许多药物合成的关键步骤利用了自由基聚合反应的特点,通过选择不同的单体和反应条件,实现对目标化合物的构建。
3. 材料科学自由基聚合反应在材料科学领域有丰富的应用。
通过控制反应条件和单体的选择,可以制备出具有特定结构和性能的高分子材料,如塑料、橡胶和纤维。
4. 生物医学工程自由基聚合反应在生物医学工程领域中也得到广泛应用。
自由基聚合反应的特征教案生命科学学院 03091115 朱孙燕一、教学目标1、根据机理分析,重点掌握自由基聚合机理的特征。
2、根据自由基聚合反应中各基元反应的速率和活化能大小,将其概括为慢反应、快增长和速终止。
3、利用图象的关系直观地了解聚合度、单体转化率和时间的关系。
4、了解自由基聚合反应的有利条件。
二、教学重点与难点1、将自由基聚合反应概括为慢引发、快增长和速终止。
2、利用图象的关系直观地了解聚合度、单体转化率和时间的关系。
区分聚合度和转化率与时间的关系。
三、教学方式利用多媒体教学四、教学过程1、引言通过以上几位同学的分析,大家应该对自由基聚合反应的机理有了定性的理解,接下来让我和大家一起来学习一下自由基聚合反应的特征。
(多媒体课件展示5条特征,让同学对整体先有一个了解,接下来逐个进行分析。
)2、提问:通过以上学习,我们可以得出自由基聚合反应在微观上可以明显地区分为哪些基元反应?回答:链的引发、增长、终止和转移等。
3、特征①讲解分析:在前面的链引发、增长、终止的学习中,我们已经知道链的引发速率是最小的,而活化能是最高的;链的增长速率极高,而活化能很低;链的终止速率极高,而活化能很低,甚至为零。
从中我们可以很明显地根据瓶颈效应得出,链的引发速率是控制整个聚合速率的关键。
因此我们还可以将自由基聚合反应特征概括为:慢引发、快增长和速终止。
4、特征②(只有链增长反应才使聚合度增加)、③(延长聚合时间主要提高转化率)。
讲解分析:在学习链引发、增长、终止时我们很明显可以知道只有链增长反应才使聚合度增加。
一个单体分子从引发、经增长和终止,转变成大分子,时间极短,不能停留在中间聚合度阶段,反应混合物紧由单体和聚合物组成。
在学习链增长时我们已经了解到了,链增长速率极高,在0.01~几秒的时间内,就可使聚合物的聚合度达到数千,甚至上万。
特别强调的一点是在聚合反应全过程中,聚合度变化较小,延长时间主要是为了提高单体的转化率。
自由基聚合反应的特征教案
生命科学学院 03091115 朱孙燕
一、教学目标
1、根据机理分析,重点掌握自由基聚合机理的特征。
2、根据自由基聚合反应中各基元反应的速率和活化能大小,将其概括为慢反应、快增长
和速终止。
3、利用图象的关系直观地了解聚合度、单体转化率和时间的关系。
4、了解自由基聚合反应的有利条件。
二、教学重点与难点
1、将自由基聚合反应概括为慢引发、快增长和速终止。
2、利用图象的关系直观地了解聚合度、单体转化率和时间的关系。
区分聚合度和转化率
与时间的关系。
三、教学方式
利用多媒体教学
四、教学过程
1、引言
通过以上几位同学的分析,大家应该对自由基聚合反应的机理有了定性的理解,接下来让我和大家一起来学习一下自由基聚合反应的特征。
(多媒体课件展示5条特征,让同学对整体先有一个了解,接下来逐个进行分析。
)2、提问:通过以上学习,我们可以得出自由基聚合反应在微观上可以明显地区分为哪些
基元反应?
回答:链的引发、增长、终止和转移等。
3、特征①讲解分析:在前面的链引发、增长、终止的学习中,我们已经知道链的引发速
率是最小的,而活化能是最高的;链的增长速率极高,而活化能很低;链的终止速率极高,而活化能很低,甚至为零。
从中我们可以很明显地根据瓶颈效应得出,链的引发速率是控制整个聚合速率的关键。
因此我们还可以将自由基聚合反应特征概括为:慢引发、快增长和速终止。
4、特征②(只有链增长反应才使聚合度增加)、③(延长聚合时间主要提高转化率)。
讲解分析:在学习链引发、增长、终止时我们很明显可以知道只有链增长反应才使聚合度增加。
一个单体分子从引发、经增长和终止,转变成大分子,时间极短,不能停留在中间聚合度阶段,反应混合物紧由单体和聚合物组成。
在学习链增长时我们已经
了解到了,链增长速率极高,在0.01~几秒的时间内,就可使聚合物的聚合度达到数千,甚至上万。
特别强调的一点是在聚合反应全过程中,聚合度变化较小,延长时间主要是为了提高单体的转化率。
接下来我们根据图表来更加直观地认识这两个特征。
图表分析:
图1
图1 图2
从图表1中我们可以很明显地看出,聚合物的分子量在极短的时间内急剧增大,随着时间的推移其变化并不是很大,所以我们说延长聚合时间主要提高转化率,而对聚合物聚合度的影响不是很大。
从图表2中可以看出在聚合过程中,聚合物浓度随着时间的推移不断提高,因此我们也可以得出延长聚合时间主要提高转化率。
书上提到了凝胶效应将使分子量增加,凝胶是不溶于任何溶剂中相当于许多线型大分子交联成一整体,分子量我们可以将其看作无穷大。
5、特征④(放热反应,低温有利)讲解分析:我们已经知道自由基聚合反应是一个放热
反应,因此我们可以根据勒沙特列原理知道低温有利于该反应的进行。
6、特征⑤(少量阻聚剂足以使聚合反应终止)(该点作一定的了解)。
7、总结回顾5条自由基聚合反应的特征。
五、教学反思
通过参加本次换位教学教学活动,进一步锻炼了我的师范技能,让我在实践中去运用理论,感受作为一名人民教师的职责。
结合我实习的小小经验,我发现自己还是在不断进步的,但同时还存在着不足。
内容简单是我初次上课的一个挑战,如何将简单的内容生动化、具体化、直观化是上课的一个闪光点,通过本次锻炼,让我进一步去重视这方面的培养。
同时教学是一个互动的过程,学生的主动需要老师作为催化剂,适当的教学幽默是教学的一个境界,我想让学生在轻松的环境下接受知识是最可取的一种教学手段,通过本次亲身体验,让我大大体会到自己的不足之处,相信不断地实践一定会锻炼我成才的。