必修2 化学方程式
- 格式:doc
- 大小:126.00 KB
- 文档页数:5

1、硫酸根离子的检验: BaCl2 + Na2SO4 ==== BaSO4↓+ 2NaCl2、碳酸根离子的检验: CaCl2 + Na2CO3 ===== CaCO3↓ + 2NaCl3、碳酸钠与盐酸反应: Na2CO3 + 2HCl ===== 2NaCl + H2O + CO2↑4、木炭还原氧化铜: 2CuO + C 高温2Cu + CO2↑5、铁片与硫酸铜溶液反应: Fe + CuSO4 ===== FeSO4 + Cu6、氯化钙与碳酸钠溶液反应:CaCl2 + Na2CO3 ===== CaCO3↓+ 2NaCl7、钠在空气中燃烧:2Na + O2 Na2O2钠与氧气反应:4Na + O2 ==== 2Na2O8、过氧化钠与水反应:2Na2O2 + 2H2O ==== 4NaOH + O2↑9、过氧化钠与二氧化碳反应:2Na2O2 + 2CO2 ==== 2Na2CO3 + O210、钠与水反应:2Na + 2H2O ==== 2NaOH + H2↑11、铁与水蒸气反应:3Fe + 4H2O(g) ==== F3O4 + 4H2↑12、铝与氢氧化钠溶液反应:2Al + 2NaOH + 2H2O ==== 2NaAlO2 + 3H2↑13、氧化钙与水反应:CaO + H2O ==== Ca(OH)214、氧化铁与盐酸反应:Fe2O3 + 6HCl ===== 2FeCl3 + 3H2O15、氧化铝与盐酸反应:Al2O3 + 6HCl ===== 2AlCl3 + 3H2O16、氧化铝与氢氧化钠溶液反应:Al2O3 + 2NaOH ===== 2NaAlO2 + H2O17、氯化铁与氢氧化钠溶液反应:FeCl3 + 3NaOH ===== Fe(OH)3↓+ 3NaCl18、硫酸亚铁与氢氧化钠溶液反应:FeSO4 + 2NaOH ==== Fe(OH)2↓+ Na2SO419、氢氧化亚铁被氧化成氢氧化铁:4Fe(OH)2 + 2H2O + O2 ==== 4Fe(OH)320、氢氧化铁加热分解:2Fe(OH)3 Fe2O3 + 3H2O↑21、实验室制取氢氧化铝:Al2(SO4)3 + 6NH3·H2O ==== 2Al(OH)3↓ + 3(NH3)2SO422、氢氧化铝与盐酸反应:Al(OH)3 + 3HCl ==== AlCl3 + 3H2O23、氢氧化铝与氢氧化钠溶液反应:Al(OH)3 + NaOH ==== NaAlO2 + 2H2O24、氢氧化铝加热分解:2Al(OH)3 Al2O3 + 3H2O25、三氯化铁溶液与铁粉反应:2FeCl3 + Fe ==== 3FeCl226、氯化亚铁中通入氯气:2FeCl2 + Cl2 ===== 2FeCl327、二氧化硅与氢氟酸反应:SiO2 + 4HF ==== SiF4 + 2H2O硅单质与氢氟酸反应:Si + 4HF ==== SiF4 + 2H2↑28、二氧化硅与氧化钙高温反应:SiO2 + CaO 高温CaSiO329、二氧化硅与氢氧化钠溶液反应:SiO2 + 2NaOH ==== Na2SiO3 + H2O30、往硅酸钠溶液中通入二氧化碳:Na2SiO3 + CO2 + H2O ===Na2CO3 + H2SiO3↓31、硅酸钠与盐酸反应:Na2SiO3 + 2HCl === 2NaCl + H2SiO3↓32、氯气与金属铁反应:2Fe + 3Cl2点燃2FeCl333、氯气与金属铜反应:Cu + Cl2 点燃CuCl234、氯气与金属钠反应:2Na + Cl2点燃2NaCl35、氯气与水反应:Cl2 + H2O ==== HCl + HClO36、次氯酸光照分解:2HClO 光照2HCl + O2↑37、氯气与氢氧化钠溶液反应:Cl2 + 2NaOH ===== NaCl + NaClO + H2O38、氯气与消石灰反应:2Cl2 + 2Ca(OH)2 ==== CaCl2 + Ca(ClO)2 + 2H2O39、盐酸与硝酸银溶液反应:HCl + AgNO3 ==== AgCl↓ + HNO340、漂白粉长期置露在空气中:Ca(ClO)2 + H2O + CO2 ==== CaCO3↓ + 2HClO41、二氧化硫与水反应:SO2 + H2O === H2SO342、氮气与氧气在放电下反应:N2 + O2放电2NO43、一氧化氮与氧气反应:2NO + O2 ==== 2NO244、二氧化氮与水反应:3NO2 + H2O ==== 2HNO3 + NO45、二氧化硫与氧气在催化剂的作用下反应:2SO2 + O2催化剂2SO346、三氧化硫与水反应:SO3 + H2O ==== H2SO447、浓硫酸与铜反应:Cu + 2H2SO4(浓) CuSO4 + 2H2O + SO2↑48、浓硫酸与木炭反应:C + 2H2SO4(浓) CO2↑+ 2SO2↑ + 2H2O49、浓硝酸与铜反应:Cu + 4HNO3(浓) ==== Cu(NO3)2 + 2H2O + 2NO2↑50、稀硝酸与铜反应:3Cu + 8HNO3(稀) 3Cu(NO3)2 + 4H2O + 2NO↑51、氨水受热分解:NH3·H2O NH3↑ + H2O52、氨气与氯化氢反应:NH3 + HCl ==== NH4Cl53、氯化铵受热分解:NH4Cl NH3↑ + HCl↑54、碳酸氢氨受热分解:NH4HCO3 NH3↑ + H2O↑ + CO2↑55、硝酸铵与氢氧化钠反应:NH4NO3 + NaOH NH3↑ + NaNO3 + H2O56、氨气的实验室制取:2NH4Cl + Ca(OH)2 CaCl2 + 2H2O + 2NH3↑57、氯气与氢气反应:Cl2 + H2点燃2HCl58、硫酸铵与氢氧化钠反应:(NH4)2SO4 + 2NaOH 2NH3↑ + Na2SO4 + 2H2O59、SO2 + CaO ==== CaSO360、SO2 + 2NaOH ==== Na2SO3 + H2O61、SO2 + Ca(OH)2 ==== CaSO3↓ + H2O62、SO2 + Cl2 + 2H2O ==== 2HCl + H2SO463、SO2 + 2H2S ==== 3S + 2H2O64、NO、NO2的回收:NO2 + NO + 2NaOH ==== 2NaNO2 + H2O65、Si + 2F2 === SiF466、Si + 2NaOH + H2O ==== Na2SiO3 +2H2↑67、硅单质的实验室制法粗硅的制取:SiO2 + 2C 高温电炉Si + 2CO(石英沙)(焦碳)(粗硅)粗硅转变为纯硅:Si(粗) + 2Cl2 SiCl4SiCl4 + 2H2高温Si(纯)+ 4HCl 必修二1、Li与O2反应(点燃): 4Li + O2 2Li2 ONa与O2反应(点燃):2Na+O2Na2O2Na与H2O反应: 2Na+2H2O===2NaOH+H2↑K与H2O反应: 2K+2H2O===2KOH+H2↑2、卤素单质F2、Cl2、Br2、I2与氢气反应:F 2 + H2=== 2HF Cl2+ H2=== 2HCl3、卤素单质间的置换反应:(1)氯水与饱和溴化钠、氯水与饱和碘化钠溶液反应:① Cl2+2NaBr===Br2+2NaCl② Cl2+2NaI===I2+2NaCl(2)溴水与碘化钠溶液反应:Br2+2NaI===I2+2NaBr4、Mg与H2O反应:Mg+2H2O === Mg(OH)2+H2↑Al与HCl反应: 2Al+6HCl===2AlCl3+3H2↑5、Na与Cl2反应(点燃):6、用电子式表示氯化氢的形成过程:1、Ba(OH)2•8H2O与NH4Cl的反应 :Ba(OH)2·8H2O+2NH4Cl==BaCl2+2NH3↑+10H2O2、原电池原理典型的原电池(Zn-Cu原电池)负极(锌):Zn-2e-===Zn2+(氧化反应)正极(铜):2H++2e-===H2↑(还原反应)电子流动方向:由锌经过外电路流向铜。


化学必修模块化学方程式汇总1.钠与氧气常温反应:4Na +O2=2Na2O2.钠与氧气点燃反应:2Na +O2Na2O23.钠与水的反应:2Na +2H2O=2NaOH + H2↑4. Na2O2与水的反应:2Na2O2+2H2O=4NaOH+O2↑5.Na2O2与CO2的反应:2Na2O2+2CO2=2Na2CO3+O26.氢气在氯气中燃烧:H2+Cl2 2HCl7.铁在氯气中燃烧:2Fe+3Cl2 2FeCl38.铜在氯气中燃烧:Cu+Cl2 CuCl29.氯气与水的反应:Cl2+H2O=HCl+HClO10.次氯酸的不稳定性:2HClO2HCl+O2↑11.氯气与氢氧化钠溶液反应(制84消毒液):Cl2+2NaOH=NaCl+NaClO+H2O12.制漂白粉:2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O13.铁与稀硫酸反应的离子方程式:Fe+2H+=Fe2++H2↑14.FeCl3溶液与Fe反应的离子方程式:2Fe3++Fe=3Fe2+15. FeCl3溶液与Cu反应的离子方程式:2Fe3++Cu=2Fe2++Cu2+16.FeCl2溶液与Cl2反应的离子方程式: 2Fe2++ Cl2=2Fe3++ 2Cl_17、向Na2CO3溶液中滴加足量稀盐酸Na2CO3+2HCl=2NaCl+H2O+CO2↑18、向NaHCO3溶液中滴加稀盐酸的离子方程式HCO3-+H+==== H2O+CO2↑19、向NaHCO3溶液中滴加NaOH溶液的离子方程式HCO3-+OH-=CO32-+H2O20、NaHCO3受热分解2NaHCO3Na2CO3+H2O+CO2↑21、向Na2CO3溶液中通入CO2气体Na2CO3+CO2+H2O=2NaHCO322、溶洞形成的两反应CaCO3+CO2+H2O =Ca(HCO3)2 Ca(HCO3)2=CaCO3+CO2↑+H2O23、高炉炼铁C+O2CO2CO2+C 2COFe2O3+3CO 2Fe+3CO224.N2与O2 N2+O22NO25.N2与H2(工业合成氨)N2+3H2 2NH326.NO与O2 2NO+O2===== 2NO227.NO2与H2O 3NO2+H2O==2HNO3+NO28.NH3与H2O NH3+H2O NH3·H2O29.NH3与HCl NH3+HCl==NH4Cl30.氨的催化氧化4NH3+5O24NO+6H2O31.NH4Cl受热分解NH4Cl NH3↑+HCl↑32.NH4HCO3受热分解NH4HCO3NH3↑+H2O+CO2↑33.实验室制氨气2NH4Cl+Ca(OH)2CaCl2+2NH3↑+2H2O34.铵盐与稀碱溶液反应的离子方程式NH4++OH-=NH3·H2O铵盐与浓碱溶液反应(或加热)的离子方程式(可用于检验铵根)NH4++OH-NH3↑+H2O35.硝酸见光或受热分解4HNO3 4NO2↑+O2↑+2H2O36.铜与稀硝酸3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O37.铜与浓硝酸Cu+4HNO3(浓)= Cu(NO3)2+2NO2↑+2H2O38.碳与浓硝酸(加热)C+4HNO3(浓)CO2↑+4NO2↑+2H2O39.硫和铁Fe+S FeS40.硫和铜2Cu+S Cu2S41.SO2溶于水SO2+H2O H2SO342.SO2通入氢硫酸中2H2S+SO2=3S↓+2H2O43.H2SO3被O2氧化2H2SO3+O2=2H2SO444.铜和浓硫酸共热Cu+2H2SO4(浓)CuSO4+SO2↑+2H2O45.碳和浓硫酸共热C+2H2SO4(浓)CO2↑+2SO2↑+2H2O46.以硫磺为原料工业制硫酸第1步S+O2SO247.以硫磺为原料工业制硫酸第2步2SO2+O2 2SO348.以硫磺为原料工业制硫酸第3步SO3+H2O=H2SO449.Mg在CO2中燃烧: Mg+CO2C+2MgO50.设计实验验证氧化性Cl2>Br2>I2 :2NaBr+Cl2=2NaCl+Br2 2KI+ Br 2=2KBr +I251.Si + O2SiO252.工业制硅SiO2 + 2C Si + 2CO ↑53.SiO2+CaO CaSiO354.NaOH溶液存放可用玻璃瓶但不用玻璃塞(可用橡胶塞)SiO2 +2NaOH = Na2SiO3 + H2O55.氢氟酸腐蚀玻璃:SiO2 +4HF = SiF4↑+ 2H2O56.制玻璃反应之一:Na2CO3 + SiO2Na2SiO3+ CO2↑57.制玻璃反应之二:CaCO3 + SiO2CaSiO3 + CO2↑58.4Al+3O22Al2O359.铝热反应2Al + Fe2O3Al2O3+2Fe (放热)60.铝与盐酸反应:2Al+6H+=2Al3++3H2↑61. 铝与氢氧化钠溶液反应:2Al+2NaOH+6H2O=2Na[Al(OH)4]+3H2↑(四羟基合铝酸钠)2Al+2OH-+6H2O = 2 [Al(OH)4]-+3H2↑62. Al2O3——两性氧化物Al2O3 +6H+ =2Al3++3H2O Al2O3 + 2OH— +3H2O =2[Al(OH)4]-63.Al(OH)3——两性氢氧化物Al(OH)3 + 3H+=Al3+ + 3H2O Al(OH)3 + OH—=[Al(OH)4]-64. Al3+与NaOH溶液Al3+ + 3OH—(少)=Al(OH)3↓Al3+ + 4OH—(足)=[Al(OH)4]- 65. Na[Al(OH)4]与稀盐酸:[Al(OH)4]-+H+ (少)= Al(OH)3↓+H2O [Al(OH)4]-+4H+(过)= Al3++4H2O 66. Al(OH)3的制备——铝盐和氨水反应[用Al2(SO4)3或AlCl3 ] (与量无关)Al3+ + 3NH3·H2O = Al(OH)3↓+3NH4+67.实验室制备氯气:MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O68.C H4+2O2C O2+2H2O69.甲烷和氯气在光照条件下的反应方程式70.C H2=C H2+3O22C O2+2H2O71.C H2=C H2+B r2C H2B r-C H2B r72.C H2=C H2+H2C H3-C H373.C H2=C H2+H2O C H3-C H2-O H74.C H2=C H2+H C l C H3-C H2C l75.2+15O212C O2+6H2O76.77.2Na + 2C2H5OH → H2↑ + 2C2H5ONa78.2CH3CH2OH+O22CH3CHO+2H2O79.CH3COOH+HOC2H5CH3COOC2H5+H2O80.CH3COOC2H5+H2O CH3COOH+HOC2H581.CH3COOCH2CH3+NaOH→CH3COONa+ CH3CH2OH82.葡萄糖在体内完全氧化C6H12O6+6O2→ 6CO2+6H2O83.制备聚乙烯:84.制备聚氯乙烯85.制备聚苯乙烯86.制备聚四氟乙烯:。

化学必修一必修二方程式汇总高中化学(人教版)必修一、必修二化学方程式汇总必修一1、硫酸根离子的检验: BaCl 2 + Na 2SO4 ==== BaSO 4↓ + 2NaCl2、碳酸根离子的检验: CaCl 2 + Na 2CO3 ===== CaCO3↓ + 2NaCl3、碳酸钠与盐酸反应 : Na CO + 2HCl ===== 2NaCl + H2O+CO↑2324、木炭还原氧化铜 : 2CuO + C 高温2Cu + CO ↑25、铁片与硫酸铜溶液反应: Fe + CuSO 4 ===== FeSO 4 + Cu6、氯化钙与碳酸钠溶液反应:CaCl2 + Na 2CO3 ===== CaCO3↓ + 2NaCl7、钠在空气中燃烧: 2Na + O2Na O22钠与氧气反应:4Na + O 2 ==== 2Na 2O8、过氧化钠与水反应:2Na2O2 + 2H 2O ==== 4NaOH + O 2↑9、过氧化钠与二氧化碳反应:2Na2O2 + 2CO 2 ==== 2Na 2CO3 + O 210、钠与水反应:2Na + 2H 2O ==== 2NaOH + H 2↑11、铁与水蒸气反应:3Fe + 4H 2O(g) ==== Fe 3 O4 + 4H 2↑12、铝与氢氧化钠溶液反应:2Al + 2NaOH + 2H 2O ==== 2NaAlO 2 + 3H 2↑13、氧化钙与水反应:CaO + H2O ==== Ca(OH) 214、氧化铁与盐酸反应:Fe2O3 + 6HCl ===== 2FeCl 3 + 3H2O15、氧化铝与盐酸反应:Al 2O3 + 6HCl ===== 2AlCl 3 + 3H2O化学必修一必修二方程式汇总16、氧化铝与氢氧化钠溶液反应:Al 2O3 + 2NaOH ===== 2NaAlO 2 + H 2O17、氯化铁与氢氧化钠溶液反应:FeCl 3 + 3NaOH ===== Fe(OH) 3↓ + 3NaCl18、硫酸亚铁与氢氧化钠溶液反应:FeSO4 + 2NaOH ==== Fe(OH) 2↓ + Na 2SO419、氢氧化亚铁被氧化成氢氧化铁:4Fe(OH)2 + 2H 2O + O 2 ==== 4Fe(OH) 320、氢氧化铁加热分解:2Fe(OH)3Fe 2O3 + 3H 2O↑21、实验室制取氢氧化铝:Al 2(SO4) 3 + 6NH 3· H2O ==== 2Al(OH) 3↓ + 3(NH 3) 2SO422、氢氧化铝与盐酸反应:Al(OH) 3 + 3HCl ==== AlCl 3 + 3H2O23、氢氧化铝与氢氧化钠溶液反应:Al(OH) 3 + NaOH ==== NaAlO 2 + 2H 2O24、氢氧化铝加热分解:2Al(OH) 3Al 2O3 + 3H 2O25、三氯化铁溶液与铁粉反应:2FeCl 3 + Fe ==== 3FeCl226、氯化亚铁中通入氯气:2FeCl 2 + Cl 2 ===== 2FeCl327、二氧化硅与氢氟酸反应: SiO+ 4HF ==== SiF4+ 2H O22硅单质与氢氟酸反应:Si + 4HF ==== SiF 4 + 2H2↑高温28、二氧化硅与氧化钙高温反应:SiO2 + CaO CaSiO 329、二氧化硅与氢氧化钠溶液反应:SiO2 + 2NaOH ==== Na 2SiO3 + H 2 O30、往硅酸钠溶液中通入二氧化碳:Na2SiO3 + CO 2 + H 2O === Na 2CO3 + H 2SiO3↓31、硅酸钠与盐酸反应: NaSiO+ 2HCl === 2NaCl + H2SiO ↓233点燃32、氯气与金属铁反应:2Fe + 3Cl 22FeCl 333、氯气与金属铜反应:Cu + Cl34、氯气与金属钠反应:2Na + Cl 2CuCl2点燃22NaCl35、氯气与水反应:Cl 2 + H 2 O ==== HCl + HClO光照36、次氯酸光照分解:2HClO2HCl + O 2↑37、氯气与氢氧化钠溶液反应: Cl2+ 2NaOH ===== NaCl + NaClO + H O238、氯气与消石灰反应:2Cl2 + 2Ca(OH) 2 ==== CaCl 2 + Ca(ClO) 2 + 2H2O39、盐酸与硝酸银溶液反应:HCl + AgNO 3 ==== AgCl ↓ + HNO 340、漂白粉长期置露在空气中:Ca(ClO) 2 + H 2O + CO2 ==== CaCO3↓ + 2HClO41、二氧化硫与水反应:SO2 + H 2O === H 2SO3放电42、氮气与氧气在放电下反应:N2 + O 22NO43、一氧化氮与氧气反应:2NO + O2 ==== 2NO 244、二氧化氮与水反应:3NO2 + H 2O ==== 2HNO3 + NO45、二氧化硫与氧气在催化剂的作用下反应:2SO + O 2催化剂2SO346、三氧化硫与水反应:SO3 + H 2O ==== H 2SO447、浓硫酸与铜反应:Cu + 2H 2SO4( 浓 )CuSO4 + 2H 2O + SO2↑48、浓硫酸与木炭反应: C + 2H 2SO4( 浓 )CO2↑ + 2SO2↑ + 2H 2O49、浓硝酸与铜反应:Cu + 4HNO3( 浓 ) ==== Cu(NO 3) 2 + 2H 2O + 2NO2↑33、氯气与金属铜反应:Cu + Cl34、氯气与金属钠反应:2Na + Cl 2CuCl2点燃22NaCl35、氯气与水反应:Cl 2 + H 2 O ==== HCl + HClO光照36、次氯酸光照分解:2HClO2HCl + O 2↑37、氯气与氢氧化钠溶液反应: Cl2+ 2NaOH ===== NaCl + NaClO + H O238、氯气与消石灰反应:2Cl2 + 2Ca(OH) 2 ==== CaCl 2 + Ca(ClO) 2 + 2H2O39、盐酸与硝酸银溶液反应:HCl + AgNO 3 ==== AgCl ↓ + HNO 340、漂白粉长期置露在空气中:Ca(ClO) 2 + H 2O + CO2 ==== CaCO3↓ + 2HClO41、二氧化硫与水反应:SO2 + H 2O === H 2SO3放电42、氮气与氧气在放电下反应:N2 + O 22NO43、一氧化氮与氧气反应:2NO + O2 ==== 2NO 244、二氧化氮与水反应:3NO2 + H 2O ==== 2HNO3 + NO45、二氧化硫与氧气在催化剂的作用下反应:2SO + O 2催化剂2SO346、三氧化硫与水反应:SO3 + H 2O ==== H 2SO447、浓硫酸与铜反应:Cu + 2H 2SO4( 浓 )CuSO4 + 2H 2O + SO2↑48、浓硫酸与木炭反应: C + 2H 2SO4( 浓 )CO2↑ + 2SO2↑ + 2H 2O49、浓硝酸与铜反应:Cu + 4HNO3( 浓 ) ==== Cu(NO 3) 2 + 2H 2O + 2NO2↑33、氯气与金属铜反应:Cu + Cl34、氯气与金属钠反应:2Na + Cl 2CuCl2点燃22NaCl35、氯气与水反应:Cl 2 + H 2 O ==== HCl + HClO光照36、次氯酸光照分解:2HClO2HCl + O 2↑37、氯气与氢氧化钠溶液反应: Cl2+ 2NaOH ===== NaCl + NaClO + H O238、氯气与消石灰反应:2Cl2 + 2Ca(OH) 2 ==== CaCl 2 + Ca(ClO) 2 + 2H2O39、盐酸与硝酸银溶液反应:HCl + AgNO 3 ==== AgCl ↓ + HNO 340、漂白粉长期置露在空气中:Ca(ClO) 2 + H 2O + CO2 ==== CaCO3↓ + 2HClO41、二氧化硫与水反应:SO2 + H 2O === H 2SO3放电42、氮气与氧气在放电下反应:N2 + O 22NO43、一氧化氮与氧气反应:2NO + O2 ==== 2NO 244、二氧化氮与水反应:3NO2 + H 2O ==== 2HNO3 + NO45、二氧化硫与氧气在催化剂的作用下反应:2SO + O 2催化剂2SO346、三氧化硫与水反应:SO3 + H 2O ==== H 2SO447、浓硫酸与铜反应:Cu + 2H 2SO4( 浓 )CuSO4 + 2H 2O + SO2↑48、浓硫酸与木炭反应: C + 2H 2SO4( 浓 )CO2↑ + 2SO2↑ + 2H 2O49、浓硝酸与铜反应:Cu + 4HNO3( 浓 ) ==== Cu(NO 3) 2 + 2H 2O + 2NO2↑33、氯气与金属铜反应:Cu + Cl34、氯气与金属钠反应:2Na + Cl 2CuCl2点燃22NaCl35、氯气与水反应:Cl 2 + H 2 O ==== HCl + HClO光照36、次氯酸光照分解:2HClO2HCl + O 2↑37、氯气与氢氧化钠溶液反应: Cl2+ 2NaOH ===== NaCl + NaClO + H O238、氯气与消石灰反应:2Cl2 + 2Ca(OH) 2 ==== CaCl 2 + Ca(ClO) 2 + 2H2O39、盐酸与硝酸银溶液反应:HCl + AgNO 3 ==== AgCl ↓ + HNO 340、漂白粉长期置露在空气中:Ca(ClO) 2 + H 2O + CO2 ==== CaCO3↓ + 2HClO41、二氧化硫与水反应:SO2 + H 2O === H 2SO3放电42、氮气与氧气在放电下反应:N2 + O 22NO43、一氧化氮与氧气反应:2NO + O2 ==== 2NO 244、二氧化氮与水反应:3NO2 + H 2O ==== 2HNO3 + NO45、二氧化硫与氧气在催化剂的作用下反应:2SO + O 2催化剂2SO346、三氧化硫与水反应:SO3 + H 2O ==== H 2SO447、浓硫酸与铜反应:Cu + 2H 2SO4( 浓 )CuSO4 + 2H 2O + SO2↑48、浓硫酸与木炭反应: C + 2H 2SO4( 浓 )CO2↑ + 2SO2↑ + 2H 2O49、浓硝酸与铜反应:Cu + 4HNO3( 浓 ) ==== Cu(NO 3) 2 + 2H 2O + 2NO2↑33、氯气与金属铜反应:Cu + Cl34、氯气与金属钠反应:2Na + Cl 2CuCl2点燃22NaCl35、氯气与水反应:Cl 2 + H 2 O ==== HCl + HClO光照36、次氯酸光照分解:2HClO2HCl + O 2↑37、氯气与氢氧化钠溶液反应: Cl2+ 2NaOH ===== NaCl + NaClO + H O238、氯气与消石灰反应:2Cl2 + 2Ca(OH) 2 ==== CaCl 2 + Ca(ClO) 2 + 2H2O39、盐酸与硝酸银溶液反应:HCl + AgNO 3 ==== AgCl ↓ + HNO 340、漂白粉长期置露在空气中:Ca(ClO) 2 + H 2O + CO2 ==== CaCO3↓ + 2HClO41、二氧化硫与水反应:SO2 + H 2O === H 2SO3放电42、氮气与氧气在放电下反应:N2 + O 22NO43、一氧化氮与氧气反应:2NO + O2 ==== 2NO 244、二氧化氮与水反应:3NO2 + H 2O ==== 2HNO3 + NO45、二氧化硫与氧气在催化剂的作用下反应:2SO + O 2催化剂2SO346、三氧化硫与水反应:SO3 + H 2O ==== H 2SO447、浓硫酸与铜反应:Cu + 2H 2SO4( 浓 )CuSO4 + 2H 2O + SO2↑48、浓硫酸与木炭反应: C + 2H 2SO4( 浓 )CO2↑ + 2SO2↑ + 2H 2O49、浓硝酸与铜反应:Cu + 4HNO3( 浓 ) ==== Cu(NO 3) 2 + 2H 2O + 2NO2↑33、氯气与金属铜反应:Cu + Cl34、氯气与金属钠反应:2Na + Cl 2CuCl2点燃22NaCl35、氯气与水反应:Cl 2 + H 2 O ==== HCl + HClO光照36、次氯酸光照分解:2HClO2HCl + O 2↑37、氯气与氢氧化钠溶液反应: Cl2+ 2NaOH ===== NaCl + NaClO + H O238、氯气与消石灰反应:2Cl2 + 2Ca(OH) 2 ==== CaCl 2 + Ca(ClO) 2 + 2H2O39、盐酸与硝酸银溶液反应:HCl + AgNO 3 ==== AgCl ↓ + HNO 340、漂白粉长期置露在空气中:Ca(ClO) 2 + H 2O + CO2 ==== CaCO3↓ + 2HClO41、二氧化硫与水反应:SO2 + H 2O === H 2SO3放电42、氮气与氧气在放电下反应:N2 + O 22NO43、一氧化氮与氧气反应:2NO + O2 ==== 2NO 244、二氧化氮与水反应:3NO2 + H 2O ==== 2HNO3 + NO45、二氧化硫与氧气在催化剂的作用下反应:2SO + O 2催化剂2SO346、三氧化硫与水反应:SO3 + H 2O ==== H 2SO447、浓硫酸与铜反应:Cu + 2H 2SO4( 浓 )CuSO4 + 2H 2O + SO2↑48、浓硫酸与木炭反应: C + 2H 2SO4( 浓 )CO2↑ + 2SO2↑ + 2H 2O49、浓硝酸与铜反应:Cu + 4HNO3( 浓 ) ==== Cu(NO 3) 2 + 2H 2O + 2NO2↑33、氯气与金属铜反应:Cu + Cl34、氯气与金属钠反应:2Na + Cl 2CuCl2点燃22NaCl35、氯气与水反应:Cl 2 + H 2 O ==== HCl + HClO光照36、次氯酸光照分解:2HClO2HCl + O 2↑37、氯气与氢氧化钠溶液反应: Cl2+ 2NaOH ===== NaCl + NaClO + H O238、氯气与消石灰反应:2Cl2 + 2Ca(OH) 2 ==== CaCl 2 + Ca(ClO) 2 + 2H2O39、盐酸与硝酸银溶液反应:HCl + AgNO 3 ==== AgCl ↓ + HNO 340、漂白粉长期置露在空气中:Ca(ClO) 2 + H 2O + CO2 ==== CaCO3↓ + 2HClO41、二氧化硫与水反应:SO2 + H 2O === H 2SO3放电42、氮气与氧气在放电下反应:N2 + O 22NO43、一氧化氮与氧气反应:2NO + O2 ==== 2NO 244、二氧化氮与水反应:3NO2 + H 2O ==== 2HNO3 + NO45、二氧化硫与氧气在催化剂的作用下反应:2SO + O 2催化剂2SO346、三氧化硫与水反应:SO3 + H 2O ==== H 2SO447、浓硫酸与铜反应:Cu + 2H 2SO4( 浓 )CuSO4 + 2H 2O + SO2↑48、浓硫酸与木炭反应: C + 2H 2SO4( 浓 )CO2↑ + 2SO2↑ + 2H 2O49、浓硝酸与铜反应:Cu + 4HNO3( 浓 ) ==== Cu(NO 3) 2 + 2H 2O + 2NO2↑33、氯气与金属铜反应:Cu + Cl34、氯气与金属钠反应:2Na + Cl 2CuCl2点燃22NaCl35、氯气与水反应:Cl 2 + H 2 O ==== HCl + HClO光照36、次氯酸光照分解:2HClO2HCl + O 2↑37、氯气与氢氧化钠溶液反应: Cl2+ 2NaOH ===== NaCl + NaClO + H O238、氯气与消石灰反应:2Cl2 + 2Ca(OH) 2 ==== CaCl 2 + Ca(ClO) 2 + 2H2O39、盐酸与硝酸银溶液反应:HCl + AgNO 3 ==== AgCl ↓ + HNO 340、漂白粉长期置露在空气中:Ca(ClO) 2 + H 2O + CO2 ==== CaCO3↓ + 2HClO41、二氧化硫与水反应:SO2 + H 2O === H 2SO3放电42、氮气与氧气在放电下反应:N2 + O 22NO43、一氧化氮与氧气反应:2NO + O2 ==== 2NO 244、二氧化氮与水反应:3NO2 + H 2O ==== 2HNO3 + NO45、二氧化硫与氧气在催化剂的作用下反应:2SO + O 2催化剂2SO346、三氧化硫与水反应:SO3 + H 2O ==== H 2SO447、浓硫酸与铜反应:Cu + 2H 2SO4( 浓 )CuSO4 + 2H 2O + SO2↑48、浓硫酸与木炭反应: C + 2H 2SO4( 浓 )CO2↑ + 2SO2↑ + 2H 2O49、浓硝酸与铜反应:Cu + 4HNO3( 浓 ) ==== Cu(NO 3) 2 + 2H 2O + 2NO2↑。

高中必修二化学方程式大全汇总(精华版)方程式是化学学科内容的重中之重。
下面是高中必修二化学方程式,希望对大家有所帮助。
高中必修二化学方程式1必修二各章节化学方程式第一章物质结构元素周期律1、li与o2反应(点燃):4li+o22li2ona与o2反应(点燃):2na+o2na2o2na与h2o反应:2na+2h2o===2naoh+h2↑k与h2o反应:2k+2h2o===2koh+h2↑2、卤素单质f2、cl2、br2、i2与氢气反应:f2+h2===2hfcl2+h2===2hclbr2+h2===2bri2+h2===2hi3、卤素单质间的置换反应:(1)氯水与饱和溴化钠、氯水与饱和碘化钠溶液反应:①cl2+2nabr===br2+2nacl②cl2+2nai===i2+2nacl(2)溴水与碘化钠溶液反应:br2+2nai===i2+2nabr4、mg与h2o反应:mg+2h2o===mg(oh)2+h2↑al与hcl反应:2al+6hcl===2alcl3+3h2↑mg与hcl反应:mg+2hcl===mgcl2+h2↑点击查看:高一必修二常用化学方程式总结第二章化学反应与能量1、ba(oh)2?8h2o与nh4cl的反应:ba(oh)2·8h2o+2nh4cl==bacl2+2nh3↑+10h2o2、原电池原理典型的原电池(zn-cu原电池)负极(锌):zn-2e-===zn2+(氧化反应)正极(铜):2h++2e-===h2↑(还原反应)、用电子式表示电子流动方向:由锌经过外电路流向铜。
总反应离子方程式:zn+2h+===zn2++h2↑3、h2o2在催化剂作用下受热分解:2h2o22h2o+o2↑4、na2so4与cacl2反应:na2so4+cacl2===caso4↓+na2co35、高炉炼铁:2c+o2===2cofe2o3+3co==2fe+3co2第三章有机化合物1、甲烷的主要化学性质(1)氧化反应(与o2的反应):ch4(g)+2o2(g)co2(g)+2h2o(l)(2)取代反应(与cl2在光照条件下的反应,生成四种不同的取代物):2、乙烯的主要化学性质(1)氧化反应(与o2的反应):c2h4+3o22co2+2h2o(2)加成反应((与br2的反应):(3)乙烯还可以和氢气、氯化氢、水等发生加成反应:ch2=ch2+h2ch3ch3ch2=ch2+hclch3ch2cl(一氯乙烷)ch2=ch2+h2och3ch2oh(乙醇)(4)聚合反应:(乙烯制聚乙烯)(氯乙烯制聚氯乙烯)3、苯的主要化学性质:(1)氧化反应(与o2的反应):2c6h6+15o212co2+6h2o br(2)取代反应:①与br2的反应:+br2+hbr②苯与硝酸(用hono2表示)发生取代反应,生成无色、不溶于水、有苦杏仁气味、密度大于水的油状液体——硝基苯。

人教版化学必修二必背化学方程式1、氯水与饱和溴化钠反应:Cl2+2NaBr===Br2+2NaCl2、氯水与饱和碘化钠溶液反应:Cl2+2NaI===I2+2NaCl3、溴水与碘化钠溶液反应:Br2+2NaI===I2+2NaBr4、Mg与H2O反应:Mg+2H2O === Mg(OH)2+H2↑5、Ba(OH)2•8H2O与NH4Cl的反应: Ba(OH)2·8H2O+2NH4Cl==BaCl2+2NH3↑+10H2O6、原电池原理典型的原电池(Zn-Cu原电池)负极(锌):Zn-2e-===Zn2+(氧化反应)正极(铜):2H++2e-===H2↑(还原反应)电子流动方向:由锌经过外电路流向铜。
总反应离子方程式:Zn+2H+===Zn2++H2↑2H2O+O2↑7、H2O2在催化剂作用下受热分解:2H2O2 催化剂△8、高炉炼铁:2C + O2 === 2CO Fe2O3 + 3CO ==2Fe + 3CO29、甲烷的主要化学性质−点燃CO2(g)+2H2O(l)(1)氧化反应(与O2的反应):CH4(g)+2O2(g)−−→(2)取代反应(与Cl2在光照条件下的反应,生成四种不同的取代物):10、乙烯的主要化学性质−点燃2CO2+2H2O(1)氧化反应(与O2的反应):C2H4+3O2−−→(2)加成反应((与Br2的反应):(3)乙烯还可以和氢气、氯化氢、水等发生加成反应:CH2=CH2 + H2CH3CH3 CH2=CH2+HCl CH3CH2Cl(一氯乙烷)CH 2=CH 2+H 2OCH 3CH 2OH (乙醇)(4)聚合反应: (乙烯制聚乙烯)①(氯乙烯制聚氯乙烯)②11、苯的主要化学性质: (1)氧化反应(与O 2的反应):2C 6H 6+15O 2−−→−点燃 12CO 2+6H 2O(2)取代反应: ① 与Br 2的反应: + Br 2 −−→−3FeBr + HBr② 苯与硝酸(用HONO 2表示)发生取代反应,生成无色、不溶于水、有苦杏仁气味、密度大于水的油状液体——硝基苯。
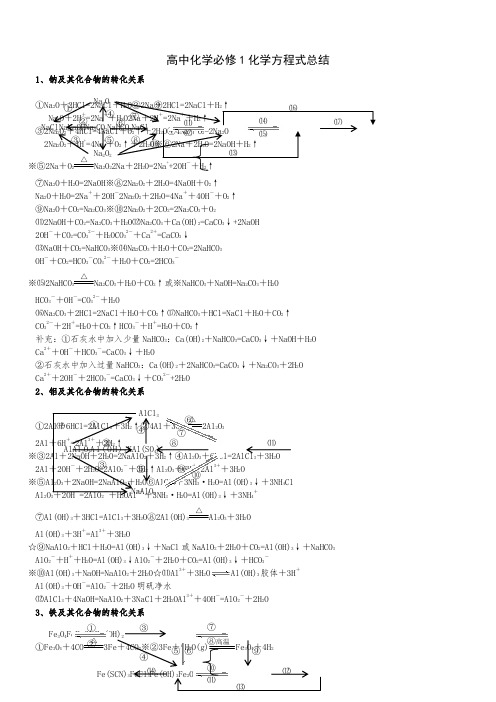
高中化学必修1化学方程式总结1、钠及其化合物的转化关系①Na 2O +2HCl=2NaCl Na 2O +2H +=2Na +③2Na 2O 2+4HCl=4NaCl ④4Na +O =2Na 2Na 2O 2+4H +=4Na ++※⑤2Na +O 2△Na 2⑦Na 2O +H 2O=2NaOH ※⑧2Na 2O 2+2H 2O=4NaOH +O 2↑Na 2⑨⑾2OH ⒀OH -※⒂HCO ⒃CO 32Ca 2Ca 22①4Al +3O 2 △2Al 2O 3 2Al ※③3H 2↑④Al 2O 3+6HCl=2AlCl 2Al ↑Al 2O 3+6H +=2Al 3++※⑤Al 2⑦Al(OH)3+3HCl=AlCl 3+3H 2O ⑧2Al(OH)3△Al 2O 3+3H 2OAl(OH)3+3H +=Al 3++3H 2O☆⑨NaAlO 2+HCl +H 2O=Al(OH)3↓+NaCl 或NaAlO 2+2H 2O +CO 2=Al(OH)3↓+NaHCO 3AlO 2-+H ++H 2O=Al(OH)3↓AlO 2-+2H 2O +CO 2=Al(OH)3↓+HCO 3-※⑩Al(OH)3+NaOH=NaAlO 2+2H 2O ☆⑾Al 3++3H 2O Al(OH)3胶体+3H +Al(OH)3+OH -=AlO 2-+2H 2O 明矾净水⑿AlCl 3+4NaOH=NaAlO 2+3NaCl +2H 2OAl 3++4OH -=AlO 2-+2H 2O 3、铁及其化合物的转化关系 ①Fe 3O 4+4CO △ 4H NaClNaNaOHNa 2CO 3Na 2O Na 2O ① ② ③ ⑤⑾ ⑿ ⒁ ⒂④Fe 3O 4FeFeCl 2Fe(OH)O 3①② ③ ⑦ ⑧ ⑩ ⑾4)23⑥ ⑦ ⑧ ⑨ ⑩③Fe +2HCl=FeCl 2+H 2↑或3Fe +2O 2点燃Fe 3O 4Fe +2H +=Fe 2++H 2↑④2Fe +3Cl 2点燃2FeCl 3※⑤2FeCl 2+Cl 2=2FeCl 3※⑥Fe +2FeCl 3=3FeCl 22Fe 2++Cl 2=2Fe 3++2Cl -Fe +2Fe 3+=3Fe 2+⑦FeCl 2+2NaOH=Fe(OH)2↓+2NaCl ⑧Fe(OH)2+2HCl=FeCl 2+2H 2O Fe 2++2OH -=Fe(OH)2↓Fe(OH)2+2H +=Fe 2++2H 2O※⑨4Fe(OH)2+O 2+2H 2O=4Fe(OH)3⑩FeCl 3+3NaOH=Fe(OH)3↓+3NaCl白色沉淀迅速变成灰绿色,最后变成红褐色Fe 3++3OH -=Fe(OH)3↓⑾Fe(OH)3+3HCl=FeCl 3+3H 2OFe 3++3H 2O Fe(OH)3胶体+3H +(净水) ⒀Fe 24①②※③SiO +4HF=SiF ④⑤ CaSiO 3※⑥SiO SiO ※⑦⑧H 25①②③2Fe +Cu=2Fe 2++④H 2+Cl 2※⑤MnO 22+Cl 2↑+2H 2O MnO 2+4H ++2Cl -2++Cl 2↑+2H 2O ※⑥Cl 2+H 2O=HCl +HClO ※⑦2HClO2HCl +O 2↑Cl 2+H 2O=H ++Cl -+HClO2HClO2H ++2Cl -+O 2↑※⑧Cl 2+2NaOH=NaCl +NaClO +H 2O ※⑨2Cl 2+2Ca(OH)2=CaCl 2+Ca(ClO)2+2H 2OSi ⑦⑧HCl 3NaClO 2 ④⑤ 点燃或光照光照光照Cl2+2OH-=Cl-+ClO-+H2O工业制漂白粉※⑩Ca(ClO)2+H2O+CO2=CaCO3↓+2HClO或Ca(ClO)2+2HCl=CaCl2+2HClO Ca2++2ClO-+H2O+CO2=CaCO3↓+2HClO或ClO-+H+=HClO漂白粉的漂白原理向漂白粉溶液中通入过量的CO2:Ca(ClO)2+2H2O+2CO2=Ca(HCO3)2+2HClO ClO-+H2O+CO2=HCO3-+HClO6、硫及其化合物的转化关系①S +O ②2H 2S +SO =3S ※③SO ④SO 3224⑤SO 2+CaO△3或SO 2+Ca(OH)2=CaSO 3↓+H 2O⑥SO 3+CaO=CaSO 4SO 2+Ca 2++2OH -=CaSO 3↓+H 2O SO 3+Ca(OH)2=CaSO 4+H 2O ⑦2CaSO 3+O 2△2CaSO 4以上三个反应为“雷雨发庄稼”原理实验室制氨气,此反应为固体反应,不能写成离子方程式。

高中化学无机反应★1、钠露置于空气中生成白色固体:4Na+O2= 2Na2O★2、钠在空气中燃烧(黄色的火焰):2Na+O2Na2O2(淡黄色固体)★3、钠在氯气中燃烧(白烟现象):2Na+Cl22NaCl★4、铜丝在氯气中剧烈燃烧(棕黄色的烟):Cu+Cl2CuCl2★5、铁在氯气中剧烈燃烧(棕褐色的烟):2Fe + 3Cl22FeCl36、铁在氧气中剧烈燃烧(火星四射,放出大量的热):3Fe +2O2点燃Fe3O4点燃2HCl★7、氢气在氯气中燃烧(苍白色火焰,瓶口有白雾):H2 + Cl2★8、钠与水反应(浮、熔、游、响、红):2Na + 2H2O =2NaOH + H2↑2Na + 2H2O = 2Na+ + 2OH - +H2 ↑9、氧化钠与氧气反应:2Na2O+ O2△2Na2O210、氧化钠与稀盐酸反应:Na2O+2HCl= 2NaCl + H2O(Na2O+2H+=2Na++ H2O)★11、钠与硫酸铜aq反应:2Na+2H2O+CuSO4=Cu(OH)2↓+Na2SO4+H2↑2Na+2H2O+Cu2+=Cu(OH)2↓+2Na++H2↑9、钠与氯化铁溶液反应:6Na+6H2O+2FeCl3=2Fe(OH)3↓+6NaCl+3H2↑6Na+6H2O+2Fe3+=Fe(OH)3↓+6Na++3H2↑★12、过氧化钠与水的反应(放热反应、Na2O2是强氧化剂,用于漂白。
)2Na2O2 + 2H2O = 4NaOH + O2↑2Na2O2 + 2H2O = 4Na+ + 4OH - +O2↑(Na2O2既是氧化剂又是还原剂)13、氧化钙与水的反应:CaO + H2O = Ca(OH)2★14、过氧化钠可用在呼吸面具和潜水艇中作为氧气来源,原因是:2Na2O2 + 2CO2 = 2Na2CO3 + O2 (Na2O2既是氧化剂又是还原剂)15、过氧化钠与稀盐酸的反应:2Na2O2 +4HCl= 4NaCl + 2H2O + O2↑2Na2O2 +4H+= 4Na+ + 2H2O + O2↑★16、苏打(纯碱)与盐酸反应:①盐酸中滴加纯碱溶液(有气泡):Na2CO3 + 2HCl = 2NaCl + H2O + CO2↑CO32- + 2H+ = H2O + CO2↑②纯碱溶液中滴加少量盐酸(无气泡):Na2CO3 + HCl = NaHCO3 + NaCl CO32- + H+ = HCO3-★17、小苏打受热分解:2NaHCO3△Na2CO3 + H2O +CO2 ↑18、固体氢氧化钠和碳酸氢钠混合物在密闭容器中加热NaHCO3 + NaOH △Na2CO3 + H2O(若是溶液中反应有离子方程式):HCO3-+ OH - = H2O + CO32-★19、小苏打(碳酸氢钠)与盐酸反应:NaHCO3+ HCl=NaCl + H2O + CO2↑HCO3-+H+=H2O+CO2 ↑★20、饱和碳酸钠溶液通入CO2气体(晶体析出):Na2CO3+H2O+CO2=2NaHCO3↓★21、少量NaHCO3和Ca(OH)2的反应:NaHCO3+Ca(OH)2=CaCO3↓+H2O+NaOHHCO3-+OH-+Ca2+=CaCO3↓+H2O★22、足量NaHCO3和Ca(OH)2的反应:2NaHCO3+Ca(OH)2=CaCO3↓+2H2O+Na2CO32HCO3-+2OH-+Ca2+=CaCO3↓+2H2O+CO32-★23、氯气溶于水(新制氯水中含H+、Cl -、ClO -、OH-(少量)、Cl2、HClO、H2O):Cl2 + H2O = HCl + HClO Cl2 + H2O = H+ + Cl - + HClO★24、次氯酸见光分解(强氧化剂、杀菌消毒,漂白剂)2HClO2HCl + O2↑★25、氯气尾气的吸收原理:Cl2+2NaOH NaCl+NaClO+H2OCl 2+2OH-Cl-+ClO-+H2O★26、工业制漂白粉的原理(石灰乳与氯气反应)及漂白粉的失效:2Ca(OH)2 + 2Cl2 =Ca(ClO)2 + CaCl2 + 2H2O 2Ca(OH)2 + 2Cl2=2Ca2++2ClO- + 2Cl -+ 2H2O Ca(ClO)2 + CO2 + H2O=CaCO3↓+ 2HClO 2HClO2HCl + O2↑(此反应若在溶液中进行时有离子反应方程式):Ca2++2ClO- + CO2 + H2O=CaCO3↓+ 2HClO★27、氯气的实验室制法(仪器:分液漏斗,圆底烧瓶):MnO2 + 4HCl(浓) MnCl2 +Cl2↑+ 2H2OMnO2 + 4H+ +2Cl-Mn2+ + Cl2↑+ 2H2O★28、氯气通常用湿润的淀粉KI试纸检测:Cl2+ 2I-= I2+2Cl-29、溴水能使湿润的淀粉KI溶液变蓝:Br2+ 2I-= I2+2Br-(单质碘遇淀粉溶液变蓝色)★30、氯酸钾与浓盐酸反应:KClO3+6HCl(浓)=KCl+ 3Cl2↑+3H2O (ClO3-+6H++5Cl-=3Cl2↑+3H2O) ★31、高锰酸钾溶液与浓盐酸反应:2KMnO4+16HCl(浓)=2KCl+2MnCl2 +5Cl2↑+8H2O2MnO4-+16H++10Cl-=2Mn2++5Cl2↑+8H2O32、次氯酸钙溶液与浓盐酸反应:Ca(ClO)2 +4HCl(浓)=CaCl2+2Cl2↑+2H2O2ClO-+4H++2Cl-=2Cl2↑+2H2O33、酸性高锰酸钾溶液中加入双氧水:2KMnO4+5H2O2+3H2SO4=K2SO4+2MnSO4+5O2↑+8H2O2MnO4-+5H2O2+6H+=2Mn2++5O2↑+8H2O。

化学必修一必修二方程式汇总必修一、必修二化学方程式汇总必修一1 、硫酸根离子的检验: B a C l2+ N a2 S O 4 = = = = B a S O 4↓ + 2 N a C l2 、碳酸根离子的检验: C a C l2+ N a 2 C O3 = = = = = C a C O 3↓ + 2 N a C l3 、碳酸钠与盐酸反应:N a 2 C O 3+ 2 H C l= = = = = 2 N a C l+ H 2 O+ C O2↑高温4 、木炭还原氧化铜: 2 C u O +C 2 C u+ C O 2↑5 、铁片与硫酸铜溶液反应: F e+ C u S O 4= = = = = F e S O 4+ C u6 、氯化钙与碳酸钠溶液反应: C a C l2+N a 2 C O 3= = = = = C a C O 3↓ +2 N a C l7 、钠在空气中燃烧: 2 N a+O 2N a 2 O 2钠与氧气反应: 4 N a+O 2= = = = 2 N a 2 O8 、过氧化钠与水反应: 2 N a 2 O 2+ 2 H 2 O = = = = 4 N a O H+O 2↑9 、过氧化钠与二氧化碳反应: 2 N a 2 O 2+ 2 C O 2= = = = 2 N a 2 C O 3+ O 21 0 、钠与水反应:2 N a+ 2 H 2 O = = = = 2 N a O H +H 2↑1 1 、铁与水蒸气反应: 3 F e+ 4 H2 O ( g )= = = = F e3 O 4+4 H 2↑1 2 、铝与氢氧化钠溶液反应: 2 A l + 2 N a O H + 2 H 2 O = = = = 2 N a A l O 2+ 3 H2↑1 3 、氧化钙与水反应: C a O +H2 O= = = = C a ( O H )21 5 、氧化铝与盐酸反应: A l2 O 3+ 6 H C l= = = = = 2 A l C l3+3 H 2 O1 6 、氧化铝与氢氧化钠溶液反应: A l2 O 3+ 2 N a O H = = = = = 2 N a A l O 2+H 2 O1 7 、氯化铁与氢氧化钠溶液反应: F e C l3+ 3 N a O H = = = = = F e ( O H )3↓+ 3 N a C l1 8 、硫酸亚铁与氢氧化钠溶液反应:F e S O 4 +2 N a O H = = = = F e ( O H )2↓+ N a 2 S O 41 9 、氢氧化亚铁被氧化成氢氧化铁: 4 F e ( O H )2+2 H 2 O +O 2= = = =4 F e ( O H )32 0 、氢氧化铁加热分解: 2 F e ( O H )3 F e 2 O 3+ 3 H 2 O ↑2 1 、实验室制取氢氧化铝: A l 2 (S O 4 )3+ 6 N H 3· H 2 O = = = =2 A l ( O H )3 ↓+ 3 ( N H 3 ) 2 S O 42 2 、氢氧化铝与盐酸反应: A l ( O H )3+3 H C l = = = = A l C l3+ 3 H 2 O2 3 、氢氧化铝与氢氧化钠溶液反应:A l ( O H )3+ N a O H = = = = N a A l O 2+ 2 H2O2 4 、氢氧化铝加热分解: 2 A l ( O H )3 A l 2 O 3+ 3 H 2 O2 5 、三氯化铁溶液与铁粉反应: 2 F e C l3+ F e= = = =3 F e C l22 6 、氯化亚铁中通入氯气: 2 F e C l2+ C l2= = = = = 2 F e C l32 7 、二氧化硅与氢氟酸反应:S i O 2+ 4 H F= = = =S i F 4+ 2 H 2 O硅单质与氢氟酸反应:S i+ 4 H F= = = =S i F 4+ 2 H 2↑高温2 8 、二氧化硅与氧化钙高温反应:S i O 2+ C a O C a S i O 32 9 、二氧化硅与氢氧化钠溶液反应:S i O 2+ 2 N a O H = = = = N a 2 S i O 3+H 2 O3 0 、往硅酸钠溶液中通入二氧化碳:N a 2 S i O 3 + C O 2 + H 2 O = = = N a 2 C O 3+H 2 S i O 3↓3 1 、硅酸钠与盐酸反应: N a 2 S i O 3 + 2 H C l = = = 2 N a C l + H 2 S i O 3↓点燃3 2 、氯气与金属铁反应: 2 F e+ 3 C l2 2 F e C l3点燃3 3 、氯气与金属铜反应: C u+ C l2 C u C l2点燃3 4 、氯气与金属钠反应: 2 N a+ C l2 2 N a C l3 5 、氯气与水反应: C l2+H 2 O = = = =H C l+H C l O光照3 6 、次氯酸光照分解: 2 H C l O 2 H C l+O 2↑3 7 、氯气与氢氧化钠溶液反应: C l2+ 2 N a O H = = = = = N a C l + N a C l O+H 2 O3 8 、氯气与消石灰反应: 2 C l2+ 2 C a ( O H ) 2= = = = C a C l2+C a ( C l O )2+ 2 H 2 O3 9 、盐酸与硝酸银溶液反应:H C l+ A g N O 3 = = = = A g C l↓ +H N O 34 0 、漂白粉长期置露在空气中: C a ( C l O )2+ H 2 O + C O 2 = = = = C a C O 3↓+2 H C l O4 1 、二氧化硫与水反应:SO2+H2O == =H2SO3放电4 2 、氮气与氧气在放电下反应:N 2+O 2 2 N O4 3 、一氧化氮与氧气反应: 2 NO +O2==== 2 NO24 4 、二氧化氮与水反应:3NO2+H2O = ===2HNO3+NO4 5 、二氧化硫与氧气在催化剂的作用下反应:2 S O 2 + O 2催化剂2 SO34 6 、三氧化硫与水反应:SO3+H2O == ==H2SO44 7 、浓硫酸与铜反应: C u+ 2 H 2 S O 4 (浓) C u S O 4+ 2 H 2 O +SO2↑4 8 、浓硫酸与木炭反应: C + 2 H2SO4(浓) C O2↑+ 2 SO2↑+ 2 H2O 4 9 、浓硝酸与铜反应: C u + 4 H N O 3 (浓)= = = = C u ( N O 3 ) 2 + 2 H 2 O+ 2 NO2↑5 0 、稀硝酸与铜反应: 3 C u + 8 H N O 3 (稀) 3 C u ( N O 3 )2+ 4 H 2 O+ 2 NO↑5 1 、氨水受热分解:NH3·H2O N H3↑+H2O5 2 、氨气与氯化氢反应:N H 3+H C l= = = =N H 4 C l5 3 、氯化铵受热分解:N H 4 C l N H 3↑ +H C l↑5 4 、碳酸氢氨受热分解:NH4HCO3N H3↑+H2O↑+CO2↑5 5 、硝酸铵与氢氧化钠反应:N H 4 N O 3 + N a O H N H 3↑ + N a N O 3 +H 2 O5 6 、氨气的实验室制取: 2 N H 4 C l+ C a ( O H )2 C a C l2+ 2 H 2 O + 2 NH3↑点燃5 7 、氯气与氢气反应: C l2+H 2 2 H C l5 8 、硫酸铵与氢氧化钠反应:(N H 4)2 S O 4+ 2 N a O H 2 N H 3↑ +N a 2 S O 4+ 2 H 2 O5 9 、 S O 2+ C a O = = = = C a S O 36 0 、 S O 2+ 2 N a O H= = = =N a 2 S O 3+H 2 O6 1 、 S O 2+ C a ( O H )2= = = = C a S O 3↓ +H 2 O6 2 、 S O 2+ C l2+ 2 H 2 O = = = = 2 H C l+H 2 S O 463、SO2+2H2S====3S+2H2O6 4 、 N O 、 N O 2的回收: N O 2+ N O + 2 N a O H = = = = 2 N a N O 2+H 2 O6 5 、 S i+ 2 F 2= = =S i F 46 6 、 S i+ 2 N a O H+H 2 O = = = =N a 2 S i O 3+ 2 H 2↑6 7 、硅单质的实验室制法高温电炉粗硅的制取:S i O 2+ 2 C S i+ 2 C O(石英沙)(焦碳)(粗硅)粗硅转变为纯硅:S i(粗)+ 2 C l2S i C l4高温必修二第一章物质结构元素周期律1 、 L i与O2反应(点燃):4 L i+O2 2 L i2ON a与 O 2反应(点燃) : 2N a + O 2N a 2 O 2N a与 H 2O反应:2N a + 2H 2 O = = = 2 N a O H + H 2↑K 与H2O反应: 2K+2H2O===2KOH+H2↑2 、卤素单质 F 2、C l2、B r2、I2与氢气反应:F 2+ H 2=== 2HF C l 2 + H 2 = = = 2 H C l Br 2 +H 2= = = 2 B rI2+H 2=== 2HI3、卤素单质间的置换反应:( 1 )氯水与饱和溴化钠、氯水与饱和碘化钠溶液反应:① C l 2 + 2 N a B r = = = B r 2 + 2 N a C l②C l 2 + 2 N a I = = = I 2 + 2 N a C l( 2 )溴水与碘化钠溶液反应: B r 2 + 2 N a I = = = I 2 + 2 N a B r4 、 M g与H2O反应:M g + 2 H2O= = =M g ( O H ) 2 +H 2↑A l与H C l反应: 2 A l + 6 H C l = = = 2 A l C l 3 + 3 H 2↑M g与H C l反应:M g + 2H C l= = =M g C l 2 +H 2↑5 、 N a与C l 2 反应(点燃):6、用电子式表示氯化氢的形成过程:第二章化学反应与能量1 、 B a ( O H )2 ?8 H 2 O 与 N H 4 C l的反应:B a ( O H ) 2 ·8H 2 O + 2 N H 4C l = = B a C l 2 + 2 N H 3↑ + 1 0 H 2 O2 、原电池原理典型的原电池(Z n - C u原电池)负极(锌):Z n - 2 e - = = = Z n 2 +(氧化反应)正极(铜): 2 H + + 2 e - = = = H 2↑(还原反应)电子流动方向:由锌经过外电路流向铜。

高中化学(人教版)必修一、必修二化学方程式汇总 必修一:BaCI 2 + Na 2SQ ==== BaSO 4 J + 2NaCI5、铁片与硫酸铜溶液反应 :Fe + CuSQ 4 ===== FeSQ 4 + Cu6、氯化钙与碳酸钠溶液反应: CaCb + Na 2CQ A7、钠在空气中燃烧: 2Na + Q 2 ― Na2Q钠与氧气反应:4Na + Q 2 ==== 2Na 2Q8、过氧化钠与水反应: 2NaO + 2H 20 ==== 4NaQH + Q 2 f9、过氧化钠与二氧化碳反应: 2Na^C 2 + 2CQ 2 ==== 2Na 2CQ + Q 210、钠与水反应: 2Na + 2H 2Q ==== 2NaQH + H 2 f11、 铁与水蒸气反应: 3Fe + 4H 20(g) ==== Fe 3Q + 4H 2 f12、 铝与氢氧化钠溶液反应: 2AI + 2NaQH + 2H 2。
==== 2NaAIQ 2 + 3H 2 f13、 氧化钙与水反应: CaO + NO ==== Ca(0H )214、 氧化铁与盐酸反应: F Q Q + 6HCI ===== 2FeCI 3 + 3H 2。
2、碳酸根离子的检验 :CaCI 2 + Na 2CQCaCQ s J + 2NaCI 3、碳酸钠与盐酸反应 :Na 2CO + 2HCI 2NaCI + H 20 + CO 2?4、木炭还原氧化铜:2CuQ + C高温 2Cu + CQ 2f1、硫酸根离子的检验 CaCQ 3 J + 2NaCI15、氧化铝与盐酸反应:AbQ + 6HCI ===== 2AICI 3 + 3H 2Q16、氧化铝与氢氧化钠溶液反应:Al 2Q + 2NaOH ===== 2NaAI0 2 + H 2O17、氯化铁与氢氧化钠溶液反应:FeCb + 3NaOH ===== Fe(OH) 3 J + 3NaCI18、硫酸亚铁与氢氧化钠溶液反应:FeSQ + 2NaOH ==== Fe(OH) 2 J + Na z SQ19、氢氧化亚铁被氧化成氢氧化铁:4Fe(OH)2 + 2H 2O + O2 ==== 4Fe(OH) 3A20、氢氧化铁加热分解:2Fe(OH)3 Fe 2Q + 3H 2O f21、实验室制取氢氧化铝:Al 2(SO4) 3 + 6NH3 • fO ==== 2Al(OH) 3 J + 3(NH 3) 2SQ22、氢氧化铝与盐酸反应:AI(OH) 3 + 3HCI ==== AICI 3 + 3H 2O23、氢氧化铝与氢氧化钠溶液反应:AI(OH) 3 + NaOH ==== NaAIO 2 + 2H 2OA24、氢氧化铝加热分解:2AI(OH) 3 Al 2Q + 3H 2O25、三氯化铁溶液与铁粉反应:2FeCI3 + Fe ==== 3FeCI 226、氯化亚铁中通入氯气:2FeCI2 + CI 2 ===== 2FeCI 327、二氧化硅与氢氟酸反应:SiO2 + 4HF ==== SiF 4 + 2H 2O硅单质与氢氟酸反应:Si + 4HF ==== SiF 4 + 2H 2 f高温28、二氧化硅与氧化钙高温反应:SiO2 + CaO CaSiO s29、二氧化硅与氢氧化钠溶液反应:SiO2 + 2NaOH ==== Na 2SQ3 + H 2O30、往硅酸钠溶液中通入二氧化碳:N@SiO3 + CO2 + H 20 === Na z CO + H 2SQ3J31、硅酸钠与盐酸反应:NaSiO3 + 2HCI === 2NaCI + H 2SQ3 J占燃32、氯气与金属铁反应:2Fe + 3CI 2 2FeCb氯气与金属铜反应: Cu + Cl 2 CuCb占燃氯气与金属钠反应: 2Na + Cl 2 2NaCI 氯气与水反应: CI 2 + H 2O ==== HCI + HCIO光昭次氯酸光照分解: 2HCIO 2HCI + O 2? 氯气与氢氧化钠溶液反应: CI 2 + 2NaOH ===== NaCI + NaCIO + H 2O 氯气与消石灰反应: 2CI 2 + 2Ca(OH) 2 ==== CaCI 2 + Ca(CIO) 2 + 2H 2O 盐酸与硝酸银溶液反应: HCI + AgNO 3 ==== AgCI J + HNO 3 漂白粉长期置露在空气中: Ca(CIO) 2 + H 2O + CO 2 ==== CaCO 3 J + 2HCIO 二氧化硫与水反应: SO + H 2O === H 2SO氮气与氧气在放电下反应: N 2 + O 2 2NO 一氧化氮与氧气反应: 2NO + O 2 ==== 2NO 2 二氧化氮与水反应: 3NO + H 2O ==== 2HNQ + NO催化剂二氧化硫与氧气在催化剂的作用下反应: 2SQ + O 2 2SO 3 三氧化硫与水反应: SO + H 2O ==== H 2SQ A浓硫酸与铜反应: Cu + 2H 2SQ (浓)—:CuSO 4 + 2H 2O + SO 2 ? A浓硫酸与木炭反应: C + 2H 2SC 4(浓)—CO 2 ? + 2SQ f + 2H 2O 浓硝酸与铜反应:Cu 33、34、 35、 36、 37、 38、 39、 40、 41、 42、 43、 44、 45、 46、 47、 48、49、+ 4HNQ(浓)==== Cu(NO 3)2 + 2H 2O + 2NO2 ?A50、稀硝酸与铜反应:3Cu + 8HNQ(稀)一3Cu(NO s) 2 + 4H 2O + 2NO TA51、氨水受热分解:H2O ——NH3 f + H 2O52、氨气与氯化氢反应:NH + HCl ==== NH 4CIA53、氯化铵受热分解:NHCI —:NH3? + HCl fA54、碳酸氢氨受热分解:NHHCO NH3? + H 2O f + CO z fA55、硝酸铵与氢氧化钠反应:NHNO + NaOH ——NH3 f + NaNO s + H 2OA56、氨气的实验室制取:2NHCI + Ca(OH) 2 ——CaCI 2 + 2H 2O + 2NH s f占燃57、氯气与氢气反应:CI2 + H 2 2HCIA58、硫酸铵与氢氧化钠反应:( NH) 2SQ + 2NaOH ― 2NH s f + Na 2SC4 + 2H 2O59、SQ + CaO ==== CaSO 360、SQ + 2NaOH ==== Na 2SQ + H 2O61、SQ + Ca(OH) 2 ==== CaSO3 J + H 2O62、SQ + CI 2 + 2H 2O ==== 2HCI + H 2SQ63、SQ + 2H 2S ==== 3S + 2H 2。

必修二全部化学方程式及其离子反应式1.镁与盐酸响应:Mg +2H+ = Mg2+ + H2↑2.铝与盐酸响应2Al + 6H+ = 2Al3+ +3H2↑3.锌与盐酸响应Zn + 2H+ = Zn2+ + H2↑4.铁与稀硫酸响应Fe + 2H+ = Fe2+ + H2↑5.氧化镁与稀硫酸响应MgO + 2H+ = Mg2+ + H2O6.氧化铁与稀盐酸响应Fe2O3 + 6H+ = 2Fe3+ + 3H2O7.氢氧化钠与稀硫酸响应OH-+ H+ = H2O8.氢氧化镁与稀盐酸响应Mg(OH)2 + 2H+ = Mg2+ + 2H2O9.硝酸银与稀盐酸响应Ag+ + Cl-= AgCl↓10.氯化钡与稀硫酸响应Ba2+ + SO42-= BaSO4↓11.氢氧化钡与稀硫酸响应Ba2++2OH-+2H++SO42-= BaSO4↓+2H2O 12.氯化镁与氢氧化钠溶液响应Mg2+ +2OH-= Mg(OH)2↓13.二氧化碳与氢氧化钠溶液响应CO2 + 2OH-== CO32-+ H2O14.过量的二氧化碳与氢氧化钠溶液响应CO2 + OH-== HCO3-15.二氧化硫与氢氧化钠溶液响应SO2 + 2OH-== SO32-+ H2O16.过量的二氧化硫与氢氧化钠溶液响应SO2 + OH-== HSO3-17.二氧化碳与澄清的石灰水响应CO2 + Ca2+ +2OH-== CaCO3↓+ H2O18.氢氧化钙溶液与纯碱溶液响应Ca2+ + CO32-== CaCO3↓19.氢氧化钡溶液与碳酸钠溶液响应Ba2+ + CO32-== BaCO3↓20.硫酸铜溶液与氢氧化钾溶液响应Cu2+ + 2OH-== Cu(OH)2↓一.物质与氧气的响应:(一)单质与氧气的响应:1.镁在空气中燃烧:2Mg+O2点燃2MgO2.铁在氧气中燃烧:3Fe+2O2点燃Fe3O43.铜在空气中受热:2Cu+O2加热2CuO4.铝在空气中燃烧:4Al+3O2点燃2Al2O35.氢气中空气中燃烧:2H2+O2点燃2H2O6.红磷在空气中燃烧:4P+5O2点燃2P2O57.硫粉在空气中燃烧:S+O2点燃SO28.碳在氧气中充分燃烧:C+O2点燃CO29.碳在氧气中不充分燃烧:2C+O2点燃2CO(二)化合物与氧气的响应:10.一氧化碳在氧气中燃烧:2CO+O2点燃2CO211.甲烷在空气中燃烧:CH4+2O2点燃CO2+2H2O12.酒精在空气中燃烧:C2H5OH+3O2点燃2CO2+3H2O二.几个分解响应:13.水在直流电的作用下分解:2H2O通电2H2↑+O2↑14.加热碱式碳酸铜:Cu2(OH)2CO3加热2CuO+H2O+CO2↑15.加热氯酸钾(有少量的二氧化锰):2KClO3MnO22KCl+3O2↑16.加热高锰酸钾:2KMnO4加热K2MnO4+MnO2+O2↑17.碳酸不稳定而分解:H2CO3===H2O+CO2↑18.高温煅烧石灰石:CaCO3高温CaO+CO2↑三.几个氧化还原响应:19.氢气还原氧化铜:H2+CuO加热Cu+H2O20.木炭还原氧化铜:C+2CuO高温2Cu+CO2↑21.焦炭还原氧化铁:3C+2Fe2O3高温4Fe+3CO2↑22.焦炭还原四氧化三铁:2C+Fe3O4高温3Fe+2CO2↑23.一氧化碳还原氧化铜:CO+CuO加热Cu+CO224.一氧化碳还原氧化铁:3CO+Fe2O3高温2Fe+3CO225.一氧化碳还原四氧化三铁:4CO+Fe3O4高温3Fe+4CO2 四.单质、氧化物、酸、碱、盐的互相关系(一)金属单质+酸盐+氢气(置换响应)26.锌和稀硫酸Zn+H2SO4=ZnSO4+H2↑27.铁和稀硫酸Fe+H2SO4=FeSO4+H2↑28.镁和稀硫酸Mg+H2SO4=MgSO4+H2↑29.铝和稀硫酸2Al+3H2SO4=Al2(SO4)3+3H2↑30.锌和稀盐酸Zn+2HCl===ZnCl2+H2↑31.铁和稀盐酸Fe+2HCl===FeCl2+H2↑32.镁和稀盐酸Mg+2HCl===MgCl2+H2↑33.铝和稀盐酸2Al+6HCl==2AlCl3+3H2↑(二)金属单质+盐(溶液)另一种金属+另一种盐34.铁和硫酸铜溶液响应:Fe+CuSO4===FeSO4+Cu35.锌和硫酸铜溶液响应:Zn+CuSO4===ZnSO4+Cu36.铜和硝酸汞溶液响应:Cu+Hg(NO3)2===Cu(NO3)2+Hg(三)碱性氧化物+酸盐+水37.氧化铁和稀盐酸响应:Fe2O3+6HCl===2FeCl3+3H2O38.氧化铁和稀硫酸响应:Fe2O3+3H2SO4===Fe2(SO4)3+3H2O39.氧化铜和稀盐酸响应:CuO+2HCl====CuCl2+H2O40.氧化铜和稀硫酸响应:CuO+H2SO4====CuSO4+H2O41.氧化镁和稀硫酸响应:MgO+H2SO4====MgSO4+H2O42.氧化钙和稀盐酸响应:CaO+2HCl====CaCl2+H2O(四)酸性氧化物+碱盐+水43.苛性钠暴露在空气中变质:2NaOH+CO2====Na2CO3+H2O 44.苛性钠吸收二氧化硫气体:2NaOH+SO2====Na2SO3+H2O 45.苛性钠吸收三氧化硫气体:2NaOH+SO3====Na2SO4+H2O 46.消石灰放在空气中变质:Ca(OH)2+CO2====CaCO3↓+H2O 47.消石灰吸收二氧化硫:Ca(OH)2+SO2====CaSO3↓+H2O(五)酸+碱盐+水48.盐酸和烧碱起响应:HCl+NaOH====NaCl+H2O49.盐酸和氢氧化钾响应:HCl+KOH====KCl+H2O50.盐酸和氢氧化铜响应:2HCl+Cu(OH)2====CuCl2+2H2O51.盐酸和氢氧化钙响应:2HCl+Ca(OH)2====CaCl2+2H2O52.盐酸和氢氧化铁响应:3HCl+Fe(OH)3====FeCl3+3H2O53.氢氧化铝药物治疗胃酸过多:3HCl+Al(OH)3====AlCl3+3H2O54.硫酸和烧碱响应:H2SO4+2NaOH====Na2SO4+2H2O55.硫酸和氢氧化钾响应:H2SO4+2KOH====K2SO4+2H2O56.硫酸和氢氧化铜响应:H2SO4+Cu(OH)2====CuSO4+2H2O57.硫酸和氢氧化铁响应:3H2SO4+2Fe(OH)3====Fe2(SO4)3+6H2O58.硝酸和烧碱响应:HNO3+NaOH====NaNO3+H2O(六)酸+盐另一种酸+另一种盐59.大理石与稀盐酸响应:CaCO3+2HCl===CaCl2+H2O+CO2↑60.碳酸钠与稀盐酸响应:Na2CO3+2HCl===2NaCl+H2O+CO2↑61.碳酸镁与稀盐酸响应:MgCO3+2HCl===MgCl2+H2O+CO2↑62.盐酸和硝酸银溶液响应:HCl+AgNO3===AgCl↓+HNO363.硫酸和碳酸钠响应:Na2CO3+H2SO4===Na2SO4+H2O+CO2↑64.硫酸和氯化钡溶液响应:H2SO4+BaCl2====BaSO4↓+2HCl(七)碱+盐另一种碱+另一种盐65.氢氧化钠与硫酸铜:2NaOH+CuSO4====Cu(OH)2↓+Na2SO4 66.氢氧化钠与氯化铁:3NaOH+FeCl3====Fe(OH)3↓+3NaCl 67.氢氧化钠与氯化镁:2NaOH+MgCl2====Mg(OH)2↓+2NaCl68.氢氧化钠与氯化铜:2NaOH+CuCl2====Cu(OH)2↓+2NaCl69.氢氧化钙与碳酸钠:Ca(OH)2+Na2CO3===CaCO3↓+2NaOH (八)盐+盐两种新盐70.氯化钠溶液和硝酸银溶液:NaCl+AgNO3====AgCl↓+NaNO3 71.硫酸钠和氯化钡:Na2SO4+BaCl2====BaSO4↓+2NaCl五.其它响应:72.二氧化碳溶解于水:CO2+H2O===H2CO373.生石灰溶于水:CaO+H2O===Ca(OH)274.氧化钠溶于水:Na2O+H2O====2NaOH75.三氧化硫溶于水:SO3+H2O====H2SO476.硫酸铜晶体受热分解:CuSO4?5H2O加热CuSO4+5H2O 77.无水硫酸铜作干燥剂:CuSO4+5H2O====CuSO4?5H2O。

高中化学(人教版)必修一、必修二相关化学方程式汇总必修一1、硫酸根离子的检验: BaCl 2 + Na2SO 4 ==== BaSO4↓+ 2NaCl2、碳酸根离子的检验: CaCl 2 + Na2CO 3 ===== CaCO3↓ + 2NaCl3、碳酸钠与盐酸反应: Na 2CO 3 + 2HCl ===== 2NaCl + H2O + CO2↑4、木炭还原氧化铜: 2CuO + C 高温2Cu + CO2↑5、铁片与硫酸铜溶液反应: Fe + CuSO4 ===== FeSO4 + Cu6、氯化钙与碳酸钠溶液反应:CaCl 2 + Na2CO 3 ===== CaCO3↓+ 2NaCl7、钠在空气中燃烧:2Na + O2 Na2O 2钠与氧气反应:4Na + O2 ==== 2Na2O8、过氧化钠与水反应:2Na 2O 2 + 2H2O ==== 4NaOH + O2↑9、过氧化钠与二氧化碳反应:2Na 2O 2 + 2CO2 ==== 2Na2CO 3 + O210、钠与水反应:2Na + 2H2O ==== 2NaOH + H2↑11、铁与水蒸气反应:3Fe + 4H2O (g ==== Fe3O 4 + 4H2↑12、铝与氢氧化钠溶液反应:2Al + 2NaOH + 2H2O ==== 2NaAlO2 + 3H2↑13、氧化钙与水反应:CaO + H2O ==== Ca(OH214、氧化铁与盐酸反应:Fe 2O 3 + 6HCl ===== 2FeCl3 + 3H2O15、氧化铝与盐酸反应:Al 2O 3 + 6HCl ===== 2AlCl3 + 3H2O16、氧化铝与氢氧化钠溶液反应:Al 2O 3 + 2NaOH ===== 2NaAlO2 + H2O17、氯化铁与氢氧化钠溶液反应:FeCl 3 + 3NaOH ===== Fe(OH3↓+ 3NaCl18、硫酸亚铁与氢氧化钠溶液反应:FeSO 4 + 2NaOH ==== Fe(OH2↓+ Na2SO 419、氢氧化亚铁被氧化成氢氧化铁:4Fe(OH2 + 2H2O + O2 ==== 4Fe(OH320、氢氧化铁加热分解:2Fe(OH3 Fe2O 3 + 3H2O ↑21、实验室制取氢氧化铝:Al 2(SO4 3 + 6NH3·H 2O ==== 2Al(OH3↓ + 3(NH3 2SO 422、氢氧化铝与盐酸反应:Al(OH3 + 3HCl ==== AlCl3 + 3H2O23、氢氧化铝与氢氧化钠溶液反应:Al(OH3 + NaOH ==== NaAlO2 + 2H2O24、氢氧化铝加热分解:2Al(OH3 Al2O 3 + 3H2O25、三氯化铁溶液与铁粉反应:2FeCl 3 + Fe ==== 3FeCl226、氯化亚铁中通入氯气:2FeCl 2 + Cl2 ===== 2FeCl327、二氧化硅与氢氟酸反应:SiO 2 + 4HF ==== SiF4 + 2H 2O硅单质与氢氟酸反应:Si + 4HF ==== SiF4 + 2H 2↑28、二氧化硅与氧化钙高温反应:SiO 2 + CaO 高温 CaSiO329、二氧化硅与氢氧化钠溶液反应:SiO 2 + 2NaOH ==== Na2SiO 3 + H2O30、往硅酸钠溶液中通入二氧化碳:Na 2SiO 3 + CO2 + H2O === Na2CO 3 +H2SiO 3↓31、硅酸钠与盐酸反应:Na 2SiO 3 + 2HCl === 2NaCl + H2SiO 3↓32、氯气与金属铁反应:2Fe + 3Cl2 点燃 2FeCl 333、氯气与金属铜反应:Cu + Cl2 点燃CuCl 234、氯气与金属钠反应:2Na + Cl2 点燃 2NaCl35、氯气与水反应:Cl 2 + H2O ==== HCl + HClO36、次氯酸光照分解:2HClO 光照2HCl + O2↑37、氯气与氢氧化钠溶液反应:Cl 2 + 2NaOH ===== NaCl + NaClO + H2O38、氯气与消石灰反应:2Cl 2 + 2Ca(OH2 ==== CaCl2 + Ca(ClO2 + 2H2O39、盐酸与硝酸银溶液反应:HCl + AgNO3 ==== AgCl↓ + HNO340、漂白粉长期置露在空气中:Ca(ClO2 + H2O + CO2 ==== CaCO3↓ + 2HClO41、二氧化硫与水反应:SO 2 + H2O === H2SO 342、氮气与氧气在放电下反应:N 2 + O2 放电 2NO43、一氧化氮与氧气反应:2NO + O2 ==== 2NO244、二氧化氮与水反应:3NO 2 + H2O ==== 2HNO3 + NO45、二氧化硫与氧气在催化剂的作用下反应:2SO 2 + O2催化剂 2SO346、三氧化硫与水反应:SO 3 + H2O ==== H2SO 4 47、浓硫酸与铜反应:Cu + 2H2SO 4(浓CuSO4 + 2H2O + SO2↑48、浓硫酸与木炭反应:C + 2H2SO 4(浓CO2 ↑+ 2SO2↑ + 2H2O49、浓硝酸与铜反应:Cu + 4HNO3(浓==== Cu(NO3 2 + 2H2O + 2NO2↑50、稀硝酸与铜反应:3Cu + 8HNO3(稀3Cu(NO3 2 + 4H2O + 2NO↑51、氨水受热分解:N H 3·H 2O NH3↑ + H2O52、氨气与氯化氢反应:NH 3 + HCl ==== NH4Cl53、氯化铵受热分解:NH 4Cl NH3↑ + HCl↑54、碳酸氢氨受热分解:NH 4HCO 3 NH3↑ + H2O ↑ + CO2↑55、硝酸铵与氢氧化钠反应:NH 4NO 3 + NaOH NH3↑ + NaNO3 + H2O56、氨气的实验室制取:2NH 4Cl + Ca(OH2CaCl2 + 2H2O + 2NH3↑ 57、氯气与氢气反应:Cl 2 + H2 点燃 2HCl58、硫酸铵与氢氧化钠反应:(NH 4)2SO 4 + 2NaOH2NH3↑ + Na2SO 4 + 2H2O59、SO 2 + CaO ==== CaSO360、SO 2 + 2NaOH ==== Na2SO 3 + H2O61、SO 2 + Ca(OH2 ==== CaSO3↓ + H2O62、SO 2 + Cl2 + 2H2O ==== 2HCl + H2SO 463、SO 2 + 2H2S ==== 3S + 2H2O 64、NO 、NO 2的回收:NO 2 + NO + 2NaOH ==== 2NaNO 2 + H2O65、Si + 2F2 === SiF466、Si + 2NaOH + H2O ==== Na2SiO 3 +2H2↑67、硅单质的实验室制法粗硅的制取:SiO 2 + 2C 高温电炉 Si + 2CO(石英沙)(焦碳)(粗硅)粗硅转变为纯硅:Si (粗) + 2Cl2SiCl4 SiCl 4 + 2H2高温 Si(纯)+ 4HCl必修二第一章物质结构元素周期律1、Li 与O 2反应(点燃): 4Li + O22Li 2 O Na 与O 2反应(点燃): 2Na+O2Na 2O 2Na 与H 2O 反应:2Na+2H2O===2NaOH+H2↑K 与H 2O 反应:2K+2H2O===2KOH+H2↑2、卤素单质F 2 、Cl 2 、Br 2 、I 2与氢气反应:F 2 + H2 === 2HF Cl 2 + H2 === 2HClBr 2 + H2 === 2Br I 2 + H2 === 2HI3、卤素单质间的置换反应:(1)氯水与饱和溴化钠、氯水与饱和碘化钠溶液反应:① Cl 2+2NaBr===Br2+2NaCl② Cl 2+2NaI===I2+2NaCl(2)溴水与碘化钠溶液反应:Br 2+2NaI===I2+2NaBr4、Mg 与H 2O 反应:Mg+2H2O === Mg(OH2+H2↑Al 与HCl 反应: 2Al+6HCl===2AlCl3+3H2↑Mg 与HCl 反应: Mg+2 HCl === MgCl2+ H2↑5、Na 与Cl 2反应(点燃):6、用电子式表示氯化氢的形成过程:第二章化学反应与能量1、Ba(OH2•8H 2O 与NH 4Cl 的反应 :Ba(OH2·8H 2O+2NH4Cl==BaCl2+2NH3↑+10H2O2、原电池原理典型的原电池(Zn-Cu 原电池)负极(锌):Zn-2e -===Zn2+(氧化反应)正极(铜):2H ++2e-===H2↑(还原反应)电子流动方向:由锌经过外电路流向铜。

高中化学必修二有机化学方程式篇一:必修2有机化学方程式汇总必修2有机化学方程式汇总1. CH4 + 2O CO2 + 2H2O 甲烷的燃烧反应2. CH4 + Cl2 CH3Cl + HCl3. CH3Cl + Cl2 CH2Cl2 + HCl4. CH2Cl + Cl光照CHCl3 + HCl 光照光照点燃甲烷的取代反应5. CHCl3 + Cl CCl4+ HCl6. CH4C +2H2 甲烷受热分解(隔绝空气)7. CH3COONa + NaOH △CH4↑+ Na2CO3甲烷的实验室制备(了解)8. C2H4 + 3O2 2CO2 + 2H2O乙烯的燃烧反应9. CH2 = CH2 + Br CH2Br—CH2Br10. CH2 = CH23CH2OH11. CH2 = CH2CaO 高温光照点燃3—CH2Br 乙烯的加成反应12. CH2 = CH23—CH313. nCH2 = CHCH2乙烯的加聚反应14. 2C6H6 +15O2 12CO2 + 6H2O苯的燃烧反应15. + Br2 苯的卤代反应16. + HO2 +H2O苯的硝化反应17. + HO3H+H2O苯的磺化反应(了解)18. + 3H2 △苯的加成反应Ni -NO2 2O 甲苯硝化反应制TNT(了解)20. C2H6O+ 3O2 2CO2 + 3H2O乙醇的燃烧反应21. 2CH3CH22CH3CH2ONa + H2↑乙醇的置换反应22. 2CH3CH2OH+O2Cu/Ag 2CH3CHO + 2H2O 乙醇的催化氧化△23. CH3CH2OH 浓硫酸 2 = C H2↑+ H2O 乙醇的消去反应(实验室制乙烯的原理)170℃24. C2H5OH+C2H5140℃C2H5OC2H5+H2O 分子间脱水成醚(了解)25. 2CH3COOH+2Na 2CH3COONa+H2↑26.2CH3COOH+Na2CO2CH3COONa+H2O+CO2↑ 27. CH33 CH3COONa+H2O+CO2↑28. CH3COOH + NaOH CH3COONa + H2O 29. 2CH3COOH + Cu(OH)(CHCOO)2Cu + 2H2O 30. CH3COOH+CH3CH23COOCH2CH3 +H2O 酯化反应31. CH3COOCH2CH33COONa+CH3CH2OH 酯的水解32. C6H12O6 (s) + 6O 6CO2 (g) + 6H2O (l) 生理氧化反应(有氧呼吸)33. C6H12O6 2CH3CH2OH + 2CO2发酵生成酒精34. C12H22O11+H2OC6H12O6+ C6H12O6蔗糖葡萄糖果糖 35. C12H22O11 + H2O 催化剂2C6H12O6麦芽唐葡萄糖催化剂催化剂浓硫酸乙酸的酸性(了解)36. (C6H10O5)n + nH2n C6H12O6淀粉葡萄糖37. (C6H10O5)n + nH2催化剂n C6H12O6 △纤维素葡萄糖催化剂双糖和多糖的水解篇二:必修2有机化学方程式汇总必修2有机化学方程式汇总1. CH4 + 2O CO2 + 2H2O 甲烷的燃烧反应2. CH4 + Cl2CH3Cl + HCl3. CH3Cl + Cl2CH2Cl2 + HCl4. CH2Cl + Cl光照CHCl3 + HCl 光照光照点燃甲烷的取代反应5. CHCl3 + Cl CCl4+ HCl6. CHC +2H2 甲烷受热分解(隔绝空气)7. CH3COONa + NaOH △CH4↑+ Na2CO3甲烷的实验室制备(了解)8. C2H4 + 3O2 点燃2CO2 + 2H2O乙烯的燃烧反应9. CH2 = CH2CH2Br—CH2B(来自: 小龙文档网:高中化学必修二有机化学方程式)r10. CH2 = CH23CH2OH11. CH2 = CH2CH3—CH2Br CaO 高温光照乙烯的加成反应12. CH2 = CH23—CH3 13. nCH2 CH 乙烯的加聚反应14. 2C6H6 +15O2 12CO2 + 6H2O苯的燃烧反应15. + Br2 苯的卤代反应16. NO2 +H2O苯的硝化反应17. 3H+H2O苯的磺化反应(了解)18. + 3H2 △苯的加成反应Ni 点燃-NO2 2O 甲苯硝化反应制TNT(了解)20. C2H6O+ 3O2点燃2CO2 + 3H2O乙醇的燃烧反应21. 2CH3CH2 2CH3CH2ONa + H2↑乙醇的置换反应22. 2CH3CH2OH+O2 Cu/Ag 2CH3CHO + 2H2O 乙醇的催化氧化△CH2 = CH2↑+ H2O 乙醇的消去反应23. CH3CH2OH 浓硫酸(实验室制乙烯的原理)170℃浓硫酸24. C2H5OH+C2H5 C2H5OC2H5+H2O 分子间脱水成醚(了解)140℃25. 2CH3 2CH3COO Na+H2↑26.2CH3COOH+Na232CH3COONa+H2O+CO2↑乙酸的酸性27. CH33 CH3COONa+H2O+CO2↑28. CH3 CH3COONa + H2O29. 2CH33COO)2Cu + 2H2O30. CH3COOH+CH3 CH3COOCH2CH3 +H2O 酯化反应31. CH3COOCH2CH33COONa+CH3CH2OH酯的水解32. C6H12O6 (s) + 6O 6CO2 (g) + 6H2O (l) 生理氧化反应(有氧呼吸)33. C6H12O催化剂6 2CH催化剂3CH 2OH + 2CO2发酵生成酒精(无氧呼吸)34. C12H22O11+H2O C6H12O6+ C6H12O6蔗糖葡萄糖果糖35. C催化剂12H22O11 + H22C6H12O6麦芽唐葡萄糖36. (C催化剂双糖和多糖的水解6H10O5)n + nH2 n C6H12O6淀粉葡萄糖37. (C催化剂6H10O5)n + nH2 △n C6H12O6纤维素葡萄糖(了解)篇三:必修二_有机化学_方程式总结必修二有机化学方程式总结甲烷和Cl2:CH4+Cl2光CH3Cl+HClCH3Cl+Cl2 CH2Cl2+HClCH2Cl2+Cl2 CHCl3+HClCHCl3+Cl2 CCl4+HCl 甲烷燃烧:CH4+2O2 2+2H2O 甲烷分解:CH4C+2H2乙烯燃烧:C2H4 +3O2 2CO2+2H2O 乙烯与Br2:C2H4+ BrC2H4Br2 乙烯与H2:C2H4+H2C2H6 乙烯与HX:C2H4+HX 3CH2X 乙烯与H2O:C2H4+H2O 3CH2OH 乙烯的加聚:nC2H4 2-CH 2 点12CO2+6H2O 3 NO2 +H2O +H2SO4(浓3H +H2O 苯与H2+3H2 Ni 乙醇和钠:2C2H5OH+2Na 2CH3COONa+H2 乙醇燃烧:C2H5OH+O2 2CO2+3H2O 乙醇催化氧化:2C2H5OH+O2CH3CHO+2H2O乙醇分子内脱水:C2H5OH浓H2SO4、170℃CH2=CH22O 乙醇分子间脱水:2C2H5OH浓H2SO4 、140℃CH3CH2OC2H5(乙醚)+H2O 注:一般醚以与氧相连的烃基加醚字命名乙醇与HX:C2H5OH+HX C2H5OX+H2O 乙酸与NaOH: CH3COOH+NaOH CH3COONa+H2O 乙酸Na2CO3:CH3COOH+Na2CO3 CH3COONa+H2O+CO2乙醇与乙酸:CH3COOH+ C2H5OH 浓硫酸、△CH3COOC2H5+H2O 乙酸乙酯水解:CH3COOC2H5+H2O CH3COOH+ C2H5OH乙酸乙酯皂化:CH3COOC2H5+NaO △CH3COONa+ C2H5OH 蔗糖水解:C12H22O11蔗+H2O 稀硫酸C6H10O6葡+ C6H10O6果麦芽糖水解:C12H22O11麦+H2O 催 2 C6H10O6葡纤维素水解:(C6H10O5)n纤+H2O 6H10O6葡淀粉水解:(C6H10O5)n淀+H2O nC6H10O6葡C17H35COOCH2 CH2OH (饱和)C17H352O 17H35COOH+CHOH C17H35COOCH2 CH2OH 软质酸甘油酯:C15H35COOCH2(不饱和)C15H35COOCH2C15H35COOCH2油酸甘油酯:C17H33COOCH2C17H33COOCH2相关热词搜索:有机化学方程式必修高中化学高二有机化学方程式必修5有机化学方程式。

必修二有机物化学方程式有机物化学方程式1.甲烷燃烧CH4+2O2→CO2+2H2O(条件为点燃)2.甲烷隔绝空气高温分解甲烷分解很复杂,以下是最终分解。
CH4→C+2H2(条件为高温高压,催化剂)3.甲烷和氯气发生取代反应CH4+Cl2→CH3Cl+HCl CH3Cl+Cl2→CH2Cl2+HClCH2Cl2+Cl2→CHCl3+HCl CHCl3+Cl2→CCl4+HCl (条件都为光照。
)4.实验室制甲烷CH3COONa+NaOH→Na2CO3+CH4(条件是CaO 加热)5.乙烯燃烧CH2=CH2+3O2→2CO2+2H2O(条件为点燃)6.乙烯和溴水CH2=CH2+Br2→CH2Br-CH2Br7.乙烯和水CH2=CH2+H2O→CH3CH2OH (条件为催化剂)8.乙烯和氯化氢CH2=CH2+HCl→CH3-CH2Cl9.乙烯和氢气CH2=CH2+H2→CH3-CH3(条件为催化剂)10.乙烯聚合nCH2=CH2→-[-CH2-CH2-]n- (条件为催化剂)11.氯乙烯聚合nCH2=CHCl→-[-CH2-CHCl-]n- (条件为催化剂)12.实验室制乙烯CH3CH2OH→CH2=CH2↑+H2O (条件为加热,浓H2SO4)13.乙炔燃烧C2H2+3O2→2CO2+H2O (条件为点燃)14.乙炔和溴水C2H2+2Br2→C2H2Br415.乙炔和氯化氢两步反应:C2H2+HCl→C2H3Cl--------C2H3Cl+HCl→C2H4Cl216.乙炔和氢气两步反应:C2H2+H2→C2H4→C2H2+2H2→C2H6(条件为催化剂)17.实验室制乙炔CaC2+2H2O→Ca(OH)2+C2H2↑18.以食盐、水、石灰石、焦炭为原料合成聚乙烯的方程式。
CaCO3 === CaO + CO22CaO+5C===2CaC2+CO2CaC2+2H2O→C2H2+Ca(OH)2C+H2O===CO+H2-----高温C2H2+H2→C2H4 ----乙炔加成生成乙烯C2H4可聚合19.苯燃烧2C6H6+15O2→12CO2+6H2O (条件为点燃)20.苯和液溴的取代C6H6+Br2→C6H5Br+HBr21.苯和浓硫酸浓硝酸C6H6+HNO3→C6H5NO2+H2O (条件为浓硫酸)22.苯和氢气C6H6+3H2→C6H12 (条件为催化剂)23.乙醇完全燃烧的方程式C2H5OH+3O2→2CO2+3H2O (条件为点燃)24.乙醇的催化氧化的方程式2CH3CH2OH+O2→2CH3CHO+2H2O(条件为催化剂)(这是总方程式)25.乙醇发生消去反应的方程式CH3CH2OH→CH2=C H2+H2O (条件为浓硫酸170摄氏度)26.两分子乙醇发生分子间脱水2CH3CH2OH→CH3CH2OCH2CH3+H2O (条件为催化剂浓硫酸140摄氏度) 27.乙醇和乙酸发生酯化反应的方程式CH3COOH+C2H5OH→CH3COOC2H5+H2O28.乙酸和镁Mg+2CH3COOH→(CH3COO)2Mg+H229.乙酸和氧化钙2CH3COOH+CaO→(CH3CH2)2Ca+H2O30.乙酸和氢氧化钠CH3COOCH2CH3+NaOH→CH3C OONa+CH3CH2OH31.乙酸和碳酸钠Na2CO3+2CH3COOH→2CH3COONa+H2O+CO2↑32.甲醛和新制的氢氧化铜HCHO+4Cu(OH)2→2Cu2O+CO2↑+5H2O33.乙醛和新制的氢氧化铜CH3CHO+2CU(OH)2=CH3COOH+CU2O+2H2O34.乙醛氧化为乙酸2CH3CHO+O2→2CH3COOH(条件为催化剂或加温)一.烯烃是指含有C=C键的碳氢化合物。
必修2化学方程式总汇
(知识点总结)
第一章物质结构元素周期律
1、Li与O2反应(点燃)
Na与O2反应(点燃)
Na与H2O反应:
K与H2O反应:
2、卤素单质F2、Cl2、Br2、I2与氢气反应
、、、
3、卤素单质间的置换反应:
(1)氯水与饱和溴化钠、氯水与饱和碘化钠溶液反应:
①②
(2)溴水与碘化钠溶液反应:
4、Mg与H2O反应:
5、Na与Cl2、反应(点燃):
6、用电子式表示氯化钠的形成过程:
用电子式表示氯分子的形成过程:
用电子式表示氯化氢的形成过程:
用电子式表示下列分子:
H2N2H2O CO2CCl4
第二章化学反应与能量
1、Ba(OH)2·8H2O与NH4Cl的反应
2、原电池原理
典型的原电池(Zn-Cu原电池)
负极(锌):(氧化反应)
正极(铜):(还原反应)
电子流动方向:由锌经过外电路流向铜。
总反应离子方程式:
3、H2O2在催化剂作用下受热分解:
4、Na2SO4与CaCl2反应:
5、高炉炼铁:
第三章有机化合物
1、甲烷的主要化学性质
(1)氧化反应(与O2的反应):
(2)取代反应(与Cl2在光照条件下的反应,生成四种不同的取代物):
①②
③④
2、乙烯的主要化学性质
(1)氧化反应(与O2的反应):
(2)加成反应(与Br2的反应):
(3)乙烯还可以和氢气、氯化氢、水等发生加成反应
①②③
(4)聚合反应:
(乙烯制聚乙烯) ①(氯乙烯制聚氯乙烯)②
3、苯的主要化学性质:
(1)氧化反应(与O2的反应):
(2)取代反应
①与Br2的反应:②硝化反应,
(3)加成反应
用镍做催化剂,苯与氢发生加成反应:
4、乙醇的重要化学性质
(1)乙醇与金属钠的反应:
(2)乙醇的氧化反应
①乙醇的燃烧
②乙醇的催化氧化反应
③乙醇在常温下的氧化反应
KMnO4/H+或K2CrO4
CH3CH2OH CH3COOH
5、乙酸的重要化学性质
(1)乙酸的酸性
①乙酸能使紫色石蕊试液变红
②乙酸能与碳酸盐反应,生成二氧化碳气体
利用乙酸的酸性,可以用乙酸来除去水垢(主要成分是CaCO3):
乙酸还可以与碳酸钠反应,也能生成二氧化碳气体:
上述两个反应都可以证明乙酸的酸性比碳酸的酸性强。
(2)乙酸的酯化反应
①反应原理(与乙醇的反应):
乙酸与乙醇反应的主要产物乙酸乙酯是一种无色、有香味、密度比水的小、不溶于水的油状液体。
6、①蔗糖水解反应:
②淀粉(纤维素)水解反应:
③油脂的重要化学性质——水解反应
a)油脂在酸性条件下的水解H+
油脂+H2O 甘油+
b)油脂在碱性条件下的水解(又叫反应)
OH-
油脂+H2O 甘油+
酶
蛋白质+H2O 各种
第四章化学与可持续发展
1、HgO受热分解:Ag2O受热分解:
2、①C 还原ZnO ②C 还原MgO
③O2还原Cu2S ④Al 还原Fe2O3(铝热反应)
⑤Fe还原CuSO4:⑥CO还原Fe2O3
3、①电解NaCl ②电解MgCl2
③电解Al2O3
4、石油的催化裂化,例如:C4H10裂化得到乙烯和乙烷:
[参考答案]
第一章 物质结构 元素周期律
1、4Li + O 2 2Li 2 O 2Na+O 2Na 2O 2
2Na+2H 2O===2NaOH+H 2↑ 2K+2H 2O===2KOH+H 2↑
2、卤素单质与氢气反应
F 2 + H 2 === 2HF Cl 2 + H 2 === 2HCl
Br 2 + H 2 === 2Br I 2 + H 2 === 2HI
3、卤素单质间的置换反应:
(1)Cl 2可以从溴化物(或碘化物)中置换出Br 2(或I 2):
①Cl 2+2NaBr=Br 2+2NaCl ②Cl 2+2KI=I 2+2KCl
(2)Br 2可以从碘化物中置换出I 2:Br 2+2KI=I 2+2KBr
4、Mg+2H 2O === Mg(OH)2↓+H 2↑ 2Al+6HCl===2AlCl 3+3H 2↑ Mg+2 HCl === MgCl2+ H 2↑
5、
氯化钠的形成过程:略`
氯分子的形成过程: 氯化氢的形成过程:
用电子式表示下列分子:略
第二章 化学反应与能量
1、 Ba(OH)2·8H 2O+2NH 4Cl==BaCl 2+2NH 3↑+10H 2O
NaOH+HCl==NaCl+H 2O
2、原电池原理
(1)概念:原电池是把化学能转变成电能的装置
(2)典型的原电池(Zn-Cu 原电池)
负极(锌):Zn-2e -=Zn 2+ (氧化反应)正极(铜):2H ++2e -=H 2↑ (还原反应)
电子流动方向:由锌经过外电路流向铜。
总反应离子方程式:Zn+2H +=Zn 2++H 2↑
3、2H 2O 2= 催化剂 △ 2H 2O+O 2↑
4、Na 2SO 4+CaCl 2=CaSO 4↓+Na 2CO 3
5、2C + O 2 = 2CO
Fe 2O 3 + 3CO ==2Fe + 3CO 2
第三章 有机化合物
1、甲烷的主要化学性质
(1)氧化反应
CH 4(g)+2O 2(g)−−→
−点燃
CO 2(g)+2H 2O(l) (2)取代反应
2、乙烯的主要化学性质
(1)氧化反应:C 2H 4+3O 2 −−→
−点燃
2CO 2+2H 2O
(2)加成反应
乙烯还可以和氢气、氯化氢、水等发生加成反应。
CH 2=CH 2 + H 2CH 3CH 3
CH 2=CH 2+HCl CH 3CH 2Cl (一氯乙烷)
CH 2=CH 2+H 2O CH 3CH 2OH (乙醇)
(3)聚合反应:
3、苯的主要化学性质
(1) 氧化反应 2C 6H 6+15O 2 −−→
−点燃 12CO 2+6H 2O
(2) 取代反应
①
+ Br 2
−−−3
F e B r
+ HBr
② 苯与硝酸(用HONO 2表示)发生取代反应,生成无色、不溶于水、有苦杏仁气味、密度大于水的油状液体——硝基苯。
+ HONO 2 浓硫酸 △ + H 2O (3) 加成反应
用镍做催化剂,苯与氢发生加成反应,生成环己烷。
+ 3H2 −−
→−催化剂
4、乙醇的重要化学性质
(1) 乙醇与金属钠的反应
2CH 3CH 2OH+2Na 2CH 3CH 2ONa+H 2↑
NO 2
(2) 乙醇的氧化反应
①乙醇的燃烧
CH 3CH 2OH+3O 2
−−→−点燃 2CO 2+3H 2O
②乙醇的催化氧化反应 2CH 3CH 2OH+O 2 −
−→−Ag
Cu 或 2CH 3CHO+2H 2O 乙醛
③乙醇在常温下的氧化反应
CH 3CH 2OH −−−−−−−−→−或酸性重铬酸钾溶液酸性4KMnO CH 3COOH
5、乙酸的重要化学性质
(3) 乙酸的酸性
①乙酸能使紫色石蕊试液变红
②乙酸能与碳酸盐反应,生成二氧化碳气体
利用乙酸的酸性,可以用乙酸来除去水垢(主要成分是CaCO 3):
2CH 3COOH+CaCO 3(CH 3COO )2Ca+H 2O+CO 2↑
乙酸还可以与碳酸钠反应,也能生成二氧化碳气体:
2CH 3COOH+Na 2CO 32CH 3COONa+H 2O+CO 2↑
上述两个反应都可以证明乙酸的酸性比碳酸的酸性强。
(4) 乙酸的酯化反应
①反应原理
乙酸与乙醇反应的主要产物乙酸乙酯是一种无色、有香味、密度比水的小、不溶于水的油
状液体。
6、C 12H 22O 11+H 2O→C 6H 12O 6+C 6H 12O 6
油脂的重要化学性质——水解反应
(1) 油脂在酸性条件下的水解
油脂+H 2O −→−
酸甘油+高级脂肪酸 (2) 油脂在碱性条件下的水解(又叫皂化反应)
油脂+H2O
−→−碱甘油+高级脂肪酸
蛋白质+H 2O −−→−酶等各种氨基酸
第四章 化学与可持续发展
略。