7-5 循环过程
- 格式:ppt
- 大小:1.27 MB
- 文档页数:14

7-3.在体积为2.0×10-3m 3 的容器中,有内能为 6.75×102J 的刚性双原子分子理想气体。
求:(1)气体的压强;(2)设分子总数为 5.4×1022 个,则分子的平均平动动能及气体的温度。
[解] (1)理想气体的内能 kT i N E 2⋅= (1) 理想气体的压强 kT VN nkT p == (2) 由(1)、(2)两式可得 5321035.110251075.6252⨯=⨯⨯⨯⨯==-V E p Pa (2)由 kT i N E 2⋅= 则 362104.51038.151075.625222232=⨯⨯⨯⨯⨯⨯==-kN E T K 又 2123105.73621038.12323--⨯=⨯⨯⨯==kT w J 7-4.容器内储有氧气,其压强为 p = 1.01×10 5 Pa ,温度为 t = 27℃。
试求:(1)单位体积内的分子数;(2)分子的平均平动动能。
解:(1)由nkT p = (2)J 1021.63001038.123232123--⨯=⨯⨯⨯==kT w 7-5.容器内某理想气体的温度T =273K ,压强p =1.00 ×10-3atm ,密度为31.25g m ρ-=⋅,求:(1)气体的摩尔质量;(2)气体分子运动的方均根速率;(3)气体分子的平均平动动能和转动动能;(4)单位体积内气体分子的总平动动能;(5)0.3mol 该气体的内能。
[解] (1)由 RT pV ν=所以 4931025.110013.11000.13333532=⨯⨯⨯⨯⨯===--ρp m kT v m (2) 气体的摩尔质量所以该气体是2N 或CO(3)气体分子的平均平动动能气体分子的转动动能(4)单位体积内气体分子的总平动动能(5)该气体的内能8-3.一定量的理想气体,其体积和压强依照V=a 的规律变化,其中a 为已知常数。


内燃机热力循环一、燃气轮机循环燃气轮机理想循环为布雷顿循环(Brayton Cycle) ,它是工质连续流动做功的一种轮机循环,如图1所示 。
它既可作内燃布雷顿循环,又可作外燃布雷顿循环。
内燃的布雷顿循环为开式循环,常用工质为空气或燃气。
外燃的布雷顿循环是闭式循环,通过热交换器对工质加热,在另一热交换器排出工质余热。
循环过程为:工质在压气机中等熵压缩1-2,在燃烧室(或热交换器中)等压加热2-3 ,在燃气轮机中等熵膨胀3-4和等压排气4-1 。
图1 燃气轮机循环燃气轮机循环的指示热效率为11k k i c ηπ-=-式中,c π为压气机中气体的压比,k 为比热比。
燃气轮机开式循环常与内燃机基本循环配合使用。
二、涡轮增压内燃机热力循环将涡轮增压技术(或燃气轮机技术)应用到内燃机上是内燃机循环的一项重大技术发展。
一方面内燃机希望获得更多的进气(或可燃混合气)充量,以提高内燃机的功率和热效率;另一方面从内燃机排出的高温、高压废气能导入燃气涡轮中再作功,推动与燃气涡轮相连(同轴)的压气机来提高进气(或可燃混合气)的压力供给内燃机,这样就成为涡轮增压内燃机。
涡轮增压内燃机有等压涡轮和变压涡轮两种系统,它们的热力循环也有所不同。
1.恒压涡轮增压内燃机热力循环图2是等压涡轮增压内燃机热力循环。
它由内燃机基本循环1→2→3’→3→4→1和燃气轮机循环7→1→5→6→7组成。
图2 等压涡轮增压内燃机热力循环压气机将气体从状态7(大气压力p0)等熵压缩到状态1(压力为p s)之后进入内燃机。
按内燃机热力循环到达状态4。
气体在排气过程进入等压涡轮时由于排气门的节流损失和排气动能在排气总管内的膨胀、摩擦、涡流等损失而变成热能,气体温度升高,体积膨胀而到达状态5。
气体从4→5 这部分能量没有利用,对内燃机来说相当于从状态4直接回到状态1。
气体在等压涡轮中从状态5等熵膨胀到状态6,然后排入大气。
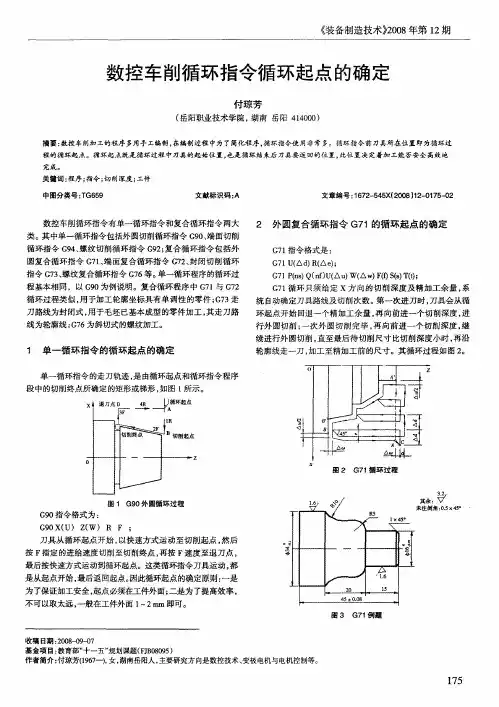
2 .变压涡轮增压内燃机热力循环变压涡轮增压内燃机热力循环如图3 。


PDCA循环的四个环节8个步骤
一、计划(Plan)环节
1.确定目标:明确组织或项目的目标和目标,它们应该是具体、明确、可衡量和可实现的。
2.分析数据:收集和分析相关数据和信息,了解当前情况和问题。
3.制定计划:根据目标和数据分析结果,制定改进计划或解决问题的
方案。
4.设定指标:设定衡量改进或解决问题的指标或标准,以便后续执行
和检查。
二、执行(Do)环节
5.实施计划:根据制定的计划,执行相关任务和活动。
6.收集数据:在执行过程中,及时收集相关数据和信息,以便后续的
检查和分析。
三、检查(Check)环节
7.分析数据:根据收集到的数据和信息,进行分析和评估,判断是否
达到预期目标。
8.总结经验:根据分析结果,总结经验教训,了解问题的原因和改进
的方向。
四、行动(Act)环节
9.提出改进方案:根据问题分析和总结经验,提出改进方案或纠正措施。
10.实施改进:根据提出的改进方案,对流程、制度、技术或管理方法等进行改进。
11.监控效果:在改进过程中,持续监控和评估改进效果,并及时修正,确保改进的可持续性。
以上是PDCA循环的四个环节和每个环节的具体步骤。
它是一个不断循环的过程,通过持续的改进和优化,使组织不断提高绩效和竞争力。
PDCA循环的核心思想是:通过计划、执行、检查和行动的循环过程,实现问题的找出、解决和纠正,不断改进和优化组织的管理和运营。
通过PDCA循环,组织可以更好地适应变化和挑战,实现持续改进和优化。




习题七7-1下列表述是否正确?为什么?并将错误更正.(1)A E Q ∆+∆=∆ (2)⎰+=V p E Q d(3)121Q Q -≠η (4)121Q Q -<不可逆η 解:(1)不正确,A E Q +∆=(2)不正确,⎰+=Vp E Q d Δ(3)不正确,121Q Q -=η(4)不正确,121Q Q -=不可逆η7-2 V p -图上封闭曲线所包围的面积表示什么?如果该面积越大,是否效率越高?答:封闭曲线所包围的面积表示循环过程中所做的净功.由于1Q A 净=η,净A 面积越大,效率不一定高,因为η还与吸热1Q 有关.7-3 如题7-3图所示,有三个循环过程,指出每一循环过程所作的功是正的、负的,还是零,说明理由.解:各图中所表示的循环过程作功都为0.因为各图中整个循环分两部分,各部分面积大小相等,而循环方向一个为逆时针,另一个为顺时针,整个循环过程作功为0.题7-3图7-4 用热力学第一定律和第二定律分别证明,在V p -图上一绝热线与一等温线不能有两个交点.题7-4图解:1.由热力学第一定律有 A E Q +∆=若有两个交点a 和b ,则 经等温b a →过程有0111=-=∆A Q E 经绝热b a →过程012=+∆A E 022<-=∆A E从上得出21E E ∆≠∆,这与a ,b 两点的内能变化应该相同矛盾.2.若两条曲线有两个交点,则组成闭合曲线而构成了一循环过程,这循环过程只有吸热,无放热,且对外做正功,热机效率为%100,违背了热力学第二定律. 7-5 一循环过程如题7-5图所示,试指出: (1)ca bc ab ,,各是什么过程;(2)画出对应的V p -图; (3)该循环是否是正循环?(4)该循环作的功是否等于直角三角形面积?(5)用图中的热量ac bc ab Q Q Q ,,表述其热机效率或致冷系数. 解:(1) a b 是等体过程bc 过程:从图知有KT V =,K 为斜率 由vRT pV = 得 K vR p =故bc 过程为等压过程 ca 是等温过程(2)V p -图如题57'-图题57'-图(3)该循环是逆循环(4)该循环作的功不等于直角三角形面积,因为直角三角形不是V p -图中的图形.(5)ab ca bc abQ Q Q Q e -+=题7-5图 题7-6图7-6 两个卡诺循环如题7-6图所示,它们的循环面积相等,试问: (1)它们吸热和放热的差值是否相同; (2)对外作的净功是否相等; (3)效率是否相同?答:由于卡诺循环曲线所包围的面积相等,系统对外所作的净功相等,也就是吸热和放热的差值相等.但吸热和放热的多少不一定相等,效率也就不相同. 7-7 评论下述说法正确与否?(1)功可以完全变成热,但热不能完全变成功;(2)热量只能从高温物体传到低温物体,不能从低温物体传到高温物体.(3)可逆过程就是能沿反方向进行的过程,不可逆过程就是不能沿反方向进行的过程. 答:(1)不正确.有外界的帮助热能够完全变成功;功可以完全变成热,但热不能自动地完全变成功; (2)不正确.热量能自动从高温物体传到低温物体,不能自动地由低温物体传到高温物体.但在外界的帮助下,热量能从低温物体传到高温物体.(3)不正确.一个系统由某一状态出发,经历某一过程达另一状态,如果存在另一过程,它能消除原过程对外界的一切影响而使系统和外界同时都能回到原来的状态,这样的过程就是 可逆过程.用任何方法都不能使系统和外界同时恢复原状态的过程是不可逆过程.有些过程 虽能沿反方向进行,系统能回到原来的状态,但外界没有同时恢复原状态,还是不可逆过程. 7-8 热力学系统从初平衡态A 经历过程P 到末平衡态B .如果P 为可逆过程,其熵变为:⎰=-BA AB T Q S S 可逆d ,如果P 为不可逆过程,其熵变为⎰=-B A A B T Q S S 不可逆d ,你说对吗?哪一个表述要修改,如何修改?答:不对.熵是状态函数,熵变只与初末状态有关,如果过程P 为可逆过程其熵变为:⎰=-BA AB T Q S S 可逆d ,如果过程P 为不可逆过程,其熵变为⎰>-B A A B T Q S S 不可逆d7-9 根据⎰=-B A A B T Q S S 可逆d 及⎰>-B A A B T Q S S 不可逆d ,这是否说明可逆过程的熵变大于不可逆过程熵变?为什么?说明理由.答:这不能说明可逆过程的熵变大于不可逆过程熵变,熵是状态函数,熵变只与初末状态有关,如果可逆过程和不可逆过程初末状态相同,具有相同的熵变.只能说在不可逆过程中,系统的热温比之和小于熵变.7-10 如题7-10图所示,一系统由状态a 沿acb 到达状态b 的过程中,有350 J 热量传入系统,而系统作功126 J .(1)若沿adb 时,系统作功42 J ,问有多少热量传入系统?(2)若系统由状态b 沿曲线ba 返回状态a 时,外界对系统作功为84 J ,试问系统是吸热还是放热?热量传递是多少?题7-10图解:由abc 过程可求出b 态和a 态的内能之差 A E Q +∆=224126350=-=-=∆A Q E J abd 过程,系统作功42=A J26642224=+=+∆=A E Q J 系统吸收热量ba 过程,外界对系统作功84-=A J30884224-=--=+∆=A E Q J 系统放热7-11 1 mol 单原子理想气体从300 K 加热到350 K ,问在下列两过程中吸收了多少热量?增加了多少内能?对外作了多少功? (1)体积保持不变; (2)压力保持不变. 解:(1)等体过程由热力学第一定律得E Q ∆= 吸热)(2)(1212V T T R iT T C E Q -=-=∆=υυ25.623)300350(31.823=-⨯⨯=∆=E Q J对外作功 0=A (2)等压过程)(22)(1212P T T R i T T C Q -+=-=υυ吸热75.1038)300350(31.825=-⨯⨯=Q J )(12V T T C E -=∆υ内能增加 25.623)300350(31.823=-⨯⨯=∆E J对外作功 5.4155.62375.1038=-=∆-=E Q A J 7-12 一个绝热容器中盛有摩尔质量为mol M ,比热容比为γ的理想气体,整个容器以速度v 运动,若容器突然停止运动,求气体温度的升高量(设气体分子的机械能全部转变为内能).解:整个气体有序运动的能量为221mu ,转变为气体分子无序运动使得内能增加,温度变化2V 21mu T C M m E =∆=∆ )1(211212mol V 2mol -==∆γu M R C u M T7-13 0.01 m 3氮气在温度为300 K 时,由0.1 MPa(即1 atm)压缩到10 MPa .试分别求氮气经等温及绝热压缩后的(1)体积;(2)温度;(3)各过程对外所作的功. 解:(1)等温压缩 300=T K 由2211V p V p = 求得体积3211210101.0101-⨯=⨯==p V p V 3m对外作功21112ln lnp pV p V V VRT A ==01.0ln 01.010013.115⨯⨯⨯⨯=31067.4⨯-=J(2)绝热压缩R C 25V =57=γ由绝热方程 γγ2211V p V p =γγ/12112)(p V p V =1121/12112)()(V p pp V p V γγγ==3411093.101.0)101(-⨯=⨯=m由绝热方程γγγγ---=22111p T p T 得K 579)10(30024.04.1111212=⨯==--T p p T T γγγγ热力学第一定律A E Q +∆=,0=Q 所以)(12molT T C M MA V --=RT M MpV mol =,)(2512111T T R RT V p A --= 35105.23)300579(25300001.010013.1⨯-=-⨯⨯⨯⨯-=A J7-14 理想气体由初状态),(11V p 经绝热膨胀至末状态),(22V p .试证过程中气体所作的功为12211--=γV p V p A ,式中γ为气体的比热容比.答:证明: 由绝热方程C V p V p pV ===γγγ2211 得γγV V p p 111=⎰=21d V V Vp A⎰-----==21)11(1d 11121111V V r V V V p v v V p A γγγγγ]1)[(112111---=-γγV VV p又 )(1111211+-+----=γγγγV V V p A 112221111--=+-+-γγγγγV V p V V p 所以 12211--=γV p V p A7-15 1 mol 的理想气体的T-V 图如题7-15图所示,ab 为直线,延长线通过原点O .求ab过程气体对外做的功.题7-15图解:设KV T =由图可求得直线的斜率K 为002V T K =得过程方程V V T K 002=由状态方程 RT pV υ= 得VRTp υ=ab 过程气体对外作功⎰=002d V v Vp A⎰⎰⎰====000020002202d 2d 2d V V V v V V RTV V RT VV V T V R V V RT A7-16 某理想气体的过程方程为a a Vp ,2/1=为常数,气体从1V 膨胀到2V .求其所做的功.解:气体作功⎰=21d V v Vp A⎰-=-==-2121)11()(d 2121222V V V VV V a V a V V a A7-17 设有一以理想气体为工质的热机循环,如题7-17图所示.试证其循环效率为1112121---=p p VV γη答:等体过程 吸热)(12V 1T T C Q -='υ)(1221V 11R V p R V p C Q Q -='= 绝热过程 03='Q等压压缩过程放热)(12p 2T T C Q -='υ)(2212P R V p R V p C -=循环效率 121Q Q-=η )1/()1/(1)()(1121212221V 2212p 12---=---=-=p p V p V p C V p V p C Q Q ννγηη题7-17图 题7-19图7-18 一卡诺热机在1000 K 和300 K 的两热源之间工作,试计算 (1)热机效率;(2)若低温热源不变,要使热机效率提高到80%,则高温热源温度需提高多少? (3)若高温热源不变,要使热机效率提高到80%,则低温热源温度需降低多少?解:(1)卡诺热机效率121T T -=η%7010003001=-=η(2)低温热源温度不变时,若%8030011=-=T η要求 15001=T K ,高温热源温度需提高500K(3)高温热源温度不变时,若%80100012=-=T η要求 2002=T K ,低温热源温度需降低100K7-19 如题7-19图所示是一理想气体所经历的循环过程,其中AB 和CD 是等压过程,BC 和DA 为绝热过程,已知B 点和C 点的温度分别为2T 和3T .求此循环效率.这是卡诺循环吗?解:(1)热机效率121Q Q -=η AB 等压过程 )(12P 1T T C Q -='υ 吸热)(P mo 1A B lT T C M MQ -=CD 等压过程 )(12P 2T T vC Q -='放热)(P mol22D C T T C M MQ Q -='-=)/1()/1(12B A B C D C A B D C T T T T T T T T T T Q Q --=--=根据绝热过程方程得到AD 绝热过程 γγγγ----=D D A A T p T p 11 BC 绝热过程 γγγγ----=C C B B T p T p 111又B C D DC BA T T T T p p p p ===231T T -=η(2)不是卡诺循环,因为不是工作在两个恒定的热源之间. 7-20 (1)用一卡诺循环的致冷机从7℃的热源中提取1000 J 的热量传向27℃的热源,需要多少功?从-173℃向27℃呢?(2)一可逆的卡诺机,作热机使用时,如果工作的两热源的温度差愈大,则对于作功就愈有利.当作致冷机使用时,如果两热源的温度差愈大,对于致冷是否也愈有利?为什么? 解:(1)卡诺循环的致冷机2122T T T A Q e -==静 7℃→27℃时,需作功 4.71100028028030022211=⨯-=-=Q T T T A J173-℃→27℃时,需作功 2000100010010030022212=⨯-=-=Q T T T A J(2)从上面计算可看到,当高温热源温度一定时,低温热源温度越低,温度差愈大,提取同样的热量,则所需作功也越多,对致冷是不利的.7-21 如题7-21图所示,1 mol 双原子分子理想气体,从初态K 300,L 2011==T V 经历三种不同的过程到达末态K 300,L 4022==T V . 图中1→2为等温线,1→4为绝热线,4→2为等压线,1→3为等压线,3→2为等体线.试分别沿这三种过程计算气体的熵变.题7-21图解:21→熵变等温过程 A Q d d = , V p A d d =,RT pV =⎰⎰==-21111221d 1d V V V V RT T T Q S S76.52ln ln!212===-R V V R S S J 1K -⋅321→→熵变⎰⎰+=-312312d d T QT Q S S32V 13p V p 12ln ln d d 2331T TC T T C T T C T TC S S T T T T +=+=-⎰⎰31→等压过程 31p p = 3211T V T V =1213V V T T = 23→等体过程 2233T p T p =3232p p T T = 1232p p T T =12V 12P 12ln ln p pC V V C S S +=-在21→等温过程中 2211V p V p =所以2ln ln ln ln1212V 12P 12R V VR V V C V V C S S ===-241→→熵变⎰⎰+=-412412d d T QT Q S S41p 42p p 12ln lnd 024T TC T T C TT C S S T T ==+=-⎰41→绝热过程111441144111----==γγγγV V T T V T V T γγγγ/121/141144411)()(,p pp p V V V p V p ===在21→等温过程中 2211V p V p =γγγ/112/121/14114)()()(V V p p p p V V ===γγ11241)(-=V V T T2ln ln 1ln12P 41P 12R V V C T T C S S =-==-γγ7-22 有两个相同体积的容器,分别装有1 mol 的水,初始温度分别为1T 和2T ,1T >2T ,令其进行接触,最后达到相同温度T .求熵的变化,(设水的摩尔热容为mol C ). 解:两个容器中的总熵变⎰⎰+=-TT T T lT T C T T C S S 12d d mo mol 0 212mol 21mol ln)ln (ln T T T C T T T T C =+=因为是两个相同体积的容器,故)()(1mol 2mol T T C T T C -=- 得212T T T += 21212mol 04)(lnT T T T C S S +=-7-23 把0℃的0.5kg 的冰块加热到它全部溶化成0℃的水,问:(1)水的熵变如何?(2)若热源是温度为20 ℃的庞大物体,那么热源的熵变化多大? (3)水和热源的总熵变多大?增加还是减少?(水的熔解热334=λ1g J -⋅) 解:(1)水的熵变612273103345.031=⨯⨯==∆T Q S J 1K -⋅(2)热源的熵变570293103345.032-=⨯⨯-==∆T Q S J 1K -⋅(3)总熵变4257061221=-=∆+∆=∆S S S J 1K -⋅熵增加。

第7章 热力学基础7-1在下列准静态过程中,系统放热且内能减少的过程是[ D ] A .等温膨胀. B .绝热压缩. C .等容升温. D .等压压缩.7-2 如题7-2图所示,一定量的理想气体从体积V 1膨胀到体积V 2分别经历的过程是:A →B 等压过程; A →C 等温过程; A →D 绝热过程 . 其中吸热最多的过程是[ A ] A .A →B 等压过程 B .A →C 等温过程.C .A →D 绝热过程. 题7-2图 D .A →B 和A → C 两过程吸热一样多.7-3 一定量某理想气体所经历的循环过程是:从初态(V 0 ,T 0)开始,先经绝热膨胀使其体积增大1倍,再经等容升温回复到初态温度T 0, 最后经等温过程使其体积回复为V 0 , 则气体在此循环过程中[ B ]A .对外作的净功为正值.B .对外作的净功为负值.C .内能增加了.D .从外界净吸收的热量为正值. 7-4 根据热力学第二定律,判断下列说法正确的是 [ D ] A .功可以全部转化为热量,但热量不能全部转化为功.B .热量可以从高温物体传到低温物体,但不能从低温物体传到高温物体.C .不可逆过程就是不能向相反方向进行的过程.D .一切自发过程都是不可逆的.7-5 关于可逆过程和不可逆过程有以下几种说法,正确的是[ A ] A .可逆过程一定是准静态过程. B .准静态过程一定是可逆过程. C .无摩擦过程一定是可逆过程.D .不可逆过程就是不能向相反方向进行的过程.7-6 理想气体卡诺循环过程的两条绝热线下的面积大小(题7-6图中阴影部分)分别为S 1和S 2 , 则二者的大小关系是[ B ] A .S 1 > S 2 . B .S 1 = S 2 .C .S 1 < S 2 .D .无法确定. 题7-6图 7-7 理想气体进行的下列各种过程,哪些过程可能发生[ D ] A .等容加热时,内能减少,同时压强升高 B . 等温压缩时,压强升高,同时吸热 C .等压压缩时,内能增加,同时吸热 D .绝热压缩时,压强升高,同时内能增加7-8 在题7-8图所示的三个过程中,a →c 为等温过程,则有[ B ] A .a →b 过程 ∆E <0,a →d 过程 ∆E <0. B .a →b 过程 ∆E >0,a →d 过程 ∆E <0. C .a →b 过程 ∆E <0,a →d 过程 ∆E >0.D .a →b 过程 ∆E >0,a →d 过程 ∆E >0. 题7-8图7-9 一定量的理想气体,分别进行如题7-9图所示的两个卡诺循环,若在p V -图上这两个循环过程曲线所围的面积相等,则这两个循环的[ D ] A .效率相等.B .从高温热源吸收的热量相等.C .向低温热源放出的热量相等.D .对外做的净功相等. 题7-9图7-10一定质量的某种理想气体在等压过程中对外作功为 200 J .若此种气体为单原子分子气体,则该过程中需吸热__500__ J ;若为双原子分子气体,则需吸热__700___ J 。
地球的水循环过程地球的水循环是指地球上水分在不同形态之间不断转化和迁移的过程。
这个过程是由太阳能的驱动和地球的重力所控制的,它在维持地球上的水资源平衡和生态系统稳定中起着至关重要的作用。
1. 蒸发和蒸腾地球上大部分的水都存在于海洋中,而蒸发是地球水循环的第一步。
当太阳照射到海洋、湖泊、河流和植被表面时,水分会受热而蒸发成为水蒸气。
此外,植物通过叶子表面的气孔释放水分,这个过程被称为蒸腾。
蒸发和蒸腾共同作用下,大量的水分被释放到大气中。
2. 水汽凝结当水蒸气升至高空时,遇到较低温度的空气,就会发生凝结现象。
这些凝结成小水滴或冰晶体的水汽形成云朵。
云朵可以是高层云、中层云或低层云,它们在大气中漂浮着,随着风的吹动而移动。
3. 降水当云朵中的水滴或冰晶体增大到一定程度时,它们就会变得足够重以至于无法被空气支撑,从而下落到地面上。
这个过程被称为降水。
降水可以是雨、雪、冰雹等形式,不同地区和季节的降水量和类型各不相同。
4. 地表径流和地下水补给降水后的水分有两种去向:一部分会形成地表径流,即沿着地表流动进入河流、湖泊和海洋;另一部分则渗入地下,补给地下水。
地表径流是重要的淡水资源,它为人类提供饮用水、灌溉水和工业用水等。
5. 蒸发和蒸腾再循环地表径流和地下水中的水分并不会永远停留在那里,它们会被太阳能再次加热,蒸发成为水蒸气,并通过蒸腾作用释放到大气中。
这样,循环就重新开始了。
这个过程可以持续多次,使得地球上的水资源得以再利用。
6. 影响因素地球的水循环过程受到多种因素的影响。
其中,太阳能是驱动水循环的主要能源,它提供了蒸发和蒸腾所需的热量。
地球的气候和地形也会对水循环产生重要影响,例如,热带地区由于气温高、降水多,水循环较为活跃;而沙漠地区则由于气温高、降水少,水循环相对较弱。
7. 水循环与生态系统地球的水循环对维持生态系统的平衡至关重要。
它为植物提供了所需的水分,促进了植物的生长和繁殖。
同时,水循环也影响着动物的生存和迁徙。
汽轮机工作流程汽轮机是一种将燃料的热能转化为机械能的设备。
它通过燃烧燃料产生高温高压的燃气,然后将燃气作用在叶轮上,从而驱动轴实现能量转换。
下面将详细介绍汽轮机的工作流程。
1. 燃烧过程汽轮机的工作流程始于燃烧过程。
燃料(如煤、石油、天然气等)在锅炉中燃烧,产生高温高压的燃气。
燃烧过程中,燃料与空气混合并点燃,释放的热能使燃气温度升高。
2. 进气过程经过燃烧后的燃气进入汽轮机的高压部分。
在进气过程中,燃气通过进气管道进入高压缸,压力逐渐增加。
同时,进气阀门控制进气量,以确保进入汽轮机的燃气温度和压力稳定。
3. 膨胀过程在汽轮机的高压缸中,燃气通过叶片组的作用进行膨胀,产生功。
高压缸是汽轮机的核心部件,其内部的叶片组可以将燃气的动能转化为机械能。
燃气在叶片组的作用下扩大体积,压力降低,同时对叶片组施加力,推动轴转动。
4. 排气过程经过高压缸的膨胀过程后,燃气进入汽轮机的中压缸。
在中压缸中,燃气继续膨胀,压力进一步降低。
然后,燃气进入低压缸,继续膨胀并产生功。
最终,燃气经过低压缸的膨胀过程,压力降至大气压力,排出汽轮机。
5. 冷却过程在汽轮机工作过程中,由于燃气的高温高压特性,需要对其进行冷却。
冷却过程可以通过引入冷却介质或采用内部冷却方式。
冷却的主要目的是保护汽轮机的叶片和其他关键部件不受高温燃气的损害。
6. 功率输出汽轮机通过轴将转动能量输出。
在汽轮机的转子上,有一个轴连接高压缸、中压缸和低压缸,当燃气通过叶片组的作用进行膨胀时,轴也随之转动。
轴的转动驱动发电机或其他负载设备运转,将机械能转化为电能或其他形式的能量输出。
7. 循环过程汽轮机的工作流程是一个循环过程。
在功率输出后,燃气排出汽轮机,经过烟囱排放到大气中。
然后,新的燃料继续进入燃烧室,进行燃烧过程,形成新的燃气,再次进入汽轮机进行工作。
这个循环过程不断重复,使汽轮机持续运转。
总结:汽轮机的工作流程包括燃烧过程、进气过程、膨胀过程、排气过程、冷却过程、功率输出和循环过程。
输液时在体内循环的原理
当进行静脉输液时,输入人体的液体经过以下循环过程:
1. 经外周静脉进入心脏
输液针头通过外周静脉将液体推入,经过肘静脉、腋静脉和锁骨静脉等,最终进入心脏的右心房。
2. 右心房通过三尖瓣进入右心室
液体从右心房流入右心室,三尖瓣阻止液体回流。
3. 右心室通过主动脉瓣推入肺动脉
右心室收缩,通过主动脉瓣把液体推入连接肺部的肺动脉。
4. 经肺部小循环和肺静脉回流左心
液体进入肺动脉分支,经过肺部毛细血管后汇集入肺静脉,再流入左心房。
5. 左心房通过二尖瓣进入左心室
液体从左心房流入左心室,二尖瓣防止液体回流。
6. 左心室通过主动脉瓣进入主动脉
左心室收缩把液体推入主动脉和全身动脉。
7. 进入体循环为组织供养
液体通过细小动脉分支为全身组织和器官供给营养和氧气。
8. 经静脉回流右心房
组织消耗后,液体从毛细静脉汇集到大静脉,最终全部回流到右心房。
这样,输液完成了从外周入心、肺部过滤后到全身循环的一个循环过程,为人体各部位输送营养。
这就是静脉输液在体内的流动原理。
八年级上册地理 -第7课水循环【教案】八年级上册地理 - 第7课水循环【教案】教学目标- 了解水循环的概念和过程- 掌握水蒸发、凝结、降水等关键词汇的意义和作用- 理解水循环在地球上的重要性和影响教学准备- 教材:八年级上册地理教材第7课- 幻灯片或多媒体设备- 视频或动画关于水循环的资源- 白板、笔、橡皮等教学用具教学过程1. 导入与复(5分钟)- 回顾上一堂课的内容,引导学生思考天气与气候的关系。
2. 新知引入(10分钟)- 利用幻灯片或多媒体设备展示水循环的图解,向学生简要介绍水循环的概念和过程。
- 通过讨论或提问,帮助学生初步了解水蒸发、凝结、降水等关键词汇的意义和作用。
3. 实践操作(20分钟)- 分发小组任务,让学生观察并记录周围的水循环现象,如水蒸发、降水等。
要求学生写下观察结果以及对应的关键词汇。
- 学生互相分享自己的观察结果,并讨论这些现象对日常生活和地球的重要性和影响。
4. 深化讲解(15分钟)- 加深学生对水循环的理解,解释其中涉及的科学原理和地理知识。
- 通过视频或动画等资源呈现更详细的水循环过程,帮助学生进一步认识其复杂性。
5. 拓展应用(10分钟)- 引导学生思考如何应用水循环的知识,例如在自然环境保护、水资源管理等方面的实践。
- 分组讨论并展示各组的应用方案,鼓励学生提出创新和可行的想法。
6. 总结与评价(5分钟)- 小结水循环的内容,确保学生对关键词汇和过程的理解与掌握。
- 对学生完成的观察任务和拓展应用方案进行评价和反馈。
教学延伸- 鼓励学生进一步探索水循环在各地区的差异和影响因素,并进行深入研究和报告。
- 提供更多的资源和案例,帮助学生理解和应用水循环的知识。
教学反思- 教师在教学过程中要关注学生的研究兴趣和理解程度,积极引导和鼓励学生的参与和思考。
- 教师应准备丰富的教学资源,通过多种形式和方法激发学生的研究兴趣和动力。