无菌传递窗技术方案
- 格式:doc
- 大小:931.00 KB
- 文档页数:29

一、传递窗是洁净级别不同的区域之间物料的传递通道。
二、平时传递窗的两门处于关闭状态。
三、在物品传递时,操作者先打开一扇门,将物品送入后,关门(从室外往洁净区内传递物品时还应打开紫外灯,灭菌30分钟,取样间除外)。
再打开另一扇门,将物品取出后,再关好门。
严禁两扇门同时打开。
四、取样间物品传递前,先打开紫外灯灭菌30分钟,关闭紫外灯,然后打开一扇门,将物品送入后,关门,再打开另一扇门,将物品取出后,再关好门。
严禁两扇门同时打开。
五、传递窗在操作结束后,应进行清洁工作,并定期进行消毒。
六、紫外灯的使用与更换
1、紫外灯使用一定时间后其辐射强度会有所下降,为保证消毒效果,一般累计使用时间不超过1000小时(或依据厂家使用说明书规定),到期更换紫外灯。
2、一经发现损坏或异常情况应及时报告管理人员,及时更换紫外灯。
七、使用和维护应予以记录。

洁净室传递窗标准洁净室传递窗是利用机械手臂或人工操作将物品或文件从一个洁净区域转移到另一个洁净区域的通道。
传递窗的一个重要功能是阻挡细菌和杂质的传播,确保洁净室内的空气质量和人员安全。
因此,在设计和使用洁净室传递窗时,必须遵循一些标准和规范。
1. 窗户材料洁净室传递窗通常由不锈钢制成。
这种材料的优点是易于清洁和消毒,同时具有较好的耐腐蚀性和耐高温性。
此外,不锈钢表面光滑,不会吸附细菌和微粒。
2. 设计参数洁净室传递窗的设计应满足洁净度等级和风量要求。
一般来说,传递窗工作时防护等级不低于IP65,并且能够满足所需的气流负压。
在传递窗的安装过程中,应严格遵守相关标准和规范。
窗户和洁净室通道的连接必须牢固,以确保物品或文件的传递过程中不会出现渗漏或其他问题。
3. 操作要求在使用洁净室传递窗时,必须遵守以下操作要求:- 在传递过程中,不得将手或其他物品伸入传递窗内部。
- 不得在传递过程中将文件或其他物品直接放入传递窗,必须使用专门的传递容器。
- 在传递窗使用过程中,必须保持室内环境清洁干燥,例如避免水和其他液体进入窗口。
4. 清洁和维护为了确保传递窗的良好工作状态和长期使用寿命,需要进行定期的清洁和维护。
定期清洁传递窗,可以去除堆积的灰尘、细菌和其他杂质,从而提高传递窗的洁净度和安全性。
此外,还需要定期检查传递窗的机械部件和密封圈等零部件,以确保其正常工作和性能。
如果发现传递窗有问题,应及时联系专业技术人员进行检修和维修。
总之,洁净室传递窗作为保证洁净环境和工作安全的重要设备,在设计、安装和使用过程中都要遵循一定的标准和规范。
只有这样,才能确保传递窗的良好运行和效果。

无菌检测阳性检测室传递窗设计无菌检测阳性检测室传递窗是在医疗环境中常见的设备之一,用于在严格的无菌条件下传递样本和实验室结果。
设计一个合理的传递窗可以有效地减少交叉感染的风险,提高工作效率。
以下是一种针对无菌检测阳性检测室传递窗的设计方案。
传递窗应具备良好的密封性能,以防止空气和细菌的交叉污染。
窗户的密封材料可以选择优质的硅胶密封条,确保窗户关闭时能够完全密封。
另外,传递窗的开启方式应设计为自动感应或脚踏开关,以避免操作人员直接接触窗户。
传递窗的材质应选择防菌、易清洁的材料。
常用的材料包括不锈钢、铝合金或特殊涂层玻璃等。
这些材料具有抗菌性能,可以有效地减少细菌的滋生和传播。
同时,为了方便清洁,传递窗的表面应平整,无缝隙,并且易于拆卸和安装。
传递窗的尺寸应根据实际需要进行设计。
窗户大小应能容纳常见的医用容器和文件,同时不占用过多的工作空间。
传递窗的高度宜设置在操作人员的舒适范围之内,使其能够轻松地将样本和结果传递给对方。
还需要考虑传递窗的通风和过滤系统。
通风系统可以保持传递窗内外的空气流通,减少细菌滋生的可能性。
过滤系统可以有效地过滤空气中的微粒和细菌,确保无菌环境的质量。
传递窗的通风和过滤系统应定期维护和更换,以保持其正常运行。
传递窗的安装位置和使用方式也需要合理规划。
传递窗宜设置在无菌检测阳性检测室的合适位置,以便操作人员能够轻松地使用。
同时,应提供合适的操作指南和培训,确保操作人员正确使用传递窗,并注意维护和清洁。
设计一个合理的无菌检测阳性检测室传递窗,需要考虑密封性能、材料选择、尺寸设计、通风和过滤系统等方面。
合理的设计可以减少交叉感染的风险,提高工作效率,为医疗环境中的无菌检测工作提供良好的支持。

洁净区传递窗性能确认方案一、目的和范围本方案旨在规定洁净区传递窗的性能确认方案,以确保其符合制药、生物制品等行业的洁净度要求。
本方案适用于新建和已运行的洁净区传递窗的性能确认。
二、传递窗的设计和构造1.传递窗应按照制药行业的相关规定进行设计,并符合生物制品等行业的特殊要求。
2.传递窗应采用不锈钢或其他耐用、易清洁的材料制造,结构应简单、紧凑,方便操作。
3.传递奤应配备可靠的密封措施,以防止洁净区内的空气外泄。
三、密封性能测试1.采用压力测试方法,在传递窗内外施加一定压力,检查其密封性能。
2.在温度变化的情况下,检测传递窗的密封性能是否保持稳定。
四、洁净度检测1.在传递窗的不同位置设置尘埃粒子计数器,检测洁净度是否符合规定要求。
2.定期对传递窗进行洁净度检测,以保证其符合生产工艺要求。
五、温度和湿度控制测试1.在传递窗内部设置温度和湿度传感器,检测其温度和湿度控制性能。
2.根据生产工艺要求,测试传递窗在不同温度和湿度条件下的性能表现。
六、消毒灭菌效果验证1.采用标准化的消毒灭菌方法,对传递窗进行消毒灭菌处理。
2.在消毒灭菌前后,分别取样检测微生物数量,以验证其消毒灭菌效果。
七、操作便捷性评估1.对操作人员进行培训,确保其熟悉传递窗的操作流程。
2.评估操作人员在各种情况下的操作效率,以确定传递窗的操作便捷性。
八、维护和保养要求1.制定传递窗的维护和保养规程,包括清洁、消毒、检修等方面的规定。
2.对操作人员进行培训,确保其掌握传递窗的维护和保养技能。
3.定期对传递窗进行检查和维修,确保其正常运行。
4.对损坏或老化部件进行及时更换,保证传递窗的性能稳定。
5.建立维护和保养记录,详细记录传递窗的运行状态和维护保养情况。
6.对维护和保养过程中发现的问题进行及时处理和反馈。
7.定期对维护和保养人员进行培训和考核,提高其技能水平和工作责任心。
8.建立维护和保养管理流程,明确各环节的责任和工作要求。

微生物传递窗操作规程微生物传递窗是一种为了保护实验人员和实验环境安全而设计的装置。
这种窗口可以防止微生物在实验室中传播和污染,从而保护实验人员和实验环境免受微生物的伤害。
但是,为了确保微生物传递窗的有效性,必须遵循一定的操作规程。
第一,关注清洁卫生。
微生物传递窗必须定期清洁和消毒。
在使用前,应先用70%的酒精擦拭传递窗内外部分,以杀灭可能存在的微生物。
在实验结束后,应及时清洗传递窗并消毒。
这有助于防止微生物在传递窗中生长和繁殖,从而避免污染。
第二,正确使用微生物传递窗。
在使用微生物传递窗时,操作人员必须穿戴防护设备,如实验手套和口罩。
此外,操作人员还应该注意传递窗的开启和关闭方式。
在使用微生物传递窗时,操作人员应该减少窗口的开放时间,以防止微生物从窗口中逸出。
第三,定期维护微生物传递窗。
微生物传递窗需要定期检查和维护,以确保其正常运行。
在操作过程中,如果发现窗口存在问题或漏洞,应及时修复或更换。
这有助于确保微生物传递窗的有效性和安全性。
第四,正确存储微生物。
在使用微生物传递窗时,操作人员应正确存储微生物。
微生物应存放在冷藏设备中,并且应标明其名称、存放日期和有效期限。
此外,在使用传递窗时,应注意微生物的传递方向。
传递方向应从无菌区域到有菌区域,以避免微生物的传播和污染。
第五,合理使用微生物传递窗。
在使用微生物传递窗时,操作人员应根据实验需要合理使用。
必须遵循操作规程,不得随意开启传递窗。
此外,在实验结束后,应及时关闭传递窗,以防止微生物的传播和污染。
微生物传递窗是实验室中非常重要的安全设备。
为了确保微生物传递窗的有效性和安全性,必须遵守一定的操作规程。
操作人员必须关注清洁卫生,正确使用微生物传递窗,定期维护,正确存储微生物,以及合理使用微生物传递窗。
只有这样,才能确保微生物传递窗的安全性和有效性,从而保护实验人员和实验环境的安全。

洁净传递窗的设计标准有哪些洁净传递窗是建筑物中常用的设备,用于传递洁净状态的物品或样品,以防止污染和交叉感染。
洁净传递窗的设计标准如下:1. 尺寸标准:洁净传递窗的尺寸应根据具体使用需求确定,但一般应符合国际洁净室技术标准,如ISO 14644-1。
具体尺寸要求应根据洁净室的级别、使用目的和传递物品的尺寸等综合考虑。
2. 材料标准:洁净传递窗的外壳及传递窗板材料应选择高品质不锈钢或玻璃等材料。
材料应光滑、无瑕疵、易清洁,并具有抗静电、抗腐蚀、抗污染等性能。
3. 密封标准:洁净传递窗应具有良好的密封性能,以阻止空气、灰尘和微生物等污染物进入传递窗内。
密封性能应符合相关标准要求,并通过测试验证。
4. 过渡区标准:洁净传递窗的过渡区应设计合理,能够最大限度地减少洁净室内外环境的交叉污染。
过渡区的尺寸、布局和通风方式等应根据洁净室的级别和传递物品的特性等因素进行考虑。
5. 操作标准:洁净传递窗的操作方式应简便易行,能够满足洁净室使用者的需求,并能避免误操作引起的污染。
操作方式可以采用手动或自动控制,应具有良好的可靠性和安全性。
6. 清洁标准:洁净传递窗应易于清洁和维护,以保持洁净室的洁净状态。
洁净传递窗的表面应光滑、无孔洞、无积尘,并具有抗污染和抗腐蚀的性能。
清洁标准应符合相关洁净室技术标准。
7. 环境适应标准:洁净传递窗应能适应不同环境的要求,并保持稳定的工作性能。
特别是在高湿度、高温度、高静电等特殊环境下,洁净传递窗应具有良好的抗干扰和抗腐蚀能力。
总之,洁净传递窗的设计应符合国际洁净室技术标准,并综合考虑洁净室的级别要求、传递物品的特性、操作人员的需求等因素,以确保洁净室的洁净状态和安全运行。
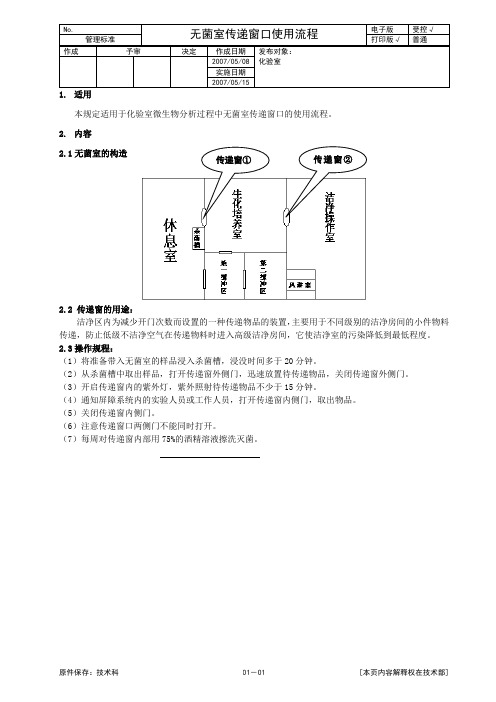
原件保存:技术科 [本页内容解释权在技术部] 01-01
本规定适用于化验室微生物分析过程中无菌室传递窗口的使用流程。
2. 内容
2.1无菌室的构造
2.2 传递窗的用途:
洁净区内为减少开门次数而设置的一种传递物品的装置,主要用于不同级别的洁净房间的小件物料传递,防止低级不洁净空气在传递物料时进入高级洁净房间,它使洁净室的污染降低到最低程度。
2.3操作规程:
(1)将准备带入无菌室的样品浸入杀菌槽,浸没时间多于20分钟。
(2)从杀菌槽中取出样品,打开传递窗外侧门,迅速放置待传递物品,关闭传递窗外侧门。
(3)开启传递窗内的紫外灯,紫外照射待传递物品不少于15分钟。
(4)通知屏障系统内的实验人员或工作人员,打开传递窗内侧门,取出物品。
(5)关闭传递窗内侧门。
(6)注意传递窗口两侧门不能同时打开。
(7)每周对传递窗内部用75%的酒精溶液擦洗灭菌。

VHP灭菌传递窗工作原理VHP(Vaporized Hydrogen Peroxide,氢氧化学气雾灭菌)灭菌传递窗是一种用于灭菌物品的装置,广泛应用于医疗机构、实验室和制药工厂等地方。
其工作原理涉及到氢氧化学气雾灭菌技术和传递窗的特殊设计。
VHP灭菌技术是一种通过将氢氧化学气雾引入密闭空间中,使其接触要灭菌的表面,通过气雾中的氢氧化学气浓度高和反应时间长来杀灭细菌,病毒和其他微生物的方法。
VHP灭菌技术具有广谱杀灭作用,能够达到更高的灭菌效果,且具有更好的杀菌深度。
1.密闭空间:VHP灭菌传递窗通过设计具有密闭性能的结构,使其内部空间与外界隔绝。
这样可以防止微生物在传递过程中的交叉感染,并确保灭菌过程中的效果。
2.氢氧化学气雾引入:在密闭空间中,通过特定的装置将氢氧化学气雾引入窗体内部。
这种气雾通常是由氢氧化学生成器产生的,通过加热液态氢氧化学制剂,使其蒸发成为气态。
气雾通过传递窗装置的设计,弥散到整个空间,与目标表面接触。
3.氢氧化学气雾杀菌:氢氧化学气雾接触到灭菌目标表面时,开始对微生物进行杀菌。
氢氧化学气雾主要通过氧化和酸化作用杀灭微生物。
其中氢氧化氢(H2O2)分解为氧气和水,氧气能够增加微生物细胞膜的通透性,并破坏微生物细胞内部的结构和功能。
同时,酸化作用会破坏微生物细胞内部的酶系系统和DNA结构,进一步杀灭微生物。
4.灭菌过程控制:VHP灭菌传递窗通常配备了专业的控制系统,用于监测和控制氢氧化学气雾浓度、温度和湿度等参数。
这些参数的控制能够保证灭菌过程的稳定性和可靠性,并确保灭菌效果的一致性。
5.氢氧化学气雾排除:灭菌后,VHP灭菌传递窗需要进行氢氧化学气雾的排除,以减少残留在窗体内部的气体对物品的影响。
通常,通过通风和加热等方法,将窗体内部的气体排除,以确保物品的安全性和纯度。
总结来说,VHP灭菌传递窗通过引入氢氧化学气雾,在密闭空间中杀灭微生物,实现对物品的灭菌效果。
通过专业控制系统的监测和控制,确保灭菌过程控制的稳定性和一致性。

VHP灭菌传递窗⼯作原理
⼯作原理介绍
VHP灭菌传递窗灭菌循环开始前的渗漏测试----将灭菌舱内所有阀门关闭,通过真空压⼒表观测压⼒上升情况,如果压⼒上升速率符合程序的规定,则认为系统密闭,可以开始预处理
1.先开启真空泵对灭菌舱抽真空,除去⽔分和湿⽓。
2.打开通风阀,冲⼊⼲燥,⽆菌空⽓。
3.当压⼒达到⼤⽓压时,再次开启真空泵,进⼀步⼲燥
5.将过氧化氢注⼊舱内,由于预处理期舱内为⾼真空,使过氧化氢得到充分扩散,⼤⼤提⾼灭菌效果。
6.灭菌结束后,真空泵开启,使舱内⽓压下降到1Torr
7.打开通风阀,向舱内冲⼊⼲燥,⽆菌空⽓,当舱内压⼒接近常压时,真空泵开始⼯作,将舱内空⽓抽出,这些残留⽓体在催化器作⽤下转化成对环境⽆害的氧⽓和⽔。
8.通风期结束,打开通风阀,新⼀轮的⽆菌空⽓重新注⼊灭菌舱内
使压⼒恢复正常,⼀个灭菌循环结束。

传递窗验证方案方案起草人:年月日方案审核人:年月日方案批准人:年月日00目录1.综述2.验证的目的3.职责与成员3.1验证委员会职责3.2质量保证部职责3.3成员3.4验证实施的时间进度4.验证内容4.1安装确认4.1.1仪器基本信息4.1.2设备档案4.1.3安装条件确认4.1.4安装确认4.2运行确认4.2.1互锁确认4.2.3辐照强度测定4.2.4紫外强度分布4.3性能确认4.4偏差处理5.拟订日常监测程序及再验证周期6.验证结果评定与结论7.附件001.综述:传递窗是一种洁净室的辅助设备,主要用于洁净区与洁净区之间,洁净区与非洁净区之间小件物品的传递,以减少洁净室的开门次数,使洁净室的污染降低到最低程度。
传递窗内安装有紫外灯,物品经紫外线照射消毒后进入洁净区。
紫外线是一种电磁辐射,波长190~350nm,其中以253.7nm的杀菌力最强,可使DNA链上相邻嘧啶碱基之间形成二聚体,抑制DNA的复制,导致突变或死亡。
紫外线的杀菌力与紫外线强度、照射时间、温度和湿度等因素有关。
2.验证的目的:通过验证确认层流洁净工作台是否能够达到设备性能指标,符合检验产品需求。
3.职责与成员3.1验证委员会职责3.1.1负责验证方案的审批3.1.2负责验证的协调工作,以保证本验证方案规定项目的顺利实施3.1.3负责验证数据及结果的审核3.1.4负责验证报告的审批3.1.5负责发放验证证书3.1.6负责再验证周期的确认3.2质量保证部职责3.2.1负责验证用样品及其它消耗性备品的准备。
3.2.2负责备品、备件的保存。
3.2.3负责设备仪器的操作。
3.2.4负责记录各种测试结果。
3.2.5负责拟订再验证项目及周期。
3.2.6负责收集各项验证、试验记录,起草验证报告,报验证委员会。
3.3成员003.4验证实施的时间进度4.验证内容4.1.1确认设备的安装是否符合原设计的条件。
4.1安装确认4.2.1互锁确认:两侧门设有互锁装置,确保两侧门不能同时处于开启状态。

传递窗说明(带吹淋)(总17页)--本页仅作为文档封面,使用时请直接删除即可----内页可以根据需求调整合适字体及大小--传递窗PASS BOX说明书苏州亚琛洁净技术有限公司一.设备常识:1.设备用途:传递窗是一种洁净室的辅助设备,其功能是作为洁净室内外物品传递之缓冲(主要用于洁净区与洁净区之间、洁净区与非洁净区之间小件物品的传递),可防止在物品传递时由于门的开启而破坏了洁净室的气流和室压,更可减少作业人员进出的次数而防止外部尘埃的进入,该设备双门有连锁控制,以达到防止交叉污染2.设备类型:传递窗根据使用条件的不同,又可区分为几种:(1).净化级别:普通型:主要用于洁净室与洁净室之间洁净型:是洁净室与非洁净区之间小件物品的传递,以减少洁净室的开门次数,把对洁净室或洁净区的污染程度降到最低。
(2).材质:钢板烤漆:箱体采用普通钢板折弯焊接成型,表面和内部作烤漆处理不锈钢:内外部不锈钢,平整光洁,内部带圆弧过渡,美观大方(3).控制方式机械联锁:保证两侧门不能同时打开,用于普通洁净场合电子联锁:内置控制面板和电磁锁,保证两侧不能同时打开,减少交叉污染3.设备特点:1. 传递窗采用不锈钢板制作,平整光洁,内置圆弧过渡,减少死角,美观大方2. 两侧门带有机械互锁或电子互锁装置使用两门不能同时打开,有效阻止交叉污染3. 传递窗上装有双层钢化玻璃视窗,便于观察同时有效保证了箱体内部的洁净度4.窗门装有密封条,确保气密性5. 增设紫外线杀菌灯和照明灯6. 增设强力磁铁,保证设备在断电等外部因素干扰下,两侧门不打开7. 控制面板带有呼叫功能按钮键,可以知道两侧情况8. 洁净传递窗内置免维护单相220V离心风机低噪音,工作状态噪音低于65分贝9.采用雅洁专用之天地磨芯铰链,门页开启安全可靠,无噪音10. 洁净传递窗装备无隔板HEPA高效过滤器,对微米的尘埃粒子的过滤效率为%11.安装简易,洁净室兼容性佳同时可根据用户要求制作各种非标准传递窗4.设备使用环境和条件:3.安全事项:(1) .基本安全事项:※本设备是室内使用型的,请不要在室外使用。

无菌车间通常会配备一个或多个传递窗用以传递各相邻房间间物品的传递,无菌车间传递窗的使用方法如下。
静止状态下传递窗的两扇门处于关闭状态,有电气照明系统的传递窗,必须先插上电源插头,接通220V/50Hz电源。
打开传递窗两侧门,快速置放待传送物件,用0.5%次氯酸钠溶液喷雾消毒传递窗,关掉传递窗两侧门。
打开传递窗内的紫外线杀菌灯,紫外光直射待传送物件不少于15分钟。
通告天然屏障系统软件内的试验工作人员或工作员,开启传递窗里侧门,取下物件。
关掉传递窗里侧门。
在使用无菌车间传递窗的时候,也是有一些使用注意事项的。
如传递窗一侧的门打开,另一侧门随即自动锁紧,所以在传递物品时,首先打开传递窗的门,将所需传递的物品放入传递窗内后,随即将传递窗的门关好,这时传递窗另一侧的门才能打开,实现物品的传递。
取物品的人员将物品取走后,也应立即将传递窗的门关好,以免影响下一次物品的传递。
如果传递窗一侧的门没有关好,强行拉开传递窗另一侧的门会导致门锁损坏,所以在使用时务必及时关好门。
常常查验紫外线杀菌灯的工作情况,按时拆换紫外灯管。
传递窗内不可以储放一切原材料或脏物。
以上就是关于无菌车间传递窗怎么使用的简单介绍,传递窗作为一种配套设备,是净化车间不可或缺的存在,起着很重要的作用,只有掌握正确的使用方法,才能更好地发挥它的传递作用,有效地避免交叉污染,提高工作效率。
当然了,找家靠谱专业的净化工程公司将这种车间装修的符合标准和要求,才能确保整个生产车间发发挥良好的作用。


洁净车间传递窗标准操作规程
目的:阐述洁净车间传递窗的标准操作程序,确保其操作步骤正确、规范化。
范围:传递窗的操作
职责:操作人员应按本规程正确操作,QA人员、车间技术管理员对本规程的实施情况进行检查、监督。
规程:
1 检查传递窗是否清洁干净,是否联锁完好;
2 打开传递窗的一扇门,将物料放入其中,关好门;
3 从另一侧打开另一扇门,将物料取出,关好门;
4 操作中注意事项:
4.1 一侧门已打开时,不能强行打开另一侧门;
4.2 门不能长期打开,放入或取出物料后须立即关好门;
4.3 爱护传递窗,防止损坏其破璃;如联锁损坏失灵,请机修人员修复后方可使用;
4.4 注意传递窗的清洁卫生,如在操作前或使用过程中发现受污,必须按规定擦洗干净;下班后按传递窗相关的清洁消毒规程对传递窗进行清洁和消毒。
5 培训要求:由生产部、生产车间对洁净车间传递窗操作工进行培训。

负压传递窗参数负压传递窗,也称为无菌传递窗或干式传递窗,是一种常用于生物制品制备和微生物实验室中的设备,它能够确保实验室外环境和实验室内环境之间的无菌隔离。
许多实验室需要使用高效无菌传递系统,以确保操作过程的安全性和有效性,并确保实验的可重复性。
负压传递窗的设备技术可以为实验室提供高效实验环境,本文将详细介绍负压传递窗的参数。
1. 操作类型参数负压传递窗可根据其操作类型分为多种类型,例如手动操作型、电子控制操作型和自动操作型等。
具体操作流程也会因操作类型的不同而差异,因此,实验室需要根据实验需求和安全要求选择相应类型的负压传递窗。
2. 光源参数3. 净化级别参数净化级别是评估负压传递窗过滤效率等级的一个重要参数,影响着实验的可靠性和安全性。
常见的净化级别参数包括高效率、超高效率和细菌滤过等级。
正确选择净化级别是确保实验室生产过程的关键步骤。
4. 孔径大小参数负压传递窗的孔径大小直接关系到其实验的操作范围。
从小型微生物生长罐到大型生物反应器,不同尺寸的孔和大小的传递窗可以应用于不同大小的实验操作。
因此,正确定义传递窗的孔径大小是确定其应用的重要条件。
5. 压力参数压力参数是控制负压传递窗中空气流速和流量大小的因素。
一个好的负压传递窗可以产生稳定的负压环境,确保实验室内的安全和卫生。
正确定义压力参数也是保证负压传递窗操作有效性的关键步骤。
6. 外观设计参数负压传递窗的外观设计是考虑设计美观、操作舒适和实验室功能性之间平衡的结果。
高端的设计可以满足实验室外观的整洁和现代化的要求,使得实验室从众多实验室中脱颖而出。
外观设计参数还包括不锈钢外壳等参数。
7. 控制系统参数控制系统包括各种操作按钮、指示灯、警告装置等设备,它们在一个负压传递窗的操作中至关重要。
正确的控制系统参数可以确保操作者能够准确地了解实验室中的操作状况,保证实验工艺流程的顺利进行。
8. 特殊附件参数额外的设备如空气净化器、风管、前房和后房等特殊附件,使得负压传递窗的应用更加便利和安全,它们可以进一步提高实验室环境和实验操作的安全性和可靠性。

传递窗的制作要求及配置
传递窗作为洁净室的一种辅助设备,主要用于洁净区与洁净区、非洁净区与洁净区之间的小件物品的传递,以减少洁净室的开门次数,最大限度的降低洁净区的污染,广泛应用于微细科技、生物实验室、制药厂、医院、食品加工业、LCD、电子厂等等一切需要空气净化的场所。
一、传递窗的制作要求及配置
传递窗主要采用不锈钢板制作,制作工艺要求平整光洁。
传递窗一般采用双门结构,两门互为连锁,每次只能打开一扇门,用于阻止交叉污染。
为了满足不同类型物品同时传递的需求,市场上还出现了多层传递窗、多格传递窗等。
为了降低物品传递过程中的的污染风险,传递窗内可配置紫外线杀菌灯、空气自净系统、灭菌器等。
为了方便长距离传递,传递窗内还可配置无动力滚筒。
为了满足使用过程中的管理需要,传递窗还可配置压差表、计时器、微电脑记录控制装置等。
二、传递窗的分类
1、按互锁形式可分:电子连锁传递窗和机械连锁传递窗;
2、按消毒、灭菌方式可分:消毒传递窗(如紫外线消毒传递窗)、灭菌传递窗(如过氧乙酸灭菌传递窗);
3、按空间净化方式可分:普通传递窗、风淋式传递窗、层流式传递窗等。

零界净化传递窗说明书传递窗是洁净工作室和洁净厂房的配套设备,能起到气闸作用,阻止净化室间的空气对流。
一. 工作原理和使用传递窗两扇门由联锁控制,使传递窗的两扇门不能同时打开,使净化室间的气流不能对流。
二. 结构特点1.传递窗箱体采用板金折弯一体经焊接处理成形。
2.本机材质:□全不锈钢□外钢板烤漆内不锈钢□全钢板烤漆内底不锈钢3.规格:外形尺寸:W *D *H工作区尺寸:W *D *H三. 技术参数1.联锁功能:一门开另一门打不开。
联锁方式:□机械联锁□电子联锁□无2.附加功能:□无□带吹淋功能Ο过滤器规格:___________Ο风机规格:__________□带压差表功能(可显示过滤器压差,检测过滤器)压差表规格:_________Pa□内部圆弧设计□紫外杀菌功能(按紫外灯开关可开启或关闭紫外灯)规格:____*______W□照明功能规格:____*______W□对讲功能□蜂鸣提示功能□消静电功能(离子棒规格:_____________)3.输入电源:□无□有_____V四. 安装使用1.对于新安装的传递窗,使用前应对工作区作清洁处理。
2.当物品需被运入洁净室时,拉开外侧门进入传递窗后,关闭门,内侧门方可开启;物品运离传递窗后,内侧门关闭。
反之,当需要离开洁净室时,也只要拉开内侧门进入传递窗,关闭门,外侧门方可打开,物品运离传递窗后,关闭外侧门。
警告:l 有紫外杀菌功能的请勿用眼睛直接看紫外灯,避免伤害眼睛。
l 请勿用有腐蚀性的介质接触或擦拭箱体,以免腐蚀表面。
五.控制部分(见附件)六、设置步骤1.按电源键,电源接通,时间窗口显示“0000”,此时电源指示灯为红色,解锁指示灯为绿色,表示此传递窗的两门是关闭状态;若解锁指示灯为红色,则说明两门中有门开着,并报警提示。
2.在待机状态下对开门延时、杀菌时间、吹淋时间进行设置,具体步骤如:l 同时按照明键和解锁键,解锁灯闪亮,进入开门延时时间设置状态,从5-100秒可调l 同时按照明键和吹淋键,红灯闪亮,进入吹淋时间设置状态,从20-9999 秒可调l 同时按照明键和杀菌键,红灯闪亮,进入杀菌时间设置状态,从20-9999,调,3.在设置状态,按风淋键,则对所要设置的时间,进行减操作,按住不放则连减。
Wenzhou Weike Biology Experiment Equipments CO.,LTD过氧化氢传递窗技术方案用户单位:安徽智飞龙科马生物药业有限公司设计单位:温州维科生物实验设备有限公司结构示意图(注:产品外观参考图,不代表实物)Wenzhou Weike Biology Experiment Equipments CO.,LTD1.背景概述随着SFDA发布的2010版GMP附录1无菌药品第六十条中指出:“无菌生产所用的包装材料、容器、设备和任何其它物品都应灭菌,并通过双扉灭菌柜进入无菌生产区,或以其它方式进入无菌生产区,但不得引入污染”。
提高了洁净区与洁净区、非洁净区与洁净区之间物品传递的要求,既最大限度地降低微粒和微生物污染的风险,最大限度地降低洁净区的污染和交叉污染。
我公司自主研发的过氧化氢传递窗,通过集成的汽化过氧化氢灭菌对传递窗内的所有暴露表面进行灭菌,取代传统紫外消毒的方法,使用该方法灭菌更彻底,能达到6-log的杀灭率。
传递窗自带的高效过滤器层流保护,当打开双斐门时形成气闸,防止交叉污染。
过氧化氢传递窗在欧美发达国家已成熟应用,VHP对嗜热脂肪芽孢杆菌(MESA LABS /ATCC7953)达到6-log的杀灭率。
汽化过氧化氢灭菌低温、常压,适用于低温灭菌的产品。
汽化过氧化氢具有良好的物料兼容性,易分解,无有害残留,最终分解为水和氧气。
2.范围本设计方案仅适安徽智飞龙科马药业有限公司的无菌传递窗。
本设计方案是根据安徽智飞龙科马药业有限公司的标准,由温州维科生物实验设备有限公司起草。
3.机械外形图说明:3.1 设备构成汽化过氧化氢灭菌传递窗一台:3.2机械外形图如下图(初步设计,最终通过双方商议决定最终尺寸):Wenzhou Weike Biology Experiment Equipments CO.,LTDWenzhou Weike Biology Experiment Equipments CO.,LTDWenzhou Weike Biology Experiment Equipments CO.,LTDWenzhou Weike Biology Experiment Equipments CO.,LTD3.3. 技术参数项目参数备注金属材料304/316L不锈钢/非金属材料聚四氟乙烯(PTFE)、硅胶、钢化玻璃/密封圈材质为硅胶/电源220V/50Hz / 总功率(W) ≤2500W /过氧化氢消耗量/批次≤100ml/批次/洁净压缩空气/批次≤1m3/批次充气密封用灭菌周期≤100min /残留浓度≤1ppm /汽化温度≤100℃/除湿湿度30%-40%RH /灭菌剂30%过氧化氢溶液分析纯腔内洁净度A级/高效过滤器H14 过滤效率99.995%杀灭率SAL≤10-6嗜热脂肪芽胞杆菌压差分辨率0.1pa /湿度分辨率0.1RH% /温度分辨率0.1℃/小时泄漏率Q/V≤0.5% /3.4工艺描述过氧化氢传递窗用于无菌物料由C/D级洁净区向A/B级洁净区传递时,去除物品或容器表面的生物污染。
共分三个步骤:Wenzhou Weike Biology Experiment Equipments CO.,LTD步骤1:物品或容器在C/D级区域放到传递窗内(放置时物品之间留有间隙,保证物品或容器最大限度的暴露在空气中,不留灭菌死角),关闭窗门后进行下一步。
步骤2:关好窗门后接通电源,开启仪器进行灭菌,可选用手动和自动运行程序两种模式,手动模式下分为除湿、调节、灭菌、排残、通风、保压六个步骤,其中汽化温度设定为85℃左右,调节周期和灭菌周期可根据实际情况进行设定,排残时间或通风时间可设置,调节间歇和灭菌间歇设置可设置,保压压差设定范围10pa-60pa。
在灭菌过程中,传递窗内的过氧化氢浓度传感器可实时监控窗内过氧化氢浓度。
步骤3:灭菌结束后,打开A/B级洁净区的传递门,从传递窗内取出被灭物品。
4.产品描述4.1产品基本配置描述过氧化氢灭菌传递窗(集成式)原理图如下图所示(详细版本可参考附近灭菌原理图):Wenzhou Weike Biology Experiment Equipments CO.,LTD4.1.1 灭菌条件1)灭菌前,环境温度保持20-30℃,并且舱内外温差不宜过大。
2)被灭物品或容器表面应干燥。
3)被灭物品或容器应为硬表面。
4)被灭物品或容器要最大限度的暴露在空气中,不留灭菌死角。
4.1.2灭菌流程汽化过氧化氢灭菌器的工作循环分四个阶段,形成除湿、灭菌条件、灭菌和排残通风换气等阶段。
图1 汽化过氧化氢无菌传递窗(集成式)的工作循环原理1)除湿阶段,将窗内湿度降低到过氧化氢灭菌的最佳湿度。
2)调节阶段,即形成灭菌条件阶段。
3)灭菌阶段,使过氧化氢蒸汽达到有效灭菌浓度并维持一定时间。
4)通风阶段,使用自循环钯触媒分解剂对舱内进行排残,同时可开启通风系统将过氧化氢蒸汽排到大气外。
4.1.3现场安装安装方式及尺寸如下图所示:过氧化氢灭菌传递窗直接从低级别区域取风。
图1俯视图密闭舱体除湿H 2O 2灭菌过滤通风层流保持生产操作 分解H 2O 2空气置换Wenzhou Weike Biology Experiment Equipments CO.,LTD图2 正视图4.1.4通风及空气过滤系统1.无菌传递窗采用垂直层流进出风模式2.通过PLC控制单元控制无菌传递窗的进出风量,在设定的舱内压差参数下,无菌传递窗可自动调节进出风量,无需人工干预。
3.进风系统:直接室内取风,先通过初效过滤棉进行初步过滤,再通过高效过滤器进入无菌传递窗;HEPA选用Camfil FARR, H14级(过滤效率≥99.995%);HEPA安装箱带有PAO/DOP检测口;HEPA前后端带有美国Dwyer的压差表,便于用户观察HEPA是否堵住。
采用德国EBM风机,最大风量为1150m3/h。
4.西门子PLC控制系统:设置三级密码;分手动运行和自动运行两种模式;失压、双门互锁报警功能USB接口数据导出,存储;运行关键参数实时显示;关键参数打印功能。
5.无菌传递窗主要部件的材质窗体外部材质采用304不锈钢;传递窗内部为圆弧角结构。
6.无菌传递窗主要装置1)集成VHP无菌传递窗正面装有显示屏可在线监测内外压差,传递窗设有急停开关,防止有紧急情况发生时可立即断开电源,蜂鸣器报警(当低压超限值时会报警)。
Wenzhou Weike Biology Experiment Equipments CO.,LTD2)传递窗设置有电源接口和电源手动开关、USB接口,电源接口设置有旋转卡口可固定电源,不易脱落。
3)预留PAO检测口,方便使用方对HEPA Filter进行完整性检测,设有PAO 发烟口和上游浓度检测口,检测方便。
4)传递窗采用双门设计,使用压缩空气充气密封,气动互锁,双门不能同时打开为传递窗内A级环境的保持提供了保障。
5)H14级HEPA Filter 对尘埃粒子具有很好的阻滞作用,为舱内提供洁净度为A级的洁净环境。
6)汽化过氧化氢通过H2O2进气口进入传递窗,对传递窗内物品表面进行灭菌。
灭菌结束传递窗内H2O2通过回气口排出传递窗,经过排残系统,钯触媒催化分解为H2O和O2,H2O2彻底分解,分解物无污染,无环境安全隐患。
7.仪器仪表采用北京久纯建传感器;采用美国西特微差压传感器;采用美国Dwyer的压差表。
4.2 相关参数描述(1)灭菌:选用SGM嗜热脂肪芽孢杆菌(ATCC7953)为挑战菌,对嗜热脂肪芽孢杆菌达到6-log杀灭率。
(2)浓度:过氧化氢蒸汽浓度达到有效灭菌浓度,并持续30~60min。
(3)排残:通风可将过氧化氢蒸汽通过钯触媒分解剂,将其浓度降至1PPM以下。
(4)洁净度:灭菌后,尘埃粒子,浮游菌,沉降菌测试均符合静态A级标准。
4.3 安全(1)舱体正面有设置急停开关;(2)设备设有接地装置;(3)电源或动力故障时设备立即停止运行,保护操作者;设备本身以及产品恢复供电时,重新开启动力必须要求人员操作。
Wenzhou Weike Biology Experiment Equipments CO.,LTD(4)设备可通过密闭性确认,其泄漏率≤0.5%/h,在灭菌过程中防止气体过氧化氢泄露,确保操作人员的安全。
5.验证5.1验证文件参考文件1)中华人民共和国《药品生产质量管理规范》;2)中华人民共和国国家标准《制药机械符合药品生产质量管理规范的通则》(JB20067-2005);3)USP<1208>Sterility Testing-Validation of Isolator System4)PIC/S“RECOMMERNDATION: ISOLATORS USED FOR ASEPTIC PROCESSING AND STERILITY TESTING”5)PDA TR34“Design and Validation of Isolator Systems for the Manufacturing and Testing of Health Care Products”6) GB 5226.1 机械电气安全机械电气设备第1部分:通用技术条件;7)《中华人民共和国药典》2010年版附录8)美国药典35版(USP 35)5.2验证内容供应商负责提供3Q验证报告文件(IQ/OQ/PQ);供应商提供IQ/OQ报告;供应商协助用户完成PQ报告。
5.3验证目录目录一、前言 ........................................................................................................................................二、目录 ........................................................................................................................................三、确认内容 ......................................................................................................................................第一部分:设计确认 ....................................................................................................................1、文件编制、审核与批准....................................................................................................2、文件修改记录 ..................................................................................................................3、验证小组人员登记表 .......................................................................................................4、目的.................................................................................................................................Wenzhou Weike Biology Experiment Equipments CO.,LTD5、基本情况 .........................................................................................................................6、执行标准和规范 ..............................................................................................................7、设计确认 .........................................................................................................................7.1 生产工艺确认 .............................................................................................................7.2 厂房设施及公用系统、电气自控和清洗消毒要求确认 ...............................................7.3 设计确认结论 ............................................................................................................. 第二部分:安装确认 ....................................................................................................................1、文件编制、审核与批准....................................................................................................2、文件修改记录 ..................................................................................................................3、验证小组人员登记表 .......................................................................................................4、目的.................................................................................................................................5、基本情况 .........................................................................................................................6、执行标准和规范 ..............................................................................................................7、安装确认 .........................................................................................................................7.1 随机文件的确认..........................................................................................................7.2 公共介质确认 .............................................................................................................7.3 安装位置和空间满足操作、在线清洗和维修确认.......................................................7.4 电气控制系统确认......................................................................................................7.5 主要机械零件和结构完整性 .......................................................................................7.6 送回风气流流向确认 ..................................................................................................7.7 安装确认结论 ............................................................................................................. 第三部分:运行确认 ....................................................................................................................1、文件编制、审核与批准....................................................................................................2、文件修改记录 ..................................................................................................................3、验证小组人员登记表 .......................................................................................................4、目的.................................................................................................................................5、基本情况 .........................................................................................................................6、执行标准和规范 ..............................................................................................................7、运行确认 .........................................................................................................................7.1 运行确认索引 .............................................................................................................7.2 控制有效性确认..........................................................................................................7.3 报警功能确认 .............................................................................................................7.4 高效过滤器完整性确认...............................................................................................7.5 密闭性确认.................................................................................................................7.6 风速确认.....................................................................................................................7.7气流流型确认 ..............................................................................................................7.8噪音确认 .....................................................................................................................7.9运行确认结论 .............................................................................................................. 第四部分:性能确认 ....................................................................................................................1、文件编制、审核与批准....................................................................................................Wenzhou Weike Biology Experiment Equipments CO.,LTD2、文件修改记录 ..................................................................................................................3、验证小组人员登记表 .......................................................................................................4、目的.................................................................................................................................5、基本情况 .........................................................................................................................6、执行标准和规范 ..............................................................................................................7、性能确认 .........................................................................................................................7.1 悬浮粒子确认 .............................................................................................................7.2 沉降菌确认.................................................................................................................7.3 浮游菌确认.................................................................................................................7.4清洁确认 .....................................................................................................................7.5调节及灭菌阶段过氧化氢浓度分布性确认 ..................................................................7.6挑战性试验确认...........................................................................................................7.7过氧化氢排残能力确认................................................................................................7.8性能确认结论 ..............................................................................................................四、确认结论 ...............................................................................................................................Wenzhou Weike Biology Experiment Equipments CO.,LTD配置清单主要部件名称型号品牌产地钣金304不锈钢中集无锡机架304不锈钢中集无锡内舱316L不锈钢中集无锡电源开关/ 施耐德法国急停开关/ 施耐德法国蜂鸣器HRBPS52CR1D4 凯昆韩国PLC Cpu226CN 西门子德国触摸液晶屏SMART700 西门子德国模拟采集模块EM235-CN 西门子德国模拟输出模块EM231-CN、EM222-CN 西门子德国针式打印机RONDA 荣达北京压差表0-500Pa DWYER 美国压力表0-0.6MPa 红旗浙江透明视窗钢化玻璃同昌浙江高压风机EHS-129 升鸿台湾离心风机G2E140 EBM 德国隔离型变压器NDK(BK)-150 正泰浙江微差压传感器SETRA 268 西特美国温湿度传感器WLHT-121S-OW2-L 兴卧龙北京接触器LC1E25 施耐德法国变频器ATV12H075M2 施耐德法国继电器RXM2L 施耐德法国高效过滤器415*415*90康斐尔瑞典高效过滤器305*305*90康斐尔瑞典气动蝶阀VT50D/VT65D 纬途无锡Wenzhou Weike Biology Experiment Equipments CO.,LTDPTC加热片Φ42*10 蜂窝电子广东钯触媒分解剂Φ(2-5)mm 沸石上海电磁阀4V100系列亚德客台湾调压过滤器GFR20系列亚德客台湾流体控制阀2V系列亚德客台湾铂电阻YL-01 钰莱上海单相三节滤波器SH710-20 上恒电子上海易耗品及备品备件清单名称品牌型号/规格每次/每天用量供应商高效过滤器康斐尔415*415*90mm/ 康斐尔过滤设备(昆山)有限公司过氧化氢溶液南京化学分析纯30% <500ml 南京化学试剂有限公司干燥剂(硅胶)上海分子筛Φ(2-6)mm 1kg或1.2升上海沸石分子筛有限公司针式打印纸荣达2卷/ 杭州星辰单片机电子有限公司Wenzhou Weike Biology Experiment Equipments CO.,LTD装箱单序号名称型号数量装箱确认开箱确认1 过氧化氢传递窗ZW-TWV025 1台2 主机电源线16A 1根3 U盘1G 1个4 气管2m 1根5 针式打印纸/ 2卷6 过氧化氢储液瓶500ml 1个7 漏斗塑料1个8 干燥剂2-6mm 6Kg9 说明书/ 1份10 装箱单/ 1份11 合格证/ 1份12 产品验收单/ 1份13 验证报告/ 1份Wenzhou Weike Biology Experiment Equipments CO.,LTD 大设备部分客户名单序号采购单位名称项目名称规格型号采购数量采购年限(台)1 安徽中淮生物科技有限公司无菌检验隔离器ZW-SV1800A 1 20112 兰州大得利制药有限公司过氧化氢灭菌器ZW-HP020 1 20113 海口奇力制药有限公司过氧化氢灭菌器ZW-HP050 1 2011 无菌传递舱ZW-C2C012 22013 汽化过氧化氢灭菌器ZW-HP020 24 海南中玉药业有限公司过氧化氢灭菌器ZW-HP020 1 20125 成都华神生物制药有限公司无菌检验隔离器ZW-HTV1400A 2 2011 移动无菌隔离器ZW-JG00201 1 2011 过氧化氢灭菌器ZW-HP020 2 2011 移动层流车定制 1 20116 石药集团中诺药业有限公司分离式无菌传递舱ZW-C2C600 7 2011过氧化氢灭菌器ZW-HP020 1 2011 7 湖南天圣药业有限公司分离式无菌传递舱ZW-C2C900 2 2012过氧化氢灭菌器ZW-HP020 2 2012 8 峨眉山通惠药业有限公司过氧化氢灭菌器ZW-HP020 1 20129 哈高科白天鹅药业集团有限公司无菌检验隔离器ZW-SV1800A 1 201210 哈药集团三精制药有限公司无菌检验隔离器ZW-SV1800A 1 2012 12 沈阳国药一心药业有限公司无菌检验隔离器ZW-SV1800A 1 201213 山东罗欣药业有限公司集成式无菌传递舱ZW-C2CV-16 1 2012 分离式无菌传递舱ZW-C2C-16 1 2012 过氧化氢灭菌器ZW-HP020 2 2012Wenzhou Weike Biology Experiment Equipments CO.,LTD14 重庆莱美药业股份有限公司集成式无菌传递舱ZW-C2CV-08 2 2012过氧化氢灭菌器ZW-HP020 1 201215 哈药集团制药总厂集成式无菌传递舱ZW-C2CV-24 11 201216 海南灵康药业集团有限公司集成式无菌传递舱ZW-C2C-24 3 201217 湖南湘药制药有限公司过氧化氢灭菌器ZW-HP020 1 201218 广东华润顺峰药业有限公司无菌传递舱(含小车)ZW-C2C-18 1 2012 VHP灭菌器ZW-HP020 1 2012 集成无菌传递舱ZW-C2CV-8 1 201219 开封明仁药业有限公司过氧化氢灭菌器ZW-HP020 1 201220 上海瑞邦生物材料有限公司过氧化氢灭菌器ZW-HP020 1 201221 海南葫芦娃制药有限公司集成无菌传递窗ZW-TW020 2 201222 哈尔滨莱博通药业有限公司集成无菌传递窗ZW-TW020 1 201223 河北圣大雪成制药有限公司无菌隔离器ZW-SV1860 1 201224 湖北华世通潜龙药业有限公司无菌隔离器ZW-SV1860 3 201225 山东鲁抗药业有限公司过氧化氢灭菌器ZW-HP020 1 201226 石家庄以岭药业股份有限公司集成无菌传递舱ZW-C2CV-8 1 201228 哈药集团制药总厂集成无菌传递舱ZW-C2CV-12 3 201329 四川方向药业有限公司集成无菌传递舱ZW-C2CV-12 4 201330 天津赛诺制药公司集成无菌传递舱ZW-C2CV-8 2 201332 桂林华诺威基因药业公司VHP传递窗ZW-TW015 1 201333 福建省山河药业有限公司无菌隔离器硬舱体内腔尺寸 1 201334 江苏汉斯通药业有限公司过氧化氢灭菌器ZW-HP020 2 201335 西安安健药业有限公司无菌隔离器ZW-SV186012013 无菌隔离器ZW-SV12001Wenzhou Weike Biology Experiment Equipments CO.,LTD36 海南全星制药有限公司集成无菌传递窗ZW-TW0302201337 湘北威尔曼制药股份有限公司VHP灭菌传递舱ZW-C2C0751201338 成都泰及康医疗科技有限公司无菌检验隔离器ZW-SV1860A1201339 重庆迪康长江制药有限公司无菌传递窗ZW-TW00512013 无菌传递窗ZW-TW0081无菌软隔离舱ZW-SV2400140 安徽省先锋制药有限公司VHP灭菌传递舱ZW-C2C-081201341 山东罗欣药业股份有限公司过氧化氢传递窗合体1201342 太极集团西南药业股份有限公司VHP无菌传递舱ZW-C2C0502201343 海南通用康力制药有限公司VHP灭菌传递舱ZW-C2C0122201344 贵州瑞和药业有限公司龙里药厂VHP传递窗ZW-TW0201201345 苏州洁诺净化科技有限公司无菌传递窗ZW-TW0202201346 哈尔滨誉衡药业股份有限公司汽化过氧化氢灭菌器ZW-HP0201201347 浙江永宁药业股份有限公司无菌传递舱C2C—0061201348 广东健信制药有限公司过氧化氢灭菌器ZW-HP0201201349 山东鲁抗医药股份有限公司过氧化氢灭菌器ZW-HP0201201350 南京星银药业集团有限公司汽化过氧化氢灭菌器ZW-HP02012013 汽化过氧化氢无菌传递窗ZW-TWV030151 昆明积大制药有限公司汽化过氧化氢无菌传递窗ZW-TWV02812013 汽化过氧化氢无菌传递舱ZW-C2CV0121Wenzhou Weike Biology Experiment Equipments CO.,LTD52 山东睿鹰先锋药业有限公司汽化过氧化氢无菌传递舱ZW-C2CV0322013 汽化过氧化氢无菌传递窗ZW-TWV0201汽化过氧化氢灭菌器ZW-HP020153 江西珍视明药业有限公司无菌检验隔离系统ZW-SV24001201354 吉林省百利电子有限公司无菌检验隔离系统ZW-SV1860按附件尺寸2201355 江西珍视明药业有限公司汽化过氧化灭菌器ZW-HP020 3 201356 烟台北方制药有限公司汽化过氧化氢无菌传递窗ZW-TWV051 12013 无菌检验隔离系统ZW-SV1800 257 四川川大华西药业股份有限公司无菌检测隔离系统ZW-SV1860 1 201358 湖北武汉五景药业有限公司无菌检测隔离系统ZW-SV1860 1 201359 北大国际医院集团西南合成制药股份有限公司汽化过氧化氢无菌传递舱ZW-C2CV0122 201360 石家庄格瑞药业有限公司无菌传递舱ZW-C2C931 1 201361 合肥惠恩生物科技有限公司汽化过氧化氢无菌传递窗ZW-TWV020 1 201362 海南伊顺药业有限公司汽化过氧化氢灭菌器ZW-HP020 1 201363 广东宏远集团药业有限公司汽化过氧化氢灭菌器ZW-HP020 12013 无菌隔离系统ZW-HL1800 164 广州创尔生物技术有限公司汽化过氧化氢灭菌器ZW-HP02012013Wenzhou Weike Biology Experiment Equipments CO.,LTD65 武汉禾元生物科技有限公司汽化过氧化氢传递窗ZW-TWV0201201366 江苏海宏制药有限公司汽化过氧化氢无菌传递窗ZW-TWV03212013 汽化过氧化氢灭菌器ZW-HP020167 哈药集团制药总厂过氧化氢灭菌器ZW-HP02012013 无菌传递舱ZW-C2C0731汽化过氧化氢蒸汽灭菌传递舱ZW-C2CV064268 浙江永宁药业股份有限公司移动式层流罩定制1201369 四川奇力制药有限公司无菌检验隔离系统ZW-SV186012013 手套侧漏仪(1个工装)ZW-GL011全封闭智能匀浆仪ZW-800D170 哈尔滨莱博通药业有限公司汽化过氧化氢无菌传递窗ZW-TWV03522013 汽化过氧化氢灭菌器ZW-HP020171 成都百裕科技制药有限公司汽化过氧化氢无菌传递窗ZW-TWV0072201372 武汉武药制药有限公司汽化过氧化氢无菌传递窗ZW-TWV012512013 汽化过氧化氢无菌传递舱ZW-HLV1800173 海口奇力制药股份有限公司无菌传递舱ZW-C2C01212013Wenzhou Weike Biology Experiment Equipments CO.,LTD汽化过氧化氢灭菌器ZW-HP020174 成都三叶草制药有限公司汽化过氧化氢无菌传递窗(600mm*600mm*700mm)ZW-TWV0201201375 石药集团欧意药业有限公司汽化过氧化氢无菌传递窗ZW-TWV025 52013 汽化过氧化氢无菌传递窗ZW-TWV0392汽化过氧化氢无菌传递舱ZW-C2CV022176 武汉武药制药有限公司汽化过氧化氢无菌传递窗ZW-TWV012512013 无菌隔离系统(硬舱)ZW-HLV1800177 河北创健药业有限公司无菌检验隔离系统ZW-SV18601201378 海南葫芦娃制药有限公司汽化过氧化氢无菌传递窗定制2201379 广东卫伦生物制药有限公司无菌传递窗ZW-TW0381201380 济南强胜光电仪器有限公司雾化过氧化氢灭菌器ZW-HWP1201381 北京悦康药业集团有限公司汽化过氧化氢灭菌器ZW-HP0201201382 东北制药集团沈阳第一制药有限公司软舱体无菌检验隔离舱ZW-SV24001201383 四川仁安药业有限责任公司汽化过氧化氢无菌传递舱ZW-C2CV01822013Wenzhou Weike Biology Experiment Equipments CO.,LTD84 海南国瑞堂制药有限公司汽化过氧化氢传递舱ZW-C2C0412013 汽化过氧化氢传递舱ZW-C2C08185 海南美好西林生物制药有限公司汽化过氧化氢灭菌器ZW-HP0202201386 广东环球制药有限公司抽真空式过氧化氢灭菌器ZW-HP0201201387 江西东风药业股份有限公司汽化过氧化氢传递舱ZW-C2CV030 22013 汽化过氧化氢传递舱ZW-C2CV0241汽化过氧化氢传递舱ZW-C2CV030 1汽化过氧化氢传递舱ZW-C2CV024 1汽化过氧化氢传递窗ZW-TWV0102汽化过氧化氢传递舱ZW-C2CV075188 湘北威尔曼制药股份有限公司汽化过氧化氢传递舱ZW-C2CV0481201389 新默真科技(北京)有限公司汽化过氧化氢灭菌器ZW-HP0201201390 广东罗浮山国药股份有限公司汽化过氧化氢传递窗ZW-TW0201201391 北京圣医耀科技发展有限责任公司汽化过氧化氢无菌传递窗ZW-TWV01522013Wenzhou Weike Biology Experiment Equipments CO.,LTD92 广州白云山拜迪生物医药有限公司汽化过氧化氢传递窗ZW-TWV0352201493 广州康臣药业有限公司汽化过氧化氢传递窗ZW-TWV0251201494 南京易亨制药有限公司汽化过氧化氢灭菌器ZW-HP0201201495 扬州一洋制药有限公司汽化过氧化氢传递窗ZW-TWVO691201496 福安药业集团庆余堂制药有限公司汽化过氧化氢灭菌器ZW-HP0201201497 成都威尔诺生物科技有限公司无菌检验隔离器ZW-SV15001201498 山西佳能达华禹制药有限公司汽化过氧化氢传递窗ZW-TWV03512014无菌检验隔离器ZW-SV1860A199 安徽省先锋制药有限公司汽化过氧化氢灭菌器ZW-HP020 1 2014 100 山东临沂费县新时代药业汽化过氧化氢传递窗ZW-TW061 1 2014 101 温州亚光机械制造有限公司无菌传递窗ZW-TW056 1 2014102 石家庄市爱尔海泰制药有限公司汽化过氧化氢传递窗ZW-TWV0423 2 2014103 南京龙福新科技实业有限公司汽化过氧化氢灭菌器ZW-HP020 1 2014 104 北京市永康药业有限公司汽化过氧化氢传递窗ZW-TWV015 1 2014105 四川援健药业有限公司取样隔离系统(含自动轧盖机)ZW-HL2700 12014 汽化过氧化氢无菌传递窗ZW-TWV075 2106 海南葫芦娃制药有限公司汽化过氧化氢灭菌器ZW-HP020 1 2014 107 北京悦康药业集团有限公司汽化过氧化氢传递舱ZW-C2CV024 3 2014Wenzhou Weike Biology Experiment Equipments CO.,LTD108 山东恒欣药业有限公司汽化过氧化氢灭菌器ZW-HP020 12014汽化过氧化氢传递窗ZW-C2CV018 1109 昆明积大制药有限公司汽化过氧化氢传递舱ZW-C2CV012 1 2014110 辽宁依生生物制药有限公司无菌检验隔离器(软舱体)ZW--SV2080 1 2014111 北大国际医院集团西南合成制药股份有限公司汽化过氧化氢无菌传递舱ZW-C2CV014 1 2014112 四川科瑞德制药有限公司无菌检验隔离器(软舱体)ZW-SV1800 12014 集成汽化过氧化氢灭菌器ZW-HP020 1113 石家庄以岭药业股份有限公司无菌检验隔离器ZW-SV1838 1 2014 114 湘北威尔曼制药股份有限公司汽化过氧化氢灭菌器ZW-HP020 1 2014115 海南伊顺药业有限公司汽化过氧化氢传递窗ZW-TWV036 12014 汽化过氧化氢传递窗ZW-TWV035 1116 武汉人福药业有限公司无菌检验隔离器ZW-SV1860 1 2014 117 海南新世通制药有限公司汽化过氧化氢灭菌器ZW-HP020 1 2014 118 哈尔滨三联药业股份有限公司无菌检查隔离器ZW-SV2400 4 2014 119 四川禾亿制药有限公司汽化过氧化氢传递窗ZW-TWV0216 1 2014 120 安徽省先锋制药有限公司VHP灭菌传递舱ZW-C2C-08 1 2014 121 黄石世星药业有限责任公司无菌检测隔离器ZW-SV1860 1 2014 122 山东恒欣药业有限公司汽化过氧化氢传递舱ZW-C2CV018 1 2014 123 黑龙江黑宝药业股份有限公司无菌检验隔离系统ZW-SV1800 1 2014Wenzhou Weike Biology Experiment Equipments CO.,LTD124重庆天地药业有限责任公司汽化过氧化氢传递窗ZW-TWV036 2 2014 汽化过氧化氢传递窗 ZW-TWV048 2 取样隔离器系统ZW-HS800 2 125 必康制药江苏有限公司 无菌隔离器 ZW-SV2400 1 2014 126 西安万隆药业股份有限公司 无菌检验隔离系统 ZW-SV2400 2 2014 127湖南方盛制药股份有限公司汽化过氧化氢传递舱ZW-C2CV018 1 2014128辽宁省食品药品监督管理局实验舱ZW-SV1800 2 2014 传递舱 ZW-SV1306 1 汽化过氧化氢灭菌器灭菌3130海南海灵化学制药有限公司无菌检验隔离系统(包含两台集菌仪) ZW-SV1800 12014131山东金城生物药业有限公司汽化过氧化氢灭菌传递舱ZW-C2CV0112014132广州白云山制药股份有限公司白云山何济公制药厂无菌检验隔离系统 ZW-SV1840 1 2014133丽珠集团福州福兴医药有限公司空间过氧化氢灭菌器ZW-HPV04 1 2014汽化过氧化氢传递窗 ZW-TWV039 1 汽化过氧化氢传递舱ZW-C2CV18 1 紫外传递窗ZW-TW039 1 134吉林四长制药有限公司无菌检验隔离系统ZW-SV1800 12014135天津新丰制药有限公司VHP 传递舱(8桶)ZW-C2CV008 12014VHP 传递舱(12桶)ZW-C2CV012 1Wenzhou Weike Biology Experiment Equipments CO.,LTD136 江西希尓康泰制药有限公司汽化过氧化氢传递舱ZW-C2CV16012014 无菌检验隔离系统ZW-SV14001纯水烟雾发生器ZW-WFG011137 南京鑫长江制药设备有限公司汽化过氧化氢传递窗ZW-TWV04012014138 原子高科股份有限公司无菌隔离系统ZW-HLV1980(硬舱)12014139 宝船生物医药科技(上海)有限公司无菌检验隔离系统ZW-SV186012014140 上海源拓净化设备厂汽化过氧化氢传递窗ZW-TWV02212014141 丽珠集团福州福兴医药有限公司无菌检验隔离系统ZW-SV240012014142 湖南方盛制药股份有限公司无菌检验隔离器ZW-SV180012014 143 山东蓝金生物工程有限公司汽化过氧化氢传递窗ZW-TWV02012014 144 南京鑫长江制药设备有限公司汽化过氧化氢传递舱内腔1.5立方12014145 南京优科制药有限公司汽化过氧化氢传递舱ZW-C2CV01012014146 海南通用三洋药业有限公司汽化过氧化氢传递舱ZW-C2CV01822014147 上海景泽生物技术有限公司汽化过氧化氢灭菌器ZW-HP50012015 汽化过氧化氢灭菌器ZW-HP020(两用)1148 云南植物药业有限公司汽化过氧化氢传递舱ZW-C2CV120022015149 天士力制药集团股份有限公司汽化过氧化氢灭菌器ZW-HP02012015 150 天津新丰制药有限公司取样隔离系统ZW-HL312012015 151 湘北威尔曼制药股份有限公司汽化过氧化氢灭菌器ZW-HP02012015Wenzhou Weike Biology Experiment Equipments CO.,LTD152 太和县市场监督检验所无菌检验隔离系统ZW-SV180012015153 广州白云山拜迪生物医药有限公司硬舱体无菌检验隔离器ZW-HLV1700 1 2015154 天津康希诺生物技术有限公司汽化过氧化氢传递窗ZW-TWV039 1 2015 155 云南植物药业有限公司无菌检验隔离系统ZW-SV1800 1 2015 156 苏州金盟生物技术有限公司VHP空间灭菌器ZW-HPV04 12015无菌检验隔离器系统ZW-SV1800 1157 江西天施康中药股份有限公司余江分公司无菌检验隔离系统ZW-SV1860 1 2015158 常州金远药业制造有限公司无菌检验隔离系统ZW-SV1800 1 2015 159 安徽丰原药业股份有限公司无菌检验隔离器ZW-SV2400 2 2015160 武汉海特生物制药股份有限公司硬舱无菌检验隔离器ZW-HLV2015 1 2015161 江西制药有限责任公司无菌检验隔离系统ZW-SV1600 1 2015 162 黄石燕舞药业有限公司无菌检验隔离系统ZW-SV1860A 1 2015163天津新丰制药有限公司汽化过氧化氢空间灭菌器ZW-HP500 12015汽化过氧化氢空间灭菌系统ZW-HPV04 1164 重庆华邦制药有限公司汽化过氧化氢传递窗ZW-TWV020 1台2015 165 新乡市常乐制药有限责任公司无菌检验隔离系统ZW-SV1800 1台2015 166 通化天实制药有限公司无菌检验隔离系统ZW-SV1800 1台2015 167 浙江康德药业有限公司负压隔离舱ZW-HLNP5080 1 2015 168 辰欣药业股份有限公司无菌检验隔离系统ZW-GLV3000 1台2015 169 南京优科制药有限公司无菌检验隔离系统ZW-SV1800 1台2015 170 温州市药检所无菌检验隔离系统ZW-SV1860 1台2015。