高等有机化学:反应机理(华东理工大学)
- 格式:ppt
- 大小:3.73 MB
- 文档页数:92

化学反应工程(网络教育)-题库注:找到所考试题直接看该试题所有题目和答案即可。
查找按键:Ctrl+F 超越高度1、可逆放热反应的最优温度随转化率xA变大而。
A、降低B、变大C、不变D、都有可能答案: A2、对自催化反应而言,必然存在最优反应时间使最大。
A、转化率B、反应速率C、收率D、选择率答案: B3、在列管式固定床反应器中进行强放热反应,为保证反应器稳定操作,若反应活化能越大,则最大允许温差。
A、越小B、越大C、不变D、不能判断答案: A4、工业反应过程优化的技术指标包括 .A、反应速率B、反应选择率C、反应工艺D、能量消耗答案: ABD5、化学反应工程的研究方法主要采用数学模型方法。
答案:正确6、在CSTR中小于平均停留时间的流体粒子占全部粒子的百分比为36.8%。
答案:错误7、若气相反应2A+B→P+S,则膨胀因子dA等于()。
A、 -1/2B、 1/2C、 2D、 -2答案: A8、活化能E与反应的热效应相关,活化能大的反应其反应热也大。
答案:错误9、理想间歇反应器中搅拌越激烈,混合越均匀,则反应速率越快。
答案:错误10、空速的物理意义是单位时间单位反应器体积所能处理进口物料的体积,单位为[时间]-1。
答案:正确11、对自催化反应A+P→P+S而言,必定存在最优反应时间使反应的转化率最大。
答案:错误12答案:外扩散消除,内扩散有影响。
13、有一全混釜反应器,已知反应器体积为100 升,流量为10升/min,试估计离开反应器的物料中,停留时间为0~1min,2~10min和大于30min的物料所占的分率。
答案:0.095,0.451,0.05014、一级液相可逆反应在等温80℃下间歇反应器中进行反应,反应物A,产物P。
已知cA0=2.00mol/L,cP0=0时,反应时间t=30min,测得cA=1.5mol/L,且该温度下平衡浓度cAe =0.5mol/L,求(a)平衡常数K;(b)反应速率常数k1和k2。

化学反应工程_华东理工大学中国大学mooc课后章节答案期末考试题库2023年1.对简单不可逆二级反应,根据要求的处理量、初浓度和转化率,所需的反应器体积最小。
参考答案:平推流2.工业反应过程优化的决策变量包括参考答案:操作方式_工艺条件_结构变量3.均相反应应该满足下述哪2个条件?参考答案:反应体系互溶_预混合过程很快4.对串联反应而言,存在一个最优反应温度使反应产物收率最大。
参考答案:错误5.化学反应工程的研究方法是经验放大方法参考答案:错误6.连续流动釜式反应器中物料浓度和温度处处相等,并且等于反应器进口物料的浓度和温度。
参考答案:错误7.理想间歇反应器中搅拌越激烈,混合越均匀,则反应速率越快。
参考答案:错误8.化学反应的前提是参与反应的所有物料达到分子尺度上的均匀,成为均一的气相或液相。
参考答案:错误9.产生返混的原因是参考答案:不均匀的速度分布_空间上的反向流动10.限制返混的措施包括参考答案:横向分割_纵向分割11.化学反应工程的研究对象是以化学实验室中进行的化学反应过程。
参考答案:错误12.化学反应工程优化的技术指标是参考答案:反应选择率_能耗_反应速率13.活化能E与反应的热效应相关,活化能大的反应其反应热也大。
参考答案:错误14.零级反应的重要特征是反应时间由残余浓度决定,与初始浓度关系不大。
参考答案:错误15.可逆放热反应的最优温度随转化率xA变大而增大。
参考答案:错误16.限制返混的措施是分割,主要是横向分割。
参考答案:正确17.理想管式反应器的径向具有严格均匀的速度分布,也就是在径向不存在浓度变化,所以反应速率随空间位置的变化将只限于轴向。
参考答案:正确18.对自催化反应A+P®P+S而言,必定存在最优反应时间使反应的转化率最大。
参考答案:错误19.小于1级的简单不可逆反应,反应转化率可以在有限时间里达到100%。
参考答案:正确20.空速1000(1/h)表示每小时能够处理的进口物料体积为反应器体积的1000倍。

化学合成反应机理化学合成是一种常用的化学方法,通过组合或转化原子、分子或离子来制备目标产物。
在化学合成中,反应机理是非常重要的。
了解反应机理可以帮助我们理解反应的原理,引导我们设计高效的合成方法,并提供有关反应条件和产物选择的信息。
一、反应机理的概念反应机理是指描述化学反应中原子、分子、离子之间发生的具体步骤和反应路径的理论模型。
它通过分析反应物和产物之间的键断裂、键形成和中间体的形成来揭示反应的本质。
反应机理可以从实验数据、理论计算和理论分析中得到。
二、核心概念:活化能和反应中间体活化能是指化学反应中反应物要通过能垒才能转变为产物的能量差。
活化能高低直接影响反应速率,活化能越高,反应速率越慢。
了解反应机理可以帮助我们了解活化能的来源,从而设计合适的反应条件来提高反应速率。
反应中间体是指在反应中暂时形成的中间产物,它们通常是不稳定的,往往很快转化为更稳定的物质。
反应中间体的存在对于理解反应机理和选择适当的合成路径非常重要。
三、反应的基本步骤1. 取代反应取代反应是一种常见的化学合成方法,包括亲核取代反应和电子取代反应。
亲核取代反应是指亲核试剂攻击电子密度较高的化合物,将原有官能团取代掉,形成新的官能团。
电子取代反应则是通过电子试剂来引发反应,改变化合物的电子分布。
2. 加成反应加成反应是指两个或多个分子之间发生共有电子对(键)的结合,形成一个新的化合物。
加成反应可以通过共轭体系的形成或破坏来实现。
加成反应在天然产物的合成中经常被使用,可以实现复杂分子骨架的构建。
3. 消除反应消除反应是指通过消除某些原子或基团,使反应物减少一个或多个分子,生成一个或多个新的化合物。
常见的消除反应包括酯中的酸或酸酐的消除,或芳香醚中的碱或醇的消除。
消除反应可以减小反应物的分子量,有助于化合物的精简合成。
四、反应机理的研究方法1. 实验方法实验方法是研究反应机理的关键手段之一。
通过实验可以获得反应物和产物的转化率、速率常数等重要数据,从而推测反应的机理模型。

有机化学八大反应机理有机化学是研究有机分子结构和反应的分支化学。
它的研究方法包括反应机理研究,反应产物的分析和结构推断,以及计算机模拟技术的应用。
反应机理研究是有机化学的核心,它的研究方法包括实验证明、模型推断和计算机模拟。
在有机化学中,有八种主要的反应机理,这八种反应机理是有机反应的基础,它们共同构成了有机反应的复杂系统。
这八种反应机理是:酸催化反应、氢转移反应、羰基反应、缩合反应、氧化反应、环化反应、加成反应和复分解反应。
首先,酸催化反应是有机反应中最常见的反应机理,它是由一种有机酸催化剂引发的。
酸催化反应可以分为三类:羧基质子化反应、烷基质子化反应和烯基质子化反应。
它们的反应机理都是酸催化剂将原料中的电子富集,使其形成质子中心,从而引发了反应。
其次是氢转移反应,它是一种重要的有机反应机理,在此反应中,原料中的一个氢原子被转移到另一个原料上,从而形成新的分子结构。
氢转移反应可以分为四类:单位氢转移反应、双位氢转移反应、羰基氢转移反应和烯基氢转移反应。
第三是羰基反应,它是指一种反应机理,在此反应中,羰基会与另一个原料发生反应,形成新的化合物。
羰基反应可以分为两类:无水羰基反应和有水羰基反应。
无水羰基反应是指在无水条件下,羰基与另一个原料发生反应,而有水羰基反应又可分为水解反应和加水羰基化反应。
第四是缩合反应,它是指两个原料发生反应,形成新的化合物的反应机理。
缩合反应可以分为三类:烷基缩合反应、羰基缩合反应和烯基缩合反应。
它们的反应机理都是两个原料的原子发生相互作用,形成新的化合物。
第五是氧化反应,它是指一种反应机理,在此反应中,氧将原料中的一个原子氧化,形成新的分子结构。
氧化反应可以分为四类:氢氧化反应、羰基氧化反应、烯基氧化反应和烃氧化反应。
它们的反应机理都是将原料中的一个原子氧化,形成新的分子结构。
第六是环化反应,它是指一种反应机理,在此反应中,原料中的一个或多个原子被添加到另一个原料上,形成新的环状结构。

第一章测试1【多选题】(2分)有机物的主要天然资源有()。
A.石油B.煤C.天然气D.生物体2【多选题】(2分)十九世纪末的物理学的三大发现是()。
A.放射性B.X射线C.电子的发现3有机碳的化合价是()。
A.四价B.二价C.一价D.三价4【单选题】(2分)共振结构式中共价键越多,能量越();电荷分布越符合电负性规律的能量越()。
①高;②低A.①②B.②①C.①①D.②②5比较常见卤素的静态电负性大小()。
A.F>Cl>Br>IB.F<Cl<Br<I6【单选题】(2分)最早发现酒石酸旋光性的化学家是()A.范特霍夫B.巴斯德C.拜尔D.门捷列夫7【单选题】(2分)A.C,D;BB.C,D;A第二章测试1【单选题】(2分)复杂取代基如何编号()。
A.从与主链相连的碳原子开始编号B.类似主链,离取代基近的一头编号2【单选题】(2分)1,2-二氯乙烷的构象-能量变化曲线与()类似。
A.丁烷B.乙烷3【单选题】(2分)下列化合物中,沸点最高的是()。
A.正戊烷B.正己烷C.异戊烷D.新戊烷4【单选题】(2分)比较卤素与烷烃的卤代反应速度()。
A.F>Cl>Br>IB.F<cl<br<i<span=""></cl<br<i<>5【单选题】(2分)下列化合物中,存在顺反异构体的是()。
A.1,1-二甲基环丁烷B.2,3-二甲基丁烷C.2,2-二甲基丁烷D.1,2-二甲基环丁烷6【单选题】(2分)肖莱马是哪国化学家及主要研究方向()。
A.德国研究烃类B.法国研究烃类C.英国研究羧酸7【单选题】(2分)四氯化碳的空间结构是()。
A.平面型B.正四面体8【单选题】(2分)n-C4H10是何烷烃()。
A.叔丁烷B.异丁烷C.正丁烷9【单选题】(2分)烷烃溴代时,伯、仲、叔氢的活性比为1:82:600,给出以下反应的主产物()。

AoC 2121t an n p n n A Ao Po P )()(--=-βAf Ao Pf C C C -=βAoPf C C =ϕ1 基本概念 1.1 优化:在一定的范围内,选择一组优惠的决策变量,使系统对于确定的评价标准达到最佳的状态。
1.2 反应速率:反应系统中某一物质在单位时间、单位反应区内的反应量。
1.3 反应转化率:反应物中某一组分转化掉的量(摩尔)与其初始量(摩尔)的比值。
常用x 表示。
1.4 选择率:对于复杂反应过程,同一反应原料可以生成几种不同的产物和无用的副产物。
此时,不同产物之间的分配比例对该反应过程的经济效益是一个非常重要的指标。
产物之间的这种分配比例可以用反应选择率 表示。
定义为已经转化掉的反应物量(摩尔)中,转化为目的产物的摩尔分率。
例:(主反应) (副反应)或又称为平均选择率。
瞬时选择率 β1.5 反应收率:得到的产物的量与投入反应系统的原料的量的比值φ。
该指标综合了选择率和反应速率两个指标的特点。
可采用摩尔收率和质量收率来表示。
以摩尔收率为例:总收率1.6 单耗:产品的原料消耗若以每份产品所需的反应原料份数来表示,就称为原料单耗,也可以用摩尔分率或质量分率来表示。
单耗与收率互成倒数。
1.7 返混:使早先进入的存在于反应器内的物料有机会与刚进入的反应物料相混合,这种混合现象称为返混现象。
1.8 排除了一切物理传递过程的影响,得到的化学反应动力学称为微观动力学或本征动力学。
在包含物理过程影响的条件下所测得的反应动力学称为宏观动力学(或称为表观反应动力学)。
1.9 基元反应和非基元反应:如果一个化学反应,反应物分子在碰撞中相互作用直接转化为生成物分子,这种化学反应称为基元反应(elementary reaction),否则就是非基元反应。
1.10 反应机理或反应历程:复杂反应要经过若干个基元反应才能完成,这些基元反应代表了反应所经过的途径,动力学上就称为反应机理或反应历程。
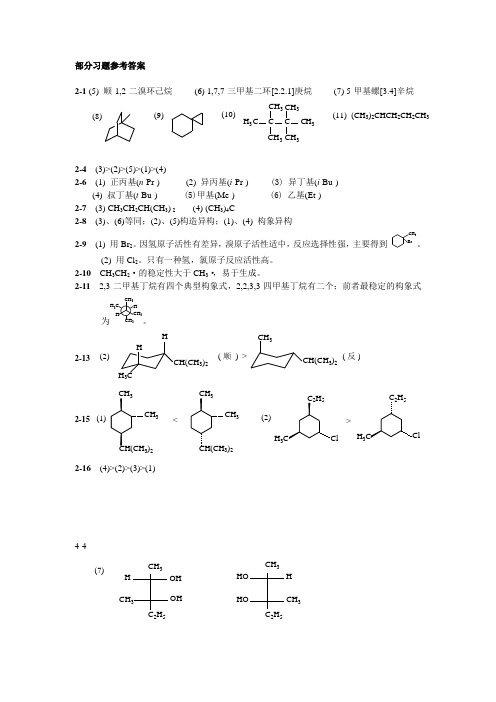
部分习题参考答案2-1 (5) 顺-1,2-二溴环己烷 (6) 1,7,7-三甲基二环[2.2.1]庚烷 (7) 5-甲基螺[3.4]辛烷(8)(9)CCCC CH 3CH 3CH 3CH 3H 3H 3(10)(CH 3)2CHCH 2CH 2CH 3(11)2-4 (3)>(2)>(5)>(1)>(4)2-6 (1) 正丙基(n -Pr-) (2) 异丙基(i -Pr-) (3) 异丁基(i -Bu-)(4) 叔丁基(t -Bu-) (5)甲基(Me-) (6) 乙基(Et-) 2-7 (3) CH 3CH 2CH(CH 3) 2 (4) (CH 3)4C2-8 (3)、(6)等同;(2)、(5)构造异构;(1)、(4) 构象异构2-9 (1) 用Br 2。
因氢原子活性有差异,溴原子活性适中,反应选择性强,主要得到CH 3Br。
(2) 用Cl 2。
只有一种氢,氯原子反应活性高。
2-10 CH 3CH 2·的稳定性大于CH 3·,易于生成。
2-11 2,3-二甲基丁烷有四个典型构象式,2,2,3,3-四甲基丁烷有二个;前者最稳定的构象式为3H 3。
CH(CH 3)2CH333)2( 顺 ) >( 反 )(2)2-133)233)2CH 3(1)H 3H 3(2)<>2-152-16 (4)>(2)>(3)>(1)4-4(7)H OH CH 3OHCH 3C 2H 5HO H HOCH 3CH 3C 2H 5(8)(CH3)2CHCOH3C OOCHCH3(CH3)2CHC OCH3O CHCH3(9)CH2Br BrBr(10)Br OCH3(11)H2C—CnCH3COOCH34-5(1)CH3CH2CH2CH CH2乙烯基烯丙基CH3CH2CH CHCH3丙烯基有顺反异构CH3CH2—C CH2CH3异丙烯基CH3CH CCH3CH3CH2CHCH(CH3)2乙烯基(2) 2,3-二甲基-2-丁烯>2-甲基-2-戊烯>反-3-己烯>顺-3-己烯>1-己烯(3)2-甲基-1-丙烯快(形成叔碳正离子)快(形成叔碳正离子)4-6(1)亲电加成反应,中间体为碳正离子,有重排(CH 3)2CHCH CH 2H(CH 3)2CHCH CH 3(CH 3)2CHCHCH 3重排CH 3 C CH 2CH 3CH 3Br(CH 3)2CCH 2CH 3Br(2) 甲醇与碳正离子结合;直接失去质子而形成醚+CH 2 CH 2 CH 3OH BrCH 2 CH OCH 3HHCH 2 CH 2OCH 3BrBrBrBr( 3 )CH 3Br CH 3BrH++++(4)CF 3CHCH 2HCF 3CHCH 3CF 3CH 2CH 2(CF 3CH 2CH 2ClCH 3OCHCH 2HCH 3OCH 2CH 2CH 3OCHCH 3 (CH 3OCHClCH 3(5)H重排Cl7(1)CH 3C CCH 2CH 2C CCH 3CH 3CH 3H H4-CH 3CCCH 2CH 2CCCH 3CH 33HCH 3CH 3CC CH 2CH 2CCCH 3CH 3HCH 3HCCCH 2CH 2C CCH 3CH 3CH 3HCH3H(2)或(3)(4)5-9(1)Br 2/CCl 4;Ag(NH 3)2NO 3, (2)顺丁稀二酸酐; Ag(NH 3)2NO 3, 5-11H 333H 33或CH 3CH 2CH 2CHCH 2CH 2CH 3CH 3H 3C C H C C 3H H CH 3H 3C C H C C H 3H CH 3或A B CDH 3CC H CH CH C CCH 3HH35-12CH 3CHC CCH 2CH 2CH 33CH 3CH 2CH 2COOH CH 3CHCOOH3CH 3CHCCH 3OCH 3A B C D ECH 3CHC CH 3CH6-1 (a) C 3H 7NO(b) C 2H 3OCl 6-332CH 2CH 3CH 3CH CHCH 2m/z =55CH 3CHCH重排CH 2CH CH 2m/z =41m/z =846-4 共轭,ε(a )>ε(b)6-5(a)227nm, (b)237nm, (c)227nm, (d)232nm 6-6(1) (a)>(b)(2)(b)>(a)(3)(a)>(b)6-8 3000~3100cm-1 C=C-H v, m 2850~2950 cm-1CH3,CH2v, s1620~1680 cm-1C=C v, m1430 cm-1CH3 δ910~1000 cm-1-C=C-H δ6-9偶合常数不同,反式偶合常数较大7-97-107-147-157-167-178-1 1) 1,4-二氯丁烷2) 2-甲基-3-氯-6-溴-1,4-己二烯3) (R)- 3-甲基-2-氯戊烷4) (S)- 1-苯基-1-溴丙烷5) 4-甲基-3-溴苯磺酸6) 3-对溴苯-1-丙烯8-5 1) (a)(CH 3)3CBr> CH 3CH 2CHBr CH 3CH 3CH 2CH 2CH 2Br>(b)CHCH 3BrCH 2BrCH 2CH 2Br>>2) (a)CH 3CH 2CH 2Br > (CH 3)2CHCH 2Br>(b)> (CH 3)3CCH 2BrCH 3CH 2CH 2CH 2Br> CH 3CH 2CHBrCH 3(CH 3)3CBr8-6 1) CH 3CH 2CH 2CH 2Br 反应较快。

华东理工大学201 –201 学年第 学期《化学反应工程》课程考试试卷开课学院:化工学院 ,专业: ,考试形式:闭卷,所需时间:120 分钟一、填充题(25分,每个空格2.5分)⑴反应活化能越小,则说明反应速率对温度变化越 。
对反应活化能E=80 kj/mol 的反应,在300K 时反应速度要求增加10%,则反应温度应变为 。
⑵工业反应过程优化的技术指标是 。
⑶一级串连反应A P S k k 12−→−−→−,k 1=1 hr -1,k 2=2 hr -1,则在CSTR 反应器中最优空时opt τ= h r 。
⑷F(t)的含义是 。
若物料在CSTR 反应器中平均停留时间20分钟,则停留时间小于20分钟的物料占总出口物料 %。
⑸判断气固催化反应外扩散影响的准数是 ,消除外扩散阻力的工程措施是。
⑹在判断内扩散影响时,当Φ ,则内扩散对反应的影响可忽略;当Φ ,则内扩散对反应的影响严重。
二、单选或多选题(16分,每题4分)⑴ 实验室反应器催化剂装填高度10cm ,操作线速度为0.25cm/s 。
若工业反应器催化剂高度为2m ,空速与实验室反应器相同,则工业反应器流体线速度为 。
a. 2.5 cm/sb. 5cm/sc. 7.5cm/sd. 10 cm/s⑵常用的流固相反应模型之一是 。
a. 全混流模型b. 多釜串联模型c. 整体模型d.平推流模型⑶ 对21E E >的串联反应S P A −→−−→−21,21,E E 分别为主副反应活化能,提高反应选择性的措施是 。
a. A c ᆳb. A c ᆳc. T ᆳd. T ᆳ⑷ CSTR 中进行放热反应,其热稳定条件要求同时满足 。
a.=g Q b.g rdQ dQ dTdT<c.g r dQ dQ dTdT>d.rg Q Q =三、图解题(24分,每题8分)⑴平行反应选择性β与转化率x A 的关系如图所示,用图解法画出产物收率最大时反应器的组合形式(PFR ,CSTR),并画出反应器设备组合示意图。

有机化学反应机理详解有机化学是研究碳和碳之间的化学反应的科学,它是化学学科中的一个重要分支。
在有机化学中,了解反应机理对于理解和预测化学反应的过程至关重要。
本文将详细解析几种常见的有机化学反应机理,以帮助读者更好地理解这一领域的知识。
一、加成反应机理加成反应是指两个或多个分子中的原子或原子团结合形成一个新的分子的反应。
其中,最常见的加成反应是亲电加成和互变异构反应。
亲电加成是一种亲电试剂与亲核试剂发生反应的过程。
亲电试剂是电子亏损的化合物,亲核试剂则是电子富余的化合物。
在亲电加成反应中,亲电试剂首先与亲核试剂发生反应,形成一个中间产物,然后中间产物再与其他试剂发生反应,最终生成产物。
例如,氢氯酸与乙烯反应的机理如下:1. 氢氯酸中的氢离子(亲电试剂)攻击乙烯中的双键(亲核试剂),形成一个中间产物,即乙基氯化物。
2. 乙基氯化物再与其他试剂发生反应,例如水,生成乙醇。
互变异构反应是指两种异构体之间发生的反应。
异构体是指分子结构相同但空间结构不同的化合物。
在互变异构反应中,一个异构体通过断裂和重组键的过程转变为另一个异构体。
例如,顺丁烯二酸和反丁烯二酸之间的互变异构反应如下:1. 顺丁烯二酸中的双键与一分子的水发生加成反应,生成一个中间产物,即顺丁烯二酸酯。
2. 顺丁烯二酸酯再与另一分子的水发生反应,断裂酯键,生成反丁烯二酸。
二、消除反应机理消除反应是指一个分子中的两个官能团之间的原子或原子团发生脱离,形成两个新的分子的反应。
最常见的消除反应是酸催化的脱水反应和碱催化的脱卤反应。
酸催化的脱水反应是指酸作为催化剂促使一个分子中的氢原子和羟基发生脱离,形成一个新的分子和水。
这种反应常见于醇类和酚类化合物。
例如,乙醇发生酸催化的脱水反应如下:1. 酸催化剂(例如浓硫酸)与乙醇发生反应,形成乙醇中的羟基离子。
2. 羟基离子与另一个乙醇分子发生反应,断裂羟基上的氢原子和乙醇中的羟基,生成乙烯和水。
碱催化的脱卤反应是指碱作为催化剂促使一个分子中的卤素原子发生脱离,形成一个新的分子和卤化氢。


化学学院硕士研究生课程内容简介学科基础课-------------学术规范与科技写作-------------课程编号:123020002001 课程类别:学科基础课课程名称:学术规范与科技写作英译名称:Academic regulation and scientificpaper writing学时:40 学分:2开课学期:1 教学方式:讲授+讨论考核方式:开卷考试适用学科:化学授课单位及教师梯队:化学学院教师内容简介:本课程着重讲述学术研究、学术规范的概念、学者治学的素质、学术忠诚与学术道德、出版与知识产权、文献包括电子文献的检索和最基本的各种学术规范,提供和评析中外理科学术失范与遵守规范的典型案例。
讲述写作研究论文与学术报告的各种规范。
参考书目:1.《学术规范读本》杨玉圣张保生,河南大学出版社2.《如何写研究论文与学术报告》Carole Slade,外语教学与研究出版社3.《学术规范导论》杨玉圣张保生,高等教育出版社4.《科学革命与卡文迪什实验室》阎康年,山西教育出版社5.《智者的旋律》吴声功,上海人民出版社6.《科学研究与道德》李光玉黄发玉,华中工学院出版社7.《对年轻科学家的忠告》P·B梅多沃,南开大学出版社8.《学术规范通论》叶继元,华东师范大学出版社-------------高等有机化学-------------课程编号:123020001002 课程类别:学科基础课课程名称:高等有机化学英文名称:Advanced Organic Chemistry学时: 40 学时学分:2 分开课学期:1 课堂形式:课堂讲授考核形式:闭卷考试适用学科:化学学院各专业(不含课程与教学法论)授课单位及教师梯队:有机专业教师内容简介:《高等有机化学》属学科基础性课程,适用于化学学科中无机化学、有机化学、分析化学、物理化学、高分子化学、材料化学与物理等。
课程用现代化学的观点即化学是研究化学键的科学,介绍化学键的理论在有机化学中的具体应用。


一、Arbuzow反应(重排)亚磷酸三烷基酯作为亲核试剂与卤代烷作用,生成烷基膦酸二烷基酯和一个新的卤代烷:卤代烷反应时,其活性次序为:R'I >R'Br >R'Cl。
除了卤代烷外,烯丙型或炔丙型卤化物、a-卤代醚、a- 或 b-卤代酸酯、对甲苯磺酸酯等也可以进行反应。
当亚酸三烷基酯中三个烷基各不相同时,总是先脱除含碳原子数最少的基团。
本反应是由醇制备卤代烷的很好方法,因为亚磷酸三烷基酯可以由醇与三氯化磷反应制得:如果反应所用的卤代烷 R'X 的烷基和亚磷酸三烷基酯 (RO)3P 的烷基相同(即 R' = R),则Arbuzow反应如下:这是制备烷基膦酸酯的常用方法。
除了亚磷酸三烷基酯外,亚膦酸酯 RP(OR')2和次亚膦酸酯 R2POR' 也能发生该类反应,例如:反应机理一般认为是按 S N2 进行的分子内重排反应:反应实例二、Arndt-Eister 反应酰氯与重氮甲烷反应,然后在氧化银催化下与水共热得到酸。
反应机理重氮甲烷与酰氯反应首先形成重氮酮(1),(1)在氧化银催化下与水共热,得到酰基卡宾(2),(2)发生重排得烯酮(3),(3)与水反应生成酸,若与醇或氨(胺)反应,则得酯或酰胺。
反应实例三、Baeyer----Villiger 反应反应机理过酸先与羰基进行亲核加成,然后酮羰基上的一个烃基带着一对电子迁移到-O-O-基团中与羰基碳原子直接相连的氧原子上,同时发生O-O键异裂。
因此,这是一个重排反应具有光学活性的3---苯基丁酮和过酸反应,重排产物手性碳原子的枸型保持不变,说明反应属于分子内重排:不对称的酮氧化时,在重排步骤中,两个基团均可迁移,但是还是有一定的选择性,按迁移能力其顺序为:醛氧化的机理与此相似,但迁移的是氢负离子,得到羧酸。
反应实例酮类化合物用过酸如过氧乙酸、过氧苯甲酸、间氯过氧苯甲酸或三氟过氧乙酸等氧化,可在羰基旁边插入一个氧原子生成相应的酯,其中三氟过氧乙酸是最好的氧化剂。

有机化学(下)(华东理工大学)智慧树知到课后章节答案2023年下华东理工大学华东理工大学第一章测试1.酚、醇等常见化合物的酸性比较为()。
A:H2CO3 >酚>水>醇 B:H2CO3 < 酚 < 水 < 醇 C:H2CO3 >酚>醇>水答案:H2CO3 >酚>水>醇2.下列化合物中()俗称苦味酸。
A:三硝基苯酚 B:三硝基甲苯 C:三硝基苯答案:三硝基苯酚3.目前工业上制备苯酚最主要的方法为()。
A:苯磺酸碱熔融法 B:异丙苯法 C:卤代苯水解法答案:异丙苯法4.下列化合物沸点最高的是()。
A:B:C:答案:5.下列化合物酸性最大的为()。
A:B: C: D:答案:6.下列化合物与乙醇钠反应时,活性最大的是 ( )A: B: C:答案:7.A:甲醇钠和叔丁基氯反应B:甲醇和叔丁醇分子间脱水C:甲基氯和叔丁醇钠反应答案:甲基氯和叔丁醇钠反应第二章测试1.下述化合物与NaHSO3反应速度最大者()。
A:丁酮 B:丁烯酮 C:丙醛答案:丙醛2.在有机合成中保护羰基的常用试剂是()。
A:B:C:D:答案:3.下列化合物中,()是半缩醛(或半缩酮),()是缩醛(或缩酮)。
A:a、c、d ; bB:b、c、d ; a答案:b、c、d ; a4.下列化合物中不能与2,4-二硝基苯肼反应的化合物是();不能发生碘仿反应的是();不能发生银镜反应的含羰基化合物是();不能发生自身羟醛缩合反应的含羰基化合物是()。
A:c ; a ;d ;aB:c ; a ;d ;b答案:c ; a ;d ;a5.下列化合物中,哪个可发生歧化反应[坎尼查诺(Cannizzaro)反应()。
A:B:C:D:答案:6.比较以下的亲核试剂与醛酮发生亲核加成反应的速度()A: B:答案:7.二酮化合物可发生分子内缩合,,内外侧α氢均有可能参与反应,产物选择性决定于()A:外侧α氢B:内侧α氢C:环状产物稳定性答案:环状产物稳定性8.碱催化下醛酮的卤代反应产物以()为主,可用于合成()A:卤代醛酮B:结构特殊羧酸C:一元取代D:三元取代E:二元取代答案:结构特殊羧酸;三元取代9.黄鸣龙还原反应适合于()条件稳定的醛酮,可把醛酮还原至()。

有机化学 华东理工大学第二版第一章 绪论思考题1-1:请区别下列化合物是无机物还是有机物 NaHCO 3 金刚石 CaC 2 淀粉 棉花 淀粉和棉花是有机物思考题1-2 指出下列化合物所含官能团的名称和所属类别:(1)CH 3-CH 2-NH 2 (2)CH 3-CH 2-SH (3)CH 3-CH 2-COOH (4)CH 3-CH 2-CH 2-Cl (5)CH 3COCH 3 (6)C 6H 5NO 2开链化合物:1-5;芳香环类:6官能团:氨基、巯基、羧基、卤素、羰基、硝基思考题1-3 写出下列化合物的Lewis 结构式并判断是否符合八隅规则 A 氨 B 水 C 乙烷 D 乙醇 E 硼烷(BH 3)N HHHC HHC H HB HH硼烷不符合八隅规则思考题1- 4 比较下列化合物中的C-H 与C-C 键长 A 乙烷 B 乙烯 C 乙炔C-H 键长次序:A > B > C ;C-C 键长次序:A > B > C思考题1-5:请写出下列化合物Lewis 结构式,并指出形式电荷甲烷 H 3N —BH 3 [H 2CNH 2]+ (CH 3)2O —BF 3 [CH 3OH 2]+ N H HHOH 3CH 3CC HH HB HHH CH HNHHB H HC HH OHH思考题1-6:请写出下列化合物共振共振结构式N HOOOHNHO思考题1-7:请写出下列化合物共振结构式,并比较稳定性大小和主要共振式。
A[CH 3OCH 2]+BH 2C=CH —CH 2+CH 2C=CH —NO 2H 2C —CH=CH 2C H HOCHHC HH CH次要共振式主要共振式A BH 2C=CH —CH 2++主要共振式主要共振式CH 2CH CNO OH 2CH C NO OH 2CH CNO O主要共振式主要共振式次要共振式思考题1-8:请解释下列异构体沸点差异。
CH 3CH 2CH 2CH 2CH 3CH 32CH 3CH 3CH 33CH 33沸点36℃28℃10℃分子的形状越是接近球状,表面积越是小,导致分子间作用力减小。