z化学式计算练习题型
- 格式:ppt
- 大小:111.50 KB
- 文档页数:21

根据化学式计算基础知识:①相对分子质量=分子中含有各原子的原子质量(原子个数×相对原子质量)之和;②元素质量比=元素的质量分数比=原子个数比×相对原子质量比;③元素的质量分数=该元素的相对原子质量×原子个数÷相对分子质量。
考查题型:①计算分子中各元素的原子个数比②计算分子的相对分子质量③计算分子中各元素的质量比④计算分子中某元素的质量分数⑤给出物质质量,计算含某元素的质量一、基础练笔:1.计算下列化学式的相对分子质量(1) 2H2O (2)氧化铁(Fe2O3) (3)碳酸钠(Na2CO3) (4)二个五氧化二磷分子(5)胆矾[CuSO4·5H2O] (6)高锰酸钾(KMnO4) (7)2KClO3(13).某元素R的氧化物RxOy,相对分子质量为M,则R元素的相对原子质量是多少?2、计算分子中各元素的质量比(1)污染的融雪剂的主要成份是醋酸钾(CH3COOK)。
请回答:醋酸钾中C、H、O元素的质量比;(2)化肥硝酸铵的化学式为(NH4NO3)。
试求:硝酸铵中N、H、O三种元素的质量比;(3)四氧化三铁(Fe3O4)中铁元素与氧元素的质量比多少?3 、计算分子中某元素的质量分数(1)计算硝酸铵(NH4NO3)中氮元素质量分数(2) 245g氯酸钾中含有氧元素的质量是多少?四、给出物质质量求元素的质量1、计算10克四氧化三铁中铁元素的质量2、80克碳酸钙中钙元素的质量3.多少 g硝酸铵(NH4NO3)含氮。
多少g碳酸氢(NH4HCO3)的含氮量与硫酸铵[(NH4)2SO4]的含氮量相同。
4、多少克二氧化碳中氧元素的质量跟36g水所含的氧元素质量相等?12.为了保证某一农作物获得㎏氮元素,则需要多少㎏硝酸铵。
五、有关混合物的计算1、计算200克纯度为90%的碳酸钙样品中钙元素的质量2、16克含NH4NO380%的化肥中含多少克氮元素?3、100克某碳酸钙样品中钙元素的质量分数为36%,求样品中碳酸钙的质量分数4、某硝酸铵样品中混有一其它化肥,经分析样品中含有氮元素36%,那么该样品混有的物可能质是A、NH4HCO3B、(NH4)2SO4C、NH4ClD、CO(NH2)2六、已知元素质量比或某元素的质量分数求化学式1、已知某物质有氮氧元素组成,其氮、氧元素质量比为7:12,求该化合物的化学式2、克某铁的氧化物中含有铁克求该铁的氧化物的化学式3、核糖的相对分子质量为150,其中含C40%、H %,其余为O,请确定化学式七、根据有关条件求相对分子质量或相对原子质量1、X2O3相对分子质量为102,则X的相对原子质量为。

与化学式有关的几种计算化学式是初中化学重要的知识点,对化学式概念的理解及有关化学式的计算技能的掌握,具有承上启下的作用。
不仅是分子、元素、原子知识的巩固、应用、加深,而且是继续学习氢、碳、铁、酸、碱、盐、化学方程式内容的基本工具。
一、计算元素种类、原子个数例1、NH4NO3中共有____种元素,_____个原子。
解析:化学式中重复出现的N只算一种,共三种,原子总数:2个氮原子+4个氢原子+3个氧原子=9例2蔗糖在充足的氧气中燃烧,生成二氧化碳和水,则蔗糖中一定有_____元素,可能有_____元素。
将蔗糖隔绝空加热生成碳和水,则蔗糖中含有的元素是_____。
解析:生成物中有CO2和H2O,共C、H、O三种元素,反应物也应有这三种,若氧元素全部由氧气提供,则蔗糖中有C、H元素,反之则蔗糖中C、H、O三种都有,可得蔗糖有一定有C、H、O三种元素都有。
二、计算相对质量1、计算相对分子质量:化学式中各原子的相对原子质量的总和,符号:Mr例1、(NH4)2SO4的相对分子质量=_____,CuSO4•5H2O的相对分子质量=______。
解析:(NH4)2SO4的相对分子质量=(14+1×4)×2+32+16×4=132CuSO4•5H2O的相对分子质量=64+32+16×4+5(1×2+16)=250 元素符号之间用“+”,元素符号与数字间用“×”,括号保留,括号前后的数字用“×”,结晶水合物中间的“•”变为“+”,不要与数学上的乘号“•”混淆。
2、计算相对原子质量例1mg化学式为RO的氧化物中含有ngR,则R的相对原子质量为____。
解析:O的质量=(m-n)gO的相对原了质量为16则O的相对原子质量的标准“1”=(m-n)/16,R的相对原子质量=n/(m-n)/16=16n/(m-n)例2、某物质化学式为H2RO4,相对分子质量为98,则R的相对原子质量为_____,该元素1个原子中有16个中子,该元素的符号为_____.解析:根据相对分子质量的计算1×2+R的相对原子质量+16×4=98R的相对原子质量=32又因:质子数+中子数=相对原子质量则R的质子数=32-16=16,R为S。

化学式计算的几种题型题型一:已知各元素原子量之比和实际质量比,求化学式例1:.X、Y两元素的相对原子质量之比为7∶2 ,X与Y形成的化合物中,X、Y两元素的质量之比为21∶8 ,则该化合物的化学式可表示为()A、X3Y2B、X3Y4C、X2Y3D、XY练习:X、Y两元素的相对原子质量之比为7∶2 ,X与Y形成的化合物中,X、Y两元素的质量之比为7∶3 ,则该化合物的分子式表示为()A、X3Y4B、X3Y2C、X2Y3D、XY题型二:已知各元素原子量之比和实际质量比,求化合价例2:已知X、Y两元素的相对原子质量之比是2∶1,由这两种元素形成的化合物中,X、Y的质量之比是2∶3,其中X的化合价为+a 。
则在化合物中Y的化合价为()A、-a/2B、-a/3C、-2a/3D、-3a/2题型三:多种元素组成的混合物中,已知一种元素的质量分数,求另一种元素的质量分数例3:在硫酸亚铁(FeSO4)和硫酸铁[Fe2(SO4)3] 的混合物中,硫的质量分数是22℅,则混合物中铁的质量分数是()A、34℅B、44℅C、66℅D、无法确定练习:由C2H4和C2H4O组成的混合气体中,经测定其中碳元素的质量分数为72%,则混合气体中氧元素的质量分数为()A、32%B、16%C、20%D、12%其他题型:1、要使CO2和CO中含有相同质量的碳元素,则CO2和CO的质量比是___________,要使CO2和CO中含有相同质量的氧元素,则CO2和CO的质量比是__________。
质量相等的CO2和CO中,氧元素和碳元素的质量比是__________。
2、在19世纪,化学家对氧化锆的化学式有争议。
经测定,锆的相对原子质量为91,其氯化物的相对分子质量是233,若氧化物中锆的化合价与氯化物中锆的化合价相同,试判断氧化锆的化学式为()A、ZrO2B、Zr2OC、Zr2O3D、ZrO3、X、Y两种元素组成的化合物甲和乙,甲的化学式为XY2,其中Y元素的质量分数为50%,乙中Y元素的质量分数为60%,则乙的化学式为()A、XYB、XY3C、X2Y3D、X3Y4、某物质R是人类生命活动中不可缺少的物质。

化学式计算专题一、根据化学式的计算可归纳为以下两种:1.计算相对分子质量例1:分别计算硝铵、蓝矾的相对分子质量解析:在计算中最好熟记常见原子团的“相对分子质量”,如M(OH-)=17、M(NH4+)=18、M(SO42-)=98、M(CO32-)=60、M(NO3-)=62等。
结晶水合物中的“·”表示“+”,不表示“×”。
(注:M表示相对分子质量)M(CuSO4·H2O)=64+96+18×5=250M(NH4NO3)=18+62=802.化合物中某元素的质量分数与延伸例2:有一包由FeSO4和Fe2(SO4)3组成的混合物,测知铁的质量分数为31%,求混合物中硫元素的质量分数。
解析:解答这类题宜用等效变式巧解。
以FeSO4为立足点,将Fe2(SO4)3变形为Fe(SO4)3/2,则原混合物可看成由Fe和SO4两种成分组成。
有:混合物中硫元素的质量分数为(1-31%)×(32/96)=69%×(1/3)=23% 例3:在FeO、Fe2O3、Fe3O4三种化合物中,等质量的铁元素结合的氧元素的质量比()A.6∶9∶8B.12∶8∶9C.2∶3∶6D.1∶3∶4解析:将它们依次变为Fe6O6、Fe6O9、Fe6O8,从中看出氧元素质量比为6∶9∶8。
选A。
例4:某硝铵化肥样品,经测得其含氮量为33.33%,求化肥中硝铵的纯度。
解析:纯度是指样品中含纯物质的质量分数。
即:纯度=(纯物质的质量/含该纯物质样品的质量)×100%此题解法甚多,如下:设样品中含NH4NO3为χ%纯NH4NO3中的氮元素的质量分数为(2N/ NH4NO3)×100%=(28/80)×100%=35%则样品中氮元素的质量分数=χ%×35%=33.33%,解得χ%=33.33%/35%=95.23%设样品中含NH4NO3为χ%因NH4NO3中氮元素的质量分数为35%(计算过程见上),由下列关系式得:关系式:NH4NO3~2N关系量:100% 35%已、未知:χ% 33.33%列比例式得:100%/χ%=35%/33.33%χ%=33.33%×100%/35%=95.23%设样品质量为100g,其中所含硝铵的质量为χ关系式:样品~NH4NO3~2N关系量:80 14×2已、未知:100g χ33.33 g列比例式得:80/χ=28/33.33gχ=33.33g×80/28=95.23g即χ%=95.23%答:该化肥样品中硝铵的纯度为95.23%。

中考化学化学式的计算专题卷(附答案)学校:___________姓名:___________班级:___________考号:___________一、选择题的化学式为SeO3,其中Se的化合价是A.+6 B.+3 C.-3 D.-62.氧化钙和碳酸钙的固体混合物质量为100g,将其高温煅烧至碳酸钙完全分解,称得剩余固体的质量为70g。
则原固体混合物中钙元素的质量分数为A.20% B.40% C.50% D.70%3.治疗手足口病的常用药物阿昔洛韦化学式为:C8H11N5O3.下列有关说法不正确的是()A.阿昔洛韦属于有机化合物B.阿昔洛韦的相对分子质量为225C.阿昔洛韦中C、H、N、O三种元素的质量比为8:11:5:3D.阿昔洛韦的一个分子中含有27个原子4.下列物质中氯元素的元素化合价最高的是()A.HClO2 B.Cl2 C.HCl D.HClO35.据报道,用于清洗龙虾的“洗虾粉”中含有柠檬酸钠、亚硫酸钠(Na2SO3)等物质,可能对人体的健康产生危害.Na2SO3中S元素的化合价为()A.+6 B.+4 C.+2 D.﹣26.据报道,目前有中学生喜欢用涂改液,经实验证明涂改液中含有许多挥发性气体的有害物质,人吸入后容易引起慢性中毒而头痛,严重者抽搐,呼吸困难。
其中二氯甲烷(CH2Cl2)就是其中的一种,下列关于的叙述正确的是()A、二氯甲烷是由碳、氢、氯三种元素组成的化合物B、二氯甲烷是由甲烷和氯气组成的混合物C、二氯甲烷中含1个碳原子、2个氢原子、2个氯原子D、二氯甲烷中碳、氢、氯元素质量比为1:2:27.绿茶中的单宁酸(化学式为C76H52O46)具有抑制血压上升、清热解毒、抗癌等功效,下列说法错误的是()A.单宁酸属于化合物B.单宁酸由碳、氢、氧三种元素组成C.单宁酸分子的相对分子质量为1700gD.一个单宁酸分子由76个碳原子、52个氢原子和46个氧原子构成8.现有32 g某可燃物在密闭容器中完全燃烧后,测得生成88 g二氧化碳和72 g水,关于该可燃物的说法正确的是()A.一定是氧化物B.只含有碳、氢两种元素C.一定含有碳、氢、氧三种元素D.一定含有碳、氢元素,可能含有氧元素9.用CO2和NH3合成尿素【CO(NH2)2】是固定和利用CO2的成功范例,其反应的化学方程式为:CO2+2NH3═CO(NH2)2+H2O.下列说法正确的是A.尿素中有2个氮原子B.尿素的相对分子质量是60gC.参加反应的CO2与NH3的质量比是44:17D.该反应是充分利用CO2的一种有效途径10.某无土栽培的营养液中含有磷酸钾(K3PO4)。

初中化学式计算题型精选题型1、求相对分子质量1、求下列物质的相对分子质量(1)KHCO3;(2)Cu2(OH)2CO3;(3)KAl(SO4)2·12H2O(4)4 CO(NH2)2;(5)3Mg2+(6) 5SO42- 。
题型2、求元素质量比2、求下列物质的各元素质量比(1)三硝基甲苯是TNT黄色炸药的主要成分,它的化学式为C6H5CH3(NO2)3,求三硝基甲苯中碳元素和氢元素的质量比是_____________。
(2)C2H5OH;(3)Fe2(SO4)3;题型3、求化合物中元素质量分数4、求下列常见氮肥中的氮元素质量分数。
(1)尿素[CO(NH2)2];(2)硝酸铵[NH4NO3];(4)硫酸铵[(NH4)2SO4];题型4、由化合物质量,求元素的质量5、3.6g水中含有的氢元素质量是多少g?6、25 g碳酸钙[CaCO3]含有的钙元素是多少g?7、6kg尿素[CO(NH2)2]所含的氮元素是多少kg?题型5、由元素的质量,求化合物质量8、多少g水中含有的氢元素质量是1g?9、人们常采用吃含碳酸钙药物的方法补钙,若要补钙4mg,需要食用多少mg 的碳酸钙?题型6、两化合物同元素质量相当,求某化合物质量10、多少g水所含氢元素的质量与1.7g氨气[NH3]所含氢元素的质量相等?11、多少g硝酸铵所含氮元素与12g尿素所含氮元素质量相当?12、多少g四氧化三铁所含铁元素质量是16g三氧化二铁中铁元素质量的两倍?13、农民用尿素给耕地的玉米施加氮肥,刚好需要120kg尿素,若改施用碳酸氢铵[NH4HCO3]达到相同的肥效,则需要碳酸氢铵的质量是多少?题型7、求原子个数比14、醋酸的化学式为CH3COOH,则碳、氢、氧原子个数比是__________;15、尿素[CO(NH2)2]中碳、氢、氧、氮四种原子个数比是__________;题型8、已知取一定数目的不同分子,求相同元素的原子个数比16、相同分子数的水分子和二氧化碳分子中,两者氧原子个数比是__________;17、32个氧气分子和25个臭氧分子中,两者氧原子个数比是__________;18、各取n个二氧化硫分子和m个三氧化硫分子,两者的氧原子个数比是____________。

化学式的计算专题训练相对原子质量:(H=1 O=16 S=32 Ca=40 C=12 Cu=63.5 Mg=24 N=14 Zn=65 Cl=35.5)一、计算相对分子质量:①H2②NaCl③MgCl2④Cu(OH)2⑤NH4NO3⑥NH4HCO3⑦C6H8O6⑧3CO(NH2)2⑨2C60二、化学式中各元素的原子个数比:①氯化钠(NaCl)中氯元素和钠元素的原子个数比是:②氯化镁(MgCl2)中氯元素和镁元素的原子个数比是:③氢氧化铜(Cu(OH)2)中铜元素、氧元素和氢元素的原子个数比是:④硝酸铵(NH4NO3)中氮元素、氢元素和氧元素的原子个数比是:⑤维生素C(C6H8O6)中碳元素、氢元素和氧元素的原子个数比是:三、计算物质组成元素的质量比:例3:计算水(H2O)中氢元素和氧元素的质量比。
解:H :O = 1×2 :16 = 2 :16 = 1 :8①氯化钠(NaCl)中氯元素和钠元素的质量比是:;②氯化镁(MgCl2)中氯元素和镁元素的质量比是:;③氢氧化铜(Cu(OH)2)中铜元素、氧元素和氢元素的质量比是:;④硝酸铵(NH4NO3)中氮元素、氢元素和氧元素的质量比是:;⑤维生素C(C6H8O6)中碳元素、氢元素和氧元素的质量比是:;⑥硫酸铵[(NH4)2SO4] 中氮、氢、硫、氧四种元素的质量比是:。
四、计算物质中某元素的质量分数:例4.计算二氧化碳(CO2)中氧元素的质量分数。
解:CO2的相对分子质量=12+16×2=44O% =44216×100% = 72.7% 练习:一、选择题1. Y2BaCu6O10是一种高温超导材料。
该化合物中,Y、Ba、O三种元素的化合价依次为+3、+2、-2价,则铜元素的化合价为()A.0价 B.+1价 C.+2价 D.+3价2. 鱼油中富含的DHA(C22H32O2)是大脑细胞形成和发育不可缺少的物质,下列关于DHA的叙述中不正确的是()A.DHA由三种元素组成 B.DHA是有机化合物C.DHA中碳、氢、氧三种元素的质量比为33︰4︰4D.DHA中氢元素的质量分数最大3. 钛铁矿主要成分的化学式为Fe TiOx,其中铁元素和钛元素的化合价均显+3价。


化学式的计算专题训练姓名:班别:座号:相对原子质量:(H=1 O=16 S=32 Ca=40 C=12 Cu=63.5 Mg=24 N=14 Zn=65 Cl=35.5)一、计算相对分子质量:例1:计算下列物质的相对分子质量①氧气(O2)②硫酸(H2SO4)③氢氧化钙[ Ca(OH)2 ]解:①O2的相对分子质量=16×2=32②H2SO4的相对分子质量=1×2+32+16×4=98③Ca(OH)2的相对分子质量=40+(16+1)×2=74练习:1.计算下列物质的相对分子质量。
①H2②NaCl③NaOH④Ca(OH)2⑤NH4NO3⑥NH4HCO3⑦H2SO4⑧CO(NH2)2⑨2C60⑩CaCO3二、化学式中各元素的原子个数比:例2:计算水(H2O)中氢元素和氧元素的原子个数比。
解:H :O = 2 :1练习:2.计算下列物质中各元素的原子个数比。
①氯化钠(NaCl)中氯元素和钠元素的原子个数比是:②氯化镁(MgCl2)中氯元素和镁元素的原子个数比是:③氢氧化铜(Cu(OH)2)中铜元素、氧元素和氢元素的原子个数比是:④硝酸铵(NH4NO3)中氮元素、氢元素和氧元素的原子个数比是:⑤维生素C(C6H8O6)中碳元素、氢元素和氧元素的原子个数比是:三、计算物质组成元素的质量比:例3:计算水(H2O)中氢元素和氧元素的质量比。
解:H :O = 1×2 :16 = 2 :16 = 1 :8练习:3.计算下列物质中各元素的质量比。
①氯化钠(NaCl)中氯元素和钠元素的质量比是:;②氯化镁(MgCl2)中氯元素和镁元素的质量比是:;③氢氧化铜(Cu(OH)2)中铜元素、氧元素和氢元素的质量比是:;④硝酸铵(NH4NO3)中氮元素、氢元素和氧元素的质量比是:;⑤维生素C(C6H8O6)中碳元素、氢元素和氧元素的质量比是:;⑥硫酸铵[(NH4)2SO4] 中氮、氢、硫、氧四种元素的质量比是:。

关于化学式的计算例题:一、相对分子质量:化学式中各原子的相对原子质量的总和。
某物质的相对分子质量=A 原子的相对原子质量×A 原子个数+B 原子的相对原子质量×B 原子个数+…例1. 计算水【H 2O 】、硫酸铝【Al 2(SO 4)3】、胆矾【CuSO 4·5H 2O 】的相对分子质量。
解:H 2O 的相对分子质量=1×2+16×1=18Al 2(SO 4)3的相对分子质量=27×2+(32+16×4)×3=342CuSO 4·5H 2O 的相对分子质量=64+32+16×4+5×(1×2+16)=250例2. 计算3SO 2、2NH 4HCO 3的相对分子质量总和。
解:3SO 2的相对分子质量总和=3×(32+16×2)=1922NH 4HCO 3的相对分子质量总和=2×(14+1×5+12+16×3)=158二.根据化学式计算化合物中各元素的质量比化合物中各元素的质量比等于各元素的相对原子质量的和之比例1. 计算水(H 2O)中各元素的质量比解:水中氢元素与氧元素的质量比为:(1×2) ﹕16=2﹕16=1﹕8也可表示为:H 2O 中H ﹕O=(1×2) ﹕16=2﹕16=1﹕8例2. 计算硫酸铵【(NH 4)2SO 4】中各元素的原子个数比及各元素的质量比。
解:(NH 4)2SO 4中N :H :S :O=(14×2):(1×8):32:(16×4)=28:8:32:64=7:2:8:16三、计算化合物中某元素的质量分数:%100⨯⨯=化合物的相对分子质量原子个数某元素的相对原子质量某元素的质量分数 例1:计算碳酸氢铵【NH 4HCO 3】中氮元素的质量分数.解:%7.17%1007914%100%34=⨯=⨯=HCO NH N N 答: 碳酸氢铵中氮元素的质量分数为17.7%。

化学化学式的计算练习题化学式是化学元素组成化合物的简化表示法,它能够明确地表示出其中所含元素以及它们的相对比例。
化学式的计算是化学中的基础知识,它需要我们掌握有关元素的原子量以及化合物的相对分子量。
以下是几个化学化学式的计算练习题,通过这些练习题的实践,我们可以更好地巩固和加深对化学式计算的理解。
练习题一:计算硫酸二铁的化学式硫酸是由硫元素、氧元素和氢元素组成的化合物,其化学式为H₂SO₄。
而二价铁离子为Fe²⁺,根据阿伦尼乌斯规则,它与氧元素形成的化合物中,每个氧原子与两个金属离子相结合。
因此,硫酸二铁的化学式为FeSO₄。
练习题二:计算乙酸钠的化学式乙酸是由碳元素、氢元素和氧元素组成的化合物,其化学式为CH₃COOH。
钠离子为Na⁺。
在乙酸钠中,一个乙酸离子中的一个氢原子被钠离子所取代,形成CH₃COONa。
因此,乙酸钠的化学式为C₂H₃O₂Na。
练习题三:计算硫酸镁的化学式硫酸是由硫元素、氧元素和氢元素组成的化合物,其化学式为H₂SO₄。
镁离子为Mg²⁺。
在硫酸镁中,一个硫酸离子中的一个氢原子被镁离子所取代,形成MgSO₄。
因此,硫酸镁的化学式为MgSO₄。
练习题四:计算氧化铜的化学式氧化铜是由铜元素和氧元素组成的化合物。
根据化合价的原则,铜的化合价为+2,氧的化合价为-2。
因此,氧化铜的化学式为CuO。
练习题五:计算硫化铁的化学式硫化铁是由铁元素和硫元素组成的化合物。
根据化合价的原则,铁的化合价为+2,硫的化合价为-2。
因此,硫化铁的化学式为FeS。
通过对以上化学式的计算练习,我们可以看到,化学式的计算需要根据元素的化合价以及离子的配位规律进行推导。
通过大量的练习,我们可以更加熟练地进行化学式的推导和计算,并深入理解元素间相对比例的关系。
总结:化学式的计算是化学中的基础知识,通过对化学式的练习题的实践,可以加深对元素化合物组成方式的理解。
在进行化学式计算时,需要掌握好元素的原子量以及化合物的相对分子量,并根据化合价和离子配位规律进行推导。

初三化学化学计算题专题训练答案及解析一、有关化学式的计算1、计算尿素CO(NH₂)₂中氮元素的质量分数。
答案:尿素中氮元素的质量分数=(氮原子的相对原子质量×氮原子个数)÷尿素的相对分子质量×100%氮原子的相对原子质量为 14,尿素的化学式为 CO(NH₂)₂,其中氮原子个数为 2。
尿素的相对分子质量= 12 + 16 +(14 + 1×2)×2 = 60氮元素的质量分数=(14×2)÷60×100% ≈ 467%解析:要计算化合物中某元素的质量分数,就用该元素原子的相对原子质量乘以原子个数,再除以化合物的相对分子质量,最后乘以100%。
在尿素中,明确氮原子的个数以及各原子的相对原子质量,按照公式准确计算即可。
2、已知氧化铁(Fe₂O₃)的相对分子质量为 160,求其中铁元素与氧元素的质量比。
答案:铁元素与氧元素的质量比=(铁原子的相对原子质量×铁原子个数)∶(氧原子的相对原子质量×氧原子个数)铁原子的相对原子质量为 56,氧原子的相对原子质量为 16。
氧化铁中,铁原子个数为 2,氧原子个数为 3。
铁元素与氧元素的质量比=(56×2)∶(16×3)= 7∶3解析:计算化合物中各元素的质量比,同样要依据各元素原子的相对原子质量和原子个数。
先分别算出铁元素和氧元素的质量,然后相比得出质量比。
二、有关化学方程式的计算1、加热分解 63g 高锰酸钾,可以得到多少克氧气?答案:设可以得到氧气的质量为 x。
2KMnO₄=△= K₂MnO₄+ MnO₂+ O₂↑316 3263g x316 / 63g = 32 / xx = 064g解析:首先写出高锰酸钾受热分解的化学方程式。
根据化学方程式找出高锰酸钾与氧气的质量比,然后设出未知量氧气的质量为 x,列出比例式进行求解。
2、实验室用 10g 碳酸钙与足量的稀盐酸反应,可制得多少克二氧化碳?答案:设生成二氧化碳的质量为 y。

化学式综合计算(人教版)试卷简介:在对化学式相关计算基本公式灵活运用的基础上,掌握综合计算的方法和解题思路。
一、单选题(共5道,每道10分)1.治疗禽流感的特效药帕拉米韦氯化钠注射液,临床证明其对H7N9型的禽流感病毒有明确疗效。
帕拉米韦的化学式为C x H28N4O4,相对分子质量为328。
则x为( )A.12B.13C.14D.152.丙氨酸是一种氨基酸,其相对分子质量是89,其中氮元素的质量分数为15.8%,则每个丙氨酸分子中含氮原子的个数为( )A.4B.3C.2D.13.已知氮的氧化物A中氮、氧元素的质量比为7:4,则A的化学式为( )A.NOB.N2OC.NO2D.N2O54.某物质中碳、氢两种元素的质量分别为6g和1g,则该物质的化学式不可能为( )A.C2H2B.C2H4C.C3H6D.CH2O5.已知硫的一种氧化物,其中含硫元素的质量分数为50%,则该氧化物中硫元素的化合价为( )A.-2B.+2C.+4D.+6二、填空题(共3道,每道15分)6.某物质由碳、氢两种元素组成,其中碳元素的质量分数为75%,则该物质中碳、氢元素的原子个数比为____。
7.地震过后,防疫部门常用到一种高效安全灭菌消毒剂,该消毒剂可表示为RO2,主要用于饮用水消毒。
实验测得该氧化物中R与O的质量比为3:8,则R的相对原子质量为____。
8.某有机物由碳、氢、氧三种元素组成,相对分子质量为102,其中氢元素的质量分数为9.8%,且每个分子中氢原子个数为氧原子个数的5倍,则该有机物的一个分子中碳、氢、氧原子的个数分别为____、____、____。

五年级化学化学式计算练习题及讲解化学式计算是化学中非常重要的基础知识,通过计算不同元素之间的化学式,我们可以准确地表示出不同物质的组成与结构。
对于五年级的学生而言,了解和掌握化学式计算的方法,是培养科学思维和提升化学素养的重要一环。
本文将为五年级学生提供一些化学式计算的练习题及其详细讲解,帮助他们更好地掌握这一知识点。
练习题一:求下列物质的化学式。
1. 氢气和氧气混合后所得的物质。
2. 一氧化氮和二氧化氮混合后所得的物质。
3. 青石和稀硫酸反应后所得的物质。
4. 金属锌和硫酸反应后所得的物质。
5. 乙醇和醋酸反应后所得的物质。
讲解一:化学式的计算是根据不同元素的化合价进行的。
化合价是指一个元素在化合物中所呈现的价态,化合价可以是正的也可以是负的。
根据化合价,我们可以推导出不同元素之间的化学式。
1. 氢气和氧气是两种气体,混合后得到的物质是水。
水的化学式为H2O,其中氢的化合价为+1,氧的化合价为-2。
2. 一氧化氮和二氧化氮是由氮和氧组成的气体。
根据化合价的规律,氮的化合价为+1或-3,氧的化合价为-2。
由于一氧化氮和二氧化氮是由相同的元素组成,它们的化合价之和应为0。
因此,一氧化氮的化合价为+1,二氧化氮的化合价为-2,它们的化学式分别为NO和NO2。
3. 青石是由铜、氧和硅组成的矿石,化学式为Cu2SiO4。
根据化合价的规律,铜的化合价为+2,氧的化合价为-2,硅的化合价为+4。
在化学式中,化合价的绝对值应当相互抵消,得到Cu2SiO4。
4. 金属锌和硫酸反应后生成硫酸锌。
硫酸锌的化学式为ZnSO4。
锌的化合价为+2,硫的化合价为+6,根据电中性原理,硫酸锌的化合价应为0,因此硫酸锌的化学式为ZnSO4。
5. 乙醇和醋酸反应后生成乙酸。
乙酸的化学式为CH3COOH。
乙醇和醋酸的共同结构为CH3,而乙酸是在此基础上添加一个COOH基团而形成的。
根据化合价的规律,碳的化合价为+4,氧的化合价为-2,氢的化合价为+1。

初三化学化学计算题专项训练及答案一、有关化学式的计算1、计算相对分子质量相对分子质量等于化学式中各原子的相对原子质量总和。
例 1:计算硫酸(H₂SO₄)的相对分子质量。
解:氢(H)的相对原子质量约为 1,硫(S)的相对原子质量约为32,氧(O)的相对原子质量约为 16。
硫酸的相对分子质量= 2×1 + 32 + 4×16 = 98练习 1:计算碳酸钙(CaCO₃)的相对分子质量。
答案:钙(Ca)的相对原子质量约为 40,碳(C)的相对原子质量约为 12,氧(O)的相对原子质量约为 16。
碳酸钙的相对分子质量= 40 + 12 + 3×16 = 1002、计算物质组成元素的质量比物质中各元素的质量比等于各元素的相对原子质量乘以原子个数之比。
例 2:计算水(H₂O)中氢元素和氧元素的质量比。
解:氢元素的相对原子质量约为1,氧元素的相对原子质量约为16。
水(H₂O)中氢元素和氧元素的质量比=(2×1)∶(1×16)=1∶8练习 2:计算二氧化碳(CO₂)中碳元素和氧元素的质量比。
答案:碳元素的相对原子质量约为 12,氧元素的相对原子质量约为16。
二氧化碳(CO₂)中碳元素和氧元素的质量比=(1×12)∶(2×16)= 3∶83、计算物质中某元素的质量分数某元素的质量分数=(该元素的相对原子质量×原子个数÷相对分子质量)×100%例 3:计算硝酸铵(NH₄NO₃)中氮元素的质量分数。
解:氮(N)的相对原子质量约为 14,氢(H)的相对原子质量约为 1,氧(O)的相对原子质量约为 16。
硝酸铵的相对分子质量= 14×2 + 1×4 + 16×3 = 80氮元素的质量分数=(14×2÷80)×100% = 35%练习 3:计算尿素CO(NH₂)₂中氮元素的质量分数。

化学式计算专题训练一、根据化学式计算相对分子质量1. 题目- 计算水(H_2O)的相对分子质量。
- 计算碳酸钙(CaCO_3)的相对分子质量。
- 计算硫酸(H_2SO_4)的相对分子质量。
解析- 对于水(H_2O):- 相对分子质量等于各原子相对原子质量之和。
- 氢原子(H)的相对原子质量约为1,氧原子(O)的相对原子质量约为16。
- 水的相对分子质量M = 2×1+16 = 18。
- 对于碳酸钙(CaCO_3):- 钙原子(Ca)的相对原子质量约为40,碳原子(C)的相对原子质量约为12,氧原子(O)的相对原子质量约为16。
- 碳酸钙的相对分子质量M = 40 + 12+3×16=100。
- 对于硫酸(H_2SO_4):- 氢原子(H)的相对原子质量约为1,硫原子(S)的相对原子质量约为32,氧原子(O)的相对原子质量约为16。
- 硫酸的相对分子质量M = 2×1+32 + 4×16=98。
二、根据化学式计算元素的质量比1. 题目- 计算水(H_2O)中氢元素和氧元素的质量比。
- 计算二氧化碳(CO_2)中碳元素和氧元素的质量比。
- 计算硝酸铵(NH_4NO_3)中氮、氢、氧三种元素的质量比。
解析- 对于水(H_2O):- 氢元素和氧元素的质量比等于它们的相对原子质量乘以原子个数之比。
- 氢原子(H)的相对原子质量约为1,氧原子(O)的相对原子质量约为16,氢原子个数为2,氧原子个数为1。
- 氢元素和氧元素的质量比=(1×2):16 = 1:8。
- 对于二氧化碳(CO_2):- 碳元素(C)的相对原子质量约为12,氧原子(O)的相对原子质量约为16,碳原子个数为1,氧原子个数为2。
- 碳元素和氧元素的质量比=12:(16×2)=3:8。
- 对于硝酸铵(NH_4NO_3):- 氮原子(N)的相对原子质量约为14,氢原子(H)的相对原子质量约为1,氧原子(O)的相对原子质量约为16。
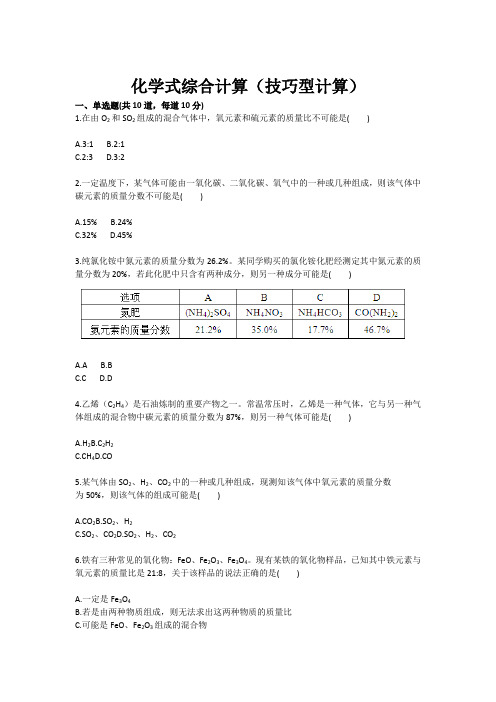
化学式综合计算(技巧型计算)一、单选题(共10道,每道10分)1.在由O2和SO2组成的混合气体中,氧元素和硫元素的质量比不可能是( )A.3:1B.2:1C.2:3D.3:22.一定温度下,某气体可能由一氧化碳、二氧化碳、氧气中的一种或几种组成,则该气体中碳元素的质量分数不可能是( )A.15%B.24%C.32%D.45%3.纯氯化铵中氮元素的质量分数为26.2%。
某同学购买的氯化铵化肥经测定其中氮元素的质量分数为20%,若此化肥中只含有两种成分,则另一种成分可能是( )A.AB.BC.CD.D4.乙烯(C2H4)是石油炼制的重要产物之一。
常温常压时,乙烯是一种气体,它与另一种气体组成的混合物中碳元素的质量分数为87%,则另一种气体可能是( )A.H2B.C2H2C.CH4D.CO5.某气体由SO2、H2、CO2中的一种或几种组成,现测知该气体中氧元素的质量分数为50%,则该气体的组成可能是( )A.CO2B.SO2、H2C.SO2、CO2D.SO2、H2、CO26.铁有三种常见的氧化物:FeO、Fe2O3、Fe3O4。
现有某铁的氧化物样品,已知其中铁元素与氧元素的质量比是21:8,关于该样品的说法正确的是( )A.一定是Fe3O4B.若是由两种物质组成,则无法求出这两种物质的质量比C.可能是FeO、Fe2O3组成的混合物D.该样品组成有两种情况7.由MgSO3、MgSO4组成的混合物中硫元素的质量分数为32%,则混合物中镁元素的质量分数为( )A.24%B.44%C.40%D.28%8.由MgSO4、Fe2(SO4)3、K2SO4三种物质组成的混合物,测得其中硫元素的质量分数为a%,则混合物中金属元素的质量分数为( )A. B.C. D.9.经测定,由甲醛(CH2O)、醋酸(CH3COOH)和丙酮(CH3COCH3)组成的混合物中,氢元素的质量分数为X%,则其混合物中氧元素的质量分数是( )A.0.5X%B.1-1.5X%C.1-7X%D.2X%10.NaHCO3和MgCO3的相对分子质量都是84,将它们以任意比混合后,测出碳元素的质量分数为1/7,则氧元素的质量分数为( )A.1/7B.2/7C.3/7D.4/7。

初一化学化学式的计算试题1.下列各物质中碳元素质量分数最大的是()A.CO B.CaCO3C. Na2CO3D.CO2【答案】A【解析】根据物质的化学式可以计算出物质中元素的质量分数,再通过比较就能得出本题的答案.解:一氧化碳中碳元素的质量分数为×100%;碳酸钙中碳元素的质量分数为×100%;碳酸钠中碳元素的质量分数为×100%;二氧化碳中碳元素的质量分数为×100%,由于上述四个质量分数的分子均相等,分母中一氧化碳的最小,因此一氧化碳中碳元素的质量分数最大.故选A.【考点】元素的质量分数计算.点评:本题主要考查化合物中元素的质量分数的计算,难度较小.2.下列关于耐高温新型陶瓷氮化硅(Si3N4)的叙述正确的是()A.氮化硅中Si、N两种元素的质量比为3:4 B.氮化硅中氮元素的质量分数为40% C.140g氮化硅中含硅元素的质量为84g D.氮化硅的相对分子质量为140g【答案】BC【解析】根据氮化硅的化学式为Si3N4,利用元素原子的相对原子质量和原子个数来进行计算.解:A、氮化硅中Si、N两种元素的质量比为28×3:14×4=3:2,故A错误;B、氮化硅中氮元素的质量分数为×100%=40%,故B正确;C、140g氮化硅中含硅元素的质量=140g××100%=84g,故C正确;D、氮化硅的相对分子质量=28×3+14×4=140≠140g,故D不正确;故选BC.【考点】有关化学式的计算和推断;化合物中某元素的质量计算.点评:根据物质的化学式可以表示物质的组成和构成,利用化学式中各元素原子的相对原子质量和原子个数可完成与化学式相关的计算.3.小明要到农资公司买8Kg的化肥硝酸铵,其中有效成分为氮元素,但是当时没有硝酸铵了,如果要是改为购买尿素,要想氮元素质量相等,则需要购买尿素Kg.【答案】[NH4NO3] [CO(NH2)2] 6【解析】首先明确尿素和硝酸铵的肥效必须相同,肥效相同即是含氮量相同,即8kg硝酸铵中含氮元素的质量必须和尿素中含氮元素的质量相同.解:尿素[CO(NH2)2]的相对分子质量是12+16+(14+2)×2=60;硝酸铵[NH4NO3]分子的相对质量为14+4+14+16×3=80;8kg尿素中含氮元素的质量为:8kg×(×100%)=2.8kg;设需要购买尿素的质量为x,则x•(×100%)=2.8kg;解之得:x=6Kg.故答案为:6.【考点】化合物中某元素的质量计算.点评:解答本题要明确确尿素和硝酸铵的肥效必须相同,肥效相同即是含氮量相同,只有这样才能建立数据之间的联系.4.不同年龄段的群体每天钙的适宜摄入量不同,哺乳期妇女每日推荐摄入量为1200mg、如图为某保健品说明书的一部分,请回答:(1)维生素D3的化学式为C27H44O,则维生素D3的相对分子质量是.(2)每片药片含钙mg.【答案】(1)384;(2)600.【解析】(1)根据相对分子质量为构成分子的各原子的相对原子质量之和,进行分析解答.(2)由题意,每片中含碳酸钙1.5g,根据化合物中某元素的质量=该化合物的质量×该元素的质量分数,进行分析解答.解:(1)维生素D3的相对分子质量是12×27+1×44+16=384.(2)由题意,每片中含碳酸钙1.5g,含钙元素的质量为1.5g×100%=0.6g=600mg.故答案为:(1)384;(2)600.【考点】标签上标示的物质成分及其含量;相对分子质量的概念及其计算;化合物中某元素的质量计算.点评:本题难度不大,考查同学们结合标签新信息、灵活运用化学式的有关计算进行分析问题、解决问题的能力.5.2008年,粮食问题成为被世界关注的热点之一.粮食的主要成分是淀粉,淀粉进入人体后,在酶的作用下转化为可被人体吸收的葡萄糖.葡萄糖的化学式为C6H12O6,则葡萄糖中碳、氢、氧元素的质量比为;碳元素的质量分数为.180g葡萄糖中含碳元素g.【答案】6:1:8;40%;72【解析】根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,化合物中元素的质量分数=×100%,化合物中某元素的质量=该化合物的质量×该元素的质量分数,进行分析解答.解:葡萄糖中碳、氢、氧元素的质量比为(12×6):(1×12):(16×6)=6:1:8.碳元素的质量分数为100%=40%.180g葡萄糖中含碳元素的质量为180g×40%=72g.故答案为:6:1:8;40%;72.【考点】元素质量比的计算;元素的质量分数计算;化合物中某元素的质量计算.点评:本题难度不大,考查同学们灵活运用化学式的有关计算进行分析问题、解决问题的能力.6.铝土矿的主要成分是Al2O3,请按要求进行计算:(1)Al2O3中铝元素与氧元素的原子个数比为.(2)Al2O3中铝元素与氧元素的质量比为.(3)求Al2O3中铝元素的质量分数(计算结果保留至0.1%)【答案】(1)2:3;(2)9:8;(3)52.9%.【解析】(1)根据Al2O3中铝元素与氧元素的原子个数进行分析解答.(2)根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析解答.(3)根据化合物中元素的质量分数=×100%,进行分析解答.解:(1)Al2O3中铝元素与氧元素的原子个数比为2:3.(2)Al2O3中铝元素与氧元素的质量比为(27×2):(16×3)=9:8.(3)Al2O3中铝元素的质量分数100%≈52.9%.故答案为:(1)2:3;(2)9:8;(3)52.9%.【考点】元素质量比的计算;元素的质量分数计算.点评:本题难度不大,考查同学们灵活运用化学式的有关计算进行分析问题、解决问题的能力.7.下列各物质中碳元素质量分数最大的是()A.CO B.CaCO3C.Na2CO3D.CO2【答案】A【解析】根据物质的化学式可以计算出物质中元素的质量分数,再通过比较就能得出本题的答案.解:一氧化碳中碳元素的质量分数为×100%;碳酸钙中碳元素的质量分数为×100%;碳酸钠中碳元素的质量分数为×100%;二氧化碳中碳元素的质量分数为×100%,由于上述四个质量分数的分子均相等,分母中一氧化碳的最小,因此一氧化碳中碳元素的质量分数最大.故选A.【考点】元素的质量分数计算.点评:本题主要考查化合物中元素的质量分数的计算,难度较小.8.小明要到农资公司买8Kg的化肥硝酸铵[NH4NO3],其中有效成分为氮元素,但是当时没有硝酸铵了,如果要是改为购买尿素[CO(NH2)2],要想氮元素质量相等,则需要购买尿素Kg.【答案】6【解析】首先明确尿素和硝酸铵的肥效必须相同,肥效相同即是含氮量相同,即8kg硝酸铵中含氮元素的质量必须和尿素中含氮元素的质量相同.解:尿素[CO(NH2)2]的相对分子质量是12+16+(14+2)×2=60;硝酸铵[NH4NO3]分子的相对质量为14+4+14+16×3=80;8kg尿素中含氮元素的质量为:8kg×(×100%)=2.8kg设需要购买尿素的质量为x,则x•(×100%)=2.8kg解之得:x=6Kg故答案为:6.【考点】化合物中某元素的质量计算.点评:解答本题要明确确尿素和硝酸铵的肥效必须相同,肥效相同即是含氮量相同,只有这样才能建立数据之间的联系.9.某氧化物由氮元素与氧元素组成,氮元素与氧元素的质量比为7:20,则此氧化物的化学式为.【答案】N2O5【解析】根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,结合题意进行分析解答.解:某氧化物由氮元素与氧元素组成,设此氧化物的化学式为Nx Oy,由氮元素与氧元素的质量比为7:20,则14x:16y=7:20,则x:y=2:5;则此氧化物的化学式为N2O5.故答案为:N2O5.【考点】元素质量比的计算.点评:本题难度不大,考查同学们灵活运用化学式的有关计算进行分析问题、解决问题的能力.10.“苹(凭)什么”是继“蒜(算)你狠”、“逗(豆)你玩”之后又一网络流行语,说的是近日苹果价格激增。