新人教版九年级化学方程式汇总(1-9单元)
- 格式:doc
- 大小:84.00 KB
- 文档页数:6

九年级—-化学方程式及现象汇总(上册课本)一、化合反应:1、镁在空气中燃烧:2Mg + O2点燃 2MgO现象:(1)发出耀眼的白光(2)放出热量(3)生成白色粉末2、铁在氧气中燃烧:3Fe + 2O2点燃 Fe3O4现象:(1)剧烈燃烧,火星四射(2)放出热量(3)生成一种黑色固体注意:瓶底要放少量水或细沙,防止生成的固体物质溅落下来,炸裂瓶底.3、铜在空气中受热:2Cu + O2△2CuO 现象:铜丝变黑。
4、铝在氧气中燃烧:4Al + 3O2点燃 2Al2O3现象:发出耀眼的白光,放热,有白色固体生成.5、氢气中空气中燃烧或爆炸:2H2 + O2点燃 2H2O现象:(1)产生淡蓝色火焰(2)放出热量(3)烧杯内壁出现水雾。
6、红(白)磷在空气中燃烧:4P + 5O2点燃 2P2O5现象:(1)发出白光(2)放出热量(3)生成大量白烟。
7、硫粉在空气中燃烧: S + O2点燃 SO2现象:(注意两种现象有差异)A、在纯的氧气中发出明亮的蓝紫火焰,放出热量,生成一种有刺激性气味的气体。
B、在空气中燃烧(1)发出淡蓝色火焰(2)放出热量(3)生成一种有刺激性气味的气体。
8、碳在氧气中充分燃烧:C + O2点燃 CO2现象:(1)发出白光(2)放出热量(3)澄清石灰水变浑浊9、碳在氧气中不充分燃烧:2C + O2点燃 2CO10、二氧化碳通过灼热碳层: C + CO2高温 2CO(吸热反应)上册111页11、一氧化碳在氧气中燃烧:2CO + O2点燃 2CO2现象:发出蓝色的火焰,放热,澄清石灰水变浑浊。
12、二氧化碳和水反应(二氧化碳通入紫色石蕊试液):CO2 + H2O == H2CO3现象:石蕊试液由紫色变成红色。
注意:某些非金属氧化物+水→酸如:SO2 + H2O == H2SO3(亚硫酸) SO3 + H2O == H2SO4(硫酸)13、生石灰溶于水:CaO + H2O == Ca(OH)2(此反应放出热量)14、用无水硫酸铜鉴定水的存在:(化学方程式不用特别记忆,但要记得这种方法及现象CuSO4 + 5H2O = CuSO4·5H2O(五水硫酸铜,胆矾)现象:白色粉末变成蓝色二、分解反应:15、水在直流电的作用下分解:2H2O 通电 2H2↑+ O2↑现象:(1)电极上有气泡产生。

(完整版)人教版九年级化学中考全册化学方程式大全初中化学方程式一、氧气的性质:(1)单质与氧气的反应:(化合反应)1.镁在空气中燃烧:2Mg + O 2点燃 2MgO2.铁在氧气中燃烧:3Fe + 2O2点燃 Fe 3O43.铜在空气中受热:2Cu + O2 2CuO4.铝在空气中燃烧:4Al + 3O2点燃 2Al2O35.氢气中空气中燃烧:2H2 + O2点燃 2H2O6.红磷在空气中燃烧(研究空气组成的实验):4P + 5O2点燃 2P2O57.硫粉在空气中燃烧: S + O2点燃 SO28.碳在氧气中充分燃烧:C + O2点燃 CO2 (2)化合物与氧气的反应:10.一氧化碳在氧气中燃烧:2CO + O2点燃 2CO211.甲烷在空气中燃烧:CH4 + 2O2点燃 CO2 + 2H2O12.酒精在空气中燃烧:C2H5OH + 3O2点燃 2CO2 + 3H2O(3)氧气的来源:13. 拉瓦锡研究空气的成分实验2HgO Hg+ O2 ↑14. 加热高锰酸钾(实验室制氧气原理1)2KMnO4K2MnO4 + MnO2 + O2↑15. 过氧化氢在二氧化锰作催化剂条件下分解反应:2H2O2MnO22H2O+ O2 ↑(实验室制氧气原理2)16加热氯酸钾(二氧化锰):(实验室制氧气原理3)2KClO3 MnO22KCl+3O2↑二、自然界中的水:17. 水在直流电的作用下分解(研究水的组成实验):2H2O 通电2H2↑+ O2 ↑18. 生石灰溶于水:CaO + H2O === Ca(OH)219. 二氧化碳可溶于水:H2O + CO2=== H2CO3三、质量守恒定律:20. 镁在空气中燃烧:2Mg + O2点燃 2MgO21. 铁和硫酸铜溶液反应:Fe + CuSO4 === FeSO4 + Cu22. 氢气还原氧化铜:H2 + CuO Cu + H2O四、碳和碳的氧化物:(1)碳的化学性质23. 碳在氧气中充分燃烧:C + O2点燃 CO224.碳在氧气中不充分燃烧:2C + O2点燃 2CO25. 木炭还原氧化铜:C+ 2CuO 高温2Cu + CO2↑26. 焦炭还原氧化铁:3C+ 2Fe2O3高温4Fe + 3CO2↑(2)煤炉中发生的三个反应:(几个化合反应)27.煤炉的底层:C + O2点燃 CO228.煤炉的中层:CO2 + C高温2CO 29.煤炉的上部蓝色火焰的产生:2CO + O2点燃 2CO2(3)二氧化碳的制法与性质:30.大理石与稀盐酸反应(实验室制二氧化碳):CaCO3 + 2HCl === CaCl2 + H2O + CO2↑31.碳酸不稳定而分解:H2CO3 === H2O + CO2↑32.二氧化碳可溶于水:H2O + CO2=== H2CO333.高温煅烧石灰石(工业制二氧化碳):CaCO3高温CaO + CO2↑34.石灰水与二氧化碳反应(鉴别二氧化碳):Ca(OH)2 + CO2 ==== CaCO3↓+ H2O (4)一氧化碳的性质:35.一氧化碳还原氧化铜:CO+ CuO Cu + CO236.一氧化碳的可燃性:2CO + O2点燃 2CO 2其它反应:37.碳酸钠与稀盐酸反应(灭火器的原理): Na2CO3 + 2HCl === 2NaCl + H2O + CO2↑五、燃料及其利用:38.甲烷在空气中燃烧:CH4 + 2O2点燃 CO2 + 2H2O39.酒精在空气中燃烧:C2H5OH + 3O2点燃 2CO2 + 3H2O40.氢气中空气中燃烧:2H2 + O2点燃 2H2O六、金属(1)金属单质 + 氧气-------- 金属氧化物(化合反应)41.镁在空气中燃烧:2Mg + O2点燃2MgO 42.铁在氧气中燃烧:3Fe + 2O2点燃 Fe3O4 43. 铜在空气中受热:2Cu + O2 2CuO44. 铝在空气中形成氧化膜:4Al + 3O2 = 2Al2O3(2)金属单质 + 酸 -------- 盐 + 氢气(置换反应)45.锌和稀硫酸(实验室制氢气)Zn + H2SO4 = ZnSO4 + H2↑46.铁和稀硫酸Fe + H2SO4 = FeSO4 + H2↑47.镁和稀硫酸Mg + H2SO4 = MgSO4 + H2↑48.铝和稀硫酸2Al +3H2SO4 = Al2(SO4)3+3H2↑49.锌和稀盐酸Zn + 2HCl=== ZnCl2+ H2↑50.铁和稀盐酸Fe + 2HCl=== FeCl2+ H2↑51.镁和稀盐酸Mg+ 2HCl=== MgCl2 + H2↑52. 铝和稀盐酸2Al + 6HCl == 2AlCl3 + 3H2↑(3)金属单质 + 盐(溶液) ------- 新金属 + 新盐(置换反应)53.铁和硫酸铜溶液反应:Fe + CuSO4 === FeSO4 + Cu54.铝和硫酸铜溶液反应:2Al +3 CuSO4 === Al2(SO4)3 + 3Cu 55.铜和硝酸汞溶液反应:Cu + AgNO3 === Cu(NO3)2 + Ag(3)金属铁的治炼原理:56.赤铁矿炼铁原理:3CO+ 2Fe2O3高温4Fe + 3CO2↑七、酸、碱、盐1、酸的化学性质(1)酸 + 金属 -------- 盐 + 氢气(见上)(2)酸 + 金属氧化物-------- 盐 + 水(复分解反应)57. 氧化铁和稀盐酸反应(除铁锈):Fe2O3 + 6HCl === 2FeCl3 + 3H2O 58.氧化铁和稀硫酸反应(除铁锈):Fe2O3 + 3H2SO4 === Fe2(SO4)3+ 3H2O 59. 氧化铜和稀盐酸反应:CuO + 2HCl ==== CuCl2 + H2O 60.氧化铜和稀硫酸反应:CuO + H2SO4 ==== CuSO4 + H2O (3)酸 + 碱 -------- 盐+ 水(中和反应)61. 盐酸和烧碱起反应:HCl + NaOH ==== NaCl +H2O62. 盐酸和氢氧化钙反应:2HCl + Ca(OH)2 ==== CaCl2 + 2H2O 63. 氢氧化铝药物治疗胃酸过多:3HCl + Al(OH)3 ==== AlCl3 + 3H2O 64. 硫酸和烧碱反应:H2SO4 + 2NaOH ==== Na2SO4 + 2H2O (4)酸 + 盐 -------- 另一种酸 + 另一种盐(复分解反应)65.大理石与稀盐酸反应:CaCO3 + 2HCl === CaCl2 + H2O + CO2↑66.碳酸钠与稀盐酸反应:Na2CO3 + 2HCl === 2NaCl + H2O + CO2↑67.碳酸氢钠与稀盐酸反应:NaHCO3 + HCl=== NaCl + H2O + CO2↑68. 硫酸和氯化钡溶液反应:H2SO4 + BaCl2 ==== BaSO4↓+ 2HCl2、碱的化学性质(1)碱 + 非金属氧化物 -------- 盐 + 水69.苛性钠暴露在空气中变质:2NaOH + CO2 ==== Na2CO3 + H2O70.苛性钠吸收二氧化硫气体:2NaOH + SO2 ==== Na2SO3 + H2O71.苛性钠吸收三氧化硫气体:2NaOH + SO3 ==== Na2SO4 + H2O72.消石灰放在空气中变质:Ca(OH)2 + CO2 ==== CaCO3↓+ H2O73. 消石灰吸收二氧化硫:Ca(OH)2 + SO2 ==== CaSO3↓+ H2O(2)碱 + 酸-------- 盐 + 水(中和反应,方程式见上)(3)碱 + 盐 -------- 另一种碱 + 另一种盐(复分解反应)74. 氢氧化钙与碳酸钠:Ca(OH)2 + Na2CO3 === CaCO3↓+ 2NaOH3、盐的化学性质(1)盐(溶液)+ 金属单质------- 另一种金属+ 另一种盐(复分解反应)75. 铁和硫酸铜溶液反应:Fe + CuSO4 === FeSO4 + Cu(2)盐 + 酸-------- 另一种酸 + 另一种盐(复分解反应)76.碳酸钠与稀盐酸反应:Na2CO3 + 2HCl === 2NaCl + H2O + CO2↑碳酸氢钠与稀盐酸反应:NaHCO3 + HCl=== NaCl + H2O + CO2↑(3)盐 + 碱 -------- 另一种碱 + 另一种盐(复分解反应)77. 氢氧化钙与碳酸钠:Ca(OH)2 + Na2CO3 === CaCO3↓+ 2NaOH 78.氯化铵加熟石灰研磨:Ca(OH)2 + 2NH4Cl === CaCl2+2H2O+2NH3↑硫酸铵加熟石灰研磨:Ca(OH)2+(NH4)2SO4 === CaS O4+2H2O+2NH3↑(4)盐+ 盐 ----- 两种新盐(复分解反应)79.氯化钠溶液和硝酸银溶液:NaCl + AgNO3 ==== AgCl↓ + NaNO3 80.硫酸钠和氯化钡:Na2SO4 + BaCl2 ==== BaSO4↓ + 2NaCl。

中考复习资料总结九年级上册化学方程式及实验现象总结一、化合反应1、木炭(碳)在空气中燃烧现象:发出红光..,放出热量,生成能使澄清石灰水变浑浊的气体;在氧气中燃烧现象:发出白光..,放出热量,生成能使澄清石灰水变浑浊的气体。
C+O2点燃CO2(充分燃烧)2C+O2点燃 2 CO (不充分燃烧)2、硫在空气中燃烧现象:发出微弱的淡蓝色......火焰,生成有刺激性气味的气体,放出热量;在氧气中燃烧现象:发出明亮的蓝紫色......火焰,生成有刺激性气味的气体,放出热量。
S+O2点燃SO23、红磷(或者白磷)在空气中燃烧现象:产生大量白烟,放出热量。
4P+5O2点燃2P2O54、注意..铁丝在空气中不能燃烧;在氧气燃烧现象:剧烈燃烧,火星四射,生成黑色固体,放出热量。
3Fe+2O2点燃Fe3O45、镁带在空气中燃烧现象:发出耀眼的白光,冒白烟,生成白色粉末,放出热量。
2Mg+O2点燃2MgO6、氢气在空气(或氧气)中燃烧现象:发出淡蓝色火焰,放出热量,火焰上罩一个干而冷的烧杯,烧杯内壁出现水雾。
2H2+O2点燃2H2O7、铜在空气中加热现象:红色固体逐渐变成黑色2Cu+O2△2CuO8、一氧化碳在空气中燃烧现象:发出蓝色火焰,放出热量,火焰上罩一个涂有澄清石灰水的烧杯,澄清石灰水变浑浊。
2CO+O2点燃2CO29、汞在加热的条件下与氧气反应:2Hg+O2△2HgO10、铝在空气中燃烧:4Al+3O2点燃2Al2O311、二氧化碳通过灼热的碳层:CO2 +C高温2CO12、二氧化碳与水反应:CO2 +H2O == H2CO3(二氧化碳通入紫色石蕊试液,溶液变红的原因)二、分解反应1、氧化汞加热分解:2HgO△2Hg+O2↑2、高锰酸钾制氧气:2KMnO4△K2MnO4+MnO2+O2↑3、氯酸钾制氧气:2KClO3MnO22KCl+3O2↑△MnO24、过氧化氢制氧气:2H2O2 2H2O+O2↑5、电解水:2H2O通电2H2↑+O2↑6、碳酸不稳定,易分解:H2CO3 === H2O+CO2↑ (二氧化碳通入石蕊试液,溶液变红,加热红色变为紫色的原因)三、其他反应1、实验室制取二氧化碳:CaCO3+2HCl==CaCl2+ H2O + CO2↑ (大理石或石灰石和稀盐酸)2、木炭还原氧化铜:C+2CuO高温2Cu+CO2↑ (CuO为黑色粉末)现象:黑色粉末逐渐变为红色,澄清石灰水变浑浊。

以下是九年级上下册化学方程式:上册:1.镁在空气中燃烧:2Mg + O2点燃2MgO2.铁在氧气中燃烧:3Fe + 2O2点燃Fe3O43.铜在空气中受热:2Cu + O2加热2CuO4.铝在空气中燃烧:4Al + 3O2点燃2Al2O35.氢气中空气中燃烧:2H2 + O2点燃2H2O6.红磷在空气中燃烧:4P + 5O2点燃2P2O57.硫粉在空气中燃烧:S + O2点燃SO28.碳在氧气中充分燃烧:C + O2点燃CO29.碳在氧气中不充分燃烧:2C + O2点燃2CO10.二氧化碳通过炽热的炭层:CO2 + C高温2CO11.一氧化碳在氧气中燃烧:2CO + O2点燃2CO212.一氧化碳还原氧化铜:CO+ CuOCu + CO213.二氧化碳和水反应(二氧化碳通入紫色石蕊试液):CO2 + H2O= H2CO314.苛性钠暴露在空气中变质:NaOH + CO2= NaCO3 + H2O15.消石灰放在空气中变质:Ca(OH)2 + CO2= CaCO3↓+ H2O16.二氧化碳通过澄清石灰水(澄清石灰水检验二氧化碳):Ca(OH)2 +CO2= CaCO3↓+ H2O下册:1.生石灰溶于水:CaO + H2O = Ca(OH)22.硫酸铜晶体受热分解:CuSO4·5H2OCuSO4 + 5H2O↑3.无水硫酸铜遇水变蓝:CuSO4+ 5H2OCuSO4·5H2O4.电解水:2H2O通电2H2↑+ O2↑5.甲烷在空气中燃烧:CH4+ 2O2点燃CO2+ 2H2O6.酒精在空气中燃烧:C2H5OH + 3O2点燃3H2O+ 2CO27.镁和盐酸反应:Mg + 2HCl = MgCl2 + H2↑8.镁和稀硫酸反应:Mg + H2SO4 = MgSO4 + H2↑9.锌和盐酸反应:Zn + 2HCl = ZnCl2 + H2↑10.锌和稀硫酸反应:Zn + H2SO4 = ZnSO4 + H2↑11.铁和盐酸反应:Fe + 2HCl = FeCl2 + H2↑12.铁和稀硫酸反应:Fe + H2SO4 = FeSO4 + H2↑13.铝和稀硫酸反应:Al + 3HCl = AlCl3 + HCl14.铝和稀硫酸反应:Al + 3HCl = AlCl3 + HCl↑15.大理石与稀盐酸反应:CaCO3+ 2HCl = CaCl2+ H2O+ CO。

初中化学方程式一、氧气的性质:( 1)单质与氧气的反应:(化合反应)1.镁在空气中燃烧: 2Mg + O 2点燃 2MgO2.铁在氧气中燃烧: 3Fe + 2O 2点燃 Fe 3O43. 铜在空气中受热:2Cu + O 2 2CuO4. 铝在空气中燃烧:4Al + 3O2 点燃2Al2O35. 氢气中空气中燃烧: 2H2 + O 2 点燃 2H 2O6.红磷在空气中燃烧(研究空气组成的实验): 4P + 5O 2点燃 2P 2O57. 硫粉在空气中燃烧:S + O 2 点燃 SO28. 碳在氧气中充分燃烧: C + O2 点燃CO2( 2)化合物与氧气的反应:10.一氧化碳在氧气中燃烧:2CO + O 点燃2CO2 211.甲烷在空气中燃烧:CH4 + 2O 2点燃 CO2 + 2H 2O 12.酒精在空气中燃烧:C HOH + 3O 点燃2 2CO + 3H O2 5 2 2( 3)氧气的来源:13.拉瓦锡研究空气的成分实验2HgO Hg+ O2↑14.加热高锰酸钾(实验室制氧气原理1)2KMnO4K2MnO4 + MnO2 + O 2↑15.过氧化氢在二氧化锰作催化剂条件下分解反应:2 2 MnO2 22↑(实验2H O 2H O+ O室制氧气原理2)16 加热氯酸钾(二氧化锰):(实验室制氧气原理 3)2KClO3MnO2 2KCl+3O2↑二、自然界中的水:17.水在直流电的作用下分解(研究水的组成实验): 2H2O 通电 2H 2↑+ O2↑18.生石灰溶于水: CaO + H2O === Ca(OH)219.二氧化碳可溶于水:H2O + CO2=== H2CO3三、质量守恒定律:20.镁在空气中燃烧: 2Mg + O2点燃 2MgO21.铁和硫酸铜溶液反应:Fe + CuSO 4 === FeSO4 + Cu22.氢气还原氧化铜:H2 + CuO Cu + H 2O四、碳和碳的氧化物:( 1)碳的化学性质23. 碳在氧气中充分燃烧: C + O 2点燃 CO224.碳在氧气中不充分燃烧:2C + O 2点燃 2CO25.木炭还原氧化铜:C+ 2CuO高温2Cu + CO2↑26.焦炭还原氧化铁:3C+ 2Fe2O3高温 4Fe + 3CO 2↑( 2)煤炉中发生的三个反应:(几个化合反应)27.煤炉的底层: C + O 2点燃 CO228.煤炉的中层:CO2 + C 高温2CO 29.煤炉的上部蓝色火焰的产生:2CO + O2点燃 2CO2( 3)二氧化碳的制法与性质:30.大理石与稀盐酸反应(实验室制二氧化碳):CaCO+ 2HCl === CaCl2+ H O + CO ↑3 2 2 31.碳酸不稳定而分解:H2CO3 === H 2O + CO2↑32.二氧化碳可溶于水:H2O + CO2=== H2CO333.高温煅烧石灰石(工业制二氧化碳):高温CaCO3CaO + CO2↑34.石灰水与二氧化碳反应(鉴别二氧化碳):Ca(OH)2 + CO 2 ==== CaCO 3 ↓+ H 2O( 4)一氧化碳的性质:35.一氧化碳还原氧化铜:CO+ CuOCu + CO 236.一氧化碳的可燃性:2CO + O 2点燃2CO 2其它反应:37.碳酸钠与稀盐酸反应 (灭火器的原理) :Na CO + 2HCl === 2NaCl + H2O + CO ↑232五、燃料及其利用:38.甲烷在空气中燃烧:CH 4 + 2O 2点燃CO 2 + 2H 2O39.酒精在空气中燃烧:C 2H 5OH + 3O 2点燃2CO 2 + 3H 2O40. 氢气中空气中燃烧:2H 2 + O 2点燃2H 2O六、金属( 1)金属单质 + 氧气 --------金属氧化 物(化合反应)41. 镁在空气中燃烧: 2Mg + O 2 点燃2MgO42. 铁在氧气中燃烧: 3Fe + 2O2点燃 Fe O3 443.铜在空气中受热:2Cu + O 22CuO44.铝在空气中形成氧化膜:4Al + 3O 2 = 2Al 2 O 3( 2 )金属单质 +酸 --------盐 +氢气 (置换反应)45. 锌和稀硫酸(实验室制氢气)Zn + H 2SO 4 = ZnSO 4 + H 2↑46. 铁和稀硫酸 Fe + H 2SO 4 = FeSO 4 + H 2↑47. 镁和稀硫酸 Mg + H 2SO 4 = MgSO 4 + H 2↑48. 铝和 稀硫 酸 2Al +3H2SO = Al (SO )3424+3H 2↑49. 锌和稀盐酸 Zn + 2HCl === ZnCl 2 + H 2↑ 50. 铁和稀盐酸 Fe + 2HCl === FeCl 2 + H 2↑ 51. 镁和稀盐酸 Mg+ 2HCl === MgCl 2 + H 2↑ 52.铝和稀盐酸2Al + 6HCl == 2AlCl3+ 3H ↑2( 3)金属单质 + 盐(溶液) -------新金属 + 新盐(置换反应) 53. 铁和硫酸铜溶液反应:Fe + CuSO 4 === FeSO 4 + Cu54. 铝和硫酸铜溶液反应:2Al +3 CuSO4=== Al 2(SO 4) 3 + 3Cu55. 铜和硝酸汞溶液反应:Cu + AgNO 3 === Cu(NO 3 ) 2 + Ag( 3)金属铁的治炼原理:56.赤铁矿炼铁原理:3CO+ 2Fe高温4Fe + 3CO ↑O223七、酸、碱、盐1、酸的化学性质( 1)酸 + 金属 --------盐 + 氢气(见上)( 2 )酸 +金属氧化物 -------- 盐 +水(复分解反应)57. 氧化铁和稀盐酸反应 ( 除铁锈 ) :Fe 2O 3 + 6HCl === 2FeCl 3 + 3H 2O58. 氧化铁和稀硫酸反应(除铁锈):Fe 2O 3 + 3H 2SO 4 === Fe 2(SO 4) 3 + 3H 2O59. 氧化铜和稀盐酸反应:CuO + 2HCl ==== CuCl 2 + H 2O60. 氧化铜和稀硫酸反应:CuO + H 2SO 4 ==== CuSO 4 + H 2O( 3)酸 + 碱 --------盐 + 水(中和反应)61. 盐酸和烧碱起反应:HCl + NaOH ==== NaCl +H 2O62. 盐酸和氢氧化钙反应:( 1)盐(溶液) + 金属单质 ------- 另一2HCl + Ca(OH) 2 ==== CaCl 2 + 2H 2O种金属 +另一种盐(复分解反应)63. 氢氧化铝药物治疗胃酸过多:75. 铁和硫酸铜溶液反应:3HCl + Al(OH) 3==== AlCl 3 + 3H 2 O Fe + CuSO4=== FeSO + Cu464. 硫酸和烧碱反应: ( 2)盐 + 酸 --------另一种酸 + 另H SO + 2NaOH ==== Na SO + 2H O 一种盐(复分解反应)242 4 2( 4)酸 + 盐 --------另一种酸 +另 76.碳酸钠与稀盐酸反应 :一种盐(复分解反应) Na 2CO 3 + 2HCl === 2NaCl + H2O + CO 2↑65.大理石与稀盐酸反应:碳酸氢钠与稀盐酸反应:CaCO 3 + 2HCl === CaCl2+ H 2O + CO 2↑NaHCO 3+ HCl=== NaCl + H 2O + CO 2↑66.碳酸钠与稀盐酸反应 :( 3 )盐 +碱 --------另一种碱 + 另Na 2CO 3 + 2HCl === 2NaCl + H 2O + CO 2↑ 一种盐(复分解反应)67.碳酸氢钠与稀盐酸反应:77. 氢氧化钙与碳酸钠:NaHCO+ HCl=== NaCl + H 2 O + CO ↑Ca(OH) + Na CO === CaCO ↓+ 2NaOH32223368. 硫酸和氯化钡溶液反应:78. 氯化铵加熟石灰研磨:H SO + BaCl 2 ==== BaSO 4 ↓+ 2HClCa(OH)2 + 2NH 4Cl === CaCl 2+2H 2O+2NH ↑ 2432、碱的化学性质硫酸铵加熟石灰研磨:( 1)碱 + 非金属氧化物--------盐 +Ca(OH) +(NH ) SO === CaSO +2H O+2NH ↑242 44 2 3水( 4)盐 +盐 -----两种新盐(复分解反69.苛性钠暴露在空气中变质:应)2NaOH + CO 2 ==== Na 2CO 3 + H 2O 79.氯化钠溶液和硝酸银溶液: 70.苛性钠吸收二氧化硫气体:NaCl + AgNO 3 ==== AgCl ↓ + NaNO 32NaOH + SO ==== Na 2 SO + H 2 O80.硫酸钠和氯化钡:2371.苛性钠吸收三氧化硫气体:Na 2SO 4 + BaCl 2 ==== BaSO 4↓ + 2NaCl2NaOH + SO 3 ==== Na 2SO 4 + H 2O72.消石灰放在空气中变质:Ca(OH)2 + CO 2 ==== CaCO 3 ↓+ H 2O73. 消石灰吸收二氧化硫:Ca(OH)2 + SO 2 ==== CaSO 3 ↓+ H 2O( 2)碱+酸 --------盐 +水(中和反应,方程式见上) ( 3)碱+盐--------另一种碱+另一种盐(复分解反应)74. 氢氧化钙与碳酸钠:Ca(OH)2 + Na 2CO 3 === CaCO 3↓+ 2NaOH3、盐的化学性质。

初中常见化学方程式总结一、物质与O2的反应:(1)单质与O2的反应:1. 镁在空气中燃烧:2Mg + O2点燃2MgO2. 铁在氧气中燃烧:3Fe + 2O2点燃Fe3O43. 铜在空气中受热:2Cu + O2加热2CuO 5.气中燃烧:2H2 + O2点燃2H2O4.铝在空气中燃烧:4Al + 3O2点燃2Al2O3 注:铝与O2的反应条件可是加热、点燃、常温下反应6. 红磷在空气中燃烧:4P + 5O2点燃2P2O57. 硫粉在空气中燃烧:S + O2点燃SO28. 碳在氧气中充分燃烧:C + O2点燃CO29. 碳在氧气中不充分燃烧:2C + O2点燃2CO(2)化合物与O2的反应:10. 一氧化碳在氧气中燃烧:2CO + O2点燃2CO2 11在空气中燃烧:CH4 + 2O2点燃CO2 +2H2O12. 酒精在空气中燃烧:C2H5OH + 3O2点燃2CO2 + 3H2O二、几个分解反应:13. 水在直流电的作用下分解:2H2O 通电2H2↑+ O2 ↑14. 高温煅烧石灰石:CaCO3高温CaO + CO2↑15. 加热氯酸钾(有少量的二氧化锰):2KClO3MnO2 2KCl + 3O2 ↑16. 加热高锰酸钾:2KMnO4加热K2MnO4 + MnO2 + O2↑17. 碳酸不稳定而分解:H2CO3 === H2O + CO2↑三.几个氧化还原反应:18. 氢气还原氧化铜:H2 + CuO 加热Cu + H2O 19. 木炭还原氧化铜:C+ 2CuO 高温2Cu+ CO2↑20. 焦炭还原氧化铁:3C+ 2Fe2O3高温4Fe + 3CO2↑21. 焦炭还原四氧化三铁:2C+ Fe3O4高温3Fe + 2CO2↑22. 一氧化碳还原氧化铜:CO+ CuO 加热Cu + CO223. 一氧化碳还原氧化铁:3CO+ Fe2O3高温2Fe + 3CO224. 一氧化碳还原四氧化三铁:4CO+ Fe3O4高温3Fe + 4CO2四.单质、氧化物、酸、碱、盐的相互关系置换反应和复分解反应没有先后顺序,可同时发生。

人教版九年级化学上下册所有的化学方程式一.物质与氧气的反应:(1)单质与氧气的反应:1. 镁在空气中燃烧:2Mg + O点燃2MgO2. 铁在氧气中燃烧:3Fe + 2O点燃Fe3O43. 铜在空气中受热:2Cu + O加热2CuO4. 铝在空气中燃烧:4Al + 3O2点燃2Al2O35. 氢气中空气中燃烧:2H2 + O2点燃2H2O6. 红磷在空气中燃烧:4P + 5O2点燃2P2O57. 硫粉在空气中燃烧:S + O2点燃SO28. 碳在氧气中充分燃烧:C + O2点燃CO29. 碳在氧气中不充分燃烧:2C + O2点燃2CO(2)化合物与氧气的反应:10. 一氧化碳在氧气中燃烧:2CO + O2点燃2CO211. 甲烷在空气中燃烧:CH4 + 2O2点燃CO2 + 2H2O12. 酒精在空气中燃烧:C2H5OH + 3O点燃2CO2 + 3H2O 二.几个分解反应:13. 水在直流电的作用下分解:2H2O 通电2H2↑+ O2↑14. 加热碱式碳酸铜:Cu2(OH)2CO3加热2CuO + H2O + CO2↑15. 过氧化氢的分解:2H2O 2MnO22H2O+O2↑15. 加热氯酸钾(有少量的二氧化锰):2KClO3加热2KCl + 3O2↑16. 加热高锰酸钾:2KMnO4加热K2MnO4 + MnO2 + O2↑17. 碳酸不稳定而分解:H2CO3 =H2O + CO2↑18. 高温煅烧石灰石:CaCO3高温CaO + CO2↑三.几个氧化还原反应:19. 氢气还原氧化铜:H2+ CuO加热Cu + H2O20. 木炭还原氧化铜:C+ 2CuO 高温2Cu + CO2↑21. 焦炭还原氧化铁:3C+ 2Fe2O高温4Fe + 3CO2↑22. 焦炭还原四氧化三铁:2C+ Fe3O高温3Fe + 2CO2↑23. 一氧化碳还原氧化铜:CO+ CuO高温Cu + CO224. 一氧化碳还原氧化铁:3CO+ Fe2 O3加热2Fe + 3CO225. 一氧化碳还原四氧化三铁:4CO+ Fe3O高温3Fe + 4CO2 四.单质、氧化物、酸、碱、盐的相互关系(1)金属单质+ 酸-------- 盐+ 氢气(置换反应)26. 锌和稀硫酸Zn + H2SO4 = ZnSO4 + H2↑27. 铁和稀硫酸Fe + H2SO4 = FeSO4 + H2↑28. 镁和稀硫酸Mg + H2SO4 = MgSO4 + H2 ↑29. 铝和稀硫酸2Al +3H2SO4 = Al2(SO4)3+3H2↑30. 锌和稀盐酸Zn + 2HCl =ZnCl2 + H2 ↑31. 铁和稀盐酸Fe + 2HCl = FeCl2 + H2↑32. 镁和稀盐酸Mg+ 2HCl =MgCl2+ H2↑33. 铝和稀盐酸2Al + 6HCl = 2AlCl3 + H2↑(2)金属单质+ 盐(溶液)------- 另一种金属+ 另一种盐34. 铁和硫酸铜溶液反应:Fe + CuSO4 =FeSO4 + Cu35. 锌和硫酸铜溶液反应:Zn + CuSO4 =ZnSO4 + Cu36. 铜和硝酸汞溶液反应:Cu + Hg(NO3)2= Cu(NO3)2+ Hg (3)碱性氧化物+酸-------- 盐+ 水37. 氧化铁和稀盐酸反应:Fe2O3 + 6HCl =2 FeCl3+ 3H2O38. 氧化铁和稀硫酸反应:Fe2O3 + 3H2SO4 = Fe2(SO4)3 + 3H2O39. 氧化铜和稀盐酸反应:CuO + 2HCl =CuCl2 + H2O40. 氧化铜和稀硫酸反应:CuO + H2SO4 = CuSO4 + H2O41. 氧化镁和稀硫酸反应:MgO + H2SO4 =MgSO4 + H2O42. 氧化钙和稀盐酸反应:CaO + 2HCl = CaCl2+ H2O(4)酸性氧化物+碱-------- 盐+ 水43.苛性钠暴露在空气中变质:2NaOH + CO2=Na2CO3 + H2O 44.苛性钠吸收二氧化硫气体:2NaOH + SO2= Na2SO3 + H2O 45.苛性钠吸收三氧化硫气体:2NaOH + SO3= Na2SO4 + H2O 46.消石灰放在空气中变质:Ca(OH)2+ CO2 =CaCO3↓+ H2O47. 消石灰吸收二氧化硫:Ca(OH)2 + SO2= CaSO3↓+ H2O (5)酸+ 碱-------- 盐+ 水48.盐酸和烧碱起反应:HCl + NaOH =NaCl +H2O49. 盐酸和氢氧化钾反应:HCl + KOH =KCl +H2O50.盐酸和氢氧化铜反应:2HCl + Cu(OH)2 = CuCl2 + 2H2O51. 盐酸和氢氧化钙反应:2HCl + Ca(OH)2 =CaCl2+ 2H2O52. 盐酸和氢氧化铁反应:3HCl + Fe(OH)3= FeCl3+ 3H2O53.氢氧化铝药物治疗胃酸过多:3HCl + Al(OH)3= AlCl3 + 3H2O54.硫酸和烧碱反应:H2 SO4 + 2NaOH = Na2SO4 + 2H2O55.硫酸和氢氧化钾反应:H2SO 4+ 2KOH =K2SO4 + 2H2O56.硫酸和氢氧化铜反应:H2SO4 + Cu(OH)2= CuSO4 + 2H2O57. 硫酸和氢氧化铁反应:3H2SO4 + 2Fe(OH)3= Fe2(SO4)3+ 6H2O58. 硝酸和烧碱反应:HNO3+ NaOH = NaNO3 +H2O(6)酸+ 盐-------- 另一种酸+ 另一种盐59.大理石与稀盐酸反应:CaCO 3+ 2HCl = CaCl2+ H2O + CO2↑60.碳酸钠与稀盐酸反应: Na2CO 3+ 2HCl = 2NaCl + H2O + CO2↑61.碳酸镁与稀盐酸反应: MgCO3 + 2HCl = MgCl2 + H2O + CO2↑62.盐酸和硝酸银溶液反应:HCl + AgNO3 = AgCl↓+ HNO363.硫酸和碳酸钠反应:Na2CO3 + H2 SO4 = Na2SO4 + H2 O + CO2↑64.硫酸和氯化钡溶液反应:H2SO4 + BaCl2 = BaSO4↓+ 2HCl (7)碱+ 盐-------- 另一种碱+ 另一种盐65.氢氧化钠与硫酸铜:2NaOH + CuSO4=Cu(OH)2↓+ Na2 SO466.氢氧化钠与氯化铁:3NaOH + FeCl3 = Fe(OH)3↓+ 3NaCl 67.氢氧化钠与氯化镁:2NaOH + MgCl2= Mg(OH)2↓+ 2NaCl68. 氢氧化钠与氯化铜:2NaOH + CuCl2= Cu(OH)2↓+ 2NaCl69. 氢氧化钙与碳酸钠:Ca(OH) 2+ Na2CO3=CaCO3↓+ 2NaOH (8)盐+ 盐----- 两种新盐70.氯化钠溶液和硝酸银溶液:NaCl + AgNO3=AgCl↓+ NaNO3 71.硫酸钠和氯化钡:Na2SO4 + BaCl2=BaSO4↓+ 2NaCl五.其它反应:72.二氧化碳溶解于水:CO2+ H2O =H2CO373.生石灰溶于水:CaO + H2O = Ca(OH)274.氧化钠溶于水:Na2 O + H2O = 2NaOH75.三氧化硫溶于水:SO3 + H2O = H2SO476.硫酸铜晶体受热分解:CuSO4·5H2加热CuSO4 + 5H2O 77.无水硫酸铜作干燥剂:CuSO4 + 5H2O =CuSO4·5H2O。

人教版九年级化学方程式大全人教版九年级化学方程式大全一. 物质与氧气的反应:(1)单质与氧气的反应:1. 镁在空气中燃烧:2 + O2 点燃 22. 铁在氧气中燃烧:3 + 2O2 点燃 3O43. 铜在空气中受热:2 + O2 加热 24. 铝在空气中燃烧:4 + 3O2 点燃 22O35. 氢气中空气中燃烧:2H2 + O2 点燃 2H2O6. 红磷在空气中燃烧:4P + 5O2 点燃 2P2O57. 硫粉在空气中燃烧: S + O2 点燃 28. 碳在氧气中充分燃烧:C + O2 点燃 29. 碳在氧气中不充分燃烧:2C + O2 点燃 2(2)化合物与氧气的反应:10. 一氧化碳在氧气中燃烧:2 + O2 点燃 2211. 甲烷在空气中燃烧:4 + 2O2 点燃 2 + 2H2O12. 酒精在空气中燃烧:C2H5 + 3O2 点燃 22 + 3H2O二.几个分解反应:13. 水在直流电的作用下分2H2O 通电 2H2 O2 ;14. 加热碱式碳酸铜:2()23 加热 2 + H2O + 2;15. 加热氯酸钾(有少量的二氧化锰):23 2 + 3O2 ;16. 加热高锰酸钾:24 加热 K24 + 2 + O2;17. 碳酸不稳定而分H23 H2O + 2;18. 高温煅烧石灰石:3 高温 + 2;三.几个氧化还原反应:19. 氢气还原氧化铜:H2 + 加热 + H2O20. 木炭还原氧化铜: 2 高温 2 + 2;21. 焦炭还原氧化铁:3 22O3 高温 4 + 32;22. 焦炭还原四氧化三铁:2 3O4 高温 3 + 22;23. 一氧化碳还原氧化铜:加热 + 224. 一氧化碳还原氧化铁:3 2O3 高温 2 + 3225. 一氧化碳还原四氧化三铁:4 3O4 高温 3 + 42四.单质、氧化物、酸、碱、盐的相互关系(1)金属单质 + 酸盐 + 氢气 (置换反应)26. 锌和稀硫酸 + H24 = 4 + H2;27. 铁和稀硫酸 + H24 = 4 + H2;28. 镁和稀硫酸 + H24 = 4 + H2;29. 铝和稀硫酸2 +3H24 = 2(4)3 +3H2;30. 锌和稀盐酸 + 2 2 + H2;31. 铁和稀盐酸 + 2 2 + H2;32. 镁和稀盐酸 2 2 + H2;33. 铝和稀盐酸2 + 6 23 + 3H2;(2)金属单质 + 盐(溶液) 另一种金属 + 另一种盐34. 铁和硫酸铜溶液反应: + 4 4 +35. 锌和硫酸铜溶液反应: + 4 4 +36. 铜和硝酸汞溶液反应: + (3)2 (3)2 +(3)碱性氧化物 +酸盐 + 水37. 氧化铁和稀盐酸反应:2O3 + 6 23 + 3H2O38. 氧化铁和稀硫酸反应:2O3 + 3H24 2(4)3 + 3H2O39. 氧化铜和稀盐酸反应: + 2 2 + H2O40. 氧化铜和稀硫酸反应: + H24 4 + H2O41. 氧化镁和稀硫酸反应: + H24 4 + H2O42. 氧化钙和稀盐酸反应: + 2 2 + H2O(4)酸性氧化物 +碱盐 + 水43.苛性钠暴露在空气中变质:2 + 2 23 + H2O44.苛性钠吸收二氧化硫气体:2 + 2 23 + H2O45.苛性钠吸收三氧化硫气体:2 + 3 24 + H2O46.消石灰放在空气中变质:()2 + 2 3 H2O47. 消石灰吸收二氧化硫:()2 + 2 3 H2O(5)酸 + 碱盐 + 水48.盐酸和烧碱起反应: + 2O49. 盐酸和氢氧化钾反应: + 2O50.盐酸和氢氧化铜反应:2 + ()2 2 + 2H2O51. 盐酸和氢氧化钙反应:2 + ()2 2 + 2H2O52. 盐酸和氢氧化铁反应:3 + ()3 3 + 3H2O53.氢氧化铝药物治疗胃酸过多:3 + ()3 3 + 3H2O54.硫酸和烧碱反应:H24 + 2 24 + 2H2O55.硫酸和氢氧化钾反应:H24 + 2 K24 + 2H2O56.硫酸和氢氧化铜反应:H24 + ()2 4 + 2H2O57. 硫酸和氢氧化铁反应:3H24 + 2()3 2(4)3 + 6H2O58. 硝酸和烧碱反应:3+ 3 2O(6)酸 + 盐另一种酸 + 另一种盐59.大理石与稀盐酸反应:3 + 2 2 + H2O + 2;60.碳酸钠与稀盐酸反应: 23 + 2 2 + H2O + 2;61.碳酸镁与稀盐酸反应: 3 + 2 2 + H2O + 2;62.盐酸和硝酸银溶液反应: + 3 ; + 363.硫酸和碳酸钠反应:23 + H24 24 + H2O + 2;64.硫酸和氯化钡溶液反应:H24 + 2 4 2(7)碱 + 盐另一种碱 + 另一种盐65.氢氧化钠与硫酸铜:2 + 4 ()2; + 2466.氢氧化钠与氯化铁:3 + 3 ()3; + 367.氢氧化钠与氯化镁:2 + 2 ()2; + 268. 氢氧化钠与氯化铜:2 + 2 ()2; + 269. 氢氧化钙与碳酸钠:()2 + 23 3 2(8)盐 + 盐两种新盐70.氯化钠溶液和硝酸银溶液: + 3 ; + 371.硫酸钠和氯化钡:24 + 2 4; + 2五.其它反应:72.二氧化碳溶解于水:2 + H2O H2373.生石灰溶于水: + H2O ()274.氧化钠溶于水:2O + H2O 275.三氧化硫溶于水:3 + H2O H2476.硫酸铜晶体受热分4;5H2O 加热 4 + 5H2O77.无水硫酸铜作干燥剂:4 + 5H2O 4;5H2化学方程式反应现象应用22点燃或;2 剧烈燃烧.耀眼白光.生成白色固体.放热.产生大量白烟白色信号弹22点燃或;2 银白液体、生成红色固体拉瓦锡实验22点燃或;2 红色金属变为黑色固体43O2点燃或;22O3 银白金属变为白色固体32O2点燃3O4 剧烈燃烧、火星四射、生成黑色固体、放热 4 + 3O2高温22O32 点燃2 剧烈燃烧、白光、放热、使石灰水变浑浊2 点燃2 剧烈燃烧、放热、刺激味气体、空气中淡蓝色火焰.氧气中蓝紫色火焰2H22 点燃2H2O 淡蓝火焰、放热、生成使无水4变蓝的液体(水) 高能燃料45O2 点燃2P2O5 剧烈燃烧、大量白烟、放热、生成白色固体证明空气中氧气含量4+2O2点燃2H22 蓝色火焰、放热、生成使石灰水变浑浊气体和使无水4变蓝的液体(水) 甲烷和天然气的燃烧2C2H2+5O2点燃2H242 蓝色火焰、放热、黑烟、生成使石灰水变浑浊气体和使无水4变蓝的液体(水) 氧炔焰、焊接切割金属232 ;2 +3O2; 生成使带火星的木条复燃的气体实验室制备氧气24; K2422; 紫色变为黑色、生成使带火星木条复燃的气体实验室制备氧气2;22; 红色变为银白、生成使带火星木条复燃的气体拉瓦锡实验2H2O通电2H22; 水通电分解为氢气和氧气电解水2()23;222; 绿色变黑色、试管壁有液体、使石灰水变浑浊气体铜绿加热433 H2O 2; 白色固体消失、管壁有液体、使石灰水变浑浊气体碳酸氢铵长期暴露空气中会消失2442; 有大量气泡产生、锌粒逐渐溶解实验室制备氢气2442; 有大量气泡产生、金属颗粒逐渐溶解24 42; 有大量气泡产生、金属颗粒逐渐溶解23H242(4)3+3H2; 有大量气泡产生、金属颗粒逐渐溶解2O3+3H2 ; 23H2O 红色逐渐变为银白色、试管壁有液体冶炼金属、利用氢气的还原性3O4+4H2 ;34H2O 黑色逐渐变为银白色、试管壁有液体冶炼金属、利用氢气的还原性3+3H2; W +3H2O 冶炼金属钨、利用氢气的还原性3+3H2 +3H2O 冶炼金属钼、利用氢气的还原性22;或点燃2 剧烈燃烧、黄色火焰离子化合物的形成、H22 点燃或光照 2 点燃苍白色火焰、瓶口白雾共价化合物的形成、制备盐酸4+2()224 蓝色沉淀生成、上部为澄清溶液质量守恒定律实验2C 2点燃2 煤炉中常见反应、空气污染物之一、煤气中毒原因2C 2点燃22 蓝色火焰煤气燃烧C + 高温2 2; 黑色逐渐变为红色、产生使澄清石灰水变浑浊的气体冶炼金属22O3+3C 高温4 32; 冶炼金属3O4+2C高温3 + 22; 冶炼金属C + 2 高温22 + H2O = H23 碳酸使石蕊变红证明碳酸的酸性H23 2 H2O 石蕊红色褪去()22= 3 H2O 澄清石灰水变浑浊应用2检验和石灰浆粉刷墙壁322 = (3)2 白色沉淀逐渐溶解溶洞的形成,石头的风化(3)2; 322; 白色沉淀、产生使澄清石灰水变浑浊的气体水垢形成.钟乳石的形成232322; 产生使澄清石灰水变浑浊的气体小苏打蒸馒头3 高温 2; 工业制备二氧化碳和生石灰3+22+ H22; 固体逐渐溶解、有使澄清石灰水变浑浊的气体实验室制备二氧化碳、除水垢23242422; 固体逐渐溶解、有使澄清石灰水变浑浊的气体泡沫灭火器原理23+22 H22; 固体逐渐溶解、有使澄清石灰水变浑浊的气体泡沫灭火器原理3+2222; 固体逐渐溶解、有使澄清石灰水变浑浊的气体 ; + 2 黑色逐渐变红色,产生使澄清石灰水变浑浊的气体冶炼金属2O3+3高温 232 冶炼金属原理3O4+4高温 342 冶炼金属原理3+3高温 32 冶炼金属原理332O233O2点燃22+4H2OC2H53O2点燃22+3H2O 蓝色火焰、产生使石灰水变浑浊的气体、放热酒精的燃烧44 银白色金属表面覆盖一层红色物质湿法炼铜、镀铜4= 4 溶液由浅绿色变为无色 (3)2 (3)223=2 (3)2 红色金属表面覆盖一层银白色物质镀银4= 4 青白色金属表面覆盖一层红色物质镀铜2O3+623+3H2O 铁锈溶解、溶液呈黄色铁器除锈2O3+623+3H2O 白色固体溶解2222O 白色固体溶解222O 黑色固体溶解、溶液呈蓝色22+ H2O 白色固体溶解22+ H2O 白色固体溶解22+ H2O 白色固体溶解H2O 白色固体溶解()2+22+2H2O 蓝色固体溶解()2+22+2H2O 白色固体溶解()3+33+3H2O 白色固体溶解胃舒平治疗胃酸过多()3+33+3H2O 红褐色沉淀溶解、溶液呈黄色()2+22+2H2O3= 3 生成白色沉淀、不溶解于稀硝酸检验—的原理2O3+3H24= 2(4)3+3H2O 铁锈溶解、溶液呈黄色铁器除锈2O3+3H24= 2(4)3+3H2O 白色固体溶解2442O 黑色固体溶解、溶液呈蓝色2442O 白色固体溶解2442O 白色固体溶解22424+2H2O()2244+2H2O 蓝色固体溶解()2244+2H2O()2244+2H2O 白色固体溶解2()3+3H242(4)3+3H2O 白色固体溶解2()3+3H242(4)3+3H2O 红褐色沉淀溶解、溶液呈黄色()2+ H2442H2O 生成白色沉淀、不溶解于稀硝酸检验42—的原理2+ H2442 生成白色沉淀、不溶解于稀硝酸检验42—的原理(3)224423 生成白色沉淀、不溶解于稀硝酸检验42—的原理223=232O 白色固体溶解23(3)22O 黑色固体溶解、溶液呈蓝色23(3)2+ H2O 白色固体溶解23(3)2+ H2O 白色固体溶解23(3)2+ H2O 白色固体溶解33+ H2O()2+23(3)2+2H2O 蓝色固体溶解()2+23(3)2+2H2O 白色固体溶解()3+33(3)3+3H2O 白色固体溶解()2+23(3)2+2H2O()3+33(3)3+3H2O 红褐色沉淀溶解、溶液呈黄色3 + H34=3H2O + 343334=(4)342223+ H2O 吸收、O2、H2中的2、2223+ H2O 2324+ H2O 处理硫酸工厂的尾气(2)3+3()33 溶液黄色褪去、有红褐色沉淀生成3+3()33 有白色沉淀生成2+2 = ()222+2 = ()22 溶液蓝色褪去、有蓝色沉淀生成H2O = ()2 白色块状固体变为粉末、生石灰制备石灰浆()223 H2O 有白色沉淀生成初中一般不用()22332 有白色沉淀生成工业制烧碱、实验室制少量烧碱()22332 有白色沉淀生成()2233; +2 有白色沉淀生成4+5H2 42O 蓝色晶体变为白色粉末42; 4+5H2O 白色粉末变为蓝色检验物质中是否含有水3 = 3 白色不溶解于稀硝酸的沉淀(其他氯化物类似反应) 应用于检验溶液中的氯离子2 + 24 = 42 白色不溶解于稀硝酸的沉淀(其他硫酸盐类似反应) 应用于检验硫酸根离子223= 32 有白色沉淀生成2()22()2; 有白色沉淀生成3+2222 ;3+2 22 2 ;43332O 生成使湿润石蕊试纸变蓝色的气体应用于检验溶液中的铵根离子4 32O 生成使湿润石蕊试纸变蓝色的气体六、化合反应1、镁在空气中燃烧:2 + O2 点燃 22、铁在氧气中燃烧:3 + 2O2 点燃 3O43、铝在空气中燃烧:4 + 3O2 点燃 22O34、氢气在空气中燃烧:2H2 + O2 点燃 2H2O5、红磷在空气中燃烧:4P + 5O2 点燃 2P2O56、硫粉在空气中燃烧: S + O2 点燃 27、碳在氧气中充分燃烧:C + O2 点燃 28、碳在氧气中不充分燃烧:2C + O2 点燃 29、二氧化碳通过灼热碳层: C + 2 高温 210、一氧化碳在氧气中燃烧:2 + O2 点燃 2211、二氧化碳和水反应(二氧化碳通入紫色石蕊试液):2 + H2O H2312、生石灰溶于水: + H2O ()213、无水硫酸铜作干燥剂:4 + 5H2O 4;5H2O14、钠在氯气中燃烧:2 + 2点燃 2七、分解反应15、实验室用双氧水制氧气:2H2O2 2 2H2 O2;16、加热高锰酸钾:24 加热 K24 + 2 + O2;17、水在直流电的作用下分2H2O 通电 2H2 O2 ;18、碳酸不稳定而分H23 H2O + 2;19、高温煅烧石灰石(二氧化碳工业制法):3 高温 + 2;八、置换反应20、铁和硫酸铜溶液反应: + 4 4 +21、锌和稀硫酸反应(实验室制氢气): + H24 4 + H2;22、镁和稀盐酸反应: 2 2 + H2;23、氢气还原氧化铜:H2 + 加热 + H2O24、木炭还原氧化铜: 2 高温 2 + 2;25、甲烷在空气中燃烧:4 + 2O2 点燃 2 + 2H2O26、水蒸气通过灼热碳层:H2O + C 高温 H2 +27、焦炭还原氧化铁:3 22O3 高温 4 + 32;九、其他28、氢氧化钠溶液与硫酸铜溶液反应:2 + 4 ()2; + 2429、甲烷在空气中燃烧:4 + 2O2 点燃 2 + 2H2O30、酒精在空气中燃烧:C2H5 + 3O2 点燃 22 + 3H2O31、一氧化碳还原氧化铜:加热 + 232、一氧化碳还原氧化铁:3 2O3 高温 2 + 3233、二氧化碳通过澄清石灰水(检验二氧化碳):()2 + 2 3 H2O34、氢氧化钠和二氧化碳反应(除去二氧化碳):2 + 2 23+ H2O35、石灰石(或大理石)与稀盐酸反应(二氧化碳的实验室制法):3 + 2 2 + H2O + 2;36、碳酸钠与浓盐酸反应(泡沫灭火器的原理): 23 + 2 2 + H2O + 2;。

化学方程式汇总(一)1.P27红(白)磷在空气中燃烧:4P + 5O2点燃2P2O5现象:(1)发出白光(2)放出热量(3)生成大量白烟。
2.P33碳在氧气中充分燃烧:C + O2点燃CO2现象:(1)发出白光(2)放出热量(3)澄清石灰水变浑浊3.P34硫粉在空气中燃烧:S + O2点燃 SO2现象:在纯的氧气中:发出明亮的蓝紫火焰,放出热量,生成有刺激性气味的气体。
在空气中燃烧:发出淡蓝色火焰,放出热量,生成有刺激性气味的气体。
4.P34铁在氧气中燃烧:3Fe + 2O2点燃Fe3O4现象:(1)剧烈燃烧,火星四射(2)放出热量(3)生成一种黑色固体注意:瓶底要放少量水或细沙,防止生成的固体物质溅落下来,炸裂瓶底。
5.P37加热高锰酸钾制取氧气:2KMnO4 △ K2MnO4 + MnO2 + O2↑6.P39用过氧化氢制氧气:2H2O2MnO2 2H2O+ O2↑7.P39加热氯酸钾和的二氧化锰的混合物制氧气:2KClO3MnO22KCl + 3O2 ↑8.P50加热氧化汞:2HgO△2Hg + O2↑9.P79氢气中空气中燃烧或爆炸:2H2 + O2点燃 2H2O现象:(1)产生淡蓝色火焰(2)放出热量(3)烧杯内壁出现水雾。
10.P80水在直流电的作用下分解:2H2O 通电 2H2↑+ O2 ↑现象:(1)电极上有气泡产生。
正氧负氢,体积比1:2(2)正极产生的气体能使带火星的木条复燃。
(3)负极产生的气体能在空气中燃烧,产生淡蓝色火焰11.P93铁与硫酸铜反应:Fe + CuSO4==Cu + FeSO4现象:铁条表面覆盖一层红色的物质,溶液由蓝色变成浅绿色。
12.P94碳酸钠粉末和稀盐酸反应:Na2CO3+2HCl==2NaCl+H2O+CO2↑13.P94镁在空气中燃烧:2Mg + O2点燃 2MgO现象:(1)发出耀眼的白光(2)放出热量(3)生成白色粉末14.P110碳在氧气中不充分燃烧:2C + O2点燃2CO15.P111焦炭还原氧化铁:3C+ 2Fe2O3高温4Fe + 3CO2↑16.P111木炭还原氧化铜:C+ 2CuO 高温2Cu + CO2↑17.P111高温下碳还原二氧化碳:C + CO2高温2CO(吸热反应)18.P113实验室制取二氧化碳的原理:CaCO3+2HCl==CaCl2+H2O+CO2↑19.P118二氧化碳和水反应:CO2 + H2O == H2CO320.P118碳酸不稳定而分解:H2CO3 == H2O + CO2↑21.P118二氧化碳通入澄清石灰水:CO2 +C a(O H)2 ==CaCO3↓+ H2O 现象:澄清石灰水变浑浊。

人教版九年级化学方程式大全一、化合反应1镁在空气中燃烧:2Mg + O2点燃2MgO 耀眼白光,大量白烟,生成白色固体,放热;2 铁在氧气中燃烧:3Fe + 2O2点燃Fe3O4剧烈燃烧,火星四射,生成黑色固体,放热;3铜在空气中受热:2Cu + O2加热2CuO 紫红色变成黑色;4 铝在空气中燃烧:4Al + 3O2点燃2Al2O3生成一种致密的氧化膜;(Al不易生锈的原因)5氢气在空气中燃烧:2H2 + O2点燃2H2O 淡蓝色火焰(不纯会发生爆炸)6 红磷在空气中燃烧:4P + 5O2点燃2P2O5大量白烟,生成白色固体;(研究空气组成的原理)7 硫粉在空气中燃烧:S + O2点燃SO2空气中淡蓝色,氧气中蓝紫色,生成一种刺激性气体;8 碳在氧气中充分燃烧:C + O2点燃CO2空气中黄光,氧气中白光;9碳在氧气中不充分燃烧:2C + O2点燃2CO 生成一种有毒气体;10生石灰溶于水:CaO + H2O = Ca(OH)2放出大量的热;(生产熟石灰的原理)11氧化钠溶于水:Na2O + H2O = 2NaOH (条件:生成的碱溶于水)12氧化钾溶于水:K2O+H2O = 2KOH (条件:生成的碱溶于水)13氧化钡溶于水:BaO+H2O = Ba(OH)2(条件:生成的碱溶于水)14二氧化碳溶于水:CO2 + H2O = H2CO3二氧化碳能使紫色石蕊溶液变红;15二氧化硫溶于水:SO2+H2O = H2SO3生成亚硫酸,形成酸雨原因;16三氧化硫溶于水:SO3 + H2O = H2SO4生成硫酸;17一氧化碳在氧气中燃烧:2CO + O2点燃2CO2蓝色火焰,可做燃料;18二氧化碳和碳反应:CO2+C高温2CO 吸热反应;19无水硫酸铜作干燥剂:CuSO4 + 5H2O = CuSO4·5H2O 白色变成蓝色,检验水;二、分解反应20水在直流电的作用下分解:2H2O 通电2H2↑+ O2 ↑两个电极有气泡产生,负氢(父亲)正氧;体积比:2:1 ;质量比:1:8 21加热碱式碳酸铜:Cu2(OH)2CO3加热2CuO + H2O + CO2↑绿色变黑色,石灰水变浑浊;22利用过氧化氢和二氧化锰的混合物制氧气:2 H2O2MnO2 2H2O+ O2 ↑气泡产生;23加热氯酸钾和二氧化锰的混合物制氧气:2KClO3MnO22KCl+3O2↑有气体生成,MnO2△作催化剂;24加热高锰酸钾:2KMnO4△K2MnO4 + MnO2 + O2↑紫黑色变黑色,有气体,管口塞棉花;25碳酸不稳定而分解:H2CO3 = H2O + CO2↑有气泡产生;26高温煅烧石灰石:CaCO3高温CaO + CO2↑工业制CO2和生石灰;27加热碳酸氢铵:NH4HCO3△H2O + CO2↑+NH3↑产生刺激性气体;28硫酸铜晶体受热分解:CuSO4·5H2O △CuSO4 + 5H2O 蓝色晶体变成白色;29碳酸氢钙分解Ca(HCO3)2==CaCO3↓+CO2↑+H2O 溶洞,石笋形成原因;三、置换反应30氢气还原氧化铜:H2 + CuO △Cu + H2O 黑色变红色,有水珠;(氢气:早出晚归;酒精灯:迟到早退)31木炭还原氧化铜:C+ 2CuO 高温2Cu + CO2↑黑色变红色,石灰水变浑浊;32焦炭还原氧化铁:3C+ 2Fe2O3高温4Fe + 3CO2↑红色变黑色(铁粉);33焦炭还原四氧化三铁:2C+ Fe3O4高温3Fe + 2CO2↑石灰水变浑浊;34锌和稀硫酸反应:Zn + H2SO4 = ZnSO4 + H2↑气泡,固体逐渐溶解;35铁和稀硫酸反应:Fe + H2SO4 = FeSO4 + H2↑气泡,固体逐渐溶解,溶液无色变浅绿色;36镁和稀硫酸反应:Mg + H2SO4 = MgSO4 + H2↑气泡,固体溶解较快;37铝和稀硫酸反应:2Al + 3H2SO4 = Al2(SO4)3 + 3H2↑气泡,固体溶解;38锌和稀盐酸反应:Zn + 2HCl= ZnCl2 + H2↑气泡,固体溶解;39铁和稀盐酸反应:Fe + 2HCl= FeCl2 + H2↑气泡,固体逐渐溶解,溶液无色变浅绿色;40镁和稀盐酸反应:Mg+ 2HCl= MgCl2 + H2↑气泡,固体溶解;41铝和稀盐酸反应:2Al + 6HCl = 2AlCl3 + 3H2↑气泡,固体溶解;42铁和硫酸铜溶液反应:Fe + CuSO4 = FeSO4 + Cu铁丝表面有一层红色物质,溶液蓝色变浅绿色;43铝和硫酸铜溶液反应:2Al + 3CuSO4 = Al2(SO4)3 +3 Cu铝表面有一层红色物质,溶液蓝色变无色;44铜和硝酸银溶液反应:Cu + 2AgNO3 = Cu(NO3)2 + 2Ag铜表面有一层银白色物质,溶液无色变蓝色;四、复分解反应45氧化铁和稀盐酸反应:Fe2O3 + 6HCl = 2FeCl3 + 3H2O (除铁锈)红色物质溶解,溶液无色变黄色;46氧化铁和稀硫酸反应:Fe2O3 + 3H2SO4 = Fe2(SO4)3 + 3H2O红色物质溶解,溶液无色变黄色(除铁锈);47氧化铜和稀盐酸反应:CuO + 2HCl = CuCl2 + H2O 黑色粉末逐渐溶解,溶液无色变蓝色;48氧化铜和稀硫酸反应:CuO + H2SO4 = CuSO4 + H2O黑色粉末逐渐溶解,溶液无色变蓝色;49氧化镁和稀硫酸反应:MgO + H2SO4 = MgSO4 + H2O 白色粉末逐渐溶解;50氧化钙和稀盐酸反应:CaO + 2HCl = CaCl2 + H2O 固体逐渐溶解;51盐酸和烧碱起反应:HCl + NaOH = NaCl +H2O 反应无现象(证明反应要引入指示剂);52盐酸和氢氧化钾反应:HCl + KOH = KCl +H2O反应无现象(证明反应要引入指示剂);53盐酸和氢氧化铜反应:2HCl + Cu(OH)2 = CuCl2 + 2H2O 蓝色固体溶解,溶液无色变成蓝色;54盐酸和氢氧化钙反应:2HCl + Ca(OH)2 = CaCl2 + 2H2O 反应无现象;55盐酸和氢氧化铁反应:3HCl + Fe(OH)3 = FeCl3 + 3H2O 红褐色固体溶解,溶液无色变黄色;56氢氧化铝药物治疗胃酸过多:3HCl + Al(OH)3 = AlCl3 + 3H2O 白色固体逐渐溶解;57硫酸和烧碱反应:H2SO4 + 2NaOH = Na2SO4 + 2H2O 反应无现象;58硫酸和氢氧化钾反应:H2SO4 + 2KOH = K2SO4 + 2H2O反应无现象;59硫酸和氢氧化铜:H2SO4 + Cu(OH)2 = CuSO4 + 2H2O 蓝色固体溶解,溶液无色变蓝色;60硫酸和氢氧化铁:3H2SO4 + 2Fe(OH)3= Fe2(SO4)3 + 6H2O 红褐色固体溶解,溶液无色变黄色;61硝酸和烧碱反应:HNO3+ NaOH = NaNO3 +H2O反应无现象;62碳酸氢钠和稀盐酸:NaHCO3 + HCl = NaCl + H2O + CO2↑有气泡产生,固体溶解;63大理石与稀盐酸:CaCO3 + 2HCl = CaCl2 + H2O + CO2↑有气泡,固体溶解;(实验室制CO2)64灭火器原理: Na2CO3 + 2HCl = 2NaCl + H2O + CO2↑有大量气泡产生;65碳酸镁与稀盐酸: MgCO3 + 2HCl = MgCl2 + H2O + CO2↑有气泡,固体溶解;66盐酸和硝酸银溶液反应:HCl + AgNO3 === AgCl↓+ HNO3有白色沉淀产生;67硫酸和碳酸钠:Na2CO3 + H2SO4 = Na2SO4 + H2O + CO2↑气泡产生,固体溶解;68硫酸和氯化钡溶液:H2SO4 + BaCl2 = BaSO4↓+ 2HCl 有白色沉淀产生;69氢氧化钠与硫酸铜:2NaOH + CuSO4 = Cu(OH)2↓+ Na2SO4有蓝色沉淀产生,溶液蓝色变无色;70氢氧化钠与氯化铁:3NaOH + FeCl3 = Fe(OH)3↓+ 3NaCl有红褐色沉淀产生,溶液黄色变无色;71氢氧化钠与氯化镁:2NaOH + MgCl2 = Mg(OH)2↓+ 2NaCl 有白色沉淀产生;72氢氧化钠与氯化铜:2NaOH + CuCl2 = Cu(OH)2↓+ 2NaCl有蓝色沉淀产生,溶液蓝色变无色;73氢氧化钙与碳酸钠:Ca(OH)2 + Na2CO3 = CaCO3↓+ 2NaOH有白色沉淀(工业制氢氧化钠);74氯化铵和熟石灰:2NH4Cl+Ca(OH)2==CaCl2+2NH3↑+2H2O 有刺激性气体产生;75氯化钠和硝酸银:NaCl + AgNO3 = AgCl↓+ NaNO3 有白色沉淀产生;76硫酸钠和氯化钡:Na2SO4 + BaCl2 = BaSO4↓+ 2NaCl 有白色沉淀产生;五、其他反应77光合作用:6CO2 + 6H2O光照C6H12O6+6O2(空气中碳循环主要原因)78葡萄糖缓慢氧化:C6H12O6+6O2点燃6CO2 + 6H2O (身体里产生热量的原因)79甲烷在空气中燃烧:CH4 + 2O2点燃CO2 + 2H2O 明亮的蓝色火焰(瓦斯气体爆炸原因)80酒精在空气中燃烧:C2H5OH + 3O2点燃2CO2 + 3H2O 蓝色火焰;81一氧化碳还原氧化铜:CO+ CuO 加热Cu + CO2 黑色变红色,石灰水变浑浊;82一氧化碳还原氧化铁:3CO+ Fe2O3高温2Fe + 3CO2红色变黑色(铁粉);(高炉炼铁原理)83一氧化碳还原四氧化三铁:4CO+ Fe3O4高温3Fe + 4CO2 (高炉炼铁原理)84苛性钠暴露在空气中变质:2NaOH + CO2 = Na2CO3 + H2O (苛性钠变质原因)85烧碱吸收二氧化硫气体:2NaOH + SO2 = Na2SO3 + H2O(SO2先和水反应生成亚硫酸)(工厂吸收SO2原理)86火碱吸收三氧化硫气体:2NaOH + SO3 = Na2SO4 + H2O (SO3先和水反应先生成硫酸)87二氧化碳能使石灰水变浑浊:Ca(OH)2 + CO2 = CaCO3↓+ H2O 石灰水变浑浊;(检验CO2原理)88消石灰吸收二氧化硫:Ca(OH)2 + SO2 = CaSO3↓+ H2O (SO2也能使石灰水变浑浊)。


初中化学方程式汇总一、氧气:(1)单质与氧气的反应:(化合反应)1.镁在空气中燃烧:2Mg + O2J^=2MgO2.铁在氧气中燃烧:3Fe + 2 O2与Fe3O43.铜在空气中受热:2Cu + O2△ 2CuO4.铝在空气中燃烧:4A1 + 3 O2点燃2A12O35.氢气中空气中燃烧:2H2+ O2工2H2O6.红磷在空气中燃烧(研究空气组成的实验):4P + 5O2 工2P2O57.硫粉在空气中燃烧:S + O2工SO28.碳在氧气中充分燃烧:C + O2CO29.碳在氧气中不充分燃烧:2C + O2三2CO(2)化合物与氧气的反应:10. 一氧化碳在氧气中燃烧:2CO + O2工2CO211.甲烷在空气中燃烧:CH4 + 2 O2工CO2 + 2H2O12.酒精在空气中燃烧:C2H50H + 3 O2三2CO2 + 3H2O(3)氧气的来源:13.玻义耳研究空气的成分实验2HgO △ Hg+ O2 f14.加热高镒酸钾:2KMnO4△ K2MnO4 + MnO2 + 02T (实验室制氧气原理1)15.过氧化氢在二氧化镒作催化剂条件下分解反应:2H2O2 MnO2 2H2O+ O”(实验室制氧气原理2)加热氯酸钾:2KC1O3血@ 2KCl + 3O2 f (实验室制氧气原理3)二、自然界中的水:△17.水在直流电的作用下分解(研究水的组成实验):2H2O 通电2H2f+ O2f18.生石灰溶于水:CaO + H2O _ Ca(OH)219.二氧化碳可溶于水:H2O + CO2一H2cO3三、质量守恒定律:20.镁在空气中燃烧:2Mg + O2点-2MgO21.铁和硫酸铜溶液反应:Fe + CuSO4 _ FeSO4 + Cu22.氢气还原氧化铜:H2 + CuO △ Cu + H2O四、碳和碳的氧化物:(1)碳的化学性质23.碳在氧气中充分燃烧:C + O2工CO224.木炭还原氧化铜:C+ 2CuO高温2Cu + CO2f25.焦炭还原氧化铁:3C+ 2Fe2O3高温4Fe + 3CO2f(2)煤炉中发生的三个反应:(几个化合反应)26.煤炉的底层:C + O2*CO227.煤炉的中层:CO2 + C高温2CO28.煤炉的上部蓝色火焰的产生:2CO + O22CO2(3)二氧化碳的制法与性质:29.大理石与稀盐酸反应(实验室制二氧化碳):CaCO3 + 2HCl == CaCl2 + H2O + CO2T30.碳酸不稳定而分解:H2cO3一H2O + CO2T31.二氧化碳可溶于水:H2O + CO2一H2cO332.高温煅烧石灰石(工业制二氧化碳):CaCO3高温CaO + CO2T33.石灰水与二氧化碳反应(鉴别二氧化碳):Ca(OH)2 + CO2― CaCO3 1+ H2O(4) 一氧化碳的性质:34.一氧化碳还原氧化铜:CO+ CuO 型Cu + CO235.一氧化碳的可燃性:2CO + O2」望=2CO2其它反应:36.碳酸钠与稀盐酸反应(灭火器的原理):Na2CO3 + 2HCl == 2NaCl + H2O + CO2T五、燃料及其利用:37.甲烷在空气中燃烧:CH4 + 2O2 工CO2 + 2H2O38.酒精在空气中燃烧:C2H50H + 3O2 三2CO2 + 3H2O39.氢气中空气中燃烧:2H2 + O2JE= 2H2O六、金属(1)金属与氧气反应:40.镁在空气中燃烧:2Mg + O2点-2MgO41.铁在氧气中燃烧:3Fe + 2O2 工Fe3O442.铜在空气中受热:2Cu + O2△ 2CuO43.铝在空气中形成氧化膜:4Al + 3O2 - 2Al2O3(2)金属单质+酸 ------- 盐+氢气(置换反应)44.锌和稀硫酸Zn + H2sO4一ZnSO4 + H2T45.铁和稀硫酸Fe + H2sO4一FeSO4 + H2T46.镁和稀硫酸Mg + H2sO4一MgSO4 + H2T47.铝和稀硫酸2Al +3H2sO4 _ Al2(SO4)3 +3 H2T48.锌和稀盐酸Zn + 2HCl ZnCl2 + H2T49.铁和稀盐酸Fe + 2HCl FeCl2 + H2T50.镁和稀盐酸Mg+ 2HCl MgCl2 + H2T51.铝和稀盐酸2Al + 6HCl == 2AlCl3 + 3 H2T(3)金属单质+盐(溶液)---------- 新金属+新盐52.铁和硫酸铜溶液反应:Fe + CuSO4FeSO4 + Cu53.锌和硫酸铜溶液反应:Zn + CuSO4ZnSO4 + Cu54.铜和硝酸汞溶液反应:Cu + Hg(NO3)2一Cu(NO3)2 + Hg (3)金属铁的治炼原理:55. 3CO+ 2Fe2O3高温4Fe + 3CO2T七、酸、碱、盐1、酸的化学性质(1)酸+金属 ------- 盐+氢气(见上)(2)酸+金属氧化物——盐+水56.氧化铁和稀盐酸反应:Fe2O3 + 6HCl 2FeCl3 + 3H2O58.氧化铜和稀盐酸反应:CuO + 2HC1 CuCl2 + H2O59.氧化铜和稀硫酸反应:CuO + H2SO4 CuSO4 + H2O (3)酸+碱 --------盐+水(中和反应)60.盐酸和烧碱起反应:HC1 + NaOH NaCl +H2O61.盐酸和氢氧化钙反应:2HCl + Ca(OH)2CaCl2 + 2H2O62.氢氧化铝药物治疗胃酸过多:3HCl + Al(OH)3 _ AlCl3 + 3H2O63.硫酸和烧碱反应:H2SO4 + 2NaOH Na2SO4 + 2H2O(4)酸+盐——另一种酸+另一种盐64.大理石与稀盐酸反应:CaCO3 + 2HCl CaCl2 + H2O + CO2T65.碳酸钠与稀盐酸反应:Na2cO3 + 2HCl 2NaCl + H2O + CO2T66.碳酸氢钠与稀盐酸反应:NaHCO3 + HCl NaCl + H2O + CO2T67.硫酸和氯化钡溶液反应:H2sO4 + BaCl2一BaSO4 1+ 2HCl 2、碱的化学性质(1)碱+非金属氧化物——盐+水68.苛性钠暴露在空气中变质:2NaOH + CO2Na2cO3+ H2O69.苛性钠吸收二氧化硫气体:2NaOH + SO2Na2sO3 + H2O70.苛性钠吸收三氧化硫气体:2NaOH + SO3Na2sO4 + H2O71.消石灰放在空气中变质:Ca(OH)2 + CO2— CaCO3 1+ H2O72.消石灰吸收二氧化硫:Ca(OH)2 + SO2— CaSO3 1+ H2O(2)碱+酸 -------盐+水(中和反应,方程式见上)(3)碱+盐 --------另一种碱+另一种盐73.氢氧化钙与碳酸钠:Ca(OH)2 + Na2cO3一CaCO』+ 2NaOH 3、盐的化学性质(1)盐(溶液)+金属单质——另一种金属+另一种盐74.铁和硫酸铜溶液反应:Fe + CuSO4 _ FeSO4 + Cu(2)盐+酸——另一种酸+另一种盐75.碳酸钠与稀盐酸反应:Na2cO3 + 2HCl 2NaCl + H2O + CO2T碳酸氢钠与稀盐酸反应:NaHCO3 + HCl NaCl + H2O + CO2T (3)盐+碱——另一种碱+另一种盐76.氢氧化钙与碳酸钠:Ca(OH)2 + Na2cO3一CaCO』+ 2NaOH (4)盐+盐-----两种新盐77.氯化钠溶液和硝酸银溶液:NaCl + AgNO3一AgCl] + NaNO378.硫酸钠和氯化钡:Na2SO4 + BaCl2BaSO/ + 2NaCl。

人教版九年级上册化学反应方程式汇总
化学反应方程式是描述化学反应过程中物质间转化关系的表达式。
本文档将为你汇总人教版九年级上册的化学反应方程式。
1. 酸碱中和反应
(1) 酸与碱中和反应
酸与碱反应会生成水和盐。
酸的通式为:HA
碱的通式为:MOH
反应方程式示例:
HA + MOH -> H2O + MA
(2) 金属与酸反应
金属与酸反应会生成盐和氢气。
金属的通式为:M
酸的通式为:HA
反应方程式示例:
M + HA -> MA + H2
2. 氧化还原反应
(1) 金属与非金属氧化物反应
金属与非金属氧化物反应会生成金属氧化物。
金属的通式为:M
非金属氧化物的通式为:Y
反应方程式示例:
2M + Y -> 2MY
(2) 碱金属与非金属氧化物反应
碱金属与非金属氧化物反应会生成碱性氧化物。
碱金属的通式为:X
非金属氧化物的通式为:Y
反应方程式示例:
2X + Y -> X2OY
3. 金属与酸的气体生成反应
金属与酸的气体生成反应会生成盐和氢气。
金属的通式为:M
酸的通式为:HA
反应方程式示例:
M + HA -> MA + H2
以上就是人教版九年级上册化学反应方程式的汇总。
希望对你的学习有所帮助!。

新人教版九年级化学方程式汇总(1-9单元)九年级化学方程式汇总教学案课型:复主备人:顾成红审核:九年级化学组总第62课时时间:201___.____ 班级______ 姓名___________ 学号______学前准备评价:完成下列化学方程式一、化合反应1、镁在空气中燃烧:2Mg + O2 → 2MgO2、铁在氧气中燃烧:3Fe + 2O2 → Fe3O43、铝在氧气中燃烧:4Al + 3O2 → 2Al2O34、氢气在空气中燃烧:2H2 + O2 → 2H2O5、红磷在空气中燃烧:4P + 5O2 → 2P2O56、硫粉在空气中燃烧:S + O2 → SO27、碳在氧气中充分燃烧:C + O2 → CO28、碳在氧气中不充分燃烧:2C + O2 → 2CO9、在空气中加热汞:2Hg + O2 → 2HgO10、氢气在氯气中燃烧:H2 + Cl2 → 2HCl11、二氧化碳通过炽热碳层:C + CO2 → 2CO12、一氧化碳在空气中燃烧:2CO + O2 → 2CO213、二氧化碳和水反应(CO2通入紫色石蕊溶液):CO2 + H2O → H2CO314、生石灰溶于水:CaO + H2O → Ca(OH)2 (该反应是放热反应)二、分解反应15、实验室用过氧化氢溶液和二氧化锰制氧气:2H2O2 → 2H2O + O2↑16、加热高锰酸钾:2KMnO4 △ → K2MnO4 + MnO2 +O2↑17、加热氯酸钾和二氧化锰制氧气:2KClO3 + 2MnO2 △ → 2KCl + 3O2↑ + 2MnO18、电解水:2H2O通电→ 2H2↑ + O2↑(一正氧二负氢)19、碳酸不稳定而分解:H2CO3 → H2O + CO2↑20、高温煅烧石灰石(二氧化碳工业制法):CaCO3高温→ CaO + CO2↑21、加热氧化汞:2HgO△ → 2Hg + O2↑三、置换反应22、氢气还原氧化铜:H2 + CuO△ → Cu + H2O23、木炭还原氧化铜:C + 2CuO高温→ 2Cu + CO2↑24、水蒸气通过灼热碳层:H2O + C高温→ H2 + CO25、焦炭还原氧化铁:3C + 2Fe2O3高温→ 4Fe + 3CO2↑1.化学反应式金属单质和酸反应会产生盐和氢气(置换反应)。

九年级化学上册化学方程式汇总1、木炭在氧气中燃烧:C + O 2点燃CO 2(在氧气中:产生使石灰水变浑浊的无色气体) 2、硫粉在氧气中燃烧: S + O 2点燃SO 2(在空气中:呈淡蓝色火焰;在氧气中:呈明亮的蓝紫色火焰,产生有刺激性气味的气体。
瓶底留少量的水,用于吸收二氧化硫) 3、磷在氧气中燃烧:4P + 5O 2点燃2P 2O 5 (产生浓厚的白烟) 4、铁在氧气中燃烧:3Fe + 2O 2点燃Fe 3O 4(剧烈燃烧,火星四射,生成黑色固体)5、镁在空气中燃烧:2Mg + O 2点燃2MgO (发出耀眼的白光,生成白色固体)6、铜在空气中加热;2Cu + O 2 2CuO (红色固体变为黑色固体)7、氢气在空气中燃烧:2H 2 + O 2点燃2H 2O(产生淡蓝色火焰,干冷烧杯壁有小水株。
或产生爆鸣声) 8、加热高锰酸钾:2KMnO 4△2MnO 4 + MnO 2 + O 2↑9、氯酸钾与二氧化锰的混合物共热:2KClO 3 2KCl + 3O 2↑ 10、实验室用过氧化氢与二氧化锰的混合物制氧气:2H 2O 2 2H 2O+ O 2↑11、水在直流电的作用下分解:2H 2O 通电2H 2↑+O 2 ↑(电极:正氧负氢;体积比:氢二氧) 12、木炭在空气中不充分燃烧:2C + O 2 点燃2CO13、一氧化碳在氧气中燃烧:2CO + O 2点燃2CO 2 (产生蓝色火焰) 14、二氧化碳通过灼热碳层: C + CO 2 高温2CO15、二氧化碳和水反应 :CO 2 + H 2O =H 2CO 3 (CO 2通入紫色石蕊试液,试液由紫色变为红色): 16、碳酸不稳定而分解:H 2CO 3 =H 2O + CO 2↑ 、高温煅烧石灰石:CaCO 3高温CaO + CO 2↑(工业上制二氧化碳的方法)18、木炭还原氧化铜:C+2CuO高温2Cu + CO 2↑(黑色逐渐变为红色、产生使澄清石灰水变浑浊的气体)19、焦炭还原氧化铁:3C+ 2Fe 2O 3高温4Fe + 3CO 2↑20、石灰石(或大理石)与稀盐酸反应(实验室制CO 2):CaCO 3 + 2HCl 错误!未找到引用源。

九年级化学方程式汇总(1-9单元)一、化合反应1、镁在空气中燃烧:镁 + 氧气 氧化镁 2Mg + O 2 点燃 2MgO2、铁在氧气中燃烧:铁 + 氧气 四氧化三铁 3Fe + 2O 2 点燃 Fe 3O 43、红磷在空气中燃烧:磷 + 氧气 五氧化二磷 4P + 5O 2 点燃 2P 2O 54、硫粉在空气中燃烧: 硫 + 氧气 二氧化硫 S + O 2 点燃 SO 25、碳在氧气中充分燃烧:碳 + 氧气 二氧化碳 C + O 2 点燃 CO 26、碳在氧气中不充分燃烧:碳 + 氧气 一氧化碳 2C + O 2 点燃 2CO7、氢气在氯气中燃烧: 氢气 + 氯气 氯化氢 H 2 + Cl 2点燃 2HCl 8、氢气在空气中燃烧:氢气 + 氧气 水 2H 2 + O 2 点燃 2H 2O 9、铝在空气中反应:铝 + 氧气 氧化铝 4Al + 3O 2 点燃 2Al 2O 310、在空气中加热汞:+−−−→加热汞氧气氧化汞 2Hg + O △ 2HgO 11、二氧化碳通过炽热碳层:碳 + 二氧化碳 一氧化碳C + CO 2 高温 2CO12、一氧化碳在空气中燃烧:一氧化碳+ 氧气 二氧化碳2CO + O 2 点燃 2CO 213、二氧化碳和水反应(CO 2通入紫色石蕊溶液):二氧化碳 + 水 碳酸CO 2 + H 2O == H 2CO 314、生石灰溶于水:生石灰 + 水 氢氧化钙 CaO + H 2O === Ca(OH)2 (该反应是放热反应)二、分解反应15、实验室用过氧化氢和二氧化锰制取氧气 :过氧化氢 水 + 氧气 2H 2O 2 2H 2O + O 2↑16、加热高锰酸钾制取氧气:高锰酸钾 锰酸钾 + 二氧化锰 + 氧气 2KMnO 4 K 2MnO 4 + MnO 2 + O 2↑ 17、加热氯酸钾和二氧化锰制取氧气:氯酸钾 氯化钾 + 氧气2KClO 3 2KCl+3O 2↑ 18、电解水:水 氢气 + 氧气 2H 2O 通电 2H 2↑+ O 2 ↑19、碳酸不稳定而分解:碳酸 水+二氧化碳 H 2CO 3 === H 2O + CO 2↑20、高温煅烧石灰石(二氧化碳工业制法):碳酸钙 氧化钙+二氧化碳CaCO 3 CaO + CO 2↑21、加热氧化汞:氧化汞 汞+氧气 2HgO 2Hg + O 2↑ 点燃 点燃点点燃 点 点点 点燃 点燃二氧化锰MnO 加热 △ 二氧化锰 加热MnO△通电 高温 加热△高温三、置换反应22、氢气还原氧化铜:氢气+氧化铜 铜+水 H 2 + CuO Cu + H 2O23、木炭还原氧化铜:碳+氧化铜 铜+水C+ 2CuO 2Cu + CO 2↑ 24、焦炭还原氧化铁:碳+氧化铁铁+二氧化碳3C+ 2Fe 2O 3 4Fe + 3CO 2↑25. 锌+稀硫酸 硫酸锌+氢气 Zn + H 2SO 4 = ZnSO 4 + H 2↑26、铁+稀硫酸 硫酸亚铁+氢气 Fe + H 2SO 4 = FeSO 4 + H 2↑27、镁+稀硫酸 硫酸镁+氢气 Mg + H 2SO 4 = MgSO 4 + H 2↑ 28、铝+稀硫酸 硫酸铝+氢气 2Al +3H 2SO 4 = Al 2(SO4)3 +3H 2↑29、锌+稀盐酸 氯化锌+氢气 Zn + 2HCl === ZnCl 2 + H 2↑30、铁+稀盐酸 氯化亚铁+氢气 Fe + 2HCl === FeCl 2 + H 2↑31、镁+稀盐酸 氯化镁+氢气 Mg+ 2HCl === MgCl 2 + H 2↑32、铝+稀盐酸 氯化铝+氢气 2Al + 6HCl == 2AlCl 3 + 3H 2↑33、铁+硫酸铜 铜+硫酸亚铁 Fe + CuSO 4 === Cu + FeSO 434、铝+硫酸铜 铜+硫酸铝 2Al + 3CuSO 4 === 3 Cu +Al 2(SO 4) 335、锌+硫酸铜 铜+硫酸锌 Zn + CuSO 4 === Cu + ZnSO 436、铜+硝酸银 硝酸银+铜 Cu + AgNO 3 === Ag + Cu(NO 3)2 四、其他反应37、氢氧化钠+硫酸铜 氢氧化铜+硫酸钠 2NaOH + CuSO 4 == Cu(OH)2↓+ Na 2SO 438、石灰石(或大理石)与稀盐酸反应(二氧化碳的实验室制法)碳酸钙+稀盐酸 氯化钙 + 水 + 二氧化碳 CaCO 3 + 2HCl === CaCl 2 + H 2O + CO 2↑39、碳酸钠与盐酸反应(泡沫灭火器的原理)碳酸钠+稀盐酸 氯化钠 + 水 + 二氧化碳 Na 2CO 3 + 2HCl === 2NaCl + H 2O + CO 2↑40、二氧化碳通过澄清石灰水(检验CO 2 ):氢氧化钙+二氧化碳 碳酸钙+水 Ca(OH)2 + CO 2 == CaCO 3↓+ H 2O41、氢氧化钠和二氧化碳反应(除去CO 2 ):氢氧化钠+二氧化碳 碳酸钠+水 加热 高温 △ 高温高温2NaOH + CO 2 ==== Na 2CO 3 + H 2O42、甲烷在空气中燃烧:甲烷+氧气 二氧化碳+水 CH 4 + 2O 2 CO 2 + 2H 2O43、酒精在空气中燃烧:酒精+氧气 二氧化碳+水 C 2H 5OH + 3O 2 2CO 2 + 3H 2O44、一氧化碳还原氧化铜:一氧化碳+氧化铜 铜+二氧化碳CO+ CuO Cu + CO 2 45、一氧化碳还原氧化铁:一氧化碳+氧化铁 铁+二氧化碳3CO+ Fe 2O 3 2Fe + 3CO 2 46、一氧化碳还原四氧化三铁:一氧化碳+四氧化三铁 铁+二氧化碳 4CO+ Fe 3O 4 3Fe + 4CO 2 五、常见的元素符号(30个)H He Li Be B 、 C N O F Ne 、Na Mg Al Si P 、S Cl Ar K Ca 、Mn Fe Cu Zn Ag 、 Ba Pt Au Hg I六、常见元素和根的化合价点燃点燃点燃 点燃加热 △ 高温高温 高温高温九年级化学方程式平常检测NO:班级___ 姓名完成下列化学方程式一、化合反应1、镁在空气中燃烧:2、铁在氧气中燃烧:3、红磷在空气中燃烧:4、硫粉在空气中燃烧:5、碳在氧气中充分燃烧:6、碳在氧气中不充分燃烧:7、氢气在氯气中燃烧:8、氢气在氢气中燃烧:3、铝在空气中反应:9、在空气中加热汞:11、二氧化碳通过炽热碳层:12、一氧化碳在空气中燃烧:13、二氧化碳和水反应(CO2通入紫色石蕊溶液):14、生石灰溶于水(该反应是放热反应):二、分解反应15、实验室用过氧化氢和二氧化锰制氧气:16、加热高锰酸钾:17、加热氯酸钾和二氧化锰制氧气:18、电解水(一正氧二负氢):19、碳酸不稳定而分解:20、高温煅烧石灰石(二氧化碳工业制法):21、加热氧化汞:三、置换反应22、氢气还原氧化铜:23、木炭还原氧化铜:24、焦炭还原氧化铁:25、锌和稀硫酸:26、铁和稀硫酸:27、镁和稀硫酸:28、铝和稀硫酸:30、锌和稀盐酸:31、铁和稀盐酸:32、镁和稀盐酸:33、铝和稀盐酸:34、铁和硫酸铜溶液反应:35、铝和硫酸铜溶液反应:36、锌和硫酸铜溶液反应:四、其他反应37、氢氧化钠溶液与硫酸铜溶液反应:38、石灰石(或大理石)与稀盐酸反应(二氧化碳的实验室制法):39、碳酸钠与盐酸反应(泡沫灭火器的原理):40、二氧化碳通过澄清石灰水(检验CO2):41、氢氧化钠和二氧化碳反应(除去CO2):42、甲烷在空气中燃烧:43、酒精在空气中燃烧:44、一氧化碳还原氧化铜:45、一氧化碳还原氧化铁:46、一氧化碳还原四氧化三铁:五、常见元素的符号(30个):化学方程式自我评价(1-9单元)NO:班级___ 姓名一、完成下列化学方程式,并指出反应类型1、铁在氧气中燃烧:2、硫粉在空气中燃烧:3、一氧化碳在空气中燃烧:4、二氧化碳和水反应(CO2通入紫色石蕊溶液):5、实验室用过氧化氢和二氧化锰制氧气:6、加热高锰酸钾:7、加热氯酸钾和二氧化锰制氧气:8、电解水:9、碳酸不稳定而分解:10、二氧化碳的实验室制法:11、二氧化碳通过澄清石灰水:12、甲烷在空气中燃烧:13、酒精在空气中燃烧:14、一氧化碳还原氧化铁:15、锌和稀硫酸:16、铁和稀盐酸:17、镁和稀盐酸:18、铁和硫酸铜溶液反应:19、铝和硫酸铜溶液反应:20、铜和硝酸汞溶液反应:二、书写常见元素和根的化合价:化学方程式自我评价(1-9单元)NO:班级___ 姓名完成下列化学方程式,并指出反应类型1、二氧化碳和水反应(CO2通入紫色石蕊溶液)2、镁在空气中燃烧:3、氢气在空气中燃烧:4、铝和稀硫酸:5、木炭还原氧化铜:6、二氧化碳通过澄清石灰水:7、红磷在空气中燃烧:8、加热氯酸钾和二氧化锰制氧气:9、硫粉在空气中燃烧:10、铁在氧气中燃烧:11、锌和稀硫酸:12、铁和稀硫酸:13、镁和稀硫酸:14、一氧化碳还原氧化铜:15、加热高锰酸钾:16、电解水:17、镁和稀盐酸:23、碳酸不稳定而分解:24、酒精在空气中燃烧:25、高温煅烧石灰石(二氧化碳工业制法):26、铝和硫酸铜溶液反应:27、铜和硝酸汞溶液反应:30、甲烷在空气中燃烧:31、铁和硫酸铜溶液反应:33、铜和硝酸汞溶液反应:常见物质的化学式检测NO:班级___ 姓名1、气体类:氧气___ 氮气___ 氢气___ 二氧化碳___ 一氧化碳___二氧化硫___ 二氧化氮___ 甲烷___ 氨气___2、液体类:水___ 双氧水____稀盐酸____稀硫酸_____ 碳酸_____ 硝酸______3、固体类:铁___铝___铜___锌___碳___白磷___红磷____ 硫磺___五氧化二磷_____ 氧化铁_____ 四氧化三铁_____二氧化锰_____氧化镁_____氧化铜_____氧化汞_____ 高锰酸钾_________锰酸钾_________氯酸钾_______4、含氯离子的物质的化学式(注意找规律)氯化氢______氯化钠_______氯化钾_____ 氯化锂_____ 氯化铵_____氯化银______氯化镁______氯化钙_____ 氯化钡______氯化锌_____ 氯化铜_____氯化亚铁____氯化铁______氯化铝______ 5、含氢氧根离子的物质的化学式氢氧化钠______ 氢氧化钾_______ 氢氧化银_______氢氧化镁________氢氧化钙 ______ 氢氧化铜_______ 氢氧化锌_______ 氢氧化钡 _______ 氢氧化铝_______氢氧化铁_______6、含铵根离子的物质的化学式氯化铵_________溴化铵 ________硫酸铵 ________碳酸铵_________7、含碳酸根离子的物质的化学式碳酸钠________ 碳酸钾________碳酸银________ 碳酸镁_________碳酸钙_________ 碳酸铜________碳酸钡________碳酸锌_________8、含硝酸根离子的物质的化学式硝酸钠________硝酸钾________ 硝酸银________ 硝酸镁_________硝酸钙________硝酸铜________ 硝酸钡________9、含硫酸根离子的物质的化学式硫酸钠________ 硫酸钾________ 硫酸银________硫酸镁__________硫酸钙________硫酸铜________硫酸锌_________硫酸钡__________硫酸亚铁____________硫酸铁_______________硫酸铝_____________常见物质的化学式1、气体类:氧气:O2氮气:N2氢气:H2二氧化碳:CO2一氧化碳:CO 二氧化硫:SO2二氧化氮:NO2甲烷:CH4氨气:NH32、液体类:水:H2O 双氧水:H2O2稀盐酸:HCl稀硫酸:H2SO4碳酸:H2CO3硝酸:HNO33、固体类:铁:Fe 铝:Al 铜:Cu 锌:Zn 碳:C白磷/红磷P 硫磺:S 五氧化二磷:P2O5氧化铁:Fe2O3四氧化三铁:Fe3O4二氧化锰:MnO2氧化镁:MgO氧化铜:CuO 氧化汞:HgO 高锰酸钾:KMnO4锰酸钾:K2MnO4 氯酸钾:KClO34、含氯离子的物质的化学式(注意找规律)氯化氢:HCl 氯化钠:NaCl 氯化钾:KCl 氯化锂:LiCl 氯化铵:NH4Cl 氯化银:AgCl 氯化镁:MgCl2氯化钙:CaCl2氯化钡:BaCl2氯化锌:ZnCl2氯化铜:CuCl2氯化亚铁:FeCl2氯化铁:FeCl3氯化铝:AlCl35、含氢氧根离子的物质的化学式氢氧化钠:NaOH 氢氧化钾:KOH 氢氧化银:AgOH氢氧化镁:Mg(OH)2氢氧化钙:Ca(OH)2氢氧化铜:Cu(OH)2氢氧化锌:Zn(OH)2氢氧化钡:Ba(OH)2氢氧化铝:Al(OH)3氢氧化铁:Fe(OH)36、含铵根离子的物质的化学式氯化铵:NH4Cl 溴化铵:NH4Br 硫酸铵:(NH4)2SO4碳酸铵:(NH4)2CO37、含碳酸根离子的物质的化学式碳酸钠:Na2CO3 碳酸钾: K2CO3碳酸银:Ag2CO3碳酸镁:MgCO3碳酸钙:CaCO3碳酸铜:CuCO3碳酸钡:BaCO3碳酸锌:ZnCO38、含硝酸根离子的物质的化学式硝酸钠:NaNO3硝酸钾:KNO3硝酸银:AgNO3硝酸镁:Mg(NO3)2硝酸钙:Ca(NO3)2硝酸铜:Cu(NO3)2硝酸钡Ba(NO3)29、含硫酸根离子的物质的化学式硫酸钠:Na2SO4硫酸钾:K2SO4硫酸银:Ag2SO4硫酸镁:MgSO4硫酸钙:CaSO4硫酸铜:CuSO4硫酸锌:ZnSO4硫酸钡:BaSO4硫酸亚铁:FeSO4硫酸铁:Fe2(SO4)3硫酸铝:Al2(SO4)3。

初三化学1-9单元化学方程式总结化学方程式是化学学习中的重要内容,它用简洁的符号和式子表达了化学反应的本质。
对于初三的同学来说,掌握好 1-9 单元的化学方程式是学好化学的关键。
下面我们就来对这些化学方程式进行一个全面的总结。
一、氧气的性质1、碳在氧气中充分燃烧:C + O₂点燃 CO₂这个方程式表示碳和氧气在点燃的条件下生成二氧化碳,是一个常见的燃烧反应。
2、碳在氧气中不充分燃烧:2C + O₂点燃 2CO当氧气不充足时,碳燃烧就会生成一氧化碳。
3、硫在氧气中燃烧:S + O₂点燃 SO₂硫在氧气中燃烧会产生明亮的蓝紫色火焰,生成有刺激性气味的二氧化硫气体。
4、红磷在氧气中燃烧:4P + 5O₂点燃 2P₂O₅红磷燃烧会产生大量的白烟,生成五氧化二磷。
5、铁在氧气中燃烧:3Fe + 2O₂点燃 Fe₃O₄铁在氧气中剧烈燃烧,火星四射,生成黑色的四氧化三铁。
二、制取氧气1、过氧化氢分解制取氧气:2H₂O₂二氧化锰 2H₂O + O₂↑在二氧化锰的催化作用下,过氧化氢分解生成水和氧气。
2、加热氯酸钾制取氧气:2KClO₃二氧化锰、加热 2KCl + 3O₂↑氯酸钾在二氧化锰作催化剂和加热的条件下分解生成氯化钾和氧气。
3、加热高锰酸钾制取氧气:2KMnO₄加热 K₂MnO₄+ MnO₂+ O₂↑高锰酸钾受热分解生成锰酸钾、二氧化锰和氧气。
三、水的电解2H₂O 通电 2H₂↑ + O₂↑通过电解水的实验,我们可以知道水在通电的条件下分解生成氢气和氧气,这个实验也证明了水是由氢元素和氧元素组成的。
四、氢气的性质1、氢气在空气中燃烧:2H₂+ O₂点燃 2H₂O氢气燃烧产生淡蓝色火焰,生成水。
2、氢气还原氧化铜:H₂+ CuO 加热 Cu + H₂O氢气在加热的条件下将氧化铜还原为铜,同时生成水。
五、碳的还原性1、木炭还原氧化铜:C + 2CuO 高温 2Cu + CO₂↑在高温条件下,木炭将氧化铜还原为铜,并生成二氧化碳。
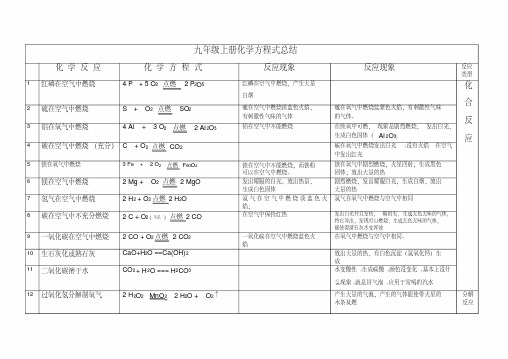
九年级化学方程式汇总教学案(1-9单元)
课型:复习主备人:顾成红审核:九年级化学组总第62课时时间:201___.____ .____ 班级______ 姓名___________学号______学前准备评价
完成下列化学方程式
一、化合反应
1、镁在空气中燃烧:2Mg + O2点燃2MgO
2、铁在氧气中燃烧:3Fe + 2O2点燃Fe3O4
3、铝在氧气中燃烧:4Al + 3O2点燃2Al2O3
4、氢气在空气中燃烧:2H2 + O2点燃2H2O
5、红磷在空气中燃烧:4P + 5O2点燃2P2O5
6、硫粉在空气中燃烧:S + O2点燃SO2
7、碳在氧气中充分燃烧:C + O2点燃CO2
8、碳在氧气中不充分燃烧:2C + O2点燃2CO
*9、在空气中加热汞:2Hg + O2HgO
*10、氢气在氯气中燃烧:H2 + Cl2点燃2HCl
*11、二氧化碳通过炽热碳层:C + CO2高温2CO
12、一氧化碳在空气中燃烧:2CO + O2点燃2CO2
13、二氧化碳和水反应(CO2通入紫色石蕊溶液):CO2 + H2O == H2CO3
*14、生石灰溶于水:CaO + H2O === Ca(OH)2(该反应是放热反应)
二、分解反应
15、实验室用过氧化氢溶液和二氧化锰制氧气:
16、加热高锰酸钾:2KMnO4K2MnO4 + MnO2 + O2↑
17、加热氯酸钾和二氧化锰制氧气:
18、电解水:2H2O 通电2H2↑+ O2 ↑(一正氧二负氢)
19、碳酸不稳定而分解:H2CO3 === H2O + CO2↑
20、高温煅烧石灰石(二氧化碳工业制法):CaCO3高温CaO + CO2↑
21、加热氧化汞:2HgO2Hg + O2↑
三、置换反应
22、氢气还原氧化铜:H2 + CuO Cu + H2O
23、木炭还原氧化铜:C+ 2CuO 高温2Cu + CO2↑
*24、水蒸气通过灼热碳层:H2O + C 高温H2 + CO
25、焦炭还原氧化铁:3C+ 2Fe2O3高温4Fe + 3CO2↑
(1)金属单质+ 酸-------- 盐+ 氢气(置换反应)
26. 锌和稀硫酸Zn + H2SO4 = ZnSO4 + H2↑
27. 铁和稀硫酸Fe + H2SO4 = FeSO4 + H2↑
28. 镁和稀硫酸Mg + H2SO4 = MgSO4 + H2↑
29. 铝和稀硫酸2Al +3H2SO4 = Al2(SO4)3 +3H2↑
30. 锌和稀盐酸Zn + 2HCl === ZnCl2 + H2↑
31. 铁和稀盐酸Fe + 2HCl === FeCl2 + H2↑
32. 镁和稀盐酸Mg+ 2HCl === MgCl2 + H2↑
33. 铝和稀盐酸2Al + 6HCl == 2AlCl3 + 3H2↑
(2)金属单质+ 盐(溶液)------- 另一种金属+ 另一种盐
34. 铁和硫酸铜溶液反应:Fe + CuSO4 === FeSO4 + Cu
35.铝和硫酸铜溶液反应:2Al + 3CuSO4 === Al 2(SO4) 3+3 Cu
36. 铜和硝酸汞溶液反应:Cu + Hg(NO3)2 === Cu(NO3)2 + Hg
37.锌和硫酸铜溶液反应:Zn + CuSO4 === ZnSO4 + Cu
38.铜和硝酸汞溶液反应:Cu+2AgNO3=2Ag+ Cu(NO3)2
四、其他反应
*39、氢氧化钠溶液与硫酸铜溶液反应:2NaOH + CuSO4 == Cu(OH)2↓+ Na2SO4 40、石灰石(或大理石)与稀盐酸反应(二氧化碳的实验室制法):
CaCO3 + 2HCl === CaCl2 + H2O + CO2↑(该反应的应用)
*41、碳酸钠与盐酸反应(泡沫灭火器的原理):
Na2CO3 + 2HCl === 2NaCl + H2O + CO2↑
42、二氧化碳通过澄清石灰水(检验CO2):
Ca(OH)2 + CO2 == CaCO3↓+ H2O (该反应的应用)
*43、氢氧化钠和二氧化碳反应(除去CO2):2NaOH + CO2 ==== Na2CO3 + H2O
44、甲烷在空气中燃烧:CH4 + 2O2点燃CO2 + 2H2O
45、酒精在空气中燃烧:C2H5OH + 3O2点燃2CO2 + 3H2O
46、一氧化碳还原氧化铜:CO+ CuO Cu + CO2
47、一氧化碳还原氧化铁:3CO+ Fe2O3高温2Fe + 3CO2
48、一氧化碳还原四氧化三铁:4CO+ Fe3O4高温3Fe + 4CO2
九年级化学方程式课堂检测(1-9单元) NO:062 时间:201 .____ .____编写:顾成红班级____ 姓名学号____作业评价完成下列化学方程式
一、化合反应
1、镁在空气中燃烧:
2、铁在氧气中燃烧:
3、铝在氧气中燃烧:
4、氢气在空气中燃烧:
5、红磷在空气中燃烧:
6、硫粉在空气中燃烧:
7、碳在氧气中充分燃烧:
8、碳在氧气中不充分燃烧:
*9、在空气中加热汞:
*10、氢气在氯气中燃烧:
*11、二氧化碳通过炽热碳层:
12、一氧化碳在空气中燃烧:
13、二氧化碳和水反应(CO2通入紫色石蕊溶液):
*14、生石灰溶于水(该反应是放热反应):
二、分解反应
15、实验室用过氧化氢和二氧化锰制氧气:
16、加热高锰酸钾:
17、加热氯酸钾和二氧化锰制氧气:
18、电解水(一正氧二负氢):
19、碳酸不稳定而分解:
20、高温煅烧石灰石(二氧化碳工业制法):
21、加热氧化汞:
三、置换反应
22、氢气还原氧化铜:
23、木炭还原氧化铜:
*24、水蒸气通过灼热碳层:
25、焦炭还原氧化铁:
(1)金属单质+ 酸-------- 盐+ 氢气(置换反应)
26. 锌和稀硫酸:
27. 铁和稀硫酸:
28. 镁和稀硫酸:
29. 铝和稀硫酸:
30. 锌和稀盐酸:
31. 铁和稀盐酸:
32. 镁和稀盐酸:
33. 铝和稀盐酸:
(2)金属单质+ 金属的化合物(溶液)------- 另一种金属+ 另一种金属的化合物
34. 铁和硫酸铜溶液反应:
35.铝和硫酸铜溶液反应:
36. 铜和硝酸汞溶液反应:
37.锌和硫酸铜溶液反应:
38.铜和硝酸汞溶液反应:
四、其他反应
*39、氢氧化钠溶液与硫酸铜溶液反应:
40、石灰石(或大理石)与稀盐酸反应(二氧化碳的实验室制法):
(该反应的应用)*41、碳酸钠与盐酸反应(泡沫灭火器的原理):
42、二氧化碳通过澄清石灰水(检验CO2):
(该反应的应用)*43、氢氧化钠和二氧化碳反应(除去CO2):
44、甲烷在空气中燃烧:
45、酒精在空气中燃烧:
46、一氧化碳还原氧化铜:
47、一氧化碳还原氧化铁:
48、一氧化碳还原四氧化三铁:
化学方程式自我评价(1-9单元)班级______ 姓名________ ___学号___ ___成绩
完成下列化学方程式,并指出反应类型(每小题3分,共100分)
1、铁在氧气中燃烧:
2、硫粉在空气中燃烧:
3、一氧化碳在空气中燃烧:
4、二氧化碳和水反应(CO2通入紫色石蕊溶液):
5、实验室用过氧化氢和二氧化锰制氧气:
6、加热高锰酸钾:
7、加热氯酸钾和二氧化锰制氧气:
8、电解水:
9、碳酸不稳定而分解:
10、二氧化碳的实验室制法:
11、二氧化碳通过澄清石灰水:
12、甲烷在空气中燃烧:
13、酒精在空气中燃烧:
14、一氧化碳还原氧化铁:
15、锌和稀硫酸:
16、铁和稀盐酸:
17、镁和稀盐酸:
18、铁和硫酸铜溶液反应:
19、铝和硫酸铜溶液反应:
20、铜和硝酸汞溶液反应:
化学方程式自我评价(1-9单元)班级______ 姓名________ ___学号___ ___成绩
完成下列化学方程式,并指出反应类型(每小题3分,共100分)
1、二氧化碳和水反应(CO2通入紫色石蕊溶液)
2、镁在空气中燃烧:
3、氢气在空气中燃烧:
4、铝和稀硫酸:
5、木炭还原氧化铜:
6、二氧化碳通过澄清石灰水:
7、红磷在空气中燃烧:
8、加热氯酸钾和二氧化锰制氧气:
9、硫粉在空气中燃烧:
10、铁在氧气中燃烧:
11、锌和稀硫酸:
12、铁和稀硫酸:
13、镁和稀硫酸:
14、一氧化碳还原氧化铜:
15、加热高锰酸钾:
16、电解水:
17、镁和稀盐酸:
23、碳酸不稳定而分解:
24、酒精在空气中燃烧:
25、高温煅烧石灰石(二氧化碳工业制法):
26、铝和硫酸铜溶液反应:
27、铜和硝酸汞溶液反应:
30、甲烷在空气中燃烧:
31、铁和硫酸铜溶液反应:
33、铜和硝酸汞溶液反应:。