最新乙苯脱氢制苯乙烯知识讲解
- 格式:doc
- 大小:32.00 KB
- 文档页数:4

乙苯脱氢制苯乙烯方程式一、引言乙苯脱氢制苯乙烯是一种重要的有机合成反应,可以通过乙苯经过脱氢反应生成苯乙烯。
本文将详细介绍乙苯脱氢制苯乙烯的反应方程式、反应机理以及相关应用和工业生产。
二、反应方程式乙苯脱氢制苯乙烯的反应方程式如下所示:C6H6CH3 -> C6H5CH=CH2 + H2反应的主要产物为苯乙烯(C6H5CH=CH2),同时生成氢气(H2)。
三、反应机理乙苯脱氢制苯乙烯的反应机理可以分为两步:1.脱氢反应(去氢化):乙苯分子中的一个氢原子(H)脱离,生成苯乙烯中的一个双键(C=C)。
2.氢迁移反应:生成的苯乙烯发生氢迁移反应,从而使乙苯中的另一个氢原子(H)脱离,生成苯乙烯中的另一个双键(C=C)。
整个反应过程如下所示:C6H6CH3 -> C6H5CH2• + H• (脱氢反应)C6H5CH2• -> C6H5CH=CH2 + H• (氢迁移反应)整个反应过程需要适当的温度和催化剂的存在。
常见的催化剂包括金属氧化物、金属螯合物等。
四、反应条件乙苯脱氢制苯乙烯的反应条件通常为高温和大气压力下进行,一般适用以下条件:•温度:500-600摄氏度•压力:1-10大气压•催化剂:常用的催化剂有二氧化铬、氧化钪、氧化镍等除了上述基本条件外,反应过程中还需要配合适当的反应时间和反应器设计,以及对产物的分离和纯化等工艺的控制。
五、应用和工业生产苯乙烯是一种重要的工业原料,广泛应用于合成橡胶、塑料、纺织品、涂料、颜料等行业。
因此,乙苯脱氢制苯乙烯在工业生产中具有重要的意义。
乙苯脱氢制苯乙烯的工业生产常采用流化床反应器或管式反应器。
工艺流程中需要考虑催化剂的选择和寿命,控制反应温度和压力等参数,以及对产物的分离和纯化等后续处理。
六、总结乙苯脱氢制苯乙烯是一种重要的有机合成反应,通过乙苯经过脱氢反应生成苯乙烯。
本文介绍了该反应的方程式、反应机理以及相关应用和工业生产。
随着化工工业的发展,乙苯脱氢制苯乙烯的研究和应用将继续得到重视,不断改进反应条件和工艺流程,以提高产率和纯度,降低能耗和环境影响。

实验13 乙苯脱氢制苯乙烯一.实验目的1.熟悉乙苯气相催化脱氢制备苯乙烯的过程,明确乙苯脱氢操作条件对产物收率的影响。
2.掌握反应温度控制和测量方法以及加料的控制与计量方法。
3.掌握反应产物的分析测试方法。
二.实验原理乙苯脱氢为可逆吸热反应:主反应: C 8H 10 C 8H 8 + H 2 △H 873K = 125 kJ/mol (2-13-1)除脱氢反应外,还发生一系列副反应,生成苯、甲苯、甲烷、乙烷、烯烃、焦油等,如:C 8H 10 C 6H 6+ C 2H 4 △H 873K = 102 kJ/mol (2-13-2)C 8H 10 + H 2 C 7H 8 + CH 4 △H 873K = - 64.4 kJ/mol (2-13-3) C 8H 10 + H 2 C 6H 6 + C 2H 6 △H 873K = - 41.8 kJ/mol (2-13-4) C 8H 10 8C + 5H 2 △H 873K = - 1.72kJ/mol (2-13-5) 乙苯脱氢反应是一个吸热、摩尔数增多并需要催化剂的复杂过程。
由于反应是吸热反应,随着温度的升高,脱氢反应加快,苯乙烯收率也迅速增加。
反应温度过高,脱氢反应加快,但苯乙烯收率增加变慢,即副反应大大加快,所以反应温度一般控制在550-610℃范围内。
反应(2-13-2)、(2-13-3)是两个主要的平行副反应,这两个副反应的平衡常数大于乙苯脱氢生成苯乙烯的平衡常数,因此,如果从热力学分析看,乙苯脱氢生产苯乙烯的可能性确实不大,所以要采用高选择性的催化剂,增加主反应的反应速率。
常用的乙苯气相催化脱氢制取苯乙烯的催化剂种类很多,通常是以铁(Fe 2O 3)为基础的多组分催化剂,助催化剂有钾(K 2O ),铬(Cr 2O 3)等。
本试验采用铁系催化剂作为乙苯气相脱氢制苯乙烯反应的催化剂。
乙苯气相脱氢制苯乙烯是一个摩尔数增多、体积增大的过程,因而在减压条件下进行对生成苯乙烯有利。

4.2 实验一 乙苯脱氢制苯乙烯一 实验目的(1)了解以乙苯为原料,氧化铁系为催化剂,在固定床单管反应器中制备苯乙烯的过程。
(2)学会稳定工艺操作条件的方法。
二 实验原理1.本实验的主副反应 主反应:副反应:在水蒸气存在的条件下,还可能发生下列反应:此外还有芳烃脱氢缩合苯乙烯聚合生成焦油和焦等。
这些连串副反应的发生不仅使反应的选择性下降,而且极易使催化剂表面结焦进而活性下降。
(1)影响本反应的因素 1)温度的影响乙苯脱氢反应为吸热反应,00>∆H,从平衡常数与温度的关系式20ln RT H T K pp ∆=⎪⎪⎭⎫ ⎝⎛∂∂可知,提高温度可增大平衡常数,从而提高脱氢反应的平衡转化率。
但是温度过高副反应增加,使苯乙烯选择性下降,能耗增大,设备材质要求增加,故应控制适宜的反应温度。
本实验的反应温度为:540~600℃。
2)压力的影响乙苯脱氢为体积增加的反应,从平衡常数与压力的关系式n p K K =γ∆⎪⎪⎭⎫⎝⎛∑i nP 总可知,当γ∆>时,降低总压总P 可使n K 增大,从而增加了反应的平衡转化率,故降低压力有利于平衡向脱氢方向移动。
本实验加水蒸气的目的是降低乙苯的分压,以提高平衡转化率。
较适宜的水蒸气用量为:水∶乙苯=1.5∶1(体积比)或8∶1(摩尔比)。
3)空速的影响乙苯脱氢反应系统中有平衡副反应和连串副反应,随着接触时间的增加,副反应也增加,苯乙烯的选择性可能下降,适宜的空速与催化剂的活性及反应温度有关,本实验乙苯的液空速以0.6h-1为宜。
(2)催化剂本实验采用氧化铁系催化剂其组成为:Fe2O3—CuO—K2O3—CeO2。
三预习与思考(1)乙苯脱氢生成苯乙烯反应是吸热还是放热反应?如何判断?如果是吸热反应,则反应温度为多少?实验室是如何来实现的?工业上又是如何实现的?(2)对本反应而言是体积增大还是减小?加压有利还是减压有利?工业上是如何来实现加减压操作的?本实验采用什么方法?为什么加入水蒸气可以降低烃分压?(3)在本实验中你认为有哪几种液体产物生成?哪几种气体产物生成?如何分析?四实验装置及流程见图4.2-1。


乙苯催化脱氢制苯乙烯的反应
乙苯催化脱氢制苯乙烯是一种重要的化学反应,常用于工业生产中。
这种反应通过催化剂的作用,将乙苯分子中的氢原子去除,形成苯乙烯分子。
苯乙烯是一种重要的有机化合物,广泛应用于橡胶、塑料、合成纤维等领域。
乙苯脱氢制苯乙烯的反应机理是一个复杂的过程,需要催化剂的参与。
常用的催化剂包括氧化锌、氧化铬、氧化铝等。
这些催化剂能够提高反应速率,降低反应温度,减少能量消耗,提高产物纯度。
在乙苯脱氢制苯乙烯的反应过程中,催化剂起着至关重要的作用。
首先,催化剂能够吸附乙苯分子,并使其发生脱氢反应,生成苯乙烯和氢气。
其次,催化剂能够促进反应物分子之间的相互作用,降低反应活化能,提高反应速率。
最后,催化剂还能够防止副反应的发生,提高产物的选择性和纯度。
乙苯脱氢制苯乙烯的反应条件包括温度、压力、催化剂种类和用量等因素。
通常情况下,反应温度在400-600摄氏度之间,压力在1-3大气压之间。
选择合适的催化剂种类和用量,可以有效提高反应效率和产物纯度。
总的来说,乙苯脱氢制苯乙烯是一种重要的工业化学反应,具有广泛的应用前景。
通过优化反应条件和催化剂的选择,可以提高产物的质量和产率,降低生产成本,推动相关行业的发展。

乙苯脱氢制苯乙烯化工11-1 朱伦伦工艺原理以乙苯为原料,按1:3~1:8水比加入过热水蒸汽,在轴径向反应器内,于高温、负压条件下,通过催化剂床层进行乙苯脱氢反应,生成苯乙烯主产品;副反应生成苯、甲苯、甲烷、乙烷、丙烷、H2、CO和CO2。
主反应:Array这是一个强吸热可逆增分子反应。
副反应是热裂解、氢化裂解和蒸汽裂解反应:C6H5CH2CH3→C6H6+C2H4C6H5CH2CH3+H2→C6H5CH3+CH4C6H5CH2CH3+H2→C6H6+C2H6C+2H2O→2H2+CO2CH4+H2O→3H2+COC2H4+2H2O→2CO+4H2水蒸汽变换反应:CO+H2O→H2+CO2在水蒸汽浓度很高时,生成苯、甲苯的反应式可能被下列反应所代替:C6H5CH2CH3+2H2O→C6H5CH3+CO2+3H2C6H5CH2CH3+2H2O→C6H6+CH4+CO2+2H2在乙苯脱氢反应中,原料乙苯中的化学杂质也发生反应,生成物还会进一步发生反应,为此,最终生成物中还含有另一些副产物,如二甲苯、异丙苯、α-甲基苯乙烯、焦油等。
影响化学反应的因素主要有:反应温度、反应压力和水蒸汽/乙苯比(简称水比)。
此外,该反应还受到反应物通过催化剂床层的液体体积时空速度(LHSV)、催化剂性能、原料乙苯中含杂质情况等影响。
反应温度:乙苯脱氢生成苯乙烯的反应为吸热反应,故乙苯转化率随着反应温度的升高而增加。
当温度升高后,不但生成苯乙烯的正反应增加,而且消耗苯乙烯的逆反应以更高的速度增加。
另外,当反应温度提高后,虽然乙苯转化率提高,但副反应(指吸热的副反应)也将加剧,故生成苯乙烯的选择性将降低,因而反应温度不宜过高。
从降低能耗和延长催化剂寿命出发,希望在保证苯乙烯单程收率的前提下,尽量采用较低的反应温度。
反应压力:对于给定的反应温度和水比,乙苯的转化率随着反应压力的降低而显著增加。
在相同的乙苯液体空速和水比下,随着反应压力降低,可相应降低反应温度,而苯乙烯的单程收率维持不变,苯乙烯选择性提高。


乙苯脱氢制苯乙烯实验注意事项
一、实验原理
乙苯脱氢是利用催化剂将乙苯加热至高温,使其分解成苯和乙烯的过程。
该反应是工业上制取苯乙烯的重要方法。
二、实验步骤
1.将催化剂(如氧化钒或氧化铁)加入反应釜中。
2.加入适量的乙苯,并通入氢气。
3.升温至500℃左右,持续反应2-3小时。
4.冷却后,收集产物并进行分析。
三、注意事项
1.实验操作时需佩戴防护手套、护目镜等个人防护装备,以免受到反应物或产物的伤害。
2.反应釜应选择耐高温、耐腐蚀的材料制成,如不锈钢或玻璃等,并保持清洁干燥。
3.催化剂的选择要根据实验需要进行调整,以保证反应效果和产物纯度。
4.通入氢气时需注意控制流量和压力,避免因过高压力导致爆炸事故发生。
5.加热时要慢慢升温,避免温度过高引起反应釜爆炸。
6.收集产物时要使用合适的容器,并进行标记和储存,以免产生混淆或误用。
7.实验结束后,要及时清洗反应釜和设备,并进行妥善保管。
四、实验安全提示
1.实验室内禁止吸烟、饮食等行为,以免引起火灾或中毒事故。
2.实验前要对设备进行检查和试运行,确保其正常工作。
3.实验操作时要严格按照操作规程进行,不得随意更改或省略步骤。
4.如遇到异常情况(如气味异常、产物颜色变化等),应立即停止操作并向有关人员报告。

乙苯脱氢制苯乙烯方程式乙苯脱氢制苯乙烯方程式一、什么是乙苯脱氢制苯乙烯?乙苯脱氢制苯乙烯是一种通过将乙苯加热至高温并在催化剂作用下去除其中的氢原子来得到苯乙烯的化学反应。
这种方法是工业上生产苯乙烯的主要方法之一。
二、反应方程式该反应的化学方程式为:C8H10 → C6H5CH=CH2 + H2即:3C8H10 → 4C6H5CH=CH2 + 2CH4三、反应机理在该反应中,催化剂通常采用铬系或铑系催化剂,它们能够促进氧化还原反应。
具体来说,催化剂会使得乙苯中的一个氢原子离开分子,并与另一个分子中的一个碳原子结合形成甲基基团。
这个甲基基团随后与另外一个分子中的一个碳原子结合形成丁二烯基团。
最终,丁二烯基团会与另外一个分子中的一个碳原子结合形成苯环,并释放出一份氢气。
四、反应条件乙苯脱氢制苯乙烯的反应条件包括温度、压力和催化剂等。
一般来说,该反应需要在高温下进行,通常在500-600℃左右。
此外,该反应需要在高压下进行,通常在1-2 MPa左右。
催化剂方面,目前最常用的是铬系或铑系催化剂。
五、反应优缺点乙苯脱氢制苯乙烯是一种高效的工业生产方法,具有以下优点:1. 反应产物纯度高:该方法可以得到较高纯度的苯乙烯产物,并且可以通过后续处理进一步提高其纯度。
2. 生产成本低:该方法使用的原料成本较低,同时也不需要使用过多能源和催化剂等。
3. 适用范围广:该方法适用于生产大量的苯乙烯,并且可以根据需要进行规模化生产。
但是,该方法也存在以下缺点:1. 需要高温高压环境:由于该方法需要在高温、高压环境下进行反应,因此需要消耗大量能源,并且设备成本也较高。
2. 催化剂使用寿命短:使用铬系或铑系催化剂进行反应时,催化剂的使用寿命较短,需要经常更换。
3. 环境污染:该方法会产生大量废气和废水等,对环境造成一定影响。
六、应用领域苯乙烯是一种重要的有机化学品,广泛应用于塑料、橡胶、纺织、涂料等行业。
因此,乙苯脱氢制苯乙烯是一个非常重要的工业生产方法,在上述领域中得到了广泛应用。

乙苯制取苯乙烯方程式介绍乙苯制取苯乙烯是一种重要的工业过程,用于生产合成橡胶、塑料和纤维等产品。
本文将深入探讨乙苯制取苯乙烯的方程式、反应机理以及相关应用。
乙苯制取苯乙烯的方程式乙苯制取苯乙烯的方程式如下所示:C6H5CH3 -> C6H5CH2 + H2乙苯制取苯乙烯的反应机理乙苯制取苯乙烯的反应机理涉及乙苯的脱氢过程。
乙苯在高温催化剂的作用下发生脱氢反应,生成苯乙烯和氢气两种产物。
具体反应机理如下:1.吸附乙苯在催化剂表面发生吸附,与催化剂形成活性物种。
2.脱氢吸附的乙苯经过脱氢反应,失去一个氢原子,生成苯乙烯。
3.产物解吸生成的苯乙烯和氢气从催化剂表面解吸,脱离催化剂。
乙苯制取苯乙烯的工业应用乙苯制取苯乙烯是一种重要的工业过程,在合成橡胶、塑料和纤维等行业有着广泛的应用。
以下是一些主要的工业应用:1.合成橡胶苯乙烯是生产合成橡胶的重要原料之一。
通过乙苯制取苯乙烯,可以提供充足的原料供应,满足合成橡胶工业的需求。
2.制造塑料苯乙烯是制造塑料的重要原料之一。
经过聚合反应,可以制得聚苯乙烯(PS)等塑料,用于制造各种日常用品和工业产品。
3.生产纤维苯乙烯还可以用于生产合成纤维。
通过乙苯制取苯乙烯,可以提供纤维工业所需的原料,用于生产合成纤维,如聚酰胺纤维等。
4.其他应用苯乙烯还可以用于生产涂料、粘合剂等。
其结构的稳定性和化学性质使其成为多种工业应用的重要原料之一。
总结乙苯制取苯乙烯是一种重要的工业过程,通过脱氢反应将乙苯转化为苯乙烯。
该反应涉及吸附、脱氢和产物解吸等过程。
乙苯制取的苯乙烯广泛应用于合成橡胶、塑料、纤维和涂料等领域,为这些行业提供了重要的原料供应。
以上就是乙苯制取苯乙烯方程式的相关内容,希望能为读者提供一些有用的信息。
感谢阅读!。

乙苯脱氢制苯乙烯引言。
苯乙烯是一种重要的有机化工产品,广泛应用于合成树脂、塑料、橡胶等工业中。
乙苯脱氢制苯乙烯是目前主要的生产工艺之一,其具有高效、低成本等优点,因此备受关注。
本文将对乙苯脱氢制苯乙烯的工艺流程、反应机理、影响因素以及发展趋势进行探讨。
一、乙苯脱氢制苯乙烯的工艺流程。
乙苯脱氢制苯乙烯的工艺流程主要包括催化剂的选择、反应条件的控制以及产品的分离纯化等步骤。
一般而言,该工艺流程可以分为以下几个步骤,乙苯的预热、蒸汽和空气的混合、催化剂的加入、反应器的加热、产物的冷却和分离等。
其中,催化剂的选择对反应的效率和产物的纯度具有重要影响,目前常用的催化剂有铬酸钠、钼酸钠、氧化铝等。
二、乙苯脱氢制苯乙烯的反应机理。
乙苯脱氢制苯乙烯的反应机理主要涉及乙苯分子的脱氢反应。
在催化剂的作用下,乙苯分子中的氢原子被去除,形成苯乙烯分子和水蒸气。
具体而言,乙苯分子首先吸附在催化剂表面,然后发生脱氢反应,生成苯乙烯和水蒸气。
反应机理的研究有助于优化工艺条件,提高反应效率和产物纯度。
三、乙苯脱氢制苯乙烯的影响因素。
乙苯脱氢制苯乙烯的反应受到多种因素的影响,包括温度、压力、催化剂种类和用量、乙苯浓度等。
其中,温度是影响反应速率和产物选择性的重要因素,一般而言,较高的温度有利于提高反应速率,但过高的温度可能导致副反应的发生。
此外,催化剂的种类和用量也对反应的效果有显著影响,不同的催化剂具有不同的活性和选择性,因此需要进行合理选择和控制。
四、乙苯脱氢制苯乙烯的发展趋势。
乙苯脱氢制苯乙烯作为一种重要的有机合成工艺,其发展趋势主要包括提高反应效率、降低生产成本、减少环境污染等方面。
为了提高反应效率,可以通过优化催化剂的性能、改进反应条件、提高乙苯转化率等途径。
同时,降低生产成本也是当前研究的重点之一,可以通过提高催化剂的稳定性和循环利用率、优化产品分离纯化工艺等手段来实现。
此外,减少环境污染也是乙苯脱氢制苯乙烯发展的重要方向,可以通过减少废水排放、提高产物纯度等途径来实现。

实验乙苯脱氢制苯乙烯乙苯脱氢制苯乙烯是一种重要的化学反应,可用于生产苯乙烯。
苯乙烯是一种重要的化学原料,广泛用于塑料、橡胶、纺织和涂料等行业。
本实验旨在使用催化剂将乙苯脱氢制为苯乙烯,同时研究不同反应条件对反应产物的影响。
实验步骤:1. 实验仪器:采用多项仪器进行实验操作,主要包括反应釜、加热器、冷却器、气体净化器、漏斗等。
2. 实验材料:本实验中使用的材料有苯乙烯、乙苯,催化剂、溶剂,以及各种实验用的试剂。
3. 反应条件:反应釜温度在350至450℃之间,催化剂量为反应物的5%,氢气流量控制在0.5至1L/min,同时保持反应时间在2到6小时。
4. 实验流程:将乙苯和催化剂加到反应釜中,逐步加热至设定的反应温度。
当达到一定的温度时,开始向反应釜中通入氢气,同时控制氢气流量和反应时间,完成反应后,用氮气吹干反应釜,并用氢气清洗。
5. 实验分析:收集反应产物,通过色谱分析、质谱分析等手段,分析反应物和产物的组成,探究不同反应条件对产物生成的影响。
实验原理:乙苯脱氢制苯乙烯是将乙苯中的甲基基团和芳香基团分离,生成苯乙烯的反应。
催化剂是反应中的关键,可以选择镍、铂、钒等金属作为催化剂。
氢气在反应中也起着重要作用,通过提供氢离子,防止反应中的芳香基团被进一步氧化。
实验结果:实验结果表明,催化剂种类、温度、氢气流量和反应时间等因素都会影响反应产物的生成。
在相同温度下,镍催化剂的反应活性高于钒催化剂。
同时,反应温度越高,产物的产量越高,但也会导致副反应的增加。
氢气流量和反应时间的控制也在一定程度上影响着反应产物的生成。
结论:本实验的结果表明,乙苯脱氢制苯乙烯是一种复杂的化学反应,受多种因素的影响。
通过对实验过程和产物的分析,可以对反应条件进行优化,使得反应产物的产量和纯度得到提高。
同时,本实验也为进一步的苯乙烯生产工艺研究提供了基础数据。
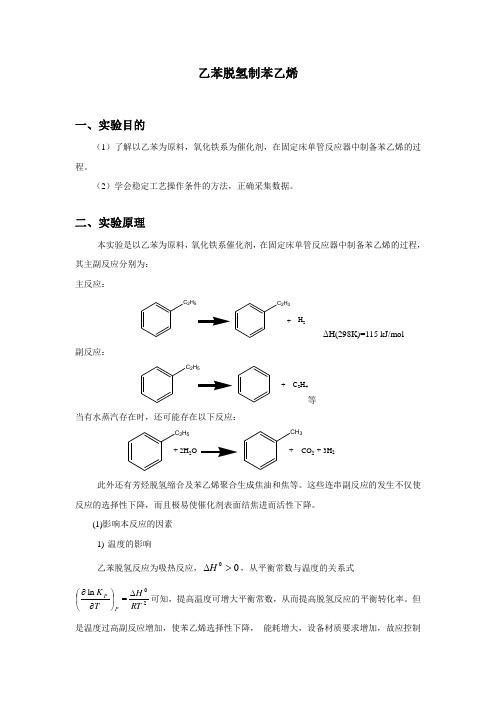
乙苯脱氢制苯乙烯一、实验目的(1)了解以乙苯为原料,氧化铁系为催化剂,在固定床单管反应器中制备苯乙烯的过程。
(2)学会稳定工艺操作条件的方法,正确采集数据。
二、实验原理本实验是以乙苯为原料,氧化铁系催化剂,在固定床单管反应器中制备苯乙烯的过程,其主副反应分别为: 主反应:C 2H5C 2H 3+H 2ΔH(298K)=115 kJ/mol副反应:C 2H5+C 2H 4等当有水蒸汽存在时,还可能存在以下反应:C 2H 5+CO 2+ 2H 2OCH 3+ 3H 2此外还有芳烃脱氢缩合及苯乙烯聚合生成焦油和焦等。
这些连串副反应的发生不仅使反应的选择性下降,而且极易使催化剂表面结焦进而活性下降。
(1)影响本反应的因素 1) 温度的影响乙苯脱氢反应为吸热反应,00>∆H ,从平衡常数与温度的关系式20ln RTH T K P P ∆=⎪⎭⎫⎝⎛∂∂可知,提高温度可增大平衡常数,从而提高脱氢反应的平衡转化率。
但是温度过高副反应增加,使苯乙烯选择性下降, 能耗增大,设备材质要求增加,故应控制适宜的反应温度。
本实验的反应温度为:540~600℃。
2) 压力的影响乙苯脱氢为体积增加的反应,从平衡常数与压力的关系式γ∆⎪⎪⎭⎫ ⎝⎛=∑i n P nP K K 总可知,当0>∆γ时,降低总压总P 可使n K 增大,从而增加了反应的平衡转化率,故降低压力有利于平衡向脱氢方向移动。
本实验加水蒸汽的目的是降低乙苯的分压,以提高平衡转化率。
较适宜的水蒸汽用量为:水:乙苯=1.5:1(体积比)=8:1 (摩尔比)。
3) 空速的影响乙苯脱氢反应系统中有平衡副反应和连串副反应,随着接触时间的增加,副反应也增加,苯乙烯的选择性可能下降,适宜的空速与催化剂的活性及反应温度有关,本实验乙苯的液空速以0.6h -1为宜。
(2)催化剂本实验采用氧化铁系催化剂其组成为:23232CeO O K CuO O Fe ---三、实验流程在汽化温度300℃,脱氢反应温度540~600℃,水:乙苯=1.5:1(体积比),相当于乙苯加料0.5毫升/分,蒸馏水0.75毫升/分(50毫升催化剂)的条件下,考察不同温度对乙苯的转化率、苯乙烯的选择性、收率的影响。


乙苯脱氢工业生产方法
乙苯脱氢是一种重要的化学反应,用于生产苯乙烯。
以下是乙苯脱氢工业生产方法的详细解答:
1. 反应原理:乙苯脱氢反应是一个吸热反应,反应方程式如下:
C8H10 → C8H8 + H2
在催化剂的存在下,乙苯分子中的乙基(-CH2CH3)与氢原子(H)发生脱氢反应,生成苯乙烯(C8H8)和氢气(H2)。
2. 催化剂:乙苯脱氢反应通常使用催化剂来提高反应速率和选择性。
常用的催化剂包括氧化铁、氧化锌、氧化铜等金属氧化物催化剂。
3. 反应条件:乙苯脱氢反应需要在适当的温度、压力和反应物浓度下进行。
一般来说,反应温度在500℃至650℃之间,压力在常压或略高于常压的条件下进行。
反应物浓度通常控制在一定范围内,以确保反应的效率和选择性。
4. 反应器:乙苯脱氢工业生产通常采用固定床反应器或流化床反应器。
在固定床反应器中,催化剂固定在反应器内,反应物通过催
化剂床层进行反应。
而在流化床反应器中,催化剂颗粒在气流的作用下悬浮在反应器内,反应物与催化剂颗粒充分接触进行反应。
5. 产物分离:反应生成的苯乙烯和氢气需要进行分离和提纯。
一般采用冷却和压缩的方法将氢气分离出来,然后通过精馏等方法将苯乙烯提纯。
6. 催化剂再生:催化剂在使用一段时间后会失活,需要进行再生。
催化剂的再生通常采用空气或蒸汽进行氧化处理,以恢复其活性。
乙苯脱氢工业生产方法是一种重要的化工工艺,用于生产苯乙烯等化学品。
通过控制反应条件、选择合适的催化剂和反应器类型,可以实现高效、经济的乙苯脱氢生产过程。



苯乙烯工艺原理您知道苯乙烯吗?这玩意儿在咱们的生活中可有着不小的作用呢!先来说说苯乙烯是咋来的。
简单来讲,它主要是通过乙苯脱氢这个过程产生的。
就好像是一场魔法变身,乙苯这个小家伙在一定的条件下,经历了一系列的变化,就变成了咱们想要的苯乙烯。
那这个过程具体是咋回事呢?您别急,听我慢慢道来。
在反应装置里,温度可是个关键角色。
得把温度控制得恰到好处,就像咱们做饭掌握火候一样。
温度太低,反应就像个懒洋洋的家伙,不怎么动弹;温度太高呢,又可能会把事情搞砸。
所以,找到那个最合适的温度点,可太重要啦!还有压力这一因素,也不能小瞧。
压力就像是给反应施加的一股力量,压力合适,反应就能顺顺利利地进行;压力不合适,反应就可能会闹脾气,达不到咱们想要的效果。
除了温度和压力,催化剂在这个过程中也是个大功臣。
它就像是反应的助推器,能让反应更快、更有效地进行。
没有它,反应可能会变得慢吞吞的,效率低下。
在整个反应过程中,各种物质就像是一群小伙伴,相互合作又相互影响。
它们在装置里一起努力,最终把乙苯变成了宝贵的苯乙烯。
再来说说反应完成后的事儿。
得到的苯乙烯可不能直接就拿去用,还得经过一系列的分离和提纯步骤。
这就像是从一堆混杂的东西里挑出咱们最想要的宝贝。
通过各种巧妙的方法,把苯乙烯和其他杂质分开,让苯乙烯变得更加纯净、更加优质。
分离提纯完了,苯乙烯就准备好去发挥它的大作用啦!它可以用来制造各种各样的东西,比如塑料、橡胶,甚至是一些合成纤维。
是不是很厉害?苯乙烯的工艺原理虽然听起来有点复杂,但其实就像是一场精心编排的舞蹈,每个步骤、每个因素都配合得恰到好处,最终才能跳出美丽的“苯乙烯之舞”。
您觉得怎么样?是不是对苯乙烯的工艺原理有了一点更有趣的认识呢?要是还有啥不明白的,随时来找我唠唠!。

实验十三乙苯脱氢制备苯乙烯一、实验目的1.了解以乙苯为原料,使用氧化铁系催化剂,在固定床单管反应器中制备苯乙烯的过程。
2.学会稳定工艺操作条件的方法。
3.掌握乙苯脱氢制苯乙烯的转化率、选择性、收率与反应温度之间的关系;找出最适宜的反应温度区域。
4.学会使用温度控制和流量控制的一般仪表、仪器。
5.了解气相色谱分析及使用方法。
二、实验内容了解并熟悉实验装置及流程,搞清物料走向及加料、出料方法。
学会使用温度控制和流量控制的一般仪表、仪器。
测定不同温度下乙苯脱氢反应的转化率、苯乙烯的选择性和收率,考察温度对乙苯脱氢反应转化率、苯乙烯选择性和收率的影响。
三、基本原理1.本实验的主副反应主反应:副反应:在水蒸气存在的条件下,还可能发生下列反应:此外还有芳烃脱氢缩合及苯乙烯聚合生成焦油等。
这些连串副反应的发生不仅使反应的选择性下降,而且极易使催化剂表面结焦导致活性下降。
2.影响本反应的因素(1)温度的影响乙苯脱氢反应为吸热反应,∆H o>0,从平衡常数与温度的关系式20ln RT H T K pp ∆=⎪⎪⎭⎫ ⎝⎛∂∂可知,提高温度可增大平衡常数,从而提高脱氢反应的平衡转化率。
但是温度过高使得副反应增加,导致苯乙烯选择性下降,能耗增大,设备材质要求增加,故应控制适宜的反应温度。
本实验的反应温度范围为:540~600℃。
(2)压力的影响乙苯脱氢为体积增加的反应,降低总压P 总可增加反应的平衡转化率,故降低压力有利于平衡向脱氢方向移动。
本实验加水蒸气的目的是降低乙苯的分压,以提高乙苯的平衡转化率。
较适宜的水蒸气用量为:水﹕乙苯=1.5﹕1(体积比)或8﹕1(摩尔比)。
(3)空速的影响乙苯脱氢反应系统中有平行副反应和连串副反应,随着接触时间的增加,副反应也随之增加,苯乙烯的选择性下降,故需采用较高的空速,以提高选择性。
适宜的空速与催化剂的活性及反应温度有关,本实验乙苯的液空速以0.6h -1为宜。
3.催化剂本实验采用以Fe 、K 为主要活性组分,添加少量的I A 、ⅡA 、I B 族氧化物为助剂的GS-08催化剂。
乙苯脱氢制苯乙烯
化工11-1 朱伦伦
工艺原理
以乙苯为原料,按1:3~1:8水比加入过热水蒸汽,在轴径向反应器内,于高温、负压条件下,通过催化剂床层进行乙苯脱氢反应,生成苯乙烯主产品;副反应生成苯、甲苯、甲烷、乙烷、丙烷、H2、CO和CO2。
主反应:Array
这是一个强吸热可逆增分子反应。
副反应是热裂解、氢化裂解和蒸汽裂解反应:
C6H5CH2CH3→C6H6+C2H4
C6H5CH2CH3+H2→C6H5CH3+CH4
C6H5CH2CH3+H2→C6H6+C2H6
C+2H2O→2H2+CO2
CH4+H2O→3H2+CO
C2H4+2H2O→2CO+4H2
水蒸汽变换反应:CO+H2O→H2+CO2
在水蒸汽浓度很高时,生成苯、甲苯的反应式可能被下列反应所代替:
C6H5CH2CH3+2H2O→C6H5CH3+CO2+3H2
C6H5CH2CH3+2H2O→C6H6+CH4+CO2+2H2
在乙苯脱氢反应中,原料乙苯中的化学杂质也发生反应,生成物还会进一步发生反应,为此,最终生成物中还含有另一些副产物,如二甲苯、异丙苯、α-甲基苯乙烯、焦油等。
影响化学反应的因素主要有:反应温度、反应压力和水蒸汽/乙苯比(简称水比)。
此外,该反应还受到反应物通过催化剂床层的液体体积时空速度(LHSV)、催化剂性能、原料乙苯中含杂质情况等影响。
反应温度:乙苯脱氢生成苯乙烯的反应为吸热反应,故乙苯转化率随着反应温度的升高而增加。
当温度升高后,不但生成苯乙烯的正反应增加,而且消耗苯乙烯的逆反应以更高的速度增加。
另外,当反应温度提高后,虽然乙苯转化率提高,但副反应(指吸热的副反应)也将加剧,故生成苯乙烯的选择性将降低,因而反应温度不宜过高。
从降低能耗和延长催化剂寿命出发,希望在保证苯乙烯单程收率的前提下,尽量采用较低的反应温度。
反应压力:对于给定的反应温度和水比,乙苯的转化率随着反应压力的降低而显著增加。
在相同的乙苯液体空速和水比下,随着反应压力降低,可相应降低反应温度,而苯乙烯的单程收率维持不变,苯乙烯选择性提高。
这一特性是由乙苯脱氢生成苯乙烯系增分子反应所决定的。
此外,苯乙烯是容易聚合的物质。
反应压力高,将有利于苯乙烯自聚,生成对装置正常运转十
分不利的聚合物,它会造成管道、设备的堵塞。
降低系统压力,则在一定程度上可抑制苯乙烯聚合。
当今苯乙烯工业生产中采用负压脱氢工艺已成为人们普遍接受的共识和发展潮流。
而脱氢反应器均采用径向反应器,则是由于这种类型反应器的催化剂床层薄,阻力小,有利于在反应区域形成负压操作条件。
水蒸汽/乙苯比(水比):在恒定的反应温度和压力下,较高的水比可使乙苯转化率提高。
因为,蒸汽降低了反应组分的分压,达到类似于降低反应压力的效果。
水蒸汽可与催化剂上生成的碳发生反应,起到减少催化剂表面结焦的作用;水蒸汽还可防止催化剂的活性组份还原为金属,有利于延长催化剂寿命。
对于绝热脱氢工艺来说,加入的过热水蒸汽更是不可缺少的供给反应热的热载体。
在相同的乙苯液体空速和反应压力下,随着水比的降低,为维持一定的苯乙烯单程收率,就需要升高反应温度,炉油中副产苯和甲苯明显增加,苯乙烯选择性下降。
尽管加入水蒸汽有许多好处,但水蒸汽加入量受到反应系统允许压力降和能耗二个因素的制约。
由于高温过热水蒸汽的比容很大,过多加入水蒸汽势必增大反应物流的体积流量,从而增加系统压力降,不利于降低反应区域压力。
此外,增加水蒸汽加入量,必将增加成本,一旦水蒸汽加入量增加到在经济上得不偿失的程度,那么提高水比将是没有意义的。
目前,先进的乙苯脱氢工艺均追求以较低的水比获得较高的苯乙烯收率。
降低水蒸汽单耗已成为衡量一个乙苯脱氢工艺路线是否先进的重要判别指标。
乙苯液体空速(LHSV):在不考虑返混的前提下,可把乙苯液体空速理解为催化剂床层中反应物在1小时内被置换的次数。
空速的倒数具有“时间”因次,称为“空时”。
可粗略地用它来衡量反应物料在催化剂床层中停留时间的长短(相对值)。
因此,空速反映了停留时间对反应的影响。
对于乙苯脱氢反应,在相同的反应压力和水比条件下,随着乙苯投料量的增大,即乙苯液体空速增大,欲维持苯乙烯单程收率不变,就得相应提高反应温度。
液体空速是催化剂性能的重要标志之一。
液体空速大,意味着反应器单位体积的生产能力大。
因此,在相同的反应条件(温度、压力、水比)下,在工艺允许范围内,追求用较大的液体空速进行生产。
催化剂:脱氢反应是乙苯在催化剂床层中,于600℃左右高温下发生的催化脱氢反应。
所用催化剂的性能除了脱氢活性之外,特别重要的是对于生成苯乙烯的选择性要高,并且在高温和水蒸汽存在条件下的稳定性要好,使用寿命要长,这些都是至关重要的。
脱氢催化剂的毒物是氯离子,必须控制进料中的氯离子含量,以防催化剂中毒失效,更重要的是在催化剂床层中不能有游离水。
催化剂床层进水,则催化剂结块和有效成份流失,导致床层阻力上升,最终影响转化率、选择性指标。
原料乙苯中杂质的影响:原料乙苯的质量,应符合SH/T1140中的一级品的指标,此时,即能满足催化剂对原料乙苯中氯离子含量的要求。
在乙苯中所含的异丙苯对脱氢反应也产生一定的影响。
异丙苯在乙苯脱氢工艺条件下同样发生脱氢反应,生成α-甲基苯乙烯。
它的反应必定占据一些催化活性中心。
乙苯异构化脱氢也生成α-甲基苯乙烯,故副产物α-甲基苯乙烯的生成量既与原料乙苯中异丙苯含量有关,也与乙苯异构化脱氢反应
有关。
实验三练习题
单选题
1.Windows操作系统是______。
A)实时操作系统B)分时操作系统
C)多任务单用户操作系统D)多任务多用户操作系统
2.在Windows中,用于在对话框的各选项之间切换的键盘按键是______。
A)Esc B)Tab C)Shift D)Alt
3.用鼠标双击Windows窗口的标题栏,有可能______。
A)隐藏该窗口B)关闭该窗口
C)最大化该窗口D)最小化该窗口
4.Windows回收站中不可能是以下内容______。
A)文件夹B)硬盘中的文件
C)快捷方式D)软盘中的文件
5.Windows“任务栏”上呈凹陷状的按钮所对应的程序是______。
A)系统正在运行的所有程序B)系统中保存的所有程序
C)系统后台运行的程序D)系统前台运行的程序
6.Windows的“控制面板”无法完成______。
A)改变桌面背景B)添加或删除输入方法
C)设置拨号网络D)添加或删除调制解调器
7.当用户不清楚某个文档或文件夹位于何处时,可以使用______命令来寻找并打开它。
A)程序B)文档
C)帮助D)搜索
8.在“资源管理器”中双击扩展名为.TXT的文件,将启动______。
A)写字板B)记事本
C)剪贴板D)Word
9.在Windows中,多义文件名?W??.TXT表示的文件范围是______。
A)主文件名长度不超过4个字符,且第一个字符为W,扩展名为TXT的所有文件
B)主文件名长度任意,且第一个字符为W,扩展名为TXT的所有文件
C)主文件名长度不超过4个字符,且第二个字符为W,扩展名为TXT的所有文件
D)主文件名长度任意,且第二个字符为W,扩展名为TXT的所有文件
10.下列有关文件夹命名规则的描述中,正确的是______。
A)文件夹名的长度可以任意
B)磁盘上所有文件夹的名称均可由用户自行命名
C)不同级的文件夹可以同名,同级的文件夹也可以同名
D)大写和小写字母在文件夹名中将被视为不同
11.Windows的媒体播放器不能处理的文件格式是______。
A)W A V文件B)JPG文件
C)A VI文件D)MPEG文件
12.在Windows资源管理器窗口中,主菜单栏中有“文件(F)”菜单,则按______键选择该菜单。
A)Alt+F B)Ctrl+F
C)Shift+F D)F
13.在上题中,它展开的下拉菜单中有“打开(O)”命令项,则按______键选择该命令项。