化学必修二专题2《化学反应与能量变化》复习
- 格式:docx
- 大小:99.86 KB
- 文档页数:18


高中化学必修二第二章化学反应与能量知识点总结第二章化学反应与能量第一节化学能与热能1、化学反应总伴随着能量的变化。
这是因为在化学反应中,断开反应物中的化学键需要吸收能量,而形成生成物中的化学键则会放出能量。
因此,化学键的断裂和形成是化学反应中能量变化的主要原因。
一个化学反应是吸收能量还是放出能量,取决于反应物总能量与生成物总能量的相对大小。
如果反应物总能量大于生成物总能量,则为放热反应;如果反应物总能量小于生成物总能量,则为吸热反应。
2、常见的放热反应和吸热反应包括:①所有的燃烧和缓慢氧化;②酸碱中和反应;③金属与酸反应制取氢气;④大多数化合反应(特殊情况:C+CO2→2CO是吸热反应)。
常见的吸热反应包括:①以C、H2、CO为还原剂的氧化还原反应,例如C(s)+H2O(g)→CO(g)+H2(g);②铵盐和碱的反应,例如Ba(OH)2·8H2O+NH4Cl→BaCl2+2NH3↑+10H2O;③大多数分解反应,例如KClO3、KMnO4、CaCO3的分解等。
3、能源可以分为一次能源和二次能源。
一次能源是指未经加工、转化的能源,例如水能、风能、生物质能、煤、石油、天然气等化石能源。
二次能源是指一次能源经过加工、转化得到的能源,例如电能(水电、火电、核电)、蒸汽、工业余热、酒精、汽油、焦炭等。
可再生资源包括太阳能、风能、地热能、潮汐能、氢能、沼气等,而不可再生资源则包括核能。
思考]一般来说,大多数化合反应是放热反应,大多数分解反应是吸热反应,放热反应都不需要加热,吸热反应都需要加热,这种说法对吗?试举例说明。
点拔:这种说法不正确。
例如,C+O2→CO2的反应是放热反应,但是需要加热才能开始反应。
反应开始后不再需要加热,因为反应放出的热量可以使反应继续下去。
另一方面,Ba(OH)2·8H2O与NH4Cl的反应是吸热反应,但是反应并不需要加热。
第二节化学能与电能1、化学能可以通过火电、原电池等方式转化为电能。

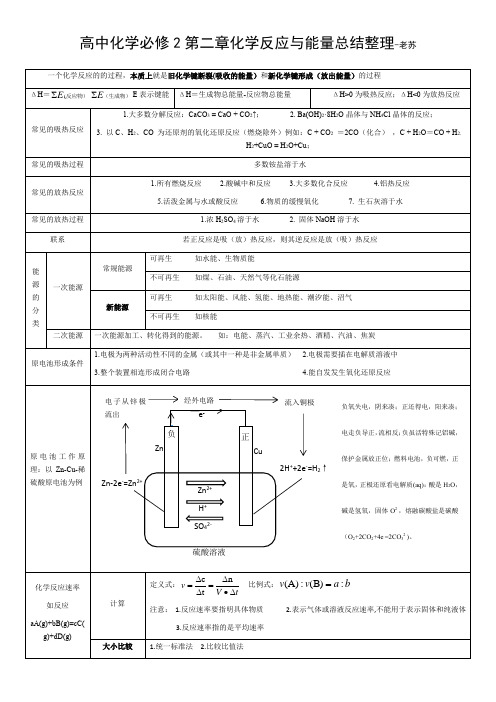
高中化学必修2第二章化学反应与能量总结整理-老苏一个化学反应的的过程,本质上就是旧化学键断裂(吸收的能量)和新化学键形成(放出能量)的过程 ΔH =(生成物)反应物)E E ∑∑-( E 表示键能 ΔH =生成物总能量-反应物总能量 ΔH>0为吸热反应;ΔH<0为放热反应常见的吸热反应1.大多数分解反应:CaCO 3 = CaO + CO 2↑;2. Ba(OH)2·8H 2O 晶体与NH 4Cl 晶体的反应;3. 以C 、H 2、CO 为还原剂的氧化还原反应(燃烧除外)例如:C + CO 2 =2CO (化合) ,C + H 2O =CO + H 2,H 2+CuO = H 2O+Cu ;常见的吸热过程多数铵盐溶于水常见的放热反应1.所有燃烧反应2.酸碱中和反应3.大多数化合反应4.铝热反应5.活泼金属与水或酸反应6.物质的缓慢氧化7. 生石灰溶于水常见的放热过程1.浓H 2SO 4溶于水2. 固体NaOH 溶于水 联系若正反应是吸(放)热反应,则其逆反应是放(吸)热反应能源的分类一次能源常规能源可再生 如水能、生物质能不可再生 如煤、石油、天然气等化石能源新能源可再生 如太阳能、风能、氢能、地热能、潮汐能、沼气不可再生 如核能二次能源一次能源加工、转化得到的能源。
如:电能、蒸汽、工业余热、酒精、汽油、焦炭 原电池形成条件1.电极为两种活动性不同的金属(或其中一种是非金属单质)2.电极需要插在电解质溶液中3.整个装置相连形成闭合电路4.能自发发生氧化还原反应原电池工作原理:以Zn -Cu -稀硫酸原电池为例化学反应速率如反应 aA(g)+bB(g)=cC(g)+dD(g)计算定义式:tV v ∆•∆=∆∆=nt c 比例式:b a v v :)B (:)A (= 注意: 1.反应速率要指明具体物质 2.表示气体或溶液反应速率,不能用于表示固体和纯液体 3.反应速率指的是平均速率 大小比较 1.统一标准法 2.比较比值法2H ++2e -=H 2↑硫酸溶液Zn -2e -=Zn 2+e -CuZn正 负H + Zn 2+ SO 42-电子从锌极流出经外电路流入铜极负氧失电,阴来凑;正还得电,阳来凑;电走负导正,流相反;负虽活特殊记铝碱,保护金属放正位;燃料电池,负可燃,正是氧,正极还原看电解质(aq):酸是H 2O ,碱是氢氧,固体O 2-,熔融碳酸盐是碳酸(O 2+2CO 2+4e -=2CO 32-)。

本章重难点专题突破一 详析化学反应中热量的变化我们在做化学实验时,经常会感受到有热量的变化,比如钠与水的反应等,其实在化学反应中,不仅有物质的变化,即新物质的生成,而且还伴随着能量的变化,有的反应是吸热的,有的反应是放热的。
而化学反应中物质变化的实质是旧化学键断裂和新化学键形成。
化学反应是化学科学研究的核心,化学反应过程中的物质变化要遵循质量守恒定律,而能量变化要遵循能量守恒定律。
在化学反应过程中一定存在着能量的变化,而这些能量变化大多数表现为热量的变化,这就实现了化学能与热能的转化。
1.从化学键的角度理解在化学变化前后,参加反应的原子的种类和个数并没有改变,只是进行了原子之间的重组和整合;原子进行重组、整合的过程,实际上就是反应物中化学键断裂和生成物中化学键形成的过程。
由于反应物中化学键的断裂要消耗能量,而生成物中化学键的形成要释放能量,因此我们将化学反应中能量变化表示为反应物――――――――――――→旧化学键断裂吸收能量新化学键形成释放能量生成物 这样,当反应中吸收的能量大于释放的能量,则反应表现为吸收能量,该反应为吸热反应; 当反应中吸收的能量小于释放的能量,则反应表现为放出能量,该反应为放热反应。
【典例1】 已知:①1 mol H 2分子中化学键断裂时需吸收436 kJ 的能量;②1 mol Cl 2分子中化学键断裂时需吸收243 kJ 的能量;③由氢原子和氯原子形成1 molHCl 分子时释放 431 kJ 的能量。
则1 mol H 2和1 mol Cl 2反应生成氯化氢气体时的能量变化为( )A .放出能量183 kJB .吸收能量183 kJC .吸收能量248 kJD .吸收能量862 kJ解析 根据反应的化学方程式:H 2+Cl 2=====点燃2HCl ,可知在反应过程中,断裂1 mol H —H键、1 molCl —Cl 键,同时形成2 mol H —Cl 键。
计算可知生成2 molHCl 气体时,吸收的热量为436 kJ +243 kJ =679 kJ ,放出的热量为431 kJ ×2=862 kJ ,故反应中放出的热量为862 kJ -679 kJ =183 kJ ,A 对。

例:灼热的炭与二氧化碳的反应、炭和水蒸气的反应、氢气还原氧化铜、Ba(OH)2·8H 2O 与NH 4Cl 的反应、大多数分解反应等。
(二)、化学能与电能⑴化学能与电能的相互转化①火力发电——化学能间接转化为电能化学能−−−→−燃烧热能−−→−蒸气机械能−−−→−发电机电能 ②原电池——化学能直接转化为电能的装置。
⑵①铜—锌原电池的工作原理:②原电池形成的一般条件:Ⅰ 有能自发进行的氧化还原反应。
Ⅱ 相连接的两个电极(金属或非金属导体及其它可以做电极材料的物质)。
Ⅲ 两电极同时与电解质溶液接触。
Ⅳ 形成闭合回路。
③原电池的实质:氧化还原反应分开在两极进行,还原剂所失去的电子通过导线转移给氧化剂。
④原电池原理的应用:Ⅰ 实验室制氢气。
为加快氢气的产生速率,可用粗Zn 或Zn 粒,先用CuSO 4溶液浸泡一会儿 或向反应液中加入少量的CuSO 4溶液。
Ⅱ 可判断金属的活泼性。
若由两种活动性不同的金属做电极,则较活泼的金属做负极(一般情况下)。
Ⅲ 制化学电源(电池)。
如干电池、蓄电池、燃料电池、高能电池。
a .一次电池:放电之后不能充电(内部的氧化还原反应是不可逆的)。
如干电池等。
b .二次电池(充电电池):在放电时所进行的氧化还原反应,在充电时可以逆向进行(一般通过充电器将交流电转变为直流电),使电池恢复到放电前的状态。
这样可以实现化学能转变为电能(放电),再由电能转变为化学能(充电)的循环。
如铅蓄电池、镍镉电池、镍氢电池等。
c .燃料电池:利用原电池的工作原理将燃料和氧化剂(如氧气)反应所放出的能量直接转化为电能。
通常通过外设装备将燃料送入原电池的负极,而将氧化剂送入原电池的正极,这时电池起着类似于试管、Ⅰ尽可能使燃料充分燃烧,提高能量的转化率。
关键是燃料与空气或氧气要尽可能充分地接触,且空气要适当过量。
Ⅱ尽可能充分地利用燃料燃烧所释放的热能,提高热能的利用率。
提高燃料的燃烧效率实质上是从多方面控制燃烧反应的条件(包括环境)。

必修二 专题2《化学反应与能量变更》复习一、化学反应的速度和限度 1. 化学反应速率(v )⑴ 定义:用来衡量化学反应的快慢,单位时间内反应物或生成物的物质的量的变更 ⑵ 表示方法:单位时间内反应浓度的削减或生成物浓度的增加来表示⑶ 计算公式:v=Δc/Δt (υ:平均速率,Δc :浓度变更,Δt :时间)单位:mol/(L •s )应速率不变。
(2)、惰性气体对于速率的影响:①恒温恒容时:充入惰性气体→总压增大,但是各分化学反应速率 意义:衡量化学反应快慢物理量 表达式:v = △c/△t 【单位:mol/(L ·min)或mol/(L ·s) 】 简洁计算:同一化学反应中各物质的反应速率之比等于各物质的化学计量数之比,也等于各物质的浓度变更量之比 影响因素 内因:反应物的结构的性质 外因 浓度:增大反应物的浓度可以增大加快反应速率;反之减小速率 温度:上升温度,可以增大化学反应速率;反之减小速率 催化剂:运用催化剂可以改变更学反应速率 其他因素:固体的表面积、光、超声波、溶剂压强(气体): 增大压强可以增大化学反应速率;反之减小速率压不变,各物质浓度不变→反应速率不变②恒温恒体时:充入惰性气体→体积增大→各反应物浓度减小→反应速率减慢2.化学反应限度:大多数化学反应都具有可逆性,故化学反应都有肯定的限度;可逆反应的限度以到达化学平衡状态为止。
在肯定条件下的可逆反应,当正反应速率等于逆反应速率、各组分浓度不再变更时,反应到达化学平衡状态。
(1)化学平衡定义:化学平衡状态:肯定条件下,当一个可逆反应进行到正逆反应速率相等时,更组成成分浓度不再变更,达到表面上静止的一种“平衡”,这就是这个反应所能达到的限度即化学平衡状态。
(2)化学平衡的特征:动:动态平衡等:υ(正)=υ(逆)≠0定:各组分的浓度不再发生变更变:假如外界条件的变更,原有的化学平衡状态将被破坏(3)化学平衡必需是可逆反应在肯定条件下建立的,不同的条件将建立不同的化学平衡状态;通过反应条件的限制,可以变更或稳定反应速率,可以使可逆反应朝着有利于人们须要的方向进行,这对于化学反应的利用和限制具有重要意义。
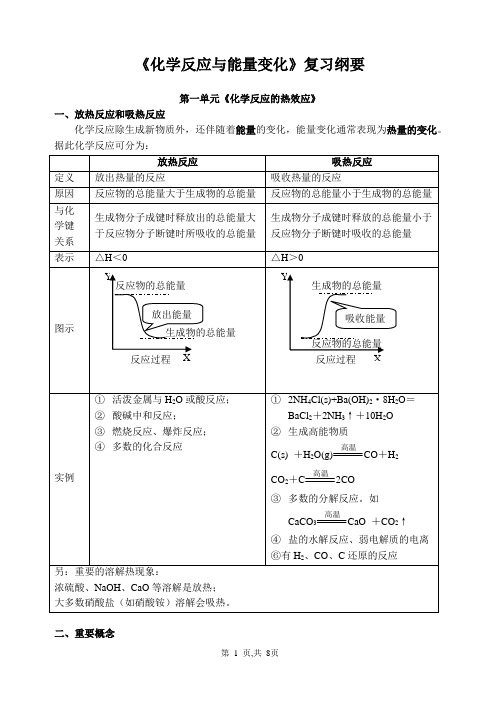
《化学反应与能量变化》复习纲要第一单元《化学反应的热效应》一、放热反应和吸热反应化学反应除生成新物质外,还伴随着能量的变化,能量变化通常表现为热量的变化。
据此化学反应可分为:二、重要概念1、反应热:当化学反应的反应物和产物的温度相同,反应中所放出或吸收的热量称为反应热。
2、焓:物质内部所具有的能量。
焓是物质的一种固有性质。
在一定条件下,一定量的物质具有确定的焓值,但目前人们无法求得,只能判断其相对值。
3、焓变:指反应产物的总焓与反应物的总焓之差。
焓变:△H =H 产物-H 反应物。
单位:kJ ·mol -1。
焓变与反应热的关系:在等压条件下,如果反应中物质的能量变化全部转化为热能的形式,没有其他形式的能量转化,这时的前后焓变即为反应热。
否则,焓变就可能还包含其他形式的能量转化,如光、电、波等。
一般说:反应热=焓变=△H4、燃烧热:25℃,101KPa 时,1mol 物质完全燃烧生成稳定化合物时所放出的热量叫做燃烧热。
一般:C→CO 2(g ),H→H 2O (l ),S→SO 2(g ),N→N 2(g )*苏教版中“标准燃烧热”:指25℃,101KPa 下,1mol 物质完全燃烧生成稳定化合物时的反应热。
或在标准态下,298K 时,1mol 物质完全燃烧的焓变,称为该物质的标准燃烧焓..... 另:写燃烧反应的热化学方程式时,一般可燃物都以1mol 为系数,其他可以是分数。
5、中和热:在稀溶液中,强酸和强碱中和反应,生成1mol H 2O 时的反应热。
注意:①强酸和强碱中和热:H +(aq)+OH -(aq)=H 2O(l);△H =-57.3kJ/mol :。
②弱酸弱碱的中和反应,放出的热会低于57.3 kJ/mol 。
③浓酸、浓碱反应,会受到稀释溶解放热的影响 三、热化学方程式1、定义:能够表示反应热的化学方程式。
2、书写注意:a.标明物质的聚集状态。
如s 、l 、g 、aq 等。

第二章 化学反应与能量第一节 化学能与热能1、在任何的化学反应中总伴有能量的变化。
原因:当物质发生化学反应时,断开反应物中的化学键要吸收能量,而形成生成物中的化学键要放出能量。
化学键的断裂和形成是化学反应中能量变化的主要原因。
一个确定的化学反应在发生过程中是吸收能量还是放出能量,决定于反应物的总能量与生成物的总能量的相对大小。
E 反应物总能量>E 生成物总能量,为放热反应。
E 反应物总能量<E 生成物总能量,为吸热反应。
2、常见的放热反应和吸热反应常见的放热反应:①所有的燃烧与缓慢氧化。
②酸碱中和反应。
③金属与酸反应制取氢气。
④大多数化合反应(特殊:C +CO 2 △ 2CO 是吸热反应)。
常见的吸热反应:①以C 、H 2、CO 为还原剂的氧化还原反应如:C(s)+H 2O(g)△ CO(g)+H 2(g)。
②铵盐和碱的反应如Ba(OH)2·8H 2O +NH 4Cl =BaCl 2+2NH 3↑+10H 2O③大多数分解反应如KClO 3、KMnO 4、CaCO 3的分解等。
[思考]一般说来,大多数化合反应是放热反应,大多数分解反应是吸热反应,放热反应都不需要加热,吸热反应都需要加热,这种说法对吗?试举例说明。
点拔:这种说法不对。
如C +O 2=CO 2的反应是放热反应,但需要加热,只是反应开始后不再需要加热,反应放出的热量可以使反应继续下去。
Ba(OH)2·8H 2O 与NH 4Cl 的反应是吸热反应,但反应并不需要加热。
第二节 化学能与电能2、原电池原理(1)概念:把化学能直接转化为电能的装置叫做原电池。
(2)原电池的工作原理:通过氧化还原反应(有电子的转移)把化学能转变为电能。
(3)构成原电池的条件:(1)电极为导体且活泼性不同;(2)两个电极接触(导线连接或直接接触);(3)两个相互连接的电极插入电解质溶液构成闭合回路。
(4)电极名称及发生的反应:负极:较活泼的金属作负极,负极发生氧化反应,电极反应式:较活泼金属-ne -=金属阳离子负极现象:负极溶解,负极质量减少。

高中化学必修二第二章化学反应与能量变化知识点总结本文档将对高中化学必修二第二章化学反应与能量变化的知识点进行总结。
1. 化学反应的能量变化化学反应中涉及能量的变化,主要包括以下几个方面:- 反应热:- 定义:指在化学反应过程中放出或吸收的热量。
- 测定方法:常用的测定方法是通过热量计测量反应过程中释放或吸收的热量。
- 表示方法:通常用反应热的值ΔH表示,单位是焦耳(J)或千焦(kJ)。
- 绝热条件下的反应:- 定义:在绝热条件下进行的化学反应,即反应过程中不向外界环境传递热量。
- 特点:绝热条件下反应,反应热全部转化为内能变化。
- 反应焓变:- 定义:指在恒定温度下,反应过程中物质的焓变化。
- 表示方法:通常用反应焓变的值ΔH表示,单位是焦耳(J)或千焦(kJ)。
- 计算方法:反应焓变可以通过物质的化学方程式以及相应的热化学方程式计算得出。
2. 热化学方程式- 定义:用化学方程式表示化学反应热变化的方程式。
- 特点:热化学方程式中通过ΔH表示反应焓变,反应方程式左右两边所表示物质的热焓之和之差就是反应焓变的大小。
3. 反应焓变的计算反应焓变的计算方法主要有以下几种:- 反应焓和化学计量数的关系;- 沿反应焓变链计算反应焓变;- 根据物质的标准热焓计算反应焓变。
4. 热力学第一定律- 定义:也称能量守恒定律,指能量可以从一种形式转化为其他形式,但总能量不变。
- 表示方法:数学形式为ΔU=Q-W,其中ΔU表示系统内能的变化,Q表示系统吸收的热量,W表示系统对外做功。
5. 化学反应的放热与吸热- 放热反应:- 定义:指化学反应过程中释放热量的反应。
- 特点:放热反应的反应热为负值,系统的能量减少,周围环境温度上升。
- 吸热反应:- 定义:指化学反应过程中吸收热量的反应。
- 特点:吸热反应的反应热为正值,系统的能量增加,周围环境温度下降。
以上是关于高中化学必修二第二章化学反应与能量变化的知识点总结,希望对你有所帮助!。

第二章 化学反应与能量变化 班级 姓名 第一节 化学能与热能1、化学反应的本质:旧化学键的断裂,新化学键的生成过程。
化学键的断裂需要吸收能量,化学键的形成会释放能量。
任何化学反应都会伴随着能量的变化。
①放出能量的反应:反应物的总能量 > 生成物的总能量②吸收能量的反应:反应物的总能量 < 生成物的总能量2、能量守恒定律:一种形式的能量可以转化为另一种形式的能量,转化的途径和能量形式可以不同,但是体系包含的总能量不变。
化学反应中的能量变化通常表现为热量的变化,即吸热或者放热。
3、常见的放热反应:①所有的燃烧反应;②酸碱中和反应;③活泼金属与酸(或水)的反应;④绝大多数的化合反应;⑤自然氧化(如食物腐败)。
常见的的吸热反应:①铵盐和碱的反应;②绝大多数的分解反应。
第二节 化学能与电能1、一次能源:直接从自然界取得的能源。
如流水、风力、原煤、石油、天然气、天然铀矿。
二次能源:一次能源经过加工,转换得到的能源。
如电力、蒸汽等。
2、原电池:将化学能转化为电能的装置。
右图是铜锌原电池的装置图。
①锌片(负极反应):22Zn e Zn -+-=,发生氧化反应;铜片(正极反应):222H e H +-+=↑,发生还原反应。
总反应:Zn+2H +=Zn 2++H 2↑②该装置中,电子由锌片出发,通过导线到铜片,电流由铜片出发,经过导线到锌片。
③该装置中的能量变化:化学能转化为电能。
④由活泼性不同的两种金属组成的原电池中,一般比较活泼的金属作原电池的负极(发生氧化反应),相对较不活泼的金属作原电池的正极(发生还原反应,正极电极本身不反应!)。
⑤构成原电池的四个条件:1、自发的氧化还原反应;2、活泼性不同的两个电极(导体);3、有电解质溶液;4、形成闭合回路。
第三节 化学反应速率和限度1、化学反应速率:通常用单位时间内反应物浓度的减少量或生成物浓度的增加量(均取正值)来表示。
浓度常以mol/L 为单位,时间常以min 或s 为单位。
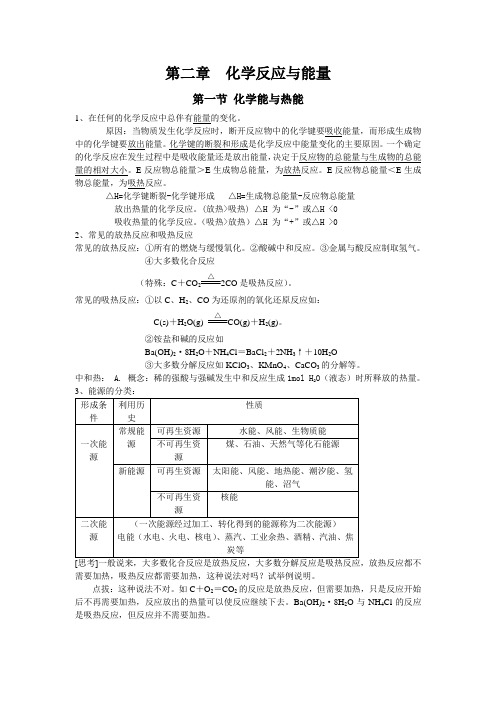
第二章化学反应与能量第一节化学能与热能1、在任何的化学反应中总伴有能量的变化。
原因:当物质发生化学反应时,断开反应物中的化学键要吸收能量,而形成生成物中的化学键要放出能量。
化学键的断裂和形成是化学反应中能量变化的主要原因。
一个确定的化学反应在发生过程中是吸收能量还是放出能量,决定于反应物的总能量与生成物的总能量的相对大小。
E反应物总能量>E生成物总能量,为放热反应。
E反应物总能量<E生成物总能量,为吸热反应。
△H=化学键断裂-化学键形成△H=生成物总能量-反应物总能量放出热量的化学反应。
(放热>吸热) △H 为“-”或△H <0吸收热量的化学反应。
(吸热>放热)△H 为“+”或△H >02、常见的放热反应和吸热反应常见的放热反应:①所有的燃烧与缓慢氧化。
②酸碱中和反应。
③金属与酸反应制取氢气。
④大多数化合反应(特殊:C+CO2△2CO是吸热反应)。
常见的吸热反应:①以C、H2、CO为还原剂的氧化还原反应如:C(s)+H2O(g)△CO(g)+H2(g)。
②铵盐和碱的反应如Ba(OH)2·8H2O+NH4Cl=BaCl2+2NH3↑+10H2O③大多数分解反应如KClO3、KMnO4、CaCO3的分解等。
中和热: A. 概念:稀的强酸与强碱发生中和反应生成1mol H2O(液态)时所释放的热量。
3、能源的分类:形成条件利用历史性质一次能源常规能源可再生资源水能、风能、生物质能不可再生资源煤、石油、天然气等化石能源新能源可再生资源太阳能、风能、地热能、潮汐能、氢能、沼气不可再生资源核能二次能源(一次能源经过加工、转化得到的能源称为二次能源)电能(水电、火电、核电)、蒸汽、工业余热、酒精、汽油、焦炭等[思考]一般说来,大多数化合反应是放热反应,大多数分解反应是吸热反应,放热反应都不需要加热,吸热反应都需要加热,这种说法对吗?试举例说明。
点拔:这种说法不对。
如C+O2=CO2的反应是放热反应,但需要加热,只是反应开始后不再需要加热,反应放出的热量可以使反应继续下去。


高中化学必修二第二章化学反应与能量变
化知识点总结
本文档将对高中化学必修二第二章的化学反应与能量变化知识点进行总结,以下是主要内容:
1. 化学反应的定义和特征
- 化学反应是物质发生改变的过程,原有物质消失,新的物质生成。
- 化学反应具有反应物和生成物、化学方程式和反应条件等特征。
2. 化学反应的类型
- 合成反应:两个或多个物质反应生成一个化合物。
- 分解反应:一个化合物分解成多个物质。
- 双替换反应:两个化合物中的阳离子和阴离子交换位置。
- 氧化还原反应:涉及氧化剂和还原剂的反应。
3. 化学方程式的书写和平衡
- 化学方程式用符号表示化学反应,包括反应物和生成物。
- 化学方程式需要平衡,即反应物和生成物的物质的种类和数量要相等。
4. 能量变化与化学反应
- 化学反应中常伴随着能量的释放或吸收。
- 放热反应:化学反应放出热量,温度升高。
- 吸热反应:化学反应吸收热量,温度降低。
- 可逆反应:既可以放热又可以吸热的反应。
5. 化学反应的速率与影响因素
- 化学反应的速率是指单位时间内反应物消失或生成物产生的量。
- 影响化学反应速率的因素有浓度、温度、催化剂等。
6. 化学平衡与化学平衡常数
- 化学平衡指反应物和生成物浓度达到一定比例后反应停止。
- 化学平衡常数表示在一定温度下,反应物和生成物浓度之比的稳定值。
以上为高中化学必修二第二章化学反应与能量变化知识点的总结,希望对您的研究有帮助。

高一化学必修二专题2《化学反应与能量变化》复习班级 姓名 座号 [知识梳理]1、化学反应的速度和限度 (1)化学反应限度:大多数化学反应都具有可逆反应的限度以到达在一定条件下的可逆反应,当等于、各组分浓度 时,反应到达化学平衡状态。
例1:某温度下,在一固定容积的容器中进行如下反应:H 2(g)+2(g) ⇌2HI(g),下列情况一定能说明反应已达到限度的是 A .压强不再随时间而改变时 B .气体的总质量不再改变时C .混合气体中各组成成分的含量不再改变时D .单位时间内每消耗1 mol I 2,同时有2 mol HI 生成时例2:下列关于燃料充分燃烧的说法.不正确的是 A .空气量越多越好 B .应通入适量的空气C .固体燃料燃烧前要粉碎D .液体燃料燃烧时可以以雾状喷出例3:100 mL 浓度为2 mol ·L -1的盐酸跟过量的锌片反应,为加快反应速率,又不影响生成氢气的总量,可采用的方法是A .加入适量的6 mol ·L -1的盐酸 B .加入数滴氯化铜溶液 C .加入适量蒸馏水 D .加入适量的氯化钠溶液 2、 化学能与热能①了解常见的吸热反应和放热反应。
常见的放热反应: 物质中的化学能转化途径:变化原因:化学键的改变 反应物中化学键的断裂: 能量生成物中化学键的形成: 能量转化形式 热能 电能放热反应: 能转化为 能吸热反应: 能转化为 能 火电: 能转化为 能再转化为 能 化学电源:原电池 实际应用:生产、生活、其它 (将 能转化为 能的装置) 化学反应速率意义:衡量 物理量表示方法:v= 【单位: 】 简单计算:同一化学反应中各物质的 等于各物质的化学计量数之比,也等于各物质的变化浓度之比影响因素内因:A. 所有燃烧反应;B. 中和反应;C. 大多数化合反应;D. 活泼金属跟水或酸反应;E. 物质的缓慢氧化常见的吸热反应: A. 大多数分解反应;※ 氯化铵与八水合氢氧化钡的反应。
其他因素:高一化学必修二专题2《化学反应与能量变化》复习班级 ___________[知识梳理]1、化学反应的速度和限度「意义:衡量表示方法:v= ___________ 【单位:- 简单计算:同一化学反应中各物质的\数之比,也等于各物质的变化浓度之比内因:温度:升高温度,可以 _________________ ;外因降低温度,可以 ------------------------ 催化剂:使用 _______________ 可以加快化学反应速率物理量等于各物质的化学计量化学 反应 速率影响 因素浓度:__________________ 可以加快反应速率, __________________ 可以加快反应速率化学反应限度:大多数化学反应都具有 ____________ ,故化学反应都有一定的限度;可逆反应的限度以到达 ______________________________ 为止在一定条件下的可逆反应,当 ____________________ 等于 ___________________ 、各组 分浓度 ___________ 时,反应到达化学平衡状态例1 :某温度下,在一固定容积的容器中进行如下反应:H(g)+ 2(g) ?2HI(g),下列情况一定能说明反应已达到限度的是A •压强不再随时间而改变时B •气体的总质量不再改变时C. 混合气体中各组成成分的含量不再改变时D. 单位时间每消耗1 mol I 2,同时有2 mol HI 生成时 例2 :下列关于燃料充分燃烧的说法.不正确的是 A .空气量越多越好 B .应通入适量的空气 C .固体燃料燃烧前要粉碎 D .液体燃料燃烧时可以以雾状喷出例3: 100 mL 浓度为2 mol -L -1的盐酸跟过量的锌片反应,为加快反应速率,又 不影响生成氢气的总量,可采用的方法是A.加入适量的6 mol L -1的盐酸 B .加入数滴氯化铜溶液C .加入适量蒸馏水D .加入适量的氯化钠溶液2、化学能与热能厂转化途径:放热反应: 化学电源: 热能吸热反应: _________ 能转化为 ______________ 能火电: _________ 能转化为 ______________ 能再转化为 ___________ 能变化原因:化学键的改变反应物中化学键的断裂: 能量物质中的化学能生成物中化学键的形成: 能量能转化为台匕 冃匕原电池(将 ____________ 能转化为_____________ 能的装置)实际应用:生产、生活、其它①了解常见的吸热反应和放热反应。
常见的放热反应:A. 所有燃烧反应;B.中和反应;C.大多数化合反应;D.活泼金属跟水或酸反应;E. 物质的缓慢氧化常见的吸热反应:A.大多数分解反应;B. C+CO 厶2C0 H2^C U O=^=C U+H3O C+H/?—CO+H3氯化铵与八水合氢氧化钡的反应。
放热反应②判断反应放热或吸热的方法:a. 当断开反应物中化学键所_________ 的能量 _______ 形成生成物中化学键所的能量时,反应放热,反之则反应吸热;b. 当________ 的总能量大于_________ 的总能量时,反应放热,反之则反应吸热。
放热反应吸热反应r ・1败卍醴Ift Array牛烛壮例1:拆开1mol H—H键,1mol N—H键,1mol N三N键分别需要吸收的能量436kJ ,391kJ , 946kJ,求:① 1moN气生成NH需_____ 热量_______ ,② 1molH2 气生成NH需_____ 热量______ ■写出热化学方程式:_____________________例2:下列说法中正确的是A. 物质发生化学反应都伴随着能量变化B. 伴有能量变化的物质变化都是化学变化C•在一个确定的化学反应关系中,反应物的总能量与生成物的总能量一定不同D •在一个确定的化学反应关系中•反应物的总能量总是高于生成物的总能量例3:下列说法中正确的是A . ImolHSO与lmolBa(OH)2完全中和所放出的热量为中和热B .中和反应都是放热反应C .氢气燃烧放出大量的热,说明参加反应的氢气和氧气总能量比生成物水的总能量高D . CO燃烧是吸热反应2、化学能与电能(1)原电池:.将化学能转化为电能的装置。
1 、构成原电池的三个主要条件2、如何判断原电池的正负极、电极反应类型3、常见原电池的电极反应:〔、原电池形成条件电解质溶液两电极以导线连接或,形成铜锌原电池(电解质:稀硫酸)负极(_),电极反应:____________________ (_____ 反应);现象:—正极(_),电极反应:____________________ (_____ 反应);现象:_总反应式:_____________________________ (溶液PH值_____ )、原电池正负极的判断:用作电源3、原电池的应用I 判断金属的活泼性加快某些反应的反应速率(2)电解池:电能转化为化学能1 、电解池的阴阳极判断、电极反应类型2、电解CuCk、饱和NaCI溶液、熔融NaCI、HO的电极反应例1:锂电池是一代新型高能电池,它以质量轻、能量高而受到了普遍重视,目前已研制成功多种锂电池。
某种锂电池的总反应式为Li+M nO=LiM nO?, 下列说确的是A • Li是正极,电极反应为Li-e -=Li+ B. Li是负极,电极反应为Li-e =Li+C. Li是负极,电极反应为Mn O+e-=M n8D. Li是负极,电极反应为Li-2e =Li2+例2:由铜、锌片和稀硫酸组成的原电池工作时,电解质溶液的pHA .不变B .先变小后变大C •逐渐变大D •逐渐变小 例3:若在铜片上镀银时,下列叙述正确的是①将铜片接在电池的正极上,②将银片接在电源的正极上,③在铜片上发生 的反应是:Ag ++e=Ag,④在银片上发生的反应是:4OHMe -=O+2HO,⑤需用CuSO 溶液,⑥需用AgNO 溶液作电解液()A.①③⑥ B •②③⑥C .①④⑤ D •②③④⑥例4:把a 、b 、c 、d 四块金属片浸人稀酸中,用导线两两相连组成原电池。
若 a 、b 相连时,a 为负极,c 、d 相连时,电流由d 到c ; a 、c 相连时c 极上产生 大量气泡,b 、d 相连时,b 上有大量气 泡产生,则四种金属的活动性 顺序由强到弱的顺序为 A. a>b>c>d B_a>c>d>b C . c>a>b>d D.b>d>c>a例5:.若某电能与化学能的转化装置(电解池或原电池)中发生反应的总反应离子方程式是:Cu+2H+===CU ++H T ,则关于该装置的说确的是A. 该装置可能是原电池,也可能是电解池B. 该装置只能是原电池,且电解质溶液为硝酸C. 该装置只能是电解池,且金属铜为该电解池的阳极D. 该装置只能是电解池,电解质溶液不可能是盐酸专题2《化学反应与能量转化》单元测试题高一() 班 _______________________ 学号()可能用到的相对原子质量: H: 1 O: 16 N: 14 Na: 23 Cl: 35.5 C: 12 Cu: 64一、选择题(本题包括11小题,每小题3分,共33分,每小题有一个选项符合题意。
)1. ------------------------ 在N 2+ 3H22NH 反应中,自反应开始至 2s 末,氨的浓度由 0变为0.4mol/L ,则以氢气的浓度变化表示该反应在 2s 的平均反应速率是 ( )A. 0.3mol/(L •) B . 0.4 mol/(L •) C2. 下列反应属于吸热反应的是 A. NaOH 溶液与盐酸反应 B3. 下列关于放热反应的说确的是A. 反应热△ H> 0的反应 B .反应物总能量比生成物总能量高的化学反应 C.反应物化学健断裂吸收的能量大于生成物化学键形成放出的能量的反应 D.反应物健能总和大于生成物键能总和的反应 4. 下列叙述中不正确的是( )A. 电解池的阳极上发生氧化反应,阴极上发生还原反应B. 原电池的正极上发生氧化反应,负极上发生还原反应C. 电镀时,镀层金属材料作阳极,待镀金属作阴极D. 用原电池作电源进行电解时,电子从原电池负极流向电解池阴极 5.右图为直流电源电解稀 Na 2SO 水溶液的装置。
通电后在石墨电极a 和b.0.6 mol/(L -s)D . 0.8 mol/(L ( ).葡萄糖在人体氧化分解 s)C. Ba(OH)2 -8H2O 与 NHCI 反应.锌粒与稀HSQ 反应制取H 2附近分别滴加一滴石蕊试液,下列实验现象中正确的是ftA. 逸出气体的体积a电极的小于b电极的B. 一电极逸出无味气体,另一电极逸出刺激性气味气体b 电极附近出现蓝色b 电极附近出现红色 6mol/L 的NaOH 溶液中,可以形成微型电池。
( )B . 4OH — 4e —= 2H 2O+ QfD. Al + 4OH 一一3e —= AlO 2 + 2H 2O① 电子总数,②原子总数,③分子总数,④物质的种类, 的总质量,⑥物质的总能量。
反应前后肯定不发生变化的是 ( )&下列说确的是A.往容器加入2molSQ 与1molO 2时,无论怎样控制反应条件,都不会生成2molSOB. 只要条件适当,任何化学反应中的反应物都能全部转化成生成物C. 当化学反应达到限度时,无论外界条件如何变化,反应体系各物质含量始终不变D. 化学反应速率理论可指导怎样在一定时间快出产品,提高原料利用率 9.下列不属于生物质能的利用的是 () A .燃烧树枝取热 B .将植物秸杆制沼气C .用淀粉制乙醇D.用太阳能发电10.下列关于氢能的开发与利用的说法,不正确的是()A .液态氢可以用作火箭的燃料 B. 氢能的开发和利用,首要解决的问题是由水制的能耗,氢气的贮存和运输C. 研究利用在光分解催化剂存在下,利用太阳能分解水制氢气D. 用电解水的方法制取 H 和Q,再通过制作氢、氧燃料电池可提高能量的利用率 11.等质量的铁与过量的盐酸在不同的试验条件下进行反应,测定在不同时间t 产生氢气体积v 的数据,根据数据绘制得到图1,则曲线a 、b 、c 、d 所对应的试验组别可能是二、选择题(本题包括6小题,每小题3分,共18分,每小题有1〜2个选项符合题意) 12. 下列有关能量转换的说确的是( )A. 煤燃烧是化学能转化为热能的过程B. 化石燃料和植物燃料燃烧时放出的能量均来源于太阳能C. 动物体葡萄糖被氧化成 CO 是热能转变成化学能的过程D. 植物通过光合作用将 CO 转化为葡萄糖是太阳能转变成热能的过程C. a 电极附近呈红色,D. a 电极附近呈蓝色, 6 •把一小块镁铝合金投到 该电池的负极反应式为一2+A. Mg — 2e = MgC. 2H +—2e —= H 2 f 7.物质发生化学变化时:⑤物质 A.①②③⑤B .①②⑤C .②⑤⑥D .①④⑤⑥组别 c(HCI)(mol LJ温度(C )状态 1 2.0 25 块状 2 2.5 30 块状 3 2.5 50 块状 42.550粉末状C. 3-4-2-1D. 1-2-4-313 .下列实验操作能使所发生的反应速率加快的是()A. 实验室用锌制H时,加入少量CuSO溶液B. 加热HO水溶液制氧气时,加入少量MnO固体气可用于燃料电池。