重要的金属元素及其化合物
- 格式:ppt
- 大小:6.03 MB
- 文档页数:97

常见金属元素及其化合物金属元素是指具有金属性质的化学元素,通常具有良好的电导性、热导性、延展性和可塑性。
金属元素被广泛应用于各个领域,例如建筑、电子、冶金、汽车等。
下面将为您介绍一些常见金属元素及其化合物。
铁(Fe)是一种常见的金属元素,其化合物主要有氧化铁、硫化铁、碳酸铁等。
氧化铁是一种红棕色的固体物质,在建筑和石材制作中常用作颜料。
硫化铁是一种黑色的矿石,常用于制备铁和钢。
碳酸铁是一种白色的结晶物质,常见于自然界中的石灰岩和大理石。
铜(Cu)是另一种常见的金属元素,其化合物主要有氧化铜、硫化铜、碳酸铜等。
氧化铜是一种黑色的固体物质,在电子和电器制造中常用作导电材料。
硫化铜是一种蓝色的矿石,常用于制备铜和铜合金。
碳酸铜是一种绿色的结晶物质,常见于自然界中的矿石和矿山。
铝(Al)是一种轻便耐腐蚀的金属元素,其化合物主要有氧化铝、氯化铝、硫酸铝等。
氧化铝是一种白色的固体物质,在建筑和电子制造中常用作绝缘材料和搅拌器。
氯化铝是一种无色的液体,常用于制备有机化合物。
硫酸铝是一种无色的液体,常用于制备矾石和其他铝盐。
锌(Zn)是一种重要的金属元素,其化合物主要有氧化锌、硫化锌、氯化锌等。
氧化锌是一种白色的固体物质,常见于生活用品和化妆品中。
硫化锌是一种白色的矿石,常用于制备锌和锌合金。
氯化锌是一种无色的固体,常用作催化剂和腐蚀抑制剂。
钠(Na)是一种常见的金属元素,其化合物主要有氯化钠、碳酸钠、亚硝酸钠等。
氯化钠是一种无色的晶体,是普通食盐的主要成分。
碳酸钠是一种白色的晶体,常用于制备碱性溶液和中和酸性物质。
亚硝酸钠是一种无色的晶体,常用于食品加工和防腐剂。
钢是一种由铁和碳组成的合金,常用于建筑和制造业。
除了碳,钢中还可以含有其他金属元素,如锰、铬、钼等。
这些金属元素能够提高钢的强度、硬度和耐腐蚀性。
总结起来,常见的金属元素及其化合物有铁(氧化铁、硫化铁、碳酸铁)、铜(氧化铜、硫化铜、碳酸铜)、铝(氧化铝、氯化铝、硫酸铝)、锌(氧化锌、硫化锌、氯化锌)、钠(氯化钠、碳酸钠、亚硝酸钠)等。


完整版)高中化学知识点总结:金属元素及其化合物高中化学知识点总结:金属元素及其化合物一、金属元素概述1.金属元素在周期表中的位置及原子结构特征金属元素分布在周期表的左下方,目前已知的112种元素中有90种金属元素。
金属元素最外层电子数一般小于4个,仅有Ge、Sn、Pb有4个,Sb、Bi有5个,Po有6个。
金属原子半径较同周期非金属原子半径大。
金属元素形成的金属单质固态时全是金属晶体。
2.金属的分类1)按冶金工业上的颜色分:黑色金属有Fe、Cr、Mn (其主要氧化物呈黑色),有色金属则是除Cr、Mn以外的所有金属。
2)按密度分:轻金属密度小于4.5g/cm³,如Na、Mg、Al;重金属密度大于4.5g/cm³,如Fe、Cu、W。
3)按存在丰度分:常见金属如Fe(4.75%)、Al(7.73%)、Ca(3.45%)等;稀有金属如锆、铪、铌等。
3.金属的物理性质1)状态:除汞外,其他金属通常为固态。
2)金属光泽:多数金属具有金属光泽。
3)易导电和导热:由于金属晶体中自由电子的运动,使金属易导电、导热。
4)延展性:金属可以压成薄片,也可以抽成细丝。
5)熔点及硬度:金属晶体中金属离子和自由电子的作用强弱决定其熔点和硬度,最高的是钨(3413℃),最低的是汞(-39℃)。
4.金属的化学性质1)与非金属单质作用。
2)与H2O作用。
3)与酸作用。
4)与碱作用,只有Al、Zn可以。
5)与盐的作用。
6)与某些氧化物的作用。
5.金属的冶炼1)热分解法(适用于不活泼金属):2HgO=2Hg+O²,2Ag2O=4Ag+O²。
2)热还原法(常用还原剂CO、H2、C活泼金属等):Fe2O3+3CO=2Fe+3CO2,Cr2O3+2Al=2Cr+Al2O3.3)电解法(适用于非常活泼的金属):2Al2O3=4Al+3O2,2NaCl=2Na+Cl2.二、碱金属元素1.钠及其化合物1)钠的物理性质:钠是一种柔软、银白色,有金属光泽的金属,具有良好的导电、导热性,密度比水小,比煤油大,熔点较低。

专题复习常见金属元素及其化合物[高考关键词]单质——氧化物(碱性氧化物)——氢氧化物(碱)——盐(阳离子)。
1•钠:活泼、还原性(保存);过氧化钠:结构特点、与水及C02反应特点;烧碱。
2•铝:还原性、与强碱反应、合金;氧化铝、氢氧化铝:两性; AI3+ :水解、净水、离子共存、铝三角转化。
3•铁: 腐蚀、变价;Fe2+ :还原性、离子共存、保存、检验;Fe3+ :氧化性、水解、离子共存、检验;Fe2+、Fe3+的相互转化。
4•铜:不活泼、冶炼;氧化物、Cu2+:颜色。
丁核心考点回扣---------------------------------------------------------------- 1.熟记几种物质的颜色Na2O2 是__________ ; Fe2°3 是 ______ ;AI(OH) 3、Fe(OH) 2 均是____________________ ;Fe(OH)3是__________; CuSO4是__________ ;FeCl3 ________ 。
答案淡黄色红棕色白色红褐色白色棕黄色2.熟悉4类特殊反应(1)Fe在CI2中燃烧,无论CI2是否过量,产物均为___________ 。
(2)Na在氧气中燃烧,无论 O2是否过量,产物均为___________ 。
(3)与水接触产生气体单质的物质有 _________ 。
(4)与水接触产生气体化合物的物质有 _________ 。
答案 (1)FeCI3⑵Na2O2⑶Na、K、Na2O2等⑷Al 2S3、Mg 3N 2、CaC23.典型元素及其化合物的特征性质(1)Na、AI、Fe、Cu四种元素的单质中:①能与水剧烈反应的是_____________ ,反应的离子方程式:___________________________ ;②能与 NaOH溶液反应的是_________ ,反应的离子方程式:____________________________ , 其中作氧化剂的是_______________________________________________________________ ;③Cu在潮湿的空气中被腐蚀的化学方程式:______________________④与氧气反应条件不同,反应产物不同的是(2)上述四种金属的氧化物中:①_______________________ 能用作供氧剂的是,写出一个化学方程式:②___________________________________________________________ 既能溶于酸溶液又能溶于强碱溶液的是______________________________________________________ ,离子方程式分别为_________________________________________________________③_________________________________________________________ 常温下为黑色固体的是_________________________________________________________________ 。

无机化学元素及化合物无机化学是研究无机物质的组成、结构、性质及其变化规律的科学,其中最基本的研究对象就是无机化学元素及其化合物。
本文将介绍无机化学元素的分类及其代表性化合物。
第一类是金属元素,具有良好的导电性、热导性和延展性。
金属元素在化合物中往往以阳离子的形式存在。
代表性金属元素有钠、铁、铜、镁、锰等。
其中,钠是一种重要的金属元素,广泛应用于制取钠盐、溶剂和代谢调节等方面。
铁是人体必需的微量元素,它构成了血红蛋白和肌红蛋白等重要物质,参与氧的运输和储存。
另外,钢铁是一种重要的构筑材料,广泛应用于建筑、桥梁和交通工具等方面。
第二类是非金属元素,具有不良的导电性和热导性。
非金属元素在化合物中往往以阴离子的形式存在。
代表性非金属元素有氢、氧、氮、碳、硫等。
其中,氢是化学元素中最简单的元素,它广泛存在于宇宙中,是太阳和恒星的主要成分。
氧是地壳中最丰富的元素,它广泛存在于水、大气和岩石中。
氧是许多化合物的组成部分,例如水、二氧化碳和硫酸等。
第三类是过渡金属元素,具有较高的熔点和较高的硬度。
过渡金属元素在化合物中可以以不同的电价态存在。
代表性过渡金属元素有铁、铜、锌、镍、铬等。
其中,铁是重要的催化剂,广泛应用于化工和有机合成等领域。
铜是重要的导电材料,广泛应用于电线、电器和电子设备等方面。
无机化合物是由两个或多个元素通过化学键连接而成的物质。
无机化合物可以根据其成分和结构进行分类。
最常见的无机化合物是盐类,由阳离子和阴离子组成。
代表性盐类有氯化钠、硫酸铜、硝酸钙等。
其中,氯化钠是普通食盐的主要成分,广泛应用于食品调味和食品加工等方面。
硫酸铜是一种重要的化工原料,广泛应用于颜料、电镀和农药等方面。
硝酸钙是一种重要的化肥,广泛应用于土壤改良和植物生长促进等方面。
总之,无机化学元素及其化合物是无机化学的研究对象,它们在人类社会和自然界中发挥着重要的作用。
通过不断深入的研究,我们可以更好地理解无机物质的性质和功能,为人类的生产和生活提供更好的支持。

常见金属元素及其化合物金属元素是指具有金属性质的化学元素,常见金属元素包括铁、铜、铝、锌、镁、钙、锡等。
这些金属元素具有良好的导电性、导热性、延展性、韧性等特点,被广泛应用于工业、建筑、电子、汽车等领域。
以下将对常见金属元素及其化合物进行介绍。
铁是最常见的金属元素之一,它在地壳中含量很丰富。
铁具有良好的韧性和可塑性,广泛应用于钢铁制造、建筑、机械加工、电子设备等领域。
铁的化合物有很多,常见的有氧化铁(Fe2O3)和硫化铁(FeS2)等。
氧化铁是一种重要的无机颜料,用于制造红、橙、黄等颜色的油漆、颜料和陶瓷;硫化铁常用于制造火柴的火头。
铜是另一种常见的金属元素,具有良好的导电性和导热性。
铜广泛应用于电子设备、电线、管道等领域。
铜的化合物有氧化铜(CuO)、硫化铜(CuS)等。
氧化铜常用作无机颜料、催化剂和电池材料;硫化铜可用于制备农药和矿石浮选剂。
铝是一种轻质金属元素,密度低、延展性好。
铝广泛用于飞机、汽车、建筑等领域。
铝的主要化合物有氧化铝(Al2O3)和硫化铝(Al2S3)等。
氧化铝是一种重要的工业原料,广泛用于制造陶瓷、搪瓷、耐火材料等;硫化铝用于制备染料和催化剂。
锌是一种重要的工业金属,具有抗腐蚀性好、导电性能优良等特点。
锌广泛应用于电镀、电池制造、建筑材料等领域。
锌的主要化合物有氧化锌(ZnO)和硫化锌(ZnS)等。
氧化锌常用于生产橡胶、涂料、油漆、化妆品等;硫化锌是一种重要的矿石,在锌冶炼过程中起着重要的作用。
镁是一种轻质金属元素,密度低、质轻。
镁广泛应用于轻金属合金、烟火制造、航空航天等领域。
镁的主要化合物有氧化镁(MgO)和硫化镁(MgS)等。
氧化镁是一种重要的耐火材料,广泛用于高温炉窑、电解槽等;硫化镁可用于制备染料和防腐剂。
钙是一种重要的金属元素,广泛存在于生物体内。
钙广泛应用于建筑材料、电子材料、钢铁冶炼等领域。
钙的主要化合物有氧化钙(CaO)和氯化钙(CaCl2)等。
氧化钙是一种重要的建筑材料,用于制备水泥、石灰等;氯化钙常用于融雪剂、防止水泥凝固等。

铁及其化合物知识点铁是我们日常生活中常见且重要的金属元素,其化合物在生产生活、工业、化学研究等方面都有着广泛的应用。
下面就让我们一起来深入了解一下铁及其化合物的相关知识。
一、铁元素的基本性质铁的原子序数是 26,位于元素周期表的第四周期第Ⅷ族。
铁的原子核外电子排布为 2、8、14、2,常见的化合价有+2 价和+3 价。
在化学反应中,铁的化学性质比较活泼,能与许多物质发生反应。
铁在纯氧中可以燃烧,生成四氧化三铁(Fe₃O₄),化学方程式为:3Fe + 2O₂=点燃= Fe₃O₄。
铁还能与稀盐酸、稀硫酸等发生置换反应,生成亚铁盐和氢气,例如:Fe + 2HCl = FeCl₂+ H₂↑ 。
二、铁的氧化物1、氧化亚铁(FeO)氧化亚铁是一种黑色粉末,其中铁为+2 价。
它不稳定,在空气中加热时迅速被氧化为四氧化三铁。
2、氧化铁(Fe₂O₃)氧化铁俗称铁红,是一种红棕色粉末,常用于涂料、油漆等工业。
其中铁为+3 价。
3、四氧化三铁(Fe₃O₄)四氧化三铁俗称磁性氧化铁,是具有磁性的黑色晶体。
它可以看作是由氧化亚铁和氧化铁组成的复杂化合物,其中有+2 价和+3 价的铁。
三、铁的氢氧化物1、氢氧化亚铁(Fe(OH)₂)氢氧化亚铁是白色沉淀,但在空气中极易被氧化,迅速变成灰绿色,最终变成红褐色的氢氧化铁。
化学方程式为:4Fe(OH)₂+ O₂+2H₂O = 4Fe(OH)₃。
2、氢氧化铁(Fe(OH)₃)氢氧化铁是红褐色沉淀,具有两性,但碱性强于酸性。
它受热易分解,生成氧化铁和水:2Fe(OH)₃=△= Fe₂O₃+ 3H₂O 。
四、铁盐和亚铁盐1、亚铁盐常见的亚铁盐有硫酸亚铁(FeSO₄)、氯化亚铁(FeCl₂)等。
亚铁盐溶液通常呈浅绿色,具有较强的还原性,容易被氧化剂氧化为铁盐。
例如,氯化亚铁溶液能被氯气氧化:2FeCl₂+ Cl₂= 2FeCl₃。
2、铁盐常见的铁盐有硫酸铁(Fe₂(SO₄)₃)、氯化铁(FeCl₃)等。

一、金属及其化合物的主要性质和转化关系1.钠及其重要化合物(1)知识主线:Na→Na2O→Na2O2→NaOH→Na2CO3→NaHCO3(2)转化关系2.铝及其重要化合物(1)知识主线:(2)转化关系3.铁及其重要化合物(1)知识主线(2)转化关系4.铜及其重要化合物(1)知识主线:(2)转化关系:二、常见阳离子的检验与判断常见阳离子的检验1.用NaOH溶液检验Cu2+产生蓝色沉淀Fe3+产生红褐色沉淀Fe2+产生白色沉淀,迅速变成灰绿色,最后变成红褐色Al3+产生白色沉淀,继续加入NaOH溶液,白色沉淀溶解NH4+共热生成能使湿润的红色石蕊试纸变蓝的气体2.特殊检验法Fe3+加入KSCN溶液呈红色,加苯酚溶液呈紫色Fe2+加入KSCN溶液无现象,滴加新制氯水或双氧,水后溶液呈红色3.焰色反应用焰色反应可检验出溶液中的K+和Na+K+火焰呈紫色(透过蓝色钴玻璃观察)Na+火焰呈黄色三、金属元素单质及其化合物1.无机化工流程题常见设问方向(1)反应速率与平衡理论的运用;(2)氧化还原反应的判断、化学方程式或离子方程式的书写;(3)利用控制pH分离除杂;(4)化学反应的能量变化;(5)实验基本操作:除杂、分离、检验、洗涤、干燥等;(6)流程中的物质转化和循环,资源的回收和利用;(7)环境保护与绿色化学评价。
2.无机化工流程题的审题技能化工生产流程题中经常会出现一些表述性词语,这些表述性词语就是隐性信息,它可以暗示我们审题所应考虑的角度。
常见的有:(1)“控制较低温度”——常考虑物质的挥发,物质的不稳定性和物质的转化等。
(2)“加过量试剂”——常考虑反应完全或增大转化率、产率等。
(3)“能否加其他物质”——常考虑会不会引入杂质或是否影响产品的纯度。
(4)“在空气中或在其他气体中”——主要考虑O2、H2O、CO2或其他气体是否参与反应或达到防氧化、防水解、防潮解等目的。
(5)“判断沉淀是否洗净”——常取少量最后一次洗涤液于试管中,向其中滴加某试剂,以检验其中的某种离子。


人体中含量最高的金属元素组成的化合物。
1、锌(Zn):人体中含量最高的微量元素,在肝脏、肾脏、骨骼、牙齿、头发中可以大量检测到,并参与多种正常生理反应。
锌是维持
蛋白质代谢、脂质代谢、维生素的吸收和新陈代谢、氨基酸激酶的活
性以及参与精子发育等活性的必要元素,还可以帮助维护免疫功能和
皮肤。
2、铜(Cu):人体中的铜含量也不低,主要分布在肝脏、心脏、肾脏、肌肉和其他组织中。
它作为一种常见的酶,可以参与多重生理反应,
如造血、新陈代谢、能量消耗和膳食酶的合成。
此外,它还与自身免
疫系统、神经功能等相关,是必要的体内元素。
3、铁(Fe):人体中的铁的主要来源是血液中的红细胞,也称为血红素,主要用来将氧气从肺部输送到全身。
血液中的铁含量适中可以保
证人体健康,但如果太多就会沉积在血管壁上,影响血液循环,增加
中风和心脏病的危险性。
4、钙(Ca):钙是人体最多的金属元素,全身中有99%的钙被存放
在骨骼和牙齿中,但另外1%的钙也被储存在身体的血液、淋巴液、髓液、软组织等地方。
钙负责维持肌肉的张力、血液的凝结、神经的传
导以及多种重要的生化反应。
5、镁(Mg):镁与钙并列,是人体所必需的金属元素,与亚硝酸盐
和萘酸共同参与人体酸碱平衡,镁容易被水溶液中的反刍动物(如人)
吸收。
它可以强化骨骼,帮助吸收维生素B6和维生素D,参与维持心脏节律,促进胆汁的分泌,以及调节胃肠道的水分平衡。

金属元素的性质和常见化合物金属元素是化学元素中的一类,具有独特的性质和广泛的应用。
本文将探讨金属元素的一般性质、常见化合物及其应用。
一、金属元素的一般性质1. 密度大:金属元素的原子通常比非金属元素的原子大,因此金属元素的密度较大。
2. 导电性好:金属元素的电子排列松散,因此电子容易自由移动,并在外界电场作用下形成电流。
3. 导热性好:金属元素的电子容易自由移动,在受热后能迅速传递热量。
4. 可塑性高:金属元素由于具有金属键,使得金属元素之间的结构松散,因此可以轻松改变形状。
5. 有延展性:金属元素的原子间有较强的金属键,因此可以拉成线、锻成薄片或制成其它形状。
二、常见金属元素和其性质1. 铁(Fe):是最常见的金属之一,具有良好的导电性和导热性。
常见的铁化合物有氧化铁(Fe2O3)、碳酸铁(FeCO3)等。
2. 铜(Cu):是一种优良的导电金属,广泛用于电缆、电器等。
常见的铜化合物有氧化铜(CuO)、硫酸铜(CuSO4)等。
3. 铝(Al):具有较轻的质量和良好的导电性,被广泛用于制造包装材料、航空器件等。
常见的铝化合物有氧化铝(Al2O3)、硫酸铝(Al2(SO4)3)等。
4. 锌(Zn):是一种常见的防腐金属,广泛用于防腐涂层和电池。
常见的锌化合物有氧化锌(ZnO)、硫酸锌(ZnSO4)等。
5. 镍(Ni):是一种重要的合金元素,广泛用于不锈钢和电池。
常见的镍化合物有氧化镍(NiO)、硫酸镍(NiSO4)等。
三、金属元素化合物的应用1. 金属氧化物:金属氧化物广泛应用于陶瓷、建筑材料、磁性材料等。
例如,氧化铁(Fe2O3)被用于制造磁铁。
2. 金属盐类:金属盐类被广泛应用于化学工业、医药和农业等领域。
例如,硫酸铜(CuSO4)被用于植物生长调节剂和水处理剂。
3. 金属合金:金属合金是由两种或两种以上金属元素组成的材料,具有优良的机械性能和耐腐蚀性。
例如,不锈钢中加入了镍(Ni),提高了抗腐蚀能力。



重要的金属元素及其化合物金属元素是物质世界中非常重要的成分之一,它们在各个领域都发挥着重要的作用。
以下是一些重要的金属元素及其化合物。
1.铁(Fe):铁是一种重要的结构材料,用于建筑、制造工具和机械。
它的化合物如氧化铁(Fe2O3)广泛用于制作铁器和磁性材料。
2.铜(Cu):铜是一种良好的导电材料,被广泛用于制作电线和电缆。
它的化合物如氧化铜(CuO)和硫酸铜(CuSO4)也被用于制作颜料、防腐剂和电池。
3.铝(Al):铝是一种轻质金属,具有良好的导电和热导性能。
它被广泛用于制造飞机、汽车和建筑材料。
铝的氧化物(Al2O3)在制陶、磨料和火箭推进剂中也有广泛应用。
4.锌(Zn):锌是一种重要的防腐金属,被用于保护铁和钢制品免受腐蚀。
锌在电池、合金和化妆品中也有应用。
锌的化合物如氧化锌(ZnO)和硝酸锌(Zn(NO3)2)被用于制作颜料、润滑剂和医药品。
5.银(Ag):银是一种优良的导电材料,广泛用于制作电子和光学器件。
银的化合物如氯化银(AgCl)和硝酸银(AgNO3)被用于摄影、杀菌和防腐。
6.镍(Ni):镍是一种重要的合金元素,常用于制作不锈钢、高温合金和电池。
镍的化合物如硫化镍(NiS)和镍碳酸(NiCO3)也被用于电镀和催化剂。
7.钛(Ti):钛具有良好的强度和耐腐蚀性能,被广泛用于航空航天、化工和医疗行业。
钛的氧化物(TiO2)广泛用于制作颜料、涂料和催化剂。
8.锡(Sn):锡是一种重要的合金元素,被用于制作锡合金和防锈剂。
锡的氧化物(SnO2)被用于制作玻璃、陶瓷和电子器件。
9.钨(W):钨具有高熔点和良好的耐腐蚀性能,被广泛用于制作灯丝、钨丝和合金。
钨的化合物如硫化钨(WS2)和钨酸(H2WO4)也被用于涂料和润滑剂。
10.铂(Pt):铂是一种珍贵的金属,具有良好的耐腐蚀性能和催化性能。
铂广泛用于制作汽车催化剂、电子器件和珠宝。
以上是一些重要的金属元素及其化合物。
这些金属元素在制造、建筑、化工、电子和医疗等领域都发挥着重要的作用,对人类社会的发展起到了至关重要的作用。
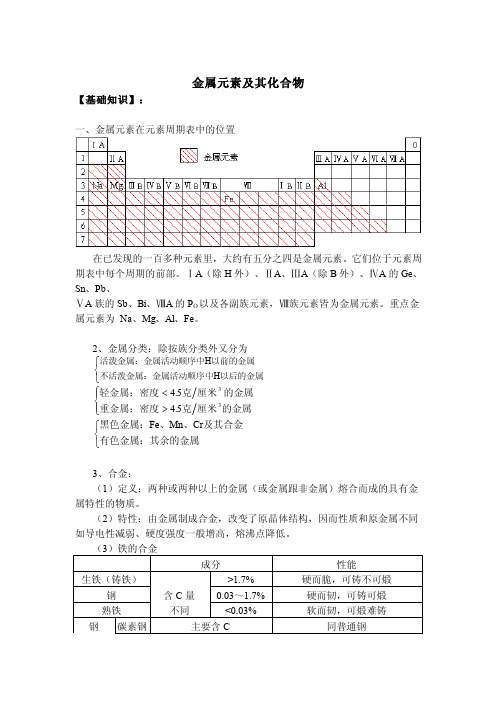
金属元素及其化合物【基础知识】:一、金属元素在元素周期表中的位置在已发现的一百多种元素里,大约有五分之四是金属元素。
它们位于元素周期表中每个周期的前部。
ⅠA (除H 外)、ⅡA 、ⅢA (除B 外)、ⅣA 的Ge 、Sn 、Pb 、ⅤA 族的Sb 、Bi 、ⅧA 的P O 以及各副族元素,Ⅷ族元素皆为金属元素。
重点金属元素为 Na 、Mg 、Al 、Fe 。
2、金属分类:除按族分类外又分为 活泼金属:金属活动顺序中以前的金属不活泼金属:金属活动顺序中以后的金属H H ⎧⎨⎩轻金属:密度克厘米的金属重金属:密度克厘米的金属<>⎧⎨⎪⎩⎪454533.. 黑色金属:、、及其合金有色金属:其余的金属Fe Mn Cr ⎧⎨⎩ 3、合金:(1)定义:两种或两种以上的金属(或金属跟非金属)熔合而成的具有金属特性的物质。
(2)特性:由金属制成合金,改变了原晶体结构,因而性质和原金属不同如导电性减弱、硬度强度一般增高,熔沸点降低。
4、金属的结构与共性(1)晶体结构:金属晶体是由金属离子和自由电子之间存在的较强作用(即金属键)而构成的单质晶体。
自由电子在外加电压作用下可定向移动故可导电加快运动后,撞击离子,交换能量,故可导热原子和离子可相对移动,故有延展性⎧⎨⎪⎩⎪金属键的强弱是由金属的价电子数和金属离子半径大小决定的,一般金属离子半径越小,离子的正电荷数越多,金属键越强。
(2)金属共性:①物理性质:多数为固体(Hg 除外):比重大;不透明;有金属光泽;导电导热性好;有延展性。
②化学性质:金属原子,最外层电子数少,易失电子而成阳离子,故金属只有还原性,在生成化合物中,金属元素均为正价。
能跟氧、非金属、水、酸、盐及其它物质反应。
5、如何比较元素金属性强弱。
(1)利用原子结构和元素周期表:在元素周期表中,同一周期从左至右元素的金属性逐渐减弱,同一主族从上到下元素的金属性逐渐增强。
(2)比较金属单跟氧气反应的能力:一般来说,金属单质跟氧气反应越容易,金属性越强,如把镁、铝分别在空气中点燃,镁可以燃烧,而铝则不能燃烧,所以金属性Mg>Al 。



镍及其化合物的相对质量镍是一种重要的金属元素,化学符号为Ni,原子序数为28,在元素周期表中位于第8组第4周期。
它是一种银白色的贵金属,具有良好的韧性、耐腐蚀性、电导率和磁性能。
镍广泛应用于制造硬质合金、不锈钢、电池等领域。
镍的相对原子质量为58.69,是一种较稳定的金属元素。
它的八个同位素中最稳定的是镍-58,相对丰度为68.077%。
镍在自然界中存在于许多矿物中,在地壳中的存在量为0.008%,其中以镍磁铁矿和红土矿为主要矿物。
镍也存在于生物体中,是一些生物体重要的微量元素,包括植物、动物和人类。
镍及其化合物在生产和应用过程中会对环境和人体产生一定的影响。
在某些情况下,人体摄入过多的镍元素会引起镍中毒。
另外,镍也会在工业过程中被释放到大气、水体和土壤中,对环境造成污染。
因此,需要采取有效的控制措施,减少镍及其化合物的排放,保护环境和人体健康。
除了镍本身外,镍化合物也是重要的产物和中间体。
一些常见的镍化合物包括氧化镍、硫酸镍、氯化镍、镍酸钠、镍铬合金等。
这些化合物的相对分子质量根据其化学式不同而有所差异,如氧化镍的相对分子质量为74.69,硫酸镍的相对分子质量为262.85,氯化镍的相对分子质量为90.92,镍酸钠的相对分子质量为208.71,镍铬合金的相对原子质量则由镍和铬的比例而定。
由于镍及其化合物在工业生产中的广泛应用,也带来了一些环境和健康问题。
例如,由于汽车尾气、钢铁、镍制品等行业的排放,空气中的镍含量较高,对人体健康产生一定的影响,如造成哮喘等呼吸系统疾病和过敏性皮炎等皮肤疾病。
此外,土壤中也存在高浓度的镍污染,对土地、植物和人畜的健康产生影响。
因此,镍及其化合物的环境污染和健康风险问题已经引起广泛关注。
人们需要采取一系列有效的控制措施,减少镍元素及其化合物的释放,在环境保护和健康保护方面做出积极的贡献。

高一铁元素及其化合物知识点汇总铁是我们日常生活中常见的元素之一,它的化合物也有着广泛的应用。
下面将就高一铁元素及其化合物的相关知识点进行汇总。
1. 铁的基本性质铁是一种金属元素,具有蓝黑色的外观和良好的导电性和导热性。
它在常温下对空气有一定的活性,容易生锈。
铁的原子序数为26,原子量为55.85。
在元素周期表中,它位于第8族,第4周期。
2. 铁的同位素铁有多个同位素,其中最稳定的是铁-56,占自然界铁的约91.7%。
其他常见的同位素有铁-54、铁-57等。
3. 铁的化合价和阳离子形态铁可以形成两种常见的氧化态:+2和+3,分别对应亚铁离子(Fe2+)和铁离子(Fe3+)。
亚铁离子具有双电荷,它是一种淡绿色溶液,并且容易被氧气氧化生成铁离子。
4. 铁的常见化合物及其性质a. 氧化铁:氧化铁是铁与氧气反应生成的产物。
它有多种形态,包括FeO、Fe2O3和Fe3O4。
氧化铁在颜料、磁性材料等方面有广泛的应用。
b. 硫酸亚铁:化学式为FeSO4,是一种淡绿色固体,可以溶于水。
硫酸亚铁是一种重要的工业化学品,常用于农业中作为植物营养元素之一。
c. 硫酸铁:化学式为Fe2(SO4)3,是一种黄褐色固体,也可以溶于水。
硫酸铁常用于制备其他铁盐,如硫酸铁铵。
d. 氢氧化亚铁:化学式为Fe(OH)2,是一种淡绿色的沉淀。
它是一种较弱的碱性物质,可以中和酸,生成相应的盐。
e. 碳酸亚铁:化学式为FeCO3,是一种白色沉淀。
碳酸亚铁是一种较不稳定的化合物,在空气中很容易分解。
5. 铁的应用铁的应用非常广泛,从建筑结构到汽车制造,都离不开铁及其合金。
铁合金,如不锈钢、铸铁等,具有良好的强度和耐腐蚀性,广泛用于工业领域。
此外,铁还用于制造磁铁、电子产品、农业肥料等。
以上便是有关高一铁元素及其化合物的知识点的汇总。
通过了解铁的基本性质、化合价和常见化合物,我们可以更好地理解铁及其化合物在生活和工业中的应用。
同时,铁元素的研究和应用也是化学领域不可忽视的一部分。