苯甲酸红外光谱的测定实验报告
- 格式:docx
- 大小:16.03 KB
- 文档页数:4

苯甲酸红外吸收光谱的测绘实验报告实验报告:苯甲酸红外吸收光谱的测绘引言:红外光谱是一种常用的分析方法,可以用于物质的结构鉴定和化学反应的研究。
本实验旨在通过苯甲酸的红外吸收光谱测绘,了解不同官能团的红外吸收特征,并通过实验结果进行分析和讨论。
实验方法:1. 实验仪器:红外光谱仪2. 实验样品:苯甲酸3. 实验步骤:a. 准备样品:将苯甲酸固体样品放置于红外吸收样品盒中。
b. 测量红外光谱:将样品盒放置于红外光谱仪中,进行红外光谱测量。
c. 记录实验数据:记录红外光谱仪所得到的光谱图。
实验结果与分析:通过对苯甲酸红外光谱图的观察,我们可以得到以下结论:1. 羧酸官能团的吸收峰:在红外光谱图中,我们可以观察到苯甲酸的羧酸官能团的吸收峰位在1700-1750 cm-1之间,这是由于羧酸官能团中的C=O键对红外光有较强的吸收能力所致。
2. 苯环的吸收峰:苯环中的C-H键对红外光谱有特定的吸收峰位。
在苯甲酸的红外光谱图中,我们可以观察到苯环上的C-H键吸收峰位在3000-3100 cm-1之间,这是由于苯环中的C-H键对红外光有较强的吸收能力所致。
3. 芳香环的吸收峰:苯环中的C=C键对红外光谱有特定的吸收峰位。
在苯甲酸的红外光谱图中,我们可以观察到苯环上的C=C键吸收峰位在1450-1600 cm-1之间,这是由于苯环中的C=C键对红外光有较强的吸收能力所致。
4. 其他官能团的吸收峰:苯甲酸中还含有其他官能团,如苯环上的甲基基团。
在红外光谱图中,我们可以观察到甲基基团的吸收峰位在2800-3000 cm-1之间,这是由于甲基基团中的C-H键对红外光有较强的吸收能力所致。
结论:通过对苯甲酸红外吸收光谱的测绘实验,我们得到了苯甲酸不同官能团的吸收峰位。
这些吸收峰位的出现与苯甲酸分子中的官能团有关,通过对吸收峰位的分析,我们可以对苯甲酸的结构进行鉴定和分析。
红外光谱是一种非常有用的分析工具,在化学研究和实验中具有广泛的应用前景。

1. 了解苯甲酸的红外光谱特征。
2. 通过实践掌握红外光谱法测定苯甲酸的方法。
3. 学会运用红外光谱仪对有机化合物进行定性分析。
二、实验原理红外光谱法是一种常用的有机化合物分析方法,其原理是:当分子中的化学键或官能团吸收特定波长的红外光时,会引起分子振动或转动能级的跃迁,从而产生红外光谱。
苯甲酸作为一种有机酸,其分子中含有羧基(-COOH),在红外光谱中会表现出特有的吸收峰。
三、实验仪器与试剂1. 仪器:红外光谱仪、样品池、电子天平、干燥器、干燥箱、烧杯、移液管、滴管等。
2. 试剂:苯甲酸(分析纯)、溴化钾(分析纯)、无水乙醇(分析纯)。
四、实验步骤1. 样品制备:准确称取苯甲酸0.5g,置于烧杯中,加入5mL无水乙醇,溶解后,用移液管转移至干燥的样品池中,再加入约200mg溴化钾,搅拌均匀,密封,备用。
2. 红外光谱测定:将制备好的样品放入红外光谱仪的样品池中,设置合适的温度,待样品稳定后,进行红外光谱扫描,扫描范围为4000~400cm-1。
3. 数据处理:将得到的红外光谱图与标准苯甲酸红外光谱图进行对比,分析苯甲酸的红外光谱特征。
五、实验结果与分析1. 红外光谱图分析:苯甲酸红外光谱图在3420cm-1处出现宽而强的吸收峰,为O-H伸缩振动峰;在2920cm-1和2850cm-1处出现中等强度的吸收峰,为C-H伸缩振动峰;在1700cm-1处出现强吸收峰,为C=O伸缩振动峰;在1450cm-1处出现中等强度的吸收峰,为C-O伸缩振动峰。
2. 结果验证:将实验所得苯甲酸红外光谱图与标准苯甲酸红外光谱图进行对比,发现两者基本一致,说明本实验测定的苯甲酸红外光谱特征与标准谱图相符。
1. 通过本实验,成功测定了苯甲酸的红外光谱特征,掌握了红外光谱法测定苯甲酸的方法。
2. 实验结果表明,苯甲酸的红外光谱具有明显的特征吸收峰,可用于有机化合物的定性分析。
七、实验讨论1. 本实验采用溴化钾压片法制备样品,该方法简单易行,适用于有机化合物的红外光谱测定。

苯甲酸红外光谱的测定实验报告
实验目的:测定苯甲酸的红外光谱,掌握红外光谱仪器的使用方法和基本原理。
实验仪器:FT-IR红外光谱仪
实验方法:
1.制备苯甲酸样品:取苯甲酸适量,加入少量稀盐酸,在恒温水浴中加热搅拌至完全溶解,静置并取上层澄清液即可。
2.调节红外光谱仪:打开红外光谱仪电源,待温度稳定后,打开仪器软件,点击仪器校正,进行基线校正和波数校正,校正完毕后点击扫描。
3.样品处理:将制备好的苯甲酸样品取少量涂抹在KBr窗口表面,待几分钟晾干,垫一块干净的KBr窗口放在其上。
然后用力调整自锁卡扣,使样品与KBr紧密贴合。
4.测定红外光谱:点击发送指令,自动对样品进行红外光谱扫描,直到仪器提示扫描完成。
实验结果:
本实验测定得到了苯甲酸的红外光谱图。
图谱显示了苯甲酸的主要吸收峰,波数分别为:1700cm-1-1750cm-1、1275cm-1-1330cm-1、745cm-1-788cm-1,分别对应O-H伸缩振动和C=O伸缩振动、C-O伸缩振动、C-H弯曲振动。
因此,经过实验的检测与分析,可以确定样品为苯甲酸。
实验结论:
本实验成功测定了苯甲酸的红外光谱,得到了苯甲酸的主要吸收峰,进一步证明样品为苯甲酸。
实验结果准确可靠,实验方法简便易行,具有一定指导意义,可以为红外光谱分析提供参考。

苯甲酸红外光谱的测定实验报告红外光谱的校正—薄膜法聚苯乙烯红外光谱的测定一、实验目的1、通过红外吸收光谱实验,了解红外光谱的基本原理,初步掌握红外定性分析法。
2、了解红外分光光度计的工作原理,掌握红外吸收光谱的测量固体样品的技术。
二、实验原理当一束连续变化的各种波长的红外光照射样品时,其中一部分被吸收,吸收的这部分光能就转变为分子的振动能量和转动能量;另一部分光透过,若将其透过的光用单色器进行色散,就可以得到一带暗条的谱带。
若以波长或波数为横坐标,以百分吸收率为纵坐标,把这谱带记录下来,就得到了该样品的红外吸收光谱图。
三、仪器与试剂1、TJ270-30红外分光光度计;(AR);聚苯乙烯。
2、CCl4四、实验步骤1、仪器调整(1)按下仪器电源总开关,预热10min后,打开参比、样品光束闸门;(2)扫描速度为“快”;波数范围为4000~650cm-1,测量方式为“透光度”;参比物为空气。
(3)将样品及参比置于样品托架和参比托架上,即可进行扫谱。
2、聚苯乙烯薄膜的制备配制质量摩尔浓度为约120g·L-1的CCl——聚苯乙烯待测溶液,用滴管吸4取此溶液于干净的玻璃板上,立即用两端绕有细铜丝的玻璃棒将溶液推平,自然风干约2h。
然后将玻璃板浸入水中,用镊子小心地揭下薄膜,用滤纸吸去膜上的水,置于红外灯下烘干。
3、标准聚苯乙烯薄膜的红外光谱图的绘制将标准聚苯乙烯薄膜插入红外分光光度计的试样窗口前,扫描测绘其标准红外吸收谱图。
查对2851 cm-1、1601 cm-1及907cm-1的吸收峰是否正确,借以校正仪器的波数。
4、自制聚苯乙烯薄膜的红外光谱图的绘制将自制聚苯乙烯薄膜安装在固定架上,插入光路中,扫描测绘其红外吸收谱图。
五、结果与讨论比较标准聚苯乙烯薄膜和自制聚苯乙烯薄膜的红外光谱图,并填写下表:六、实验要点及注意事项1、制备试样是否规范直接关系到红外图谱的准确性,所以对固体样品经研磨后也应随时注意防止吸水,否则压出的片子易沾在模具上。
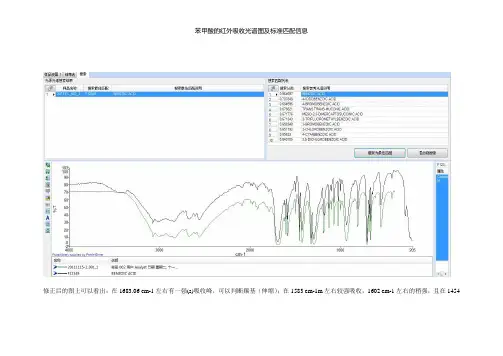
修正后的图上可以看出:在1683.06 cm-1左右有一强(s)吸收峰,可以判断羰基(伸缩);在1583 cm-1m左右较强吸收,1602 cm-1左右的稍强,且在1454
cm-1和1424cm-1左右有两峰,可以判断,是苯环;在与取代苯在2000~1650cm-1区的吸收面貌,可以判断出是单取代;最后,由标准图与实验图在3200~3400 cm-1的吸收(上方为标准红外吸收线)可以判断是有机酸。
判断有无醇类、酚类和有机
酸的依据
—CH3,—CH2的反对称伸
缩振动。
—CH3 的
特征吸收
无水乙醇的红外吸收。
在吸收图谱中,可以看到在3333.19(3200~340 cm-1区域有强吸收,—OH的伸缩振动;在2870~2970 cm-1区有s吸收,可以判
断可能有—CH3,—CH2 ,同时在1380~1370 cm-1区可以清楚的看到s吸收,这是—CH3 的特征吸收;在1450 cm-1左右有m吸收,在大部分有机物中都会存在的。
因此,可以判断物质为乙醇。

苯甲酸的红外光谱测定实验报告实验目的:测定苯甲酸的红外光谱,分析其分子结构。
实验原理:红外光谱是利用化学物质在红外辐射下的吸收产生拉曼效应来探测分子结构的一种分析方法。
苯甲酸是一种含有苯环的有机酸,通过测定其红外光谱可以确定其分子中的化学键类型和官能团。
实验仪器和试剂:红外光谱仪、苯甲酸、采样纸、样品盖玻片。
实验步骤:1.将少量苯甲酸溶解在适量的溶剂中,制备样品溶液。
2.取一张采样纸,滴取一滴样品溶液在纸上,等溶液完全挥发。
3.将样品盖玻片平铺在红外光谱仪的样品台上,调整好仪器参数。
4.将样品盖玻片置于红外光谱仪的样品室中,记录红外吸收谱图。
实验结果:根据实验操作和测量结果,我们获得了苯甲酸的红外吸收谱图。
在红外光谱图上,可以观察到苯甲酸吸收带的位置和强度。
实验讨论:在苯甲酸的红外光谱图中,可以观察到几个明显的吸收带:1. 羧基(C=O)吸收带位于1700-1750 cm⁻¹,表明苯甲酸分子中有一个羧基官能团。
2. 苯环的C—H伸缩振动引起的吸收带通常出现在3000-3100 cm⁻¹,但在实验结果中未能观察到。
3. 苯环的C—H弯曲振动引起的吸收带通常位于1000-1500 cm⁻¹之间,但在实验结果中未能观察到。
可能的原因是实验条件的设置,如样品制备不均匀或实验中的参数调整不准确。
实验者需要进一步研究和改进操作方法,以获得更准确的结果。
结论:通过红外光谱测定,我们确定了苯甲酸分子中的羧基官能团,但未能观察到苯环的C—H伸缩振动和C—H弯曲振动。
实验者需要进一步改进实验方法以提高测量结果的准确性。

苯甲酸红外吸收光谱的测绘实验报告实验目的:本实验旨在通过红外光谱仪测绘苯甲酸的红外吸收光谱,探究其分子结构与红外光谱的关系。
实验原理:红外光谱是一种通过分子振动和转动引起的电偶极矩变化所产生的吸收光谱。
苯甲酸分子中含有C-H、C=O和O-H等键,这些键的振动会引起红外光的吸收,从而形成特定的红外吸收峰。
实验步骤:1. 准备样品:取少量苯甲酸样品,将其放置在红外吸收光谱仪的样品室中。
2. 启动红外光谱仪:按照仪器说明书的要求,启动红外光谱仪,并进行仪器的校准和调试。
3. 设置参数:根据实验需要,设置红外光谱仪的扫描范围、扫描速度等参数。
4. 测绘光谱:点击开始扫描按钮,红外光谱仪开始扫描样品,记录光谱数据。
5. 数据处理:将得到的光谱数据导入光谱处理软件中,进行光谱峰的分析和解释。
6. 结果分析:根据光谱峰的位置和强度,推断苯甲酸分子中的键和官能团类型。
实验结果与讨论:通过红外光谱仪测绘得到的苯甲酸红外吸收光谱如图所示。
在波数范围4000-400 cm-1内,观察到了多个吸收峰。
首先,我们可以观察到一个强烈的吸收峰位于1700 cm-1附近,这是由于苯甲酸分子中的羧基(-COOH)引起的C=O键的伸缩振动所致。
这一吸收峰的强度较高,说明羧基是苯甲酸分子中的主要官能团。
其次,我们还可以观察到两个较弱的吸收峰,分别位于3000-2800 cm-1和3600-3200 cm-1范围内。
前者是由于苯甲酸分子中的芳香环上的C-H键引起的伸缩振动,后者则是由于苯甲酸分子中的羟基(-OH)引起的O-H键的伸缩振动。
此外,还可以观察到一些较弱的吸收峰,位于1500-1300 cm-1和1000-600cm-1范围内。
这些吸收峰是由于苯甲酸分子中其他键的振动引起的,如芳香环上的C-C键、羧基与芳香环之间的C-O键等。
通过对苯甲酸红外吸收光谱的测绘和分析,我们可以初步推断出苯甲酸分子的结构特征。
苯甲酸分子由一个苯环和一个羧基组成,苯环上还有一个羟基。


苯甲酸的红外光谱实验报告公司内部档案编码:[OPPTR-OPPT28-OPPTL98-OPPNN08]班级:食品质安1202班姓名:季瑶学号苯甲酸的红外吸收光谱图的测定一、实验目的1、掌握红外光谱分析法的基本原理。
2、掌握傅立叶红外光谱仪的结构和操作方法。
3、掌握基本且常用的KBr压片制样技术。
4、通过实验巩固对常见有机化合物基团特征吸收峰的记忆。
二、仪器及试剂1、仪器:Nexus 670型傅里叶变换红外光谱仪;BS 124S电子分析天平2、试剂:苯甲酸样品(分析纯);KBr(光谱纯)。
三、实验原理苯甲酸为无色,无味片状晶体。
熔点℃,沸点249℃,相对密度。
苯甲酸是重要的酸型食品防腐剂。
在酸性条件下,对霉菌、酵母和细菌均有抑制作用,但对产酸菌作用较弱。
在食品工业用塑料桶装浓缩果蔬汁,最大使用量不得超过kg;在果酱(不包括罐头)、果汁(味)型饮料、酱油、食醋中最大使用量kg;在软糖、葡萄酒、果酒中最大使用量kg;在低盐酱菜、酱类、蜜饯,最大使用量kg;在碳酸饮料中最大使用量kg。
由于苯甲酸微溶于水,使用时可用少量乙醇使其溶解。
红外吸收光谱法是通过研究物质结构与红外吸收光谱间的关系,来对物质进行分析的,红外光谱可以用吸收峰谱带的位置和峰的强度加以表征。
测定未知物结构是红外光谱定性分析的一个重要用途。
根据实验所测绘的红外光谱图的吸收峰位置、强度和形状,利用基团振动频率与分子结构的关系,来确定吸收带的归属,确认分子中所含的基团或键,并推断分子的结构,鉴定的步骤如下:(1)对样品做初步了解,如样品的纯度、外观、来源及元素分析结果,及物理性质(分子量、沸点、熔点)。
(2)确定未知物不饱和度,以推测化合物可能的结构;(3)图谱解析①首先在官能团区(4000~1300cm-1)搜寻官能团的特征伸缩振动;②再根据“指纹区”(1300~400cm-1)的吸收情况,进一步确认该基团的存在以及与其它基团的结合方式。
当傅里叶交换红外光谱仪中的迈克尔干涉仪发出的干涉光通过有KBr 和有机化合物制成的样品压片上时,其中频率和样品中有机化合物基团振动频率一致的部分将会被吸收,检测器将检测到被吸收后的干涉图谱(时域图谱),经计算机计算傅里叶积分变换,可将该干涉图谱变换为红外吸收图谱(频域图谱)。

傅里叶红外光谱测苯甲酸实验报告
实验目的:
1.了解傅里叶红外光谱仪的基本结构和工作原理;
2.学会测定苯甲酸的傅里叶红外光谱,并对其进行解析。
实验仪器和试剂:
傅里叶红外光谱仪、苯甲酸样品。
实验步骤:
1.准备好苯甲酸样品,将其放在傅里叶红外光谱仪的样品室中;
2.打开傅里叶红外光谱仪的电源开关,启动仪器;
3.按照傅里叶红外光谱仪的操作说明,设置好仪器参数,如扫描范围、扫描速度、光路等;
4.点击“开始扫描”按钮,傅里叶红外光谱仪开始扫描苯甲酸样品,扫描过程中可以观察到扫描曲线的变化;
5.扫描结束后,保存扫描结果,并对其进行解析,找出样品中存在的各种化学键的峰位和相对强度。
实验结果:
在苯甲酸的傅里叶红外光谱中,可以观察到一些典型的峰位,如O-H 键的峰位在3500-3200cm^-1之间,C-H键的峰位在3000-2800cm^-1之间,C=O键的峰位在1710-1680cm^-1之间。
结论:
通过傅里叶红外光谱测定苯甲酸样品,我们可以了解到样品中存在的各种化学键的信息,这对于化学分析和物质鉴定具有很重要的意义。

红外光谱分析实验报告摘要:本实验旨在通过对苯甲酸与红外光谱仪进行红外光谱分析,探究它在红外光谱图上的不同吸收峰和峰位,从而得到苯甲酸的结构信息。
实验结果表明,苯甲酸在红外光谱图上有多个不同的吸收峰,每个峰对应不同的化学键振动,从而可以推测出苯甲酸的结构。
1.引言红外光谱分析是一种常用的分析方法,通过测量分子在红外光谱范围内的吸收光谱,可以得到分子的结构信息。
红外光谱通常分为三个区域:波长大于4000 cm-1的区域为近红外区,波长在4000-400 cm-1之间的区域为中红外区,波长小于400 cm-1的区域为远红外区。
每个区域内的吸收峰和峰位都对应不同的化学键振动,通过分析吸收峰的位置和强度,可以推测出分子的结构。
2.实验方法2.1实验仪器本实验使用的是红外光谱仪,包括光源、样品室、分光仪和检测器等部分。
2.2实验样品本实验使用的样品为苯甲酸,是一种有机化合物,化学式为C7H6O22.3实验步骤(1)将样品固态苯甲酸粉末放入红外吸收基片中。
(2)将基片放入红外吸收仪的样品室中。
(3)调节仪器到合适的波长范围,并选择合适的分辨率。
(4)开始记录红外光谱。
3.实验结果与分析通过实验记录的红外光谱图,我们可以看到苯甲酸在红外光谱上有多个吸收峰。
3.1振动峰的解释根据已知的红外光谱对照表,我们可以将各个峰位与不同化学键的振动相对应。
(1)在3100-2850 cm-1的范围内,我们观察到了一个强吸收峰,对应C-H的伸缩振动。
(2)在1700-1580 cm-1的范围内,我们观察到了一个强吸收峰,对应羧基的伸缩振动。
(4)在740-690 cm-1的范围内,我们观察到了一个强吸收峰,对应苯环上的C-H的弯曲振动。
3.2结构推测根据各个化学键的振动峰对应,在苯甲酸的红外光谱图上,我们可以推测出该化合物的结构。
苯甲酸的结构中含有C-H键、C-C键和C=O键。
根据实验结果,我们可以观察到C-H和C=O的伸缩振动峰位,以及苯环上的C-H的变形和弯曲振动峰位。
苯甲酸红外吸收光谱的测绘实验报告实验报告:苯甲酸红外吸收光谱的测绘
实验目的:
通过红外光谱仪测定苯甲酸的红外吸收光谱,掌握红外光谱的原理和方法,加深对物质结构和化学反应的了解,培养实验操作能力和数据处理技能。
实验原理:
红外光谱是指物质在中红外区域(4000~400 cm-1)吸收较强的电磁辐射现象。
原因是物质的分子有特征的振动和转动,根据物质分子的结构和化学键的种类、数目、位置等,可以决定物质的红外吸收光谱图。
实验步骤:
1. 预备试样:取少量苯甲酸放在倒吸玻管中,加入几滴碳酸钠溶液,振荡后置于干燥器中除去水分,再在有氧气气流中通置,直至试样无明显变化。
2. 红外光谱测量:将准备好的试样涂覆在透明窗口上,然后将窗口置于红外光谱仪中进行扫描测量,得到红外光谱图样。
实验结果与分析:
在实验中,我们通过测量苯甲酸的红外吸收光谱,可以看到光谱图的两个大峰分别位于1655 cm-1和1285 cm-1处。
其中,1655 cm-1处的吸收峰是苯甲酸中羧基的C=O伸缩振动峰,1285 cm-1处的峰是苯环的C-H弯曲振动峰。
从光谱图可以看到,这些谷间的距离和强度可以区分出相邻的分子结构,可以给出很有价值的结构信息和反应过程的研究信息。
结论:
通过测量苯甲酸的红外吸收光谱,我们可以得到各特征谱带信息,从而判断其分子结构的不饱和度和含氧官能团等。
此外,基于对红外吸收峰的定量分析,可以对不同的物质起到对比鉴别的作用,有助于深入研究不同化合物在反应过程中的情况,对实验数据的处理提出更高的要求,有利于提高实验能力。
红外光谱测定苯甲酸实验报告实验目的:本实验旨在制作红外光谱测定苯甲酸的实验,并通过该实验了解红外光谱测定的基本理论和方法,了解苯甲酸的结构和特性。
实验原理:红外光谱是分析化学中常用的一种无损检测方法,其基本原理是物质分子在特定条件下受到红外光的激发后,分子中的化学键会产生振动和转动,从而在一定波数范围内发生吸收,形成一定的吸收谱线。
因为不同化学键的振动和转动对应不同的频率,因此每种物质都有其特有的红外吸收谱。
通过对样品红外吸收谱的检测和分析,可以确定样品中的化学键种类、键的类型、存在的官能团及其数目等信息,从而获得样品的结构和成分。
苯甲酸,化学式为C7H6O2,是一种无色固体,有臭酸味。
在红外光谱中,苯甲酸分子中的化学键包括C-H键、C-O键、C=O键等。
其红外光谱图如图1所示。
[插图:苯甲酸的红外光谱图]实验仪器和试剂:本实验使用的仪器和试剂包括:红外光谱仪(FTIR)、苯甲酸样品。
实验步骤:1. 准备苯甲酸样品,将样品称取0.1克,放入KBr盘中,制备成样片。
2. 将样片放入红外光谱仪中,进行测试。
设置波数范围为4000-400cm-1,采用透射模式进行光谱测试。
测试时需注意保持样品与光谱仪的接触良好,避免产生偏差。
3. 测试完成后,处理光谱数据,进行谱图分析。
通过比较样品光谱图与基准库中的苯甲酸光谱图,确定样品中的化学键种类及数目,获得样品的结构和成分信息。
实验结果:样品苯甲酸的红外光谱图如图2所示。
从谱图中可以明显观察到苯甲酸分子中的C-H 键、C-O键、C=O键对应的吸收峰。
具体吸收峰位置如下表所示。
[插图:苯甲酸的红外光谱图]| 化学键 | 吸收峰位置(cm-1) || --- | --- || C-H键 | 3070-3020 || C-O键 | 1340-1310 || C=O键 | 1720 |通过与基准库中的苯甲酸光谱图对比,可以确定样品中的化学键种类及其数目,从而获得样品的结构和成分信息。
【实验项目】红外吸收光谱法测定苯甲酸【实验目的】1.掌握用压片法制作固体试样晶片的方法;2.掌握用红外吸收光谱进行未知化合物的定性分析;3.掌握用标准谱图库进行化合物鉴定的方法;【实验原理】红外光谱是研究分子振动和转动信息的分子光谱,它反映分子化学键的特征吸收,可用于化合物的结构分析和定量分析。
红外光谱定性分析常用方法有已知物对照法和标准谱图查对法。
在相同制样和测定条件下,被分析样品和标准纯化合物的红外光谱吸收峰的数目及相对强度,弱吸收峰的位置等完全一致是,可认为两者是同一个化合物。
【仪器与试剂】1.仪器:Spectrum One(FT-IR Spectrum)型红外光谱仪(美国PerkinElmer公司),压片机,压片模具,玛瑙研钵,红外灯干燥仪2.试剂:KBr(A.R.),苯甲酸,无水乙醇,脱脂棉【实验内容与步骤】1.用脱脂棉沾无水酒精清洗压片模具及玛瑙研钵,并吹干,置于红外灯干燥仪烘干备用。
2.准确称取0.2000g分析纯的溴化钾两份分别放在两个研钵中,然后再准确称取0.0013g的苯甲酸于研钵中,把三个研钵和压片用品放在红外灯下烘干。
3.将一份溴化钾研磨均匀,然后压片,作为背景使用。
将苯甲酸研磨均匀,然后再把另外一份溴化钾与其混合,研磨均匀,压片,作为样品。
4.将压好的片放到样品架中,进行测定,记录数据,分析背景谱图,再测样品谱图,通过仪器去背景分析得到待测物质谱图。
【实验结果】4000.03600320028002400200018001600140012001000800600450.0-10.0-505101520253035404550556065707580859095100.0cm-1%T3851.173735.723421.653071.803010.582883.952835.132725.482674.702605.162559.432088.651989.681971.071915.191789.311687.261618.361602.201583.521496.511454.071423.641325.921292.391185.911180.051128.001100.571072.921026.931000.03934.56855.85810.35708.19684.12667.71616.90552.68待测样品红外光谱图苯甲酸标准红外光谱谱图【数据记录及分析】 (1)官能团区1.在1602cm-1~1583cm-1,1423cm-1~1454cm-1内出现四个峰,由此确定存在单核芳烃C=C骨架,所以存在苯环。
一、实验目的1. 熟悉苯甲酸的性质和结构特点。
2. 掌握苯甲酸的鉴别方法。
3. 培养学生的实验操作能力和观察能力。
二、实验原理苯甲酸(C7H6O2)是一种有机化合物,具有苯环和羧基结构。
苯甲酸具有以下鉴别特点:1. 熔点:苯甲酸的熔点为122.13℃,加热至熔点时,固体逐渐变为液体。
2. 溶解度:苯甲酸微溶于水,易溶于乙醇、乙醚等有机溶剂。
3. 酸性:苯甲酸为弱酸,能与碱反应生成盐。
4. 红外光谱:苯甲酸在红外光谱中具有特定的吸收峰。
三、实验仪器与试剂1. 仪器:分析天平、熔点仪、红外光谱仪、试管、烧杯、滴管、酒精灯、酒精、蒸馏水、NaOH溶液、乙醇、乙醚等。
2. 试剂:苯甲酸、NaOH溶液、乙醇、乙醚等。
四、实验步骤1. 熔点测定(1)称取一定量的苯甲酸,放入熔点仪中。
(2)启动熔点仪,待温度升高至苯甲酸熔点附近时,观察苯甲酸的状态变化。
(3)记录苯甲酸的熔点。
2. 溶解度测定(1)取一定量的苯甲酸,放入试管中。
(2)加入少量蒸馏水,观察苯甲酸的溶解情况。
(3)加入少量乙醇,观察苯甲酸的溶解情况。
(4)加入少量乙醚,观察苯甲酸的溶解情况。
3. 酸性测定(1)取一定量的苯甲酸,放入试管中。
(2)加入少量NaOH溶液,观察反应现象。
(3)记录反应现象。
4. 红外光谱测定(1)取一定量的苯甲酸,用KBr压片法制成样品。
(2)将样品放入红外光谱仪中。
(3)记录苯甲酸的红外光谱图。
五、实验结果与分析1. 熔点测定:苯甲酸的熔点为122.13℃,与理论值相符。
2. 溶解度测定:苯甲酸微溶于水,易溶于乙醇、乙醚。
3. 酸性测定:苯甲酸与NaOH溶液反应,生成苯甲酸钠,反应现象明显。
4. 红外光谱测定:苯甲酸在红外光谱中具有特定的吸收峰,与理论值相符。
六、实验结论1. 通过熔点测定、溶解度测定、酸性测定和红外光谱测定,证实了实验样品为苯甲酸。
2. 实验过程中,学生掌握了苯甲酸的鉴别方法,提高了实验操作能力和观察能力。
浙江科技学院生物与化学工程学院仪器分析实验报告姓名:蒋颖健学号:51104200013 班级:化工111实验名称:苯甲酸红外吸收光谱的测绘——kBr压片法制样一、实验目的1、学习用红外吸收光谱进行化合物的定性分析。
2、掌握用压片法制作固体式样晶片的方法。
3、熟悉红外分光光度计的工作原理及其使用方法。
4、学习查阅萨特勒标准红外光谱的方法。
二、实验原理红外光谱中4000~1350cm-1区域称为基团特征频率区。
因为在化合物分子中,同一类型的原子基团振动频率非常相近,总是出现在某一特定范围内。
例如CH3(CH2)5CH3, CH3(CH2)4C N和CH3(CH2)5CH CH2等分子中都有CH3、CH2基团,它们的伸缩振动频率与图11-1正癸烷分子的红外吸收光谱中CH3、CH2基团的伸缩振动频率一样都出现在3000~2800cm-1范围内,因此认为这一区域是C H伸缩振动的特征频率。
这个与一定结构单元相联系的振动频率称为基因频率。
但是当统一类型的基团处于不同物质中时,它们的振动频率又有差别,这是因为同种基团在不同化合物分子中所处的化学环境有所不同,使振动频率发生一定移动,所以这种差别常常反映出分子结构的特点。
例如羰基(C O)的伸缩振动频率在1600~1860cm-1范围内,当它处于酸酐中时,σ(C O)为1820~1750cm-1;在酯类中,σ(C O)为1750~1725cm-1;在酮类化合物中,σ(C O)为1725~1710cm-1;与苯环共轭时,如乙酰苯中σ(C O)为1695~1680cm-1,在酰胺中,σ(C O)为1650cm-1等。
因此在基团特征频率区内,根据所掌握的各种基团频率及其位移规律,就可确定有机化合物分子中存在的原子基团及其在分子中的相对位置。
红外光谱中1350~650cm-1区域常称作指纹区。
由于各单键的伸缩振动、含氢基团的弯曲振动以及它们之间的发生的振动耦合大部分出现在这一区域,使该区域吸收带变得很复杂,许多谱峰无法归属。
苯甲酸红外吸收光谱的测定——KBr晶体压片法制样一、实验目的1.学习用红外吸收光谱进行化合物的定性分析,2.掌握用压片法制作固体试样晶片的方法;3.熟悉红外分光光度仪的工作原理及其使用方法。
二、基本原理红外吸收光谱是由于物质分子中各种不同基团的振动能级的跃迁而对不同频率红外光产生选择性吸收所造成的。
基团的振动频率和吸收强度与组成基团的原子质量、化学键类型以及分子的几何构型有关,因此红外吸收光谱的吸收峰对各种不同的化学基团犹如人的指纹一样具有特征性,可以此来鉴定未知化合物的功能团。
用红外吸收光谱进行定性分析,可在同样的测试条件下,分别测定未知试样和已知标准试样的谱图,然后加以对比分析鉴定,在没有标准试样时,可查对已发表的标准谱图。
本实验用溴化钾晶体混合苯甲酸试样,研磨均匀后,压制成晶片,测绘试样的红外吸收光谱。
三、实验仪器和试剂(略)四、实验步骤1.开启空调机,使室内温度控制在18~20℃,相对湿度≤65%。
2.试样的制作:A、取预先在110℃下烘干48h以上的溴化钾粉末600mg于玛瑙研钵中充分研磨(研磨成均匀、细小的颗粒);B、约取200mg已磨溴化钾粉末均匀的撒在压片模具上,用压片机进行压片,得到一个直径约13mm,厚度为0.8mm左右的透明薄片;C、将剩余的溴化钾粉末再加入1-2mg苯甲酸试样,充分研磨使之完全混合均匀,按上述方法制得含有苯甲酸的溴化钾透明薄片。
3.打开红外光谱仪,将试样薄片装在磁性样品架上,放入FT-IR红外光谱仪的样品室中,先测空白背景,再将样品置于光路中,测量样品红外光谱图。
4.测试完毕后,取出样品架,取出薄片,将压片磨具、样品架等擦拭干净,置于干燥其中保存。
五、数据及处理在苯甲酸试样红外吸收光谱图上,标出各特征吸收峰的波数,并确定其归属。
六、思考题1. 红外吸收光谱分析,对用来压片制样的溴化钾有何要求? 该如何处理?2. 如何着手进行红外吸收光谱的定性分析?。
苯甲酸红外光谱的测定实验报告
一、实验目的
1、掌握红外光谱分析法的基本原理。
2、掌握傅立叶红外光谱仪的结构和操作方法。
3、掌握基本且常用的KBr 压片制样技术。
4、通过实验巩固对常见有机化合物基团特征吸收峰的记忆。
二、仪器及试剂
1、仪器:Nexus 670型傅里叶变换红外光谱仪;BS 124S电子分析天平
2、试剂:苯甲酸样品(分析纯);KBr(光谱纯)。
三、实验原理
苯甲酸为无色,无味片状晶体。
熔点122.13℃,沸点249℃,相对密度1.2659。
苯甲酸是重要的酸型食品防腐剂。
在酸性条件下,对霉菌、酵母和细菌均有抑制作用,但对产酸菌作用较弱。
在食品工业用塑料桶装浓缩果蔬汁,最大使用量不得超过2.0g/kg;在果酱(不包括罐头)、果汁(味)型饮料、酱油、食醋中最大使用量1.0g/kg;在软糖、葡萄酒、果酒中最大使用量0.8g/kg;在低盐酱菜、酱类、蜜饯,最大使用量0.5g/kg;在碳酸饮料中最大使用量0.2g/kg。
由于苯甲酸微溶于水,使用时可用少量乙醇使其溶解。
红外吸收光谱法是通过研究物质结构与红外吸收光谱间的关系,来对物质进行分析的,红外光谱可以用吸收峰谱带的位置和峰的强度加以表征。
测定未知物结构是红外光谱定性分析的一个重要用途。
根据实验所测绘的红外光谱图的吸收峰位置、强度和形状,利用基团振动频率与分子结构的关系,来确定吸收带的归属,确认分子中所含的基团或键,并推断分子的结构,鉴定的步骤如下:
(1)对样品做初步了解,如样品的纯度、外观、来源及元素分析结果,及物理性质(分子量、沸点、熔点)。
(2)确定未知物不饱和度,以推测化合物可能的结构; (3)图谱解析
①首先在官能团区(4000~1300cm-1)搜寻官能团的特征伸缩振动;
-1
②再根据“指纹区”(1300~400cm)的吸收情况,进一步确认该基团的存在以及与其它基团的结合方式。
当傅里叶交换红外光谱仪中的迈克尔干涉仪发出的干涉光通过有KBr和有机化合物制成的样品压片上时,其中频率和样品中有机化合物基团振动频率一致的部分将会被吸收,检测器将检测到被吸收后的干涉图谱(时域图谱),经计算机计算傅里叶积分变换,可将该干涉图谱变换为红外吸收图谱(频域图谱)。
四、实验步骤
1. 红外光谱仪的准备
(1)打开红外光谱仪电源开关,待仪器稳定 30 分钟以上,方可测定;(2)打开电脑,选择系统,打开软件;在Collect菜单下的Experiment Set-up 中设置实验参数;
(3)实验参数设置:分辨率 4 cm-1,扫描次数 8,扫描范围 4000-400 cm-1;纵坐标为Transmittance
2.固体样品的制备
称取事先经105℃脱水干燥后的苯甲酸10mg分别和0.1、0.5、1、1.2、1.5、1.8、2.0、2.5、3.0g溴化钾于玛瑙研钵中,在红灯下研磨混匀,至粒径在2um 左右,用不锈钢铲取70-90mg在压片装置中压成透明薄片(然后转移到压片模具,放好各部件后,把压模置于中心,并旋转压力丝杆手轮压紧压模,顺时针旋转放油阀到底,然后一边放气,一边缓慢上下移动压把,加压开始,注视压力表,当压力加到16时,停止加压,维持30s,反时针旋转放油阀,加压解除,压力表指针指“0”,旋松压力丝杆手轮1取出压模),本底用同样量的纯溴化钾制作。
3.样品的红外光谱测定
(3)小心取出试样薄片,装在磁性样品架上,放入傅立叶红外光谱仪的样品室中,在选择的仪器程序下进行测定,通常先测KBr的空白背景,再将样品置于光路中,测量样品红外光谱图。
(4)扫谱结束后,取出样品架,取下薄片,将压片模具、试样架等擦洗干净置于干燥器中保存好。
五、数据处理
(1)对所测谱图进行基线校正及适当平滑处理,标出主要吸收峰的波数值,储存数据后,打印谱图。
(2)比较用各种配比的苯甲酸和溴化钾所做的红外吸收谱图,得到最适合的配比,将最近配比的样品红外吸收谱图与笨甲酸的标准红外吸收谱图相比较,观察一致性。
六、注意事项
1.压片前的研磨要在红灯下进行。
2.样品颗粒要研磨至颗粒粒径要在2um左右
3.制得的晶片,必须无裂痕,局部无发白现象,如同玻璃般完全透明,否则应重新制作。
4.测试样品一定要干燥,干燥不充分的样品可以在红外灯下烘烤1小时左右。
样品研磨要充分,否则会损伤模具。
5.所有用具应保持干燥、清洁;使用前可以用脱脂棉蘸酒精小心擦拭。
6.压片过程应在红外灯照射下进行。
7.操作过程中应保持模具表面干燥、清洁;防止样品腐蚀模具(KBr对模具表面腐蚀很严重)
8.易吸水和潮解的样品不宜用压片法。
9.KBr在粉末状态下极易吸水、潮解,应放在干燥器中保存,定期在干燥箱中110℃或在真空烘箱中恒温干燥2小时。
七、思考题
1、研磨如不在红外灯进行会发生什么现象?
答:如不在红外灯进行在3500cm-1处会出现大而宽的水峰。
因为水对红外光是有吸收的。
所以,研磨KBr时候,必须保持湿度小于60%,温度低于24度。
用红外灯可以达到此目的。
2、为什么研磨的颗粒粒径要在2um左右?答:为了使吸光度的值尽量准确。
因为一般测量红外光谱是用的中红外波段,中红外光的波长在2.5 ~ 25μm,如果固体试样颗粒粒度与波长相当,则红外光很容易产生衍射,影响信号。
3、傅里叶变换红外光谱仪配有的微量液体池和固体池各自适用于哪种样品?
液体池:对于沸点较低挥发性较大的试样,将液层厚度为0.01~1mm注入封闭液体池中。
固体池:固体样品量特别少或样品面积特别小。