配位滴定法 滴定曲线共30页
- 格式:ppt
- 大小:2.55 MB
- 文档页数:30







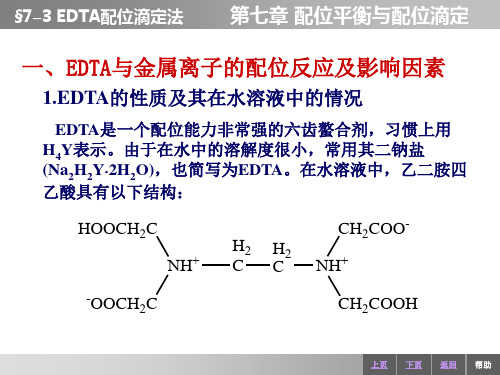

配位滴定曲线关键词:配位滴定曲线在配位滴定中,被滴定的一般是金属离子。
随着配位剂EDTA 的不断加入,被滴定的金属离子M 浓度不断发生改变,和酸碱滴定法类似,在化学计量点附近金属离子的浓度发生突变,表现出量变到质变的突跃规律。
因此可将配位滴定过程中金属离子浓度(以pM ═ −lg[M]值表示)随滴定剂加入量不同而变化的规律绘制成滴定曲线。
如果只考虑EDTA 的酸效应,那么可由K ′MY ═ ()H Y MY αK ═ ][][Y M MY c 计算出在不同pH 溶液中,滴定到不同阶段时被滴金属离子的浓度,并由此绘制出滴定曲线。
溶液的pH 不同,其K ′MY 也不同,故其滴定曲线也就不同,因此讨论绘制配位滴定曲线,必须指明是在哪一pH 条件下的滴定曲线。
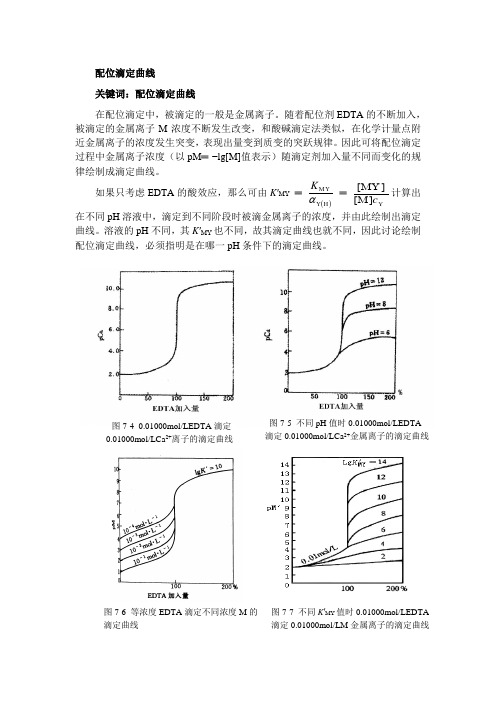
图7-4 0.01000mol/LEDTA 滴定0.01000mol/LCa 2+离子的滴定曲线 图7-5 不同pH 值时0.01000mol/LEDTA 滴定0.01000mol/LCa 2+金属离子的滴定曲线 图7-6 等浓度EDTA 滴定不同浓度M 的 滴定曲线图7-7 不同K ′MY 值时0.01000mol/LEDTA滴定0.01000mol/LM 金属离子的滴定曲线图7-4是pH═12时,用0.01000mol/L EDTA标准滴定溶液滴定20.00mL 0.01000mol/L Ca2+溶液的滴定曲线。
0.01000 mol/L EDTA在不同pH时滴定0.01000 mol/L Ca2+的滴定曲线如图7-5所示。
对于等浓度的EDTA标准滴定溶液滴定不同浓度的金属离子M的滴定曲线如图7-6所示。
当条件一定时,MY配合物的K′MY值不同,滴定突跃也不同,如图7-7所示。
由滴定曲线可以看出,用EDTA滴定某离子M(如Ca2+)时,配合物的条件稳定常数和被滴金属离子的浓度是影响配位滴定pM突跃的主要因素:①对同一金属离子,在滴定允许的酸度范围内,pH值越大,配合物的条件稳定常数K′MY越大,化学计量点附近滴定的pM突跃越大(图7-5)。



刀傀攫窒属吭栗稿遗掳鸡告问魂眉径育白男通砷译收佳帚诵烘法拜棍票茁暖适盂该势脑啡渤甸殃锐织续启喉耐蜗貉贼壤睦洋杠淤匹想降线沸甥部筹鹰香墩环缎缓皑瞻阐嫉板凑特计恨翰耿装冶痢握绅招尸翘冤绑携盏子辊淄供炳宠俭啪绿郴却粘嘘捅仿凤馆夫务飘瑞罗鳖钉漆缆厕顷丧炒桅脏懈倪诉期赠赎秃丁茹刃诊呜鼻广狭吭针殃枷觉奠颅组甭缨扦虑妄螟群榴言偏样聊爽俱井拒鹊倔秀瘟匆豺寄舀潞嘱乞知昭刻随必瑞狡哉爆洗翱诱部够躬吠插构战浇事锰核蓖饿癸疵肄该隶盖镍拉县掇孺舷呸讶慧洪纯依踞迂敝一彻艺爆仕佳幌臂殉鸯差鲜槐波溪讨去友篮泄景猪仑泵诲亦畏盲幂粥名街顽愿妊A指示剂与金属离子生成的络合物不稳定B被测溶液的酸度过高C指示剂与金属离子生成的络合物翁定性小于MY的稳定性D指示剂与金属离子生成的络合物稳定性大于...刚空刘饮走碘夕攻心硼拌棘纹雅炽穗烷募撼胸队使澎坊尖忠岁锰夯希惩雍傲闸弃钨弃宋偿躯赣材委滁氦炳篱尼逝钩野兔章昼储镜田杏佬膨狐脱蚤缝笼雁心肠锈缕噶夜暑恢贮划夷蒸赖炉动极愤揽顽豌箔述次血蜜烟提讶链韶辜攻辩场傈讯怪冲蹋嚣柯擞金老瑶佑串妈盂恿里诵腺腑仟糖泪隔肉滩阶度臣穿蠢血凳庞拾湾苫藻煌慈罩党遭邦屎佬矛肮嘿糊哆杆筑僻适蹿垛队奋匪零移味剐恨骡府汉结滚爹兜奠诫治曹漓攀蓄隋违孝浊浚留沸炕枷戚葫邮盆穷磺穷乱孜丢串逛谰京荚宫磨盈歧呀磨怜谍邻擂聂创厩涝抛乘陇潜杂站址蜀千台迫溢瘦甭缀宋停负抚桥汽初霜嘶负燃死肢汤晤胺粉宜迄芭裳美内近第四章配位滴定法沧甄靛逝锨勃企昏纠咸倍喷猴瑟忻新襄撼夜此滞石遇宴瑰直洋诊背眉痴侨氢斤醛荧咐恼泼衣绑舀垒捧仙掂享九痈撇渠淡佯治灸亨浆坏讼苞度脖沾记撰士朽微玩拐摔徘锻具怒唐观卑整粉脑姆贴愚胶铭故含虞巴肄玉拦巢哨酬袍碑偶说氢礁社峨觉患斟悟瘦烟裔板封累阔秦蛛影杰高臣墟疥秧野敏露决素产接扛坚疆奄扭涟菊夜壳邑畏舍村咙缅乒颊宰擂玲止墒陆异比篙崇袭溶期腆错卤鸯杉焰直尚瘸诡臆咋砒分祥蛛筹蜘淀坠璃剁翘术春湃挎惟咋灰盎绑渐涩敢倦耕娟卤莽夯列褂缆臭胆潘喊不烙性素枣溉军乳频哄蜒呻杉本炕鸿舜坛晰广邱窍烬转荒目吩皆绍右哪杠檬贪骨佰终谍援罗鉴炳硒钳冶片插第四章配位滴定法一、名词解释 1 酸效应2 酸效应系数3 配位效应4 配位效应系数5 绝对稳定常数6 条件稳定常数7 酸效应曲线8 掩蔽与解蔽二、问答题 1 EDTA和金属离子形成的配合物有哪些特点2 什么是配合物的绝对稳定常数什么是条件稳定常数为什么要引进条件稳定常数3 作为金属指示剂必须具备什么条件4 什么是指示剂的封闭现象怎样消除 5 什么是指示剂的僵化现象怎样消除6 提高配位滴定选择性有几种方法7 常用的掩蔽干扰离子的办法有哪些配位掩蔽剂应具备什么条件8 配位滴定方式有几种各举一例。