
前列腺癌根治性放疗规范
目前在前列腺癌根治性放疗靶区勾画上欧美国家已基本形成共识,参照美国放疗肿瘤学研
究组(RTOG关于前列腺癌的放疗靶区勾画建议、美国国立综合癌症网络(NCCN和欧洲泌尿
协会制定的前列腺癌诊治指南,并结合我们的临床实践,对局限期前列腺癌根治性放疗的靶区勾画提出规范化建议。
衷"用棉危阻勺事分組的疗尺内分泌治打朮诅
定险分ifl UtfetS中危餾
Tl-T2a T2l>-T2c T3-T4
RSA >- H)PSA 为10-20 瞅nl PS A - 20 n^M
(;£< 7 ■*>+GS=7 好分
戒疗及商3n-(:RTEilMRT
3t^CRTdt 1MRT
(76^81
3D-CRT或IMRT F *81
分蚩常疗175,6-79,2 Gy >G头联合新辆阳2精助内
分蛇治疗斗-6 6月内分締箱疗
2 V年
总列!9n T JM:B+SV*(2-23 rmj L,讪朴2-2.^ 1 rri +
就护翼丈it爲全你屛.前罚睥特并蚩拭原:GS,恪靈轨评令详D-(:RT*三母适殆就井和MRT.谒爱就疔浮¥?料录俅
-:軒卓巴社杆禺1 \M :> 15唏r则增加北ItlS
1、体位固定及CT定位:定位前4小时可口服4% 1000 ml稀释的肠道对比剂,定位前排空直肠, 憋尿充盈膀胱。CT定位采取仰卧位,体模固定,层厚3 mm扫描,扫描范围从腰4椎体下缘至坐骨结节下3 cm。
2前列腺及精囊腺靶区勾画
(1)局限低危前列腺癌放疗靶区只包括前列腺;局限中危前列腺癌或盆腔淋巴结转移几率
< 15%勺局限高危前列腺癌放疗靶区包括前列腺和精囊腺。
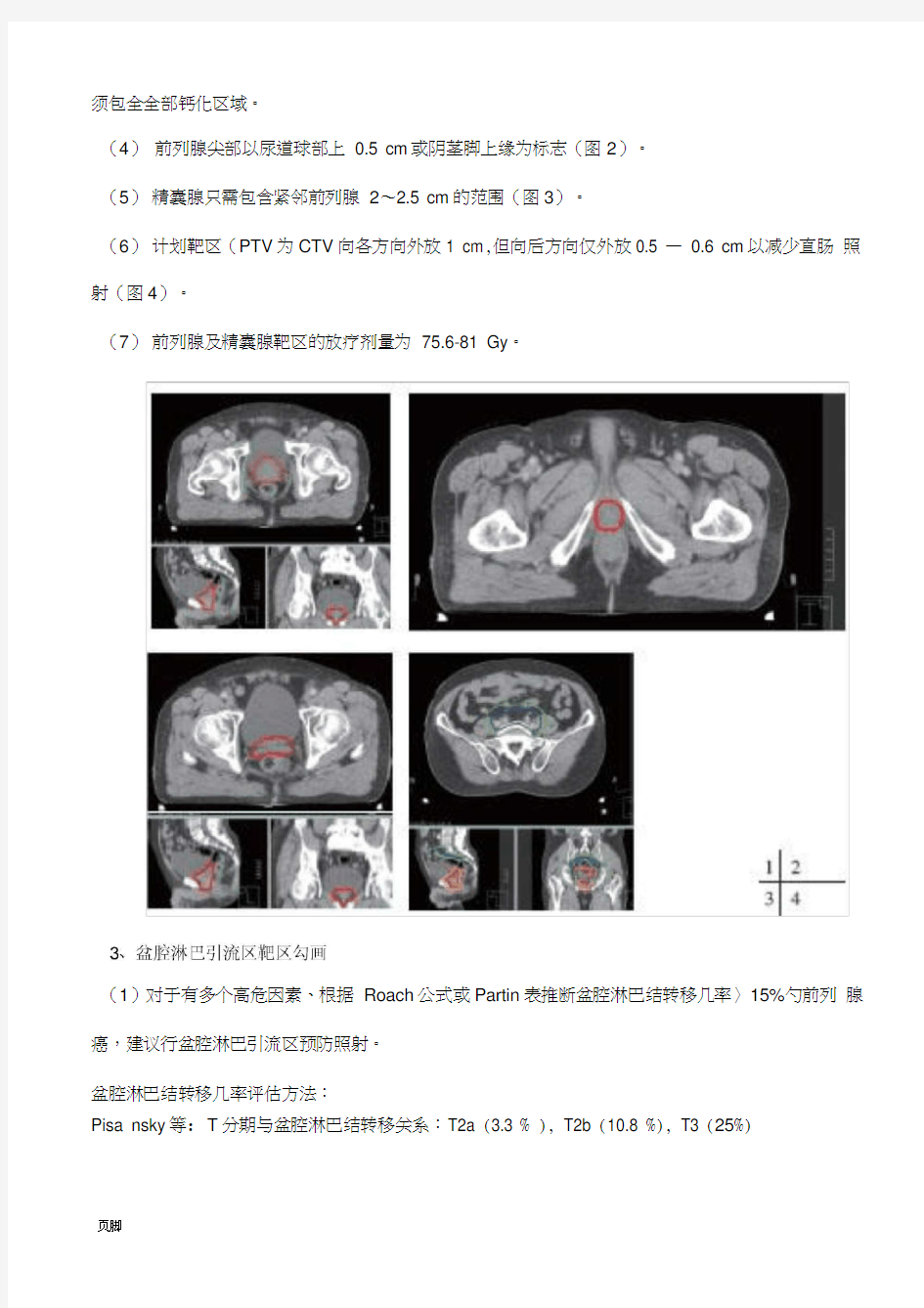
(2)前列腺癌往往为多发灶,且CT和磁共振成像(MR)无法检测出前列腺内的全部病灶,因此,前列腺癌难以勾画肿瘤靶区(GTV转移淋巴结除外),只勾画临床靶区(CTV (图1) < (3)前列腺靶区勾画自前列腺底至前列腺尖的全部前列腺组织(图1),若前列腺存在钙化,
须包全全部钙化区域。
(4)前列腺尖部以尿道球部上0.5 cm或阴茎脚上缘为标志(图2)。
(5)精囊腺只需包含紧邻前列腺2?2.5 cm的范围(图3)。
(6)计划靶区(PTV为CTV向各方向外放1 cm,但向后方向仅外放0.5 —0.6 cm以减少直肠照射(图4)。
(7)前列腺及精囊腺靶区的放疗剂量为75.6-81 Gy。
(1)对于有多个高危因素、根据Roach公式或Partin表推断盆腔淋巴结转移几率〉15%勺前列腺癌,建议行盆腔淋巴引流区预防照射。
盆腔淋巴结转移几率评估方法:
Pisa nsky等:T分期与盆腔淋巴结转移关系:T2a (3.3 % ), T2b (10.8 %), T3 (25%)
Roach公式:Node(+)=[2/3PSA+(Gleason-6)]%
> 15%t较大盆腔淋巴结转移危险;〉30%t很大盆腔淋巴结转移危险
前列腺癌盆腔淋巴结转移可能性估计(Partin表):
(2)盆腔淋巴引流区范围:从L5与S1交界水平勾画至耻骨联合上缘水平。
(3)盆腔淋巴引流区应包括髂外淋巴结、髂内淋巴结、闭孔淋巴结。CTV勾画包括髂血管及其外7 mm距离,一般不包含过多的小肠、膀胱、骨及肌肉(图5)。
(4)骶1—3椎体水平应包括髂内、髂外淋巴结和骶前淋巴结(图6),骶前包含椎体前1.5?2 cm (图5)。
(5)骶3椎体以下包括髂内、髂外外淋巴结及闭孔淋巴结,骶前淋巴结勾画终止于梨状肌出现层面(图7)。
(6) 髂外淋巴结一直要勾画至股骨头顶端层面,即腹股沟韧带处(髂外动脉与股动脉分界处, 即定位CT 所示股骨头顶端层面水平)(图8)。
(7) 闭孔淋巴结要勾画至耻骨联合上缘水平(图 9)。
(8) 盆腔淋巴引流区PTV 为CTV 外放0.5 cm (图4)。
(9) 盆腔淋巴引流区预防剂量为45-50 Gy ,对于影像学明确证实的盆腔转移淋巴结, 剂量不低 于 70 Gy 。
4、正常组织和结构勾画 (1)主要勾画直肠、膀胱、股骨头、小肠、和结肠等正常组织和结构(图 10)。
直肠从坐骨结节水平勾画至骶 3椎体水平,膀胱勾画全膀胱体积,股骨头勾画全股骨头范
围,小肠勾画PTV 层面及PTV 以上3个层面的小肠体积(层厚0.3 cm ),结肠勾画PTV 层面及 PTV 以上3个层面的结肠体积(图10)。
團示ftSWE 及正章绢纭和络沟勾刊
(2)正常组织器官剂量限制如下:直肠V50(接受50 Gy的体积百分比,余此类推)< 50%极限V7(X 20%膀胱V50< 50%极限V7(X 30%股骨头V50 < 5%小肠V5C X 5% 最大剂量< 52 G y;结肠,V50< 10% 最大剂量w 55 Gy。
5、采用3D-CRT或IMRT,若放疗剂量>78 Gy,建议使用图像引导放疗(IGRT)。
前列腺癌包括盆腔淋巴引流区的靶区勾画pla n1
前列腺癌根治性放疗规范 目前在前列腺癌根治性放疗靶区勾画上欧美国家已基本形成共识,参照美国放疗肿瘤学研究组(RTOG)关于前列腺癌的放疗靶区勾画建议、美国国立综合癌症网络(NCCN)和欧洲泌尿协会制定的前列腺癌诊治指南,并结合我们的临床实践,对局限期前列腺癌根治性放疗的靶区勾画提出规范化建议。 1、体位固定及CT定位:定位前4小时可口服4% 1000 ml稀释的肠道对比剂,定位前排空直肠,憋尿充盈膀胱。CT定位采取仰卧位,体模固定,层厚3 mm扫描,扫描范围从腰4椎体下缘至坐骨结节下3 cm。 2、前列腺及精囊腺靶区勾画 (1)局限低危前列腺癌放疗靶区只包括前列腺;局限中危前列腺癌或盆腔淋巴结转移几率 ≤15%的局限高危前列腺癌放疗靶区包括前列腺和精囊腺。 (2)前列腺癌往往为多发灶,且CT和磁共振成像(MRI)无法检测出前列腺内的全部病灶,因此,前列腺癌难以勾画肿瘤靶区(GTV,转移淋巴结除外),只勾画临床靶区(CTV)(图1)。(3)前列腺靶区勾画自前列腺底至前列腺尖的全部前列腺组织(图1),若前列腺存在钙化,须包全全部钙化区域。 (4)前列腺尖部以尿道球部上0.5 cm或阴茎脚上缘为标志(图2)。
(5)精囊腺只需包含紧邻前列腺2~2.5 cm的范围(图3)。 (6)计划靶区(PTV)为CTV向各方向外放1 cm,但向后方向仅外放0.5—0.6 cm以减少直肠照射(图4)。 (7)前列腺及精囊腺靶区的放疗剂量为75.6-81 Gy。 3、盆腔淋巴引流区靶区勾画 (1)对于有多个高危因素、根据Roach公式或Partin表推断盆腔淋巴结转移几率>15%的前列腺癌,建议行盆腔淋巴引流区预防照射。 盆腔淋巴结转移几率评估方法: Pisansky等: T分期与盆腔淋巴结转移关系:T2a(3.3%),T2b(10.8%),T3(25%)。Roach公式:Node(+)=[2/3PSA+(Gleason-6)]% >15%有较大盆腔淋巴结转移危险;>30%有很大盆腔淋巴结转移危险。 前列腺癌盆腔淋巴结转移可能性估计(Partin表):
常见肿瘤靶区勾画集团标准化工作小组 #Q8QGGQT-GX8G08Q8-GNQGJ8-MHHGN#
前列腺癌根治性放疗靶区建议 作者:中国医学科学院肿瘤医院放疗科刘跃平李晔雄王维虎房辉来源:中国医学论坛报日期:2012-03-30 随着人均寿命的延长,我国老年人口的不断增加,的发病率逐年上升。放疗是前列腺癌根治性治疗手段之一,从局限低、中、高危前列腺癌到盆腔淋巴结转移,甚至远处转移前列腺癌,放疗均有广泛的应用。对于局限期前列腺癌,放疗可取得与手术相当的疗效且并发症的发生较少。 近年来,随着各种放疗新技术的出现和发展,前列腺癌的放疗越来越准确,正常组织的保护则更可靠,因此,接受放疗的患者越来越多。我们参照美国放疗肿瘤学研究组(RTOG)关于前列腺癌的勾画建议、美国国立综合癌症网络(NCCN)和欧洲泌尿协会制定的前列腺癌诊治指南,并结合我们的临床实践,对局限期前列腺癌根治性放疗的靶区勾画提出参考性建议,旨在使前列腺癌放疗靶区定义规范化和合理化。 从表1得知,前列腺癌靶区勾画主要包括前列腺、精囊腺及盆腔淋巴引流区,对局限期前列腺癌根治性放疗的靶区确定,我们提出如下建议。 1CT定位及放疗 ·定位前时排空膀胱和直肠,口服1000ml稀释的肠道对比剂,然后憋尿充盈膀胱。CT定位采取仰卧位,体模固定,层厚3mm扫描,扫描范围从腰4椎体下缘至坐骨结节下3cm。 ·建议采用3D-CRT或IMRT,若放疗剂量≥78Gy,建议使用图像引导放疗(IGRT)。 2前列腺及精囊腺靶区勾画
·局限低危前列腺癌放疗靶区只包括前列腺;局限中危前列腺癌或盆腔淋巴结转移几率≤15%的局限高危前列腺癌放疗靶区包括前列腺和精囊腺。 ·前列腺癌往往为多发灶,且CT和磁共振成像(MRI)无法检测出前列腺内的全部病灶,因此,前列腺癌难以勾画大体靶区(GTV,转移淋巴结除外),我们只勾画临床靶区(CTV)(图1)。 ·前列腺靶区勾画自前列腺底至前列腺尖的全部前列腺组织(图1),若前列腺存在钙化,须包全全部钙化区域。 ·前列腺尖部以尿道球部上cm或阴茎脚上缘为标志(图2)。 ·精囊腺只需包含紧邻前列腺2~cm的范围(图3)。 ·计划靶区(PTV)为CTV向各方向外放1cm,但向后方向仅外放cm以减少直肠照射(图4)。 ·前列腺和精囊腺的放疗剂量为~81Gy。 3盆腔淋巴引流区靶区勾画 ·对于有多个高危因素、根据Roach公式或Partin表推断盆腔淋巴结转移几率>15%的前列腺癌,建议行盆腔淋巴引流区预防照射。 ·盆腔淋巴引流区从腰5椎体与骶1椎体交界处(L5与S1交接水平)勾画至耻骨联合上缘水平。
百度文库 【前列腺癌放疗】 一、适应症及治疗原则 放射治疗是局限期和局部晚期前列腺癌的根治性治疗手段。早期患者(T1-2N0M0)行根治性放射治疗,其局部控制率和10年无病生存率与前列腺癌根治术相似。局部晚期前列腺癌(T3-4N0M0)治疗原则以放疗和内分泌治疗为主。转移性癌可行姑息性放疗,以减轻症状、改善生活质量。 近年来,三维适形放疗和调强适形放疗成为前列腺癌的主要治疗方式,在此基础上,CT 引导的螺旋断层放疗不但克服了摆位误差,而且减少了正常组织的受照剂量,从而提高可以治疗剂量,达到更好的疗效,逐渐被广泛地应用于临床。可以说,如TOMO精确放疗的先进放疗技术已使早、中、晚期前列腺癌全部摆脱了无可奈何的境地。 二、放射治疗 (一)前列腺癌根治性放疗 1、定位 患者在定位1小时前饮1000ml水+泛影葡胺20ml,定位前排空直肠。仰卧于腹部平架上,双手上举抱肘置额前,用热塑成型体膜固定下腹部。利用激光灯标记定位中心,在体膜上描记3个“十”字,然后用把3个不透光铅点贴在3个“十”字的中心。 进行模拟CT扫描,扫描范围为真骨盆上下5cm,层间距5mm。 激光灯对准腹部平架上刻度为15的位置,保持患者不动,拿下体膜。在患者体表用皮肤墨水描记激光灯所示的体侧的两个“十”字和体表的前正中线。 将定位CT图像传输到计划系统工作站,登记确认。 2、治疗计划设计 (1)靶区勾画 A、CTV:CTV包括整个前列腺及其包膜。中危或高危患者,CTV还需包括精囊。对于淋
巴结转移可能性>15%,或者T2c-T4期并且Gleason评分≥6的局限期前列腺癌患者,CTV可以考虑包括盆腔淋巴引流区 B、PTV:前列腺和精囊:CTV外放,后方为5mm,其他方向为10mm。盆腔淋巴引流区:CTV外放,头脚方向为10mm,前后左右为7—10mm。 (2)剂量学要求 A、常规剂量 传统的放射治疗根据分期不同,将照射剂量定位T1a期64Gy,T1b-c期66—70Gy,T2-3期70—72Gy。目前认为,无论对于任何分期患者,根治性放疗剂量至少未66—70Gy。 如盆腔淋巴结需行预防性照射,则盆腔野照射45—50Gy,然后缩野至前列腺区(前列腺±精囊腺),补量20—25Gy,总剂量仍为65—70Gy。 但实践证明,常规剂量照射疗效并不理想。 B、高剂量照射 由于前列腺精确放疗技术的不断革新,目前的适形放疗、调强放疗以及螺旋断层放疗(TOMO放射治疗系统)已经可以在减少正常组织的受照剂量同时,最大限度地提高照射剂量。 MD Anderson癌症中心研究了1127例T1-4N0M0患者采取不同剂量放疗的结果,得出中危性肿瘤的照射剂量和生化控制的关系,发现在65—77Gy剂量范围,肿瘤的生化控制与剂量成直线关系。其前瞻性随机试验得出结论,治疗前PSA>10的患者照射78Gy后局控率高于70Gy组。同时,利用超分割5次*33.5Gy治疗前列腺癌的Ⅰ期临床实验研究结果,通过周密的治疗计划,每日对靶区进行校对,超分割治疗前列腺癌是可行的,且急性期及晚期泌尿道和胃肠道副反应可以接受,通过增大剂量达到提高生化控制率并降低复发率有可能实现。 总体而言,前列腺的放疗根治量至少为70Gy;低于此剂量,效果明显下降。对于中危肿瘤,照射剂量升高(至少在80Gy水平)具有显著的生化治疗效果。 3、计划评价,确认及报告签字 医师审核剂量分布和DVH图,确保计划达到临床剂量学要求,并予确认。 4、模拟机校位 把扫描的CT图像与计划打印的治疗中心层CT图像进行比较,保证两者是在同一解剖层面。然后测量治疗中心与体表的距离,与治疗计划所得数据比较,保证误差在1mm以内。 5、治疗(加速器)验证 第一次治疗时根据治疗中心摆位,拍摄0°和90°的治疗中心验证片,与治疗计划打印
Open Access Original Article Published 07/18/2013 DOI: 10.7759/cureus.128 Copyright ? 2013 Smith et al. Distributed under Creative Commons CC-BY 3.0Comparative Review of Consensus-Based Clinical T arget Volume De?nitions for Prostate Radiotherapy Graham Smith, George Rodrigues Corresponding author: George Rodrigues 1. Department of Epidemiology and Biostatistics, W estern University, London ON, Canada, N6A 5C1 2. Department of Oncology, London Health Sciences Centre; Schulich School of Medicine & Dentistry, W estern University, London, Ontario, CA Categories: Radiation Oncology, Epidemiology & Public Health, Urology Keywords: clinical target volume, prostate cancer, contouring, guidelines, radiation therapy, consensus guidelines How to cite this article Smith G, Rodrigues G (2013-07-18 10:50:36 UTC) Comparative Review of Consensus-Based Clinical T arget V olume De?nitions for Prostate Radiotherapy. Cureus 5(7): e128. doi:10.7759/cureus.128 Abstract Background: A major obstacle in the delivery of postoperative radiation therapy (RT) for prostate cancer is accurate delineation of the tumor targets and organs at risk. Although postoperative prostate cancer contouring atlases are quite common, there is still no widely accepted contouring guideline. The purpose of this study is to critically review the various postoperative prostate RT treatment planning consensus guidelines or atlases currently available. Methods: A literature search was conducted using various electronic databases with the key terms: prostate, contour, planning tumour volume, clinical target volume, delineation or de?nition, guidelines or atlas, and radiation oncology. The search was limited to English publications from the years 1985 to 2011. Results: A total of seven publications relating to contouring guidelines for postoperative prostate radiotherapy were identi?ed. There are four distinct consensus guidelines developed by major institutions: Princess Margaret Hospital, the Australian and New Zealand Radiation Oncology Genito-Urinary Group, the European Organization for Research and Treatment of Cancer, and the Radiation Therapy Oncology Group. Conclusions: After reviewing the consensus contouring guidelines for postoperative prostate cancer radiation therapy that were available in the literature, it is clear that there disagreement with regards to what anatomical borders should be used for delineating an appropriate
958?主堡鲨屡之£型苤查!!!i生!!旦筮!!鲞筮!!塑堡!也』堕丛:旦!!!些 塑!!!i:!!!:!!,堕!:!! 前列腺癌局部治疗新进展 黄红星麦智鹏 前列腺癌局部治疗作为非根治性的治疗方式,具有创伤小、并发症少等优点,通常被应用于晚期前列腺癌的姑息性治疗,如放疗后复发性前列腺癌的挽救性治疗。1引。随着 PSA筛查的广泛应用和穿刺技术的不断提高,越来越多低级别、局限性的前列腺癌被发现。避免过度治疗是目前关于此类前列腺癌在治疗上的研究热点。近年来,由于模板定位下的经会阴穿刺和多参数MRI的发展,准确定位前列腺癌灶和评估肿瘤的恶性程度成为可能。3“。另外,关于前列腺癌病理多灶性和主要肿瘤概念的提出,为前列腺特定癌灶的局部消除提供理论的可行性’6J。对于部分早期前列腺癌,不少研究初步表明了局部治疗在疗效和并发症上都有满意的结果L『”J。因此,局部治疗在前列腺癌的治疗领域有了新的定位和应用。 一、前列腺癌局部治疗的适应证及治疗范围 前列腺癌的根治性治疗手段,如根治性前列腺切除术或前列腺癌根治性放疗,是前列腺癌标准的治疗方式。然而, 这些治疗手段导致的并发症(如尿失禁、勃起功能障碍和直肠瘘等却严重影响患者的生活质量。另外,对于选择主动监测的低危前列腺癌患者,有研究发现其中很大一部分都因肿瘤的恶性程度被低估或肿瘤进展而最终选择根治性治疗方式。在这些接受根治性前列腺切除术患者的大体病理标本中,大部分都会发现有临床意义的肿瘤。1…。主动监测仅适用于部分低危前列腺癌患者。虽然前列腺癌局部治疗目前处于研究阶段,但初步结果表明局部治疗既可兼顾控瘤效果又能有效减少并发症07’9J。因此,不少学者认为局部治疗可应用于低、中危的前列腺癌患者。1“。对于其治疗适应证, 目前的专家共识是:预期寿命≥10年,PSA<,15ng/ml,临床 T分期≤T2。,穿刺Gleason评分≤3+4分且穿刺或影像学检查无肿瘤包膜外或精囊腺侵犯¨…。
前列腺癌的内外放射治疗 上海市东方医院 同济大学附属东方医院 放疗科 秦庆亮 前列腺癌发病率 黑人最高,(150/10万男性),白人其次,黄种人最低(1/10万男性)。 在过去10年中,CaP在亚洲国家和地区的发病率明显提高,分别增加1.34-4.7倍。我国则增高了2.3倍。 在亚洲国家中日本最高(18.1/10万),韩国最低(3.87/10万),我国北京市的发病率为 4.55/10万,但亚洲国家整体发病水平仍明显低于欧美国家。 目前CaP的发病率在我国男性肿瘤中具第11位,死亡率居第16位。 治疗——密切随访观察 适用于A1期低危患者,定期复查血PSA水平及相应的影象学检查,以确定患者病变是否有进展。 治疗——手术治疗 包括根治性手术和姑息性手术。 对晚期肿瘤患者为解除其膀胱颈部梗阻可行姑息性的经尿道电切除术,目的仅在于缓解梗阻症状。 对临床分期为A2期、B期的患者可行根治性前列腺切除术。 根治手术一般限于预期寿命>10年的患者。 放射治疗的优越性 ?放疗是目前肿瘤治疗(手术,放疗,化疗)主要手段之一 ?技术方法可靠,疗效肯定 ?放射治疗可保留病人的器官生理功能 ?适用广,可治疗各部位的肿瘤 ?年龄大/体质差/多次手术者,均可接受放疗 ?治疗副作用相对少,不一定需住院 ?三维立体放射技术可最大程度杀伤肿瘤,且使肿瘤邻近正常组织的放射损伤最小化放射治疗(RADIOTHERAPY)分类: 远距离体外放射治疗(TELETHERAPY) 低能射线,如X线kv级(低LET射线); 高能X线, ?电子线, 以及60Co-γ线; 重粒子如快中子(Neutron),质子(Proton), 氦核,中微子,碳离子,α粒子(高LET射线) 近距离体内放射治疗(BRACHYTHERAPY) 组织间插植(Interstitial); 腔內照射(Intra-cavitary); 术中放射治疗(Intra-operative); 放射性粒子植入(如125-I inserted); 放射源体表敷贴模(Mould); 靶向治疗(Targeted) 体外放射治疗采用的照射技术
前列腺癌根治性放疗靶区建议 中国医科院肿瘤医院放疗科 刘跃平 李晔雄 王维虎 房辉 随着人均寿命的延长,我国老年人口不断增加,威胁着老年男性健康的前列腺癌发病率逐年上升。放射治疗是前列腺癌的重要治疗手段,放疗从局限低中高危的前列腺癌到盆腔淋巴结转移或远处转移的前列腺癌都能发挥积极作用。对于局限期前列腺癌,放射治疗可取得与手术相当的疗效但治疗并发症却比根治性前列腺切除术更低,近年来随着放射治疗技术的不断进步,三维适形放疗、调强放射治疗、立体定向放疗、以及影像引导放疗等新技术的出现和发展,使前列腺癌靶区放疗越来越准确,而正常组织的保护则更为可靠,因而接受放射治疗的病例越来越多,为了能使前列腺癌放疗靶区规范和合理,我们参照了美国放射肿瘤协会(RTOG)关于前列腺癌放疗靶区勾画建议、美国国家癌症综合治疗指南(NCCN)、欧洲泌尿协会前列腺癌诊治指南、并结合我们的临床实践,对局限期前列腺癌根治性放疗的靶区勾画提出参考性建议。依据危险因素分组的局限期前列腺癌放疗及内分泌治疗建议以及放疗靶区建议见表1。 表1:依据危险因素分组的局限期前列腺癌放疗及内分泌治疗建议以及放疗靶区建议 危险分组 低危组 中危组 高危组 危险评价指标 T1–T2a PSA <10 ng/mL GS <7 T2b–T2c PSA 10–20 ng/mL GS 7 T3–T4 PSA >20 ng/mL GS 8–10 放疗及内分泌 治疗建议 3DCRT/IMRT=75.6‐79.2Gy 3DCRT/IMRT = 76‐81 Gy +新辅助及辅助内分 泌治疗4‐6个月 3DCRT/IMRT≧81 Gy +新辅助及辅助内 分泌治疗2‐3年 放疗靶区建议 前列腺 前列腺+ 2‐2.5 cm SV 前列腺 + 2‐2.5 cm SV + 盆腔淋巴引流区 (LNM >15%) 缩写:PSA:前列腺特异性抗原;GS:(Gleason score)格里森评分;3DCRT:三维适形放疗;IMRT:调强适形放疗;Gy:戈瑞,放疗剂量单位;SV:(seminal vesicle)精囊腺;LNM:淋巴结转移。 从上表可以得知,前列腺癌靶区勾画主要包括前列腺、精囊腺、及盆腔淋巴引流区,对局限期前列腺癌根治性放疗靶区确定我们提出如下建议: 1. CT定位及放疗建议: 1.1 定位前1小时排空膀胱和直肠,口服1000ml稀释的肠道对比剂,然后憋尿充盈膀胱。
前列腺癌肿瘤标志物的研究现状 【摘要】前列腺癌是西方国家的多发病,在我国亦成上升趋势,如何更早、更准确的发现和诊断前列腺癌,对该病的治疗和患者的预后显得十分重要。 【Abstract】Prostate cancer whose morbidity is uptrend in our country,is a frequently-occurring disease in western world.It’s becoming significant for patients’treatment and prognosis to diagnose the disease earlier and more precisely. 【Keywords】prostate cancer,tumor marker,PSME 前列腺癌(Prostate Cancer)是欧美男性中最常见的恶性肿瘤,其死亡率已超过肺癌,成为发达国家男性第一致死率恶性肿瘤。在我国,前列腺癌诊出率呈升高趋势。因此,前列腺癌的早期诊断显得尤为重要,现就前列腺癌肿瘤标志物研究进展叙述如下。 1 前列腺癌特异性膜抗原前列腺特异性膜抗原(prostate-specific membrane antigen,PSMA)是存在于前列腺细胞膜的一种多功能的Ⅱ型跨膜蛋白,由750个氨基酸残基组成。编码PSMA的蛋白质具有叶酸水解酶和N-乙酰基α-连接二肽酶两种活性,与其生物学性质有关。研究发现,PSMA具有较高的前列腺组织特异性,在区分前列腺癌和其他类型恶性肿瘤的敏感度和特异性分别是65.9%和94.5%,因此PSMA仍然是前列腺癌细胞上一个相当敏感的、高度特异性的抗原物质。唐庆来等[1]在进行了PSMA与PSA在不同分期前列腺癌组织中的表达差异性研究后发现,PSMA在前列腺组织良、恶性鉴别中优于PSA,且临床分期越晚,其表达越强,与肿瘤恶性程度成正相关。因此PSMA是较PSA更具特异性的前列腺癌瘤标志物,可作为前列腺癌预后评估的重要指标。 2 前列腺特异性膜抗原剪切变异体 可变剪接是通过对外显子、内含子选择性的切除和保留,使剪接后的转录体发生变化,从而改变原基因的结构和功能,进而编码不同功能的蛋白质。PSME 便是PSMA可变剪切后的一种变异体。此外,PSMA还有PSM’、PSMC、PSMD 三种变异体。目前对这四种剪切变异体的研究还停留在组织表达鉴定水平。研究发现,PSM’、PSM-C和PSM-D均位于细胞浆内,缺少蛋白质的跨膜区,属非跨膜蛋白,缺乏PSMA原有生物学功能及诊断和治疗前列腺癌时的靶细胞定位作用。而PSME为一种跨膜蛋白,是通过RT-PCR从前列腺癌组织中获得。相关研究发现,PSM-E比PSMA具有更高的前列腺组织特异性,且高表达于前列腺癌组织,并与前列腺癌恶性程度呈正相关,随癌肿Gleason评分的增高而表达增加,比PSMA具有更高的肿瘤特异性。随着对PSME生物特性认识的加深,PSME 有望成为诊断和治疗前列腺癌新的细胞靶抗原。 3 早期前列腺特异性抗原(EPCA及EPCA-2)
前列腺癌根治性放疗靶区建议 作者:中国医学科学院肿瘤医院放疗科刘跃平李晔雄王维虎房辉来源:中国医学论坛报日期: 2012-03-30 此文章来源于https://www.doczj.com/doc/7516172766.html, 随着人均寿命的延长,我国老年人口的不断增加,前列腺癌的发病率逐年上升。放疗是前列腺癌根治性治疗手段之一,从局限低、中、高危前列腺癌到盆腔淋巴结转移,甚至远处转移前列腺癌,放疗均有广泛的应用。对于局限期前列腺癌,放疗可取得与手术相当的疗效且并发症的发生较少。 近年来,随着各种放疗新技术的出现和发展,前列腺癌的放疗越来越准确,正常组织的保护则更可靠,因此,接受放疗的患者越来越多。我们参照美国放疗肿瘤学研究组(RTOG)关于前列腺癌的放疗靶区勾画建议、美国国立综合癌症网络(NCCN)和欧洲泌尿协会制定的前列腺癌诊治指南,并结合我们的临床实践,对局限期前列腺癌根治性放疗的靶区勾画提出参考性建议,旨在使前列腺癌放疗靶区定义规范化和合理化。 从表1得知,前列腺癌靶区勾画主要包括前列腺、精囊腺及盆腔淋巴引流区,对局限期前列腺癌根治性放疗的靶区确定,我们提出如下建议。
1CT定位及放疗 ·定位前时排空膀胱和直肠,口服1000 ml稀释的肠道对比剂,然后憋尿充盈膀胱。CT定位采取仰卧位,体模固定,层厚3 mm扫描,扫描范围从腰4椎体下缘至坐骨结节下3 cm。 ·建议采用3D-CRT或IMRT,若放疗剂量≥78 Gy,建议使用图像引导放疗(IGRT)。 2前列腺及精囊腺靶区勾画 ·局限低危前列腺癌放疗靶区只包括前列腺;局限中危前列腺癌或盆腔淋巴结转移几率≤15%的局限高危前列腺癌放疗靶区包括前列腺和精囊腺。 ·前列腺癌往往为多发灶,且CT和磁共振成像(MRI)无法检测出前列腺内的全部病灶,因此,前列腺癌难以勾画大体靶区(GTV,转移淋巴结除外),我们只勾画临床靶区(CTV)(图1)。 ·前列腺靶区勾画自前列腺底至前列腺尖的全部前列腺组织(图1),若前列腺存在钙化,须包全全部钙化区域。 ·前列腺尖部以尿道球部上0.5 cm或阴茎脚上缘为标志(图2)。 ·精囊腺只需包含紧邻前列腺2~2.5 cm的范围(图3)。 ·计划靶区(PTV)为CTV向各方向外放1 cm,但向后方向仅外放0.5 cm以减少直肠照射(图4)。 ·前列腺和精囊腺的放疗剂量为75.6~81 Gy。
前列腺癌根治性放疗规 目前在前列腺癌根治性放疗靶区勾画上欧美国家已基本形成共识,参照美国放疗肿瘤学研究组(RTOG)关于前列腺癌的放疗靶区勾画建议、美国国立综合癌症网络(NCCN)和欧洲泌尿协会制定的前列腺癌诊治指南,并结合我们的临床实践,对局限期前列腺癌根治性放疗的靶区勾画提出规化建议。 1、体位固定及CT定位:定位前4小时可口服4% 1000 ml稀释的肠道对比剂,定位前排空直肠,憋尿充盈膀胱。CT定位采取仰卧位,体模固定,层厚3 mm扫描,扫描围从腰4椎体下缘至坐骨结节下3 cm。 2、前列腺及精囊腺靶区勾画 (1)局限低危前列腺癌放疗靶区只包括前列腺;局限中危前列腺癌或盆腔淋巴结转移几率 ≤15%的局限高危前列腺癌放疗靶区包括前列腺和精囊腺。 (2)前列腺癌往往为多发灶,且CT和磁共振成像(MRI)无法检测出前列腺的全部病灶,因此,前列腺癌难以勾画肿瘤靶区(GTV,转移淋巴结除外),只勾画临床靶区(CTV)(图1)。(3)前列腺靶区勾画自前列腺底至前列腺尖的全部前列腺组织(图1),若前列腺存在钙化,须包全全部钙化区域。 (4)前列腺尖部以尿道球部上0.5 cm或阴茎脚上缘为标志(图2)。
(5)精囊腺只需包含紧邻前列腺2~2.5 cm的围(图3)。 (6)计划靶区(PTV)为CTV向各方向外放1 cm,但向后方向仅外放0.5—0.6 cm以减少直肠照射(图4)。 (7)前列腺及精囊腺靶区的放疗剂量为75.6-81 Gy。 3、盆腔淋巴引流区靶区勾画 (1)对于有多个高危因素、根据Roach公式或Partin表推断盆腔淋巴结转移几率>15%的前列腺癌,建议行盆腔淋巴引流区预防照射。 盆腔淋巴结转移几率评估方法: Pisansky等: T分期与盆腔淋巴结转移关系:T2a(3.3%),T2b(10.8%),T3(25%)。Roach公式:Node(+)=[2/3PSA+(Gleason-6)]% >15%有较大盆腔淋巴结转移危险;>30%有很大盆腔淋巴结转移危险。 前列腺癌盆腔淋巴结转移可能性估计(Partin表):
龙源期刊网 https://www.doczj.com/doc/7516172766.html, 前列腺癌治疗研究进展 作者:郭文 来源:《上海医药》2011年第01期 中图分类号:R983 文献标识码:A 文章编号:1006-1533(2011)01-0023-02 前列腺癌在男性的致死性癌症中居第二位。由于前列腺癌的绝对发病率会随着年龄的增大呈线性增加,老年人患病的几率非常大。近年来,社会老龄化现象又在日趋严重,因此,庞大且持续增长的患者群使得前列腺癌治疗领域颇具开发潜力。尽管有着如此巨大的市场需求,但由于前列腺是一个非常特殊的人体组织,常规的抗癌化疗药物很难渗入其内部并发挥疗效,这对治疗造成了极大的困难,也导致到目前为止,有效的治疗药物寥寥无几。因此,如何开发有效的治疗药物刻不容缓。近来,美国丹德里昂公司(Dendreon)获批的前列腺癌疫苗Provenge和美国安进公司(Amgen)的单克隆抗体Prolia由于独具特色的治疗优势从而成为倍受瞩目的焦点,给前列腺癌治疗带来新的希望和曙光。 1流行病学 如今,前列腺癌已快速上升为全球性的疾病。尽管该疾病的发病率曾经仅在欧美发达国家较高、在亚洲和拉丁美洲等发展中国家较低,但随着亚洲及拉美国家社会经济的飞速发展、人民生活水平的不断提高以及饮食结构的逐渐欧化,使得这些国家前列腺癌的发病率在过去几年里亦在急剧增高。 据世界卫生组织公布的最新统计资料,仅中国、印度和日本这三个远东主要经济大国,每年新增的前列腺癌患者总数就有数百万之众,再加上欧美和拉丁美洲的前列腺癌患者,估计全球前列腺癌患者总数将超过1000万人。另据美国国家癌症研究所(National Cancer Institute)的 统计数据显示,2009年在美国新诊断出罹患前列腺癌的患者约为19.2万例,且其中约2.7万患者因该疾病而死亡。 前列腺癌有效治疗药物较少,这是因为:治疗前列腺癌主要考虑患者的年龄以及健康状态和疾病恶化率。生长缓慢的肿瘤可以通过持续观察,早期的肿瘤可以通过根治性前列腺切除术