高一化学化学反应的限度
- 格式:pdf
- 大小:1.27 MB
- 文档页数:9

化学反应的速率与限度逐字稿
化学反应的速率和限度是化学反应中非常重要的两个概念。
化学反应速率是指化学反应进行的快慢程度,通常用单位时间内反应物或生成物浓度的变化来表示。
影响化学反应速率的因素有很多,其中最主要的因素是反应物的浓度、温度、催化剂等。
在其他条件不变的情况下,增加反应物的浓度、升高温度、使用催化剂等都可以加快化学反应的速率。
化学反应的限度是指化学反应在一定条件下所能达到的最大程度,也就是反应物和生成物之间的平衡状态。
当反应达到限度时,正反应速率和逆反应速率相等,反应物和生成物的浓度不再发生变化。
化学反应的限度可以通过平衡常数来表示,平衡常数越大,反应越容易进行,达到平衡时生成物的浓度也就越大。
在实际应用中,我们经常需要控制化学反应的速率和限度。
例如,在工业生产中,为了提高生产效率,需要加快化学反应的速率;而在环境保护中,为了减少污染物的排放,需要控制化学反应的限度。
因此,了解化学反应的速率和限度对于我们理解和应用化学反应具有非常重要的意义。
以上就是我为你提供的关于化学反应的速率与限度的逐字稿,希望对你有所帮助!如果你还有其他问题或需要进一步的解释,请随时向我提问。

化学高一知识点归纳必修一1.化学高一知识点归纳必修一篇一化学反应的限度——化学平衡(1)化学平衡状态的特征:逆、动、等、定、变。
①逆:化学平衡研究的对象是可逆反应。
②动:动态平衡,达到平衡状态时,正逆反应仍在不断进行。
③等:达到平衡状态时,正方应速率和逆反应速率相等,但不等于0。
即v 正=v逆≠0。
④定:达到平衡状态时,各组分的浓度保持不变,各组成成分的含量保持一定。
⑤变:当条件变化时,原平衡被破坏,在新的条件下会重新建立新的平衡。
(2)判断化学平衡状态的标志:①VA(正方向)=VA(逆方向)或nA(消耗)=nA(生成)(不同方向同一物质比较)②各组分浓度保持不变或百分含量不变③借助颜色不变判断(有一种物质是有颜色的)④总物质的量或总体积或总压强或平均相对分子质量不变(前提:反应前后气体的总物质的量不相等的反应适用,即如对于反应xA+yBzC,x+y≠z)2.化学高一知识点归纳必修一篇二化学能与热能1、在任何的化学反应中总伴有能量的变化。
原因:当物质发生化学反应时,断开反应物中的化学键要吸收能量,而形成生成物中的化学键要放出能量。
化学键的断裂和形成是化学反应中能量变化的主要原因。
一个确定的化学反应在发生过程中是吸收能量还是放出能量,取决于反应物的总能量与生成物的总能量的相对大小。
E反应物总能量>E生成物总能量,为放热反应。
E反应物总能量2、常见的.放热反应和吸热反应常见的放热反应:①所有的燃烧与缓慢氧化。
②酸碱中和反应。
③金属与酸反应制取氢气。
④大多数化合反应(特殊:是吸热反应)。
常见的吸热反应:①以C、H2、CO为还原剂的氧化还原反应如:②铵盐和碱的反应如Ba(OH)2·8H2O+NH4Cl=BaCl2+2NH3↑+10H2O③大多数分解反应如KClO3、KMnO4、CaCO3的分解等。
3.化学高一知识点归纳必修一篇三物质的量的单位――摩尔1.物质的量(n)是表示含有一定数目粒子的集体的物理量。


高中化学反应的限度教案教学目标:1. 了解化学反应的限度概念和计算方法;2. 理解化学反应中限度反应物和多余反应物的概念;3. 掌握化学反应的平衡态和反应物的转化率计算方法。
导入:通过实验演示或图像展示引出化学反应的限度概念,并引发学生对限度反应物和多余反应物的讨论。
教学内容:1. 化学反应中的限度:- 定义:限度反应物是一个反应物中最先用完的反应物;多余反应物是在反应结束后仍有剩余的反应物。
- 计算方法:通过反应方程式和物质的量之间的关系,确定反应物的数量比较。
2. 化学反应的平衡态:- 定义:当反应物和生成物的浓度达到一定比例时,反应达到平衡态。
- 反应物的转化率:反应物的转化率表示反应物被转化为生成物的比例。
- 计算方法:通过实验数据或平衡式中的系数,计算反应物的转化率。
实例练习:1. 对于反应式2H2 + O2 -> 2H2O,如果有3mol H2和2mol O2参与反应,求限度反应物和多余反应物。
2. 对于反应式N2 + 3H2 -> 2NH3,如果有4mol N2和8mol H2参与反应,求反应的平衡态下N2的转化率。
实践应用:让学生通过实验或模拟实验,验证化学反应的限度概念,并计算反应物的转化率。
检测评价:布置相关练习题,检测学生对化学反应限度概念和计算方法的掌握程度。
拓展延伸:引导学生思考在实际生活和工业生产中化学反应的限度如何影响反应过程和产物得率。
课堂总结:总结化学反应的限度概念和计算方法,强化学生对本节课内容的理解和记忆。
教学反思:根据学生反馈和实际教学效果,及时调整教学内容和方法,以提高学生的学习效果和兴趣。

高中化学反应限度的教案
年级:高中
主题:反应限度
教学目标:
1. 理解化学反应中的限度概念。
2. 掌握如何计算反应的限度。
3. 能够根据反应的限度计算出产物的产生量。
4. 掌握化学反应中的相关计算技巧。
教学准备:
1. PowerPoint或其他教学工具。
2. 化学实验材料。
3. 计算工具。
教学活动:
1. 导入:通过引用日常生活中的化学反应例子,引起学生对反应限度的兴趣和认识。
2. 知识讲解:讲解反应限度的概念和计算方法,介绍相关的基本概念和公式。
3. 案例分析:给学生几个实际反应的例子,让他们根据反应物的量和限度来计算产量。
4. 实验操作:进行一个简单的化学实验,让学生亲自操作并根据实验结果计算反应的限度和产量。
5. 讨论总结:让学生分享实验结果和计算过程,进行讨论和总结,帮助他们进一步理解和巩固所学知识。
评估方法:
1. 口头提问:随堂随机提问学生相关知识点。
2. 实验报告:要求学生完成实验报告,包括实验目的、方法、结果和讨论。
3. 小测验:进行一次简单的考试,检测学生对反应限度的掌握程度。
教学延伸:
1. 拓展知识:介绍更复杂的反应限度计算方法,并让学生进行更多实验。
2. 实践应用:邀请专业化学家或工程师来分享他们在实际工作中如何应用反应限度概念。
3. 研究课题:让学生自选一个关于反应限度的研究课题进行探究,展示成果并进行讨论。

高中化学反应限度教案
学科:化学
年级:高中
课时:1
教学目标:
1.了解化学反应中限度的概念和意义。
2.掌握如何通过反应物的量来计算产物的生成量。
3.能够应用限度概念解决化学反应实际问题。
教学内容:
1.化学反应限度的定义和计算方法。
2.如何根据反应物的量来计算产物的生成量。
3.限度在化学反应中的应用。
教学重点:
1.化学反应中限度的概念和计算方法。
2.限度概念在化学反应中的应用。
教学难点:
1.掌握如何根据反应物的量来计算产物的生成量。
2.能够独立解决化学反应限度的实际问题。
教学过程:
一、导入(5分钟)
教师通过化学反应中的实例引入化学反应限度的概念,启发学生思考。
二、讲解(15分钟)
1.讲解化学反应中限度的定义和计算方法。
2.介绍如何根据反应物的量来计算产物的生成量。
三、示例演练(15分钟)
教师通过示例演练,让学生掌握计算方法。
四、操练(15分钟)
学生在教师指导下进行练习,巩固所学知识。
五、拓展(5分钟)
教师引导学生探讨限度概念在其他化学反应中的应用。
六、总结(5分钟)
教师总结课堂内容,强调重点和难点。
七、作业布置(5分钟)
教师布置相关练习题目作为课后作业,巩固所学知识。
教学反思:
通过本节课的教学,学生对化学反应限度的概念有了清晰的了解,掌握了相关计算方法,能够应用于实际问题中。
在未来的教学中,可以通过更多的练习和案例,帮助学生更好地掌握和应用化学反应限度的知识。

高一年级化学必修2化学反应的速率和限度知识点化学是一门以实验为基础的自然科学。
小编准备了高一年级化学必修2化学反响的速率和限度知识点,希望你喜欢。
一、化学反响的速率和限度1、化学反响的速率(1)概念:化学反响速率通常用单位时间内反响物浓度的减少量或生成物浓度的增加量(均取正值)来表示。
谋略公式:v(B)= =①单位:mol/(L?s)或mol/(L?min)②B为溶液或气体,若B为固体或纯液体不谋略速率。
③重要纪律:速率比=方程式系数比(2)影响化学反响速率的因素:内因:由到场反响的物质的结协商性质决定的(主要因素)。
外因:①温度:升高温度,增大速率②催化剂:一般加快反响速率(正催化剂)③浓度:增加C反响物的浓度,增大速率(溶液或气体才有浓度可言)④压强:增大压强,增大速率(适用于有气体到场的反响)⑤别的因素:如光(射线)、固体的表面积(颗粒巨细)、反响物的状态(溶剂)、原电池等也会改变化学反响速率。
2、化学反响的限度--化学均衡(1)化学均衡状态的特性:逆、动、等、定、变。
①逆:化学均衡研究的工具是可逆反响。
②动:动态均衡,抵达均衡状态时,正逆反响仍在不断举行。
③等:抵达均衡状态时,正方应速率和逆反响速率相等,但不即是0。
即v正=v逆0。
④定:抵达均衡状态时,各组分的浓度保持不变,各组成成分的含量保持一定。
⑤变:当条件变化时,原均衡被毁坏,在新的条件下会重新建立新的均衡。
(3)鉴别化学均衡状态的标志:① VA(正偏向)=VA(逆偏向)或nA(消耗)=nA(生成)(不同偏向联合物质比较)②各组分浓度保持不变或百分含量不变③借助颜色不变鉴别(有一种物质是有颜色的)④总物质的量或总体积或总压强或均匀相对分子质量不变(条件:反响前后气体的总物质的量不相等的反响适用,即如敷衍反响xA+yB zC,x+yz )高一年级化学必修2化学反响的速率和限度知识点就为大众先容到这里,希望对你有所帮助。
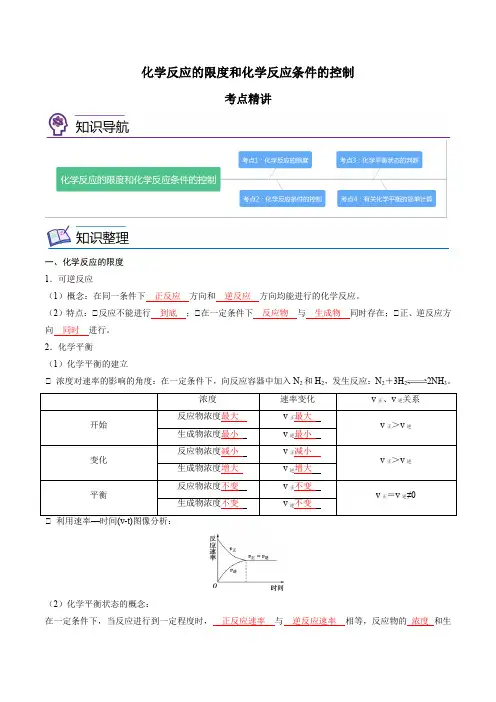
化学反应的限度和化学反应条件的控制考点精讲一、化学反应的限度1.可逆反应(1)概念:在同一条件下正反应方向和逆反应方向均能进行的化学反应。
(2)特点:①反应不能进行到底;①在一定条件下反应物与生成物同时存在;①正、逆反应方向同时进行。
2.化学平衡(1)化学平衡的建立① 浓度对速率的影响的角度:在一定条件下,向反应容器中加入N2和H2,发生反应:N2+3H22NH3。
浓度速率变化v、v关系(2)化学平衡状态的概念:在一定条件下,当反应进行到一定程度时,正反应速率与逆反应速率相等,反应物的浓度和生成物的 浓度 都不再改变,达到一种表面静止的状态,称之为 化学平衡 状态。
(3)化学反应的限度是指可逆反应在一定条件下所能达到或完成的 最大 程度,即该反应进行的限度。
化学反应的限度决定了反应物在该条件下转化为生成物的最大 转化率 。
(4)转化率=n (已被转化的反应物)n (初始反应物)×100%。
(5)影响因素:改变反应条件,可以在一定程度上改变该反应的化学 平衡 状态。
3.化学反应的限度(1)化学平衡状态是可逆反应达到的一种特殊状态,是在给定条件下化学反应所能达到的或完成的最大程度,任何可逆反应在给定条件下的进程都有一定的限度。
(2)不同条件下,同一可逆反应的化学反应限度不同;相同条件下,不同反应的化学反应限度也不同。
(3)化学反应的限度决定了反应物在该条件下转化为生成物的最大转化率。
二、化学反应条件的控制 1.化学反应条件的控制(1)目的:促进 有利 的化学反应,抑制 有害 的化学反应。
(2)基本措施①改变化学反应速率:改变反应体系的 温度 、物质的 浓度 、气体的 压强 、固体的 表面积 以及催化剂的合理使用等。
①改变可逆反应进行的限度:改变 可逆反应 体系的温度、物质的浓度、气体的压强等。
(3)考虑因素:控制反应条件的成本和实际可能性。
2.提高煤的燃烧效率(1)煤燃烧时,将煤块粉碎成煤粉目的是增大与空气中O 2的 接触面积 ,煤粉燃烧 更充分 ,反应速率快;通入适当过量的空气可以使煤粉充分燃烧,生成CO 2,放出更多的热量;若空气不足,会造成煤燃烧不完全,生成CO ,产生热量减少,且会造成污染。



6.1.3化学反应速率与反应限度(第3课时)一、教学目标1.了解可逆反应及特点。
2.理解化学平衡状态的特征及标志,会判断可逆反应的平衡状态。
3.了解控制反应条件在生产、生活和科学研究中的作用。
二、教学重点及难点重点化学平衡状态的特征及标志难点可逆反应的平衡状态的判断三、教学方法问题解决法、讨论法、讲授法四、教学工具PPT五、教学过程【导入】思考:氯水的成分有哪些?【投影】氯水图片,氯水呈浅黄绿色【生】三分四离三分子:H2O、Cl2、HClO四离子:H+、Cl-、ClO-、OH-【问】还有氯气,说明什么?【生】说明Cl2没有完全反应完。
【讲述】说明溶解的Cl2只有一部分与水发生了化学反应,反应只能进行到一定的限度。
所以氯气与水的反应方程式用“⇌”,而不是“=”。
Cl2+H2O ⇌ HCl+HClO二、化学反应限度【讲述】化学反应限度是在给定的条件下,化学反应所能达到或完成的最大程度,即该反应的限度。
要点1:给定的条件——条件改变,化学反应的限度是可能被可改变的;同一可逆反应在不同条件(如温度、浓度、压强等)下,其反应的限度不同。
【投影】播放二氧化氮和四氧化二氮的转化在冰水和热水中的反应视频要点2:化学反应所能达到或完成的最大程度——决定了反应物在该条件下的最大转化率。
【讲述】可逆反应(1)定义:在同一条件下,既能向正反应方向进行,还能向逆反应方向进行的化学反应。
书写可逆反应的化学方程式时,不用“=”,用“⇌”。
(2)特征⇌双向性:反应物正向反应逆向反应生成物。
⇌双同性:正、逆反应是在同一条件下同时进行的。
⇌共存性:反应物和生成物同时存在。
即:反应物不能完全转化为生成物。
一、实验探究:FeCl3溶液与KI溶液的反应1、操作:实验现象:溶液颜色由无色变为褐色。
实验结论:有I2生成。
2、操作:实验现象:溶液分层,下层为浅绿色,上层油状液体呈紫色。
实验结论:有Fe2+和I2生成。
3、操作:实验现象:溶液变为血红色实验结论:下层清液中含有未反应的Fe3+【讲述】说明即使碘化钾过量,反应后的溶液中仍存在铁离子,只有一部分铁离子与碘化钾发生了化学反应,反应只能进行到一定的限度。
第3课时 化学反应的限度 化学平衡状态课程标准课标解读1.通过实验认识化学反应的限度、可逆反应和化学平衡的含义。
2.了解化学平衡的建立和特征,掌握化学平衡状态的判断方法。
3.了解化学平衡在生产和科学研究中的作用。
1.了解可逆反应的含义,知道可逆反应在一定条件下能达到化学平衡状态。
(宏观辨识与微观探析)2.能用一定的理论模型理解正、逆反应速率相等指反应达到化学平衡状态,通过分析推理认识化学平衡的特征。
(证据推理与模型认知)3.对于可逆反应,理解正、逆反应速率相等和组分含量一定是判断化学反应的平衡状态的依据,会根据压强、密度、相对分子质量等间接因素判断化学反应的平衡状态。
(变化观念与平衡思想)知识点01 可逆反应和化学反应的限度1.可逆反应(1)概念:在同一条件下,既能向正反应方向又能向逆反应方向进行的化学反应。
(2)特征:在一定条件下,可逆反应有以下特征: ①正反应和逆反应同时进行。
②反应物和生成物同时存在。
③反应没有完全进行到底。
(3)表示:在可逆反应的化学方程式中,用“”号代替“===”号。
2.化学反应的限度根据可逆反应的特征,可知可逆反应有一定的限度。
(1)说明Cl 2和H 2O 的反应是可逆反应的证据是:氯水既含有Cl 2、H 2O 、HClO 分子,也含有H +、Cl -、ClO -等离子。
化学方程式为Cl 2+H 2OHCl+HClO 。
目标导航知识精讲(2)化学反应限度的实验探究少量FeCl3溶液和过量KI溶液反应,从反应后的溶液中分离出I2的实验操作是向反应后的溶液中加入苯,振荡、静置,实验现象是溶液分为两层,上层为紫红色。
检验反应后的溶液中仍然存在Fe3+的操作和现象是取下层液体,滴加KSCN溶液,溶液变为红色。
【即学即练1】下列关于可逆反应的说法正确的是()A.正反应和逆反应在相同条件下同时进行B.氯化铵分解和氨气与氯化氢反应生成氯化铵属于可逆反应C.可逆反应达到一定限度后,反应就停止了D.同一可逆反应的正反应进行的程度一定大于逆反应的进行程度答案:A解析:正逆反应是在相同条件下同时进行的,A正确;氯化铵分解和氨气与氯化氢反应生成氯化铵是在不同条件下进行的,不是可逆反应,B错误;可逆反应达到一定限度后,反应没有停止,正反应速率和逆反应速率相等,C错误;同一可逆反应中,正反应进行的程度与逆反应进行的程度与反应物的性质有关,有的可逆反应正反应进行的程度大,有的可逆反应逆反应进行的程度大,D错误。