2017届高考化学二轮复习 第一篇 专题三 元素及其化合物 .
- 格式:ppt
- 大小:966.50 KB
- 文档页数:30

2017年高考化学二轮复习专题能力提升练十二第一篇专题通关攻略专题三元素及其化合物3 常见有机物及其应用编辑整理:尊敬的读者朋友们:这里是精品文档编辑中心,本文档内容是由我和我的同事精心编辑整理后发布的,发布之前我们对文中内容进行仔细校对,但是难免会有疏漏的地方,但是任然希望(2017年高考化学二轮复习专题能力提升练十二第一篇专题通关攻略专题三元素及其化合物3 常见有机物及其应用)的内容能够给您的工作和学习带来便利。
同时也真诚的希望收到您的建议和反馈,这将是我们进步的源泉,前进的动力。
本文可编辑可修改,如果觉得对您有帮助请收藏以便随时查阅,最后祝您生活愉快业绩进步,以下为2017年高考化学二轮复习专题能力提升练十二第一篇专题通关攻略专题三元素及其化合物3 常见有机物及其应用的全部内容。
专题能力提升练十二常见有机物及其应用(建议用时:20分钟)1.(2016·石家庄二模)下列关于有机物说法正确的是()A。
米酒变酸的过程涉及了氧化反应B。
汽油、柴油、植物油都是碳氢化合物C.含5个碳原子的有机物分子中最多可形成4个碳碳单键D。
蛋白质的水解和油脂的皂化都是由高分子生成小分子的过程【解析】选A.米酒的主要成分是乙醇,变为乙酸的过程是被氧化的过程,A项正确;汽油、柴油都是碳氢化合物,但植物油是碳氢氧化合物,B项错误;当五个碳原子形成环状时最多可形成5个碳碳单键,如,C项错误;油脂的皂化是酯类的碱性水解,油脂是高级脂肪酸和甘油(丙三醇)形成的酯,不属于高分子,所以油脂皂化不是高分子生成小分子的过程,D项错误。
【易错提醒】油脂为高级脂肪酸甘油酯,不是高分子化合物,油脂可在酸性或碱性条件下水解,油脂在碱性条件下的水解反应又称为皂化反应.2。
(2016·天水二模)化学来源于生活,又服务于生活。
下列有关物质性质及应用的说法中正确的是( )A.纤维素和淀粉均属于多糖,均可供人体组织的营养需要B.聚氯乙烯塑料广泛应用于塑料薄膜、食品包装袋等C。

第一部分 专题三 第11讲1.(2017·北京卷)根据SO 2通入不同溶液中实验现象,所得结论不正确的是导学号 43864372( C )2342体现了SO 2的还原性,A 正确;B .SO 2与H 2S 在溶液发生反应SO 2+2H 2S =3S↓+2H 2O ,体现了SO 2的氧化性,B 正确;C .SO 2使酸性KMnO 4溶液褪色,这是SO 2在酸性溶液中还原KMnO 4生成Mn 2+,体现了SO 2的还原性,C 错误;D .SO 2与Na 2SiO 3溶液产生胶状沉淀,根据较强酸制较弱酸,可得结论酸性:H 2SO 3>H 2SiO 3,D 正确。
答案选C 。
2.(2017·江苏卷)下列有关物质性质与用途具有对应关系的是导学号 43864373( A )A .Na 2O 2吸收CO 2产生O 2,可用作呼吸面具供氧剂B .ClO 2具有还原性,可用于自来水的杀菌消毒C .SiO 2硬度大,可用于制造光导纤维D .NH 3易溶于水,可用作制冷剂[解析] A .过氧化钠可以和二氧化碳反应生成氧气,A 正确;B .因二氧化氯具有氧化性才用于自来水的杀菌消毒,B 错误;C .二氧化硅透光性好,用于制造光导纤维,C 错误;D .液氨气化时吸收大量热,所以氨可用作制冷剂,D 错误。
3.(2017·江苏卷)在给定条件下,下列选项所示的物质间转化均能实现的是导学号 43864374( C )A .Fe ――→Cl 2点燃FeCl 2――→Fe(OH)2B .S ――→O 2点燃SO 3――→H 2O H 2SO 4 C .CaCO 3――→高温CaO ――→SiO 2高温CaSiO 3 D .NH 3――→O 2催化剂,△NO ――→H 2O HNO 3[解析] A .铁与氯气反应只能生成氯化铁,A 错误; B .硫在空气或氧气中燃烧只能生成二氧化硫,B 错误;C .两步均能实现,C 正确;D .NO 不与H 2O 反应,D 错误。

元素及其化合物的复习思路和复习策略江苏省大港中学程薇元素及其化合物知识是高中化学的重要内容,约占整个高中化学内容的四分之一左右。
在高考中占15%左右。
知识零碎,化学反应多,学生已学易忘,老师在引导学生复习时也往往是将课本内容简单重复,认为无啥可讲,这样造成的结果是复习效率低。
如何有效地引导学生复习并落实好元素化合物知识,下面谈谈我个人的一些不成熟做法:一、复习思路以“元素→单质→氧化物(氢化物)→存在”为线索;学习具体的单质、化合物时既可以“结构→性质→用途→制法”为思路,又可从该单质到各类化合物之间的横向联系形成知识网进行复习,抓住知识的点、线、面进行学习,由具体到一般,化繁为简,有计划的使之系统化、规律化,抓元素知识与理论知识的结合点,发挥理论的指导作用。
并注意新旧知识的的联系和对比,注意相似物质的对比,如:氧化钠、过氧化钠,二氧化硫和二氧化碳,浓硫酸和稀硫酸等,将元素化合物知识形成一个完整的知识网络。
即总复习全面抓,普遍的知识规律化,零碎的知识系统化二、复习策略(一)把握重点,突出主干知识考试说明对常见元素的单质及其重要化合物的基本要求是:了解元素原子核外电子排布的周期性与元素性质的递变关系.掌握典型金属和典型非金属在周期表中的位置及与其性质的关系.了解其他常见金属和非金属元素的单质及其化合物.1.ⅠA和ⅡA族元素--典型的金属(1)了解钠的物理性质,掌握钠和镁的化学性质.(2)从原子的核外电子排布,理解ⅠA、ⅡA族元素(单质、化合物)的相似性和递变性.(3)以氢氧化钠为例,了解重要的碱的性质和用途。
了解钠的重要化合物。
2.卤族元素--典型的非金属(1)以氯为例,了解卤族元素的物理性质和化学性质.(2)从原子的核外电子排布,理解卤族元素(单质、化合物)的相似性和递变性.(3) 掌握氯气的化学性质,了解几种重要的含卤化合物的性质和用途3.其他常见的非金属元素(如:H、O、S、N、P、C、Si)(1)了解这些元素的单质及某些氧化物、氢化物的性质。

年级高三学科化学版本苏教版内容标题无机非金属元素及其化合物【本讲教化信息】一. 教学内容:无机非金属元素及其化合物二. 教学目标驾驭氯、氧、硫、氮、磷、碳、硅所在主族元素性质的相像性、递变规律和特别性;重点驾驭几种常见典型物质的物理性质和化学性质;驾驭硫酸、硝酸的化学性质;驾驭氯气、二氧化硫、一氧化氮、二氧化氮、二氧化碳、氨气、氢气的试验室制法和气体的收集与尾气的汲取。
三. 教学重点、难点常见非金属元素的性质及相互关系四. 教学过程:元素化合物是中学化学的主体,这部分内容与基本概念、基本理论相互渗透,与化学试验、化学计算联系紧密。
复习元素化合物,要运用规律、把握关键、抓住重点、联系实际、编织元素化合物的科学体系。
元素化合物学问复习中要留意相像、相近内容的总结归纳。
如SO2、CO2、SO3、P2O5、SiO2等都是酸性氧化物,它们的性质有相像之处也有相异点。
高考命题时常会把这种关系编入试题中。
近几年的高考试题中这种趋向比较明显,值得大家重视。
说明:1. 氯元素的学问网络2. 次氯酸、漂白粉的性质HClO分子的结构式为H-O-Cl(氧处于中心),所以电子式为。
次氯酸、次氯酸钙等有多方面的性质,常常用到以下几方面性质:(1)HClO是一种弱酸,与碳酸比较电离实力有如下关系:H2CO3>HClO>HCO3-,请分析下列反应:少量二氧化碳通入NaClO溶液中:NaClO + CO2+H2O=NaHCO3+HClO氯气通入碳酸氢钠溶液中:Cl2+NaHCO3=NaCl+CO2↑+HClO(2)ClO-是一种弱酸的酸根离子,能发生水解反应:ClO-+H2O HClO+OH-,所以次氯酸钙溶液显碱性。
若遇到铁盐、铝盐易发生双水解:3ClO-+Fe3++3H2O=Fe(OH)3↓+3HClO(3)HClO和ClO-都具有强氧化性,无论酸性、碱性条件下都可以跟亚铁盐、碘化物、硫化物等发生氧化还原反应,但不能使品红溶液褪色。

2017年新考纲学习体会玉林市一中1.化学学科特点和基本研究方法(都是要求“了解”)2.化学基本概念和基本理论(1)物质的组成、性质和分类②理解物理变化与化学变化的区别与联系。
③理解混合物和纯净物、单质和化合物、金属和非金属的概念。
④理解酸、碱、盐、氧化物的概念及其相互联系。
(2)化学用语及常用物理量①熟记并正确书写常见元素的名称、符号、离子符号。
②熟悉常见元素的化合价。
能根据化合价正确书写化学式(分子式),或根据化学式判断元素的化合价。
⑤理解质量守恒定律。
⑥能正确书写化学方程式和离子方程式,并能进行有关计算。
⑧能根据微粒(原子、分子、离子等)物质的量、数目、气体体积(标准状况下)之间的相互关系进行有关计算。
(3)溶液③理解溶液中溶质的质量分数概念,并能进行有关计算。
(4)物质结构和元素周期律④掌握元素周期律的实质。
⑤以第3周期为例,掌握同一周期内元素性质的递变规律与原子结构的关系。
⑥以ⅠA和ⅦA族为例,掌握同一主族内元素性质递变规律与原子结构的关系。
(5)化学反应与能量①掌握常见氧化还原反应的配平和相关计算。
⑦能运用盖斯定律进行有关反应焓变的计算。
⑧能书写电极反应和总反应方程式。
(6)化学反应速率和化学平衡④能利用化学平衡常数进行相关计算。
⑤理解外界条件(浓度、温度、压强、催化剂等)对反应速率和化学平衡的影响(7)电解质溶液(8)以上各部分知识的综合应用。
3.常见无机物及其应用(1)常见金属元素(如Na、Mg、Al、Fe、Cu等)(2)常见非金属元素(如H、C、N、O、Si、S、Cl等)(3)以上各部分知识的综合应用4.常见有机物及其应用(9)以上各部分知识的综合应用。
5.化学实验基础(3)掌握化学实验的基本操作。
能识别化学品标志。
(4)掌握常见气体的实验室制法(包括所用试剂、反应原理、仪器和收集方法)。
(5)能对常见的物质进行检验、分离和提纯,能根据要求配制溶液。
(6)能根据实验试题要求,做到:①设计、评价或改进实验方案;②了解控制实验条件的方法;③分析或处理实验数据,得出合理结论;(7)以上各部分知识与技能的综合应用。




魁夺市安身阳光实验学校非金属元素单质及其重要化合物(限时:45分钟)一、选择题1.(2015·课标全国Ⅰ)我国清代《本草纲目拾遗》中记叙无机药物335种,其中“强水”条目下写道:“性最烈,能蚀五金……其水甚强,五金八石皆能穿滴,惟玻璃可盛。
”这里的“强水”是指( )A.氨水B.硝酸C.醋 D.卤水解析:根据题意,“强水”能溶解大多数金属和矿物,所以为硝酸。
答案:B2.(2014·高考江苏卷)下列各组物质中,不满足组内任意两种物质在一定条件下均能发生反应的是( )物质组别甲乙丙A Al HCl NaOHB NH3O2HNO3C SiO2NaOH HFD SO2Ca(OH)2NaHCO3解析:A.Al与HCl、NaOH溶液都能反应生成H2,HCl溶液与NaOH溶液能发生中和反应。
B.NH3与O2在催化剂、高温条件下反应生成NO和H2O;O2与HNO3不能发生反应;NH3与HNO3反应生成NH4NO3。
C.SiO2与NaOH溶液、HF溶液分别发生反应:SiO2+2NaOH===Na2SiO3+H2O、SiO2+4HF===SiF4↑+2H2O;NaOH溶液与HF溶液发生中和反应。
D.SO2为酸性氧化物,可与Ca(OH)2溶液反应生成盐;H2SO3的酸性强于H2CO3,SO2可与NaHCO3溶液反应生成CO2;Ca(OH)2溶液可与NaHCO3溶液反应生成CaCO3沉淀。
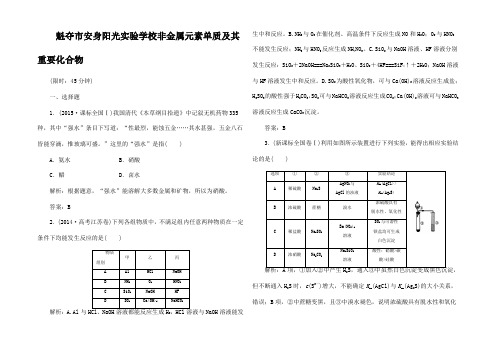
答案:B3.(新课标全国卷Ⅰ)利用如图所示装置进行下列实验,能得出相应实验结论的是( )选项①②③实验结论A 稀硫酸Na2SAgNO3与AgCl的浊液K sp(AgCl)>K sp(Ag2S)B 浓硫酸蔗糖溴水浓硫酸具有脱水性、氧化性C 稀盐酸Na2SO3Ba(NO3)2溶液SO2与可溶性钡盐均可生成白色沉淀D 浓硝酸Na2CO3Na2SiO3溶液酸性:硝酸>碳酸>硅酸2但不断通入H2S时,c(S2-)增大,不能确定K sp(AgCl)与K sp(Ag2S)的大小关系,错误;B项,②中蔗糖变黑,且③中溴水褪色,说明浓硫酸具有脱水性和氧化性,正确;C 项,③中产生白色沉淀,是SO 2在酸性条件下被NO -3氧化成SO 2-4的缘故,结论错误;D 项,浓硝酸具有挥发性,可能进入③中与Na 2SiO 3反应产生沉淀,即结论不准确,错误。

2017年高考化学二轮复习专题能力提升练十一第一篇专题通关攻略专题三元素及其化合物2 非金属元素单质及其重要化合物编辑整理:尊敬的读者朋友们:这里是精品文档编辑中心,本文档内容是由我和我的同事精心编辑整理后发布的,发布之前我们对文中内容进行仔细校对,但是难免会有疏漏的地方,但是任然希望(2017年高考化学二轮复习专题能力提升练十一第一篇专题通关攻略专题三元素及其化合物2 非金属元素单质及其重要化合物)的内容能够给您的工作和学习带来便利。
同时也真诚的希望收到您的建议和反馈,这将是我们进步的源泉,前进的动力。
本文可编辑可修改,如果觉得对您有帮助请收藏以便随时查阅,最后祝您生活愉快业绩进步,以下为2017年高考化学二轮复习专题能力提升练十一第一篇专题通关攻略专题三元素及其化合物2 非金属元素单质及其重要化合物的全部内容。
专题能力提升练十一非金属元素单质及其重要化合物(建议用时:20分钟)一、选择题1.(2016·天水二模)屠呦呦因发现了青蒿素这种抗疟良药而获得2015年诺贝尔奖,这充分说明了“化学让人们生活更美好”。
下列不属于化学反应在生活中的应用的是( )A。
将氧化铁添加到油漆中制红色油漆B.用氯气给自来水消毒C.将黏土烧制成精美的瓷器D.用食醋清洗水壶中的水垢【解析】选A。
将氧化铁添加到油漆中制红色油漆不是化学变化,A错误;用氯气给自来水消毒属于化学变化,B正确;将黏土烧制成精美的瓷器发生化学反应,C正确;用食醋清洗水壶中的水垢属于化学变化,D正确。
2。
(2016·龙岩一模)Si、SiO2广泛用于制造晶体管、光导纤维等。
下列有关说法正确的是( )A.附着油污的晶体管可用碱液浸泡B。
光导纤维遇碱会影响光信号传输C.工业上用SiO2热分解法冶炼硅D.自然界中硅以游离态形式存在【解析】选B。
晶体管中的硅可以和碱液反应,所以附着油污的晶体管不可用碱液浸泡,A错误;SiO2用于制造光导纤维,而SiO2会和碱液反应,故会影响光信号传输,B正确;工业上冶炼高纯硅有以下几个过程:①SiO2+2C Si+2CO↑,②Si+2Cl2SiCl4,③SiCl4+2H2Si+4HCl,C错误;硅是亲氧元素,在自然界中硅以化合态形式存在,D错误。