河北省2020-2021年高二上学期化学第一次月考试卷(I)卷
- 格式:doc
- 大小:284.00 KB
- 文档页数:13


2023-2024学年河北省石家庄第一中学高二上学期10月月考化学试题1.下列装置或过程能实现化学能转化为电能的是A.银锌纽扣电池 C.太阳能电池 D.天然气燃烧2.瑞典ASES公司设计的曾用于驱动潜艇的液氨—液氧燃料电池示意图如图所示,下列有关说法正确的是()A.电池工作时,Na +向电极1移动B.电池工作一段时间后停止,溶液pH值不变C.电极1发生的电极反应为2NH 3+6OH --6e - ===N 2↑+6H 2 OD.用该电池做电源电解精炼铜,理论上每消耗0.2 mol NH 3 的同时阳极会得到19.2g 纯铜3.用惰性电极电解一定浓度的硫酸铜溶液,通电一段时间后,向所得的溶液中加入0.1molCu2(OH)2CO3后恰好恢复到电解前的浓度和pH(不考虑CO2的溶解)。
则电解过程中共转移的电子的物质的量为A.0.2mol B.0.4mol C.0.6mol D.0.8mol4.下列电子排布式中,表示的是激发态原子的是A.1s 2 2s 2 2p 5B.C.D.5.利用如图装置进行实验,开始时,a、b两处液面相平,密封好,放置一段时间。
下列说法不正确的是A.a管发生吸氧腐蚀,b管发生析氢腐蚀B.一段时间后,a管液面高于b管液面C.a处溶液的不变,b处溶液的减小D.a、b两处具有相同的电极反应式:6.在如图装置中,观察到图1装置铜电极上产生大量无色气泡,而图2装置中铜电极上无气泡产生,铬电极上产生大量有色气泡。
下列叙述不正确的是A.图1装置中 Cu 电极上电极反应式是B.图2装置中 Cu 电极上发生的电极反应为C.图2装置中 Cr电极上电极反应式为D.两个装置中,电子均由 Cr电极经导线流向 Cu 电极7. X、Y、Z、M、Q五种短周期主族元素,原子序数依次增大。
X的2s轨道全充满,Y的s能级电子数量是p能级的两倍,M原子核外有8种运动状态不同的电子,Q是短周期中除稀有气体元素外原子半径最大的元素。

河北省邢台市2022届高三上学期第一次月考 化学试题1.化学与生活密切相关。
下列说法错误的是 A. 用白磷作包装食品的脱氧剂 B. 食品保鲜膜能减缓食品中水分的蒸发 C. 用液氨作制冷剂冷藏物品 D. 用臭氧对医疗器械进行消毒【答案】A 【解析】【详解】A. 白磷着火点低,容易自燃,所以不宜用白磷作包装食品的脱氧剂,故A 错误;B. 食品保鲜膜用的是聚乙烯塑料不通透,密封效果好,能减缓食品中水分的蒸发,故B 正确;C. 液氨挥发为气体需要吸收热量,所以可以用作制冷剂冷藏物品,故C 正确;D. 臭氧具有强氧化性,可以用于对医疗器械进行消毒,故D 正确;答案:A 。
2.臭氧已成为夏季空气污染的元凶,地表产生氧的机理如图所示。
下列说法正确的是A. NO 是反应③的催化剂B. O 3、O 是反应的中间体C. 反应①②③均是氧化还原反应D. 产生臭氧的化学方程式为3O 22O 3【答案】D 【解析】【详解】由图可知NO 2是反应的催化剂,故A 错误;NO 和O 原子是反应的中间体,O 3是反应的产物,故B 错误;反应②是非氧化还原反应,故C 错误;D.根据反应图示知产生臭氧的化学方程式为3O 2=太阳光催化剂2O 3,故D正确;答案:D 。
3.下列说法错误的是A. 液态二氧化碳灭火剂可扑灭一般的起火,也适用于金属起火B. 常用高温和紫外线对医疗器械进行消毒,是因为高温和紫外线可使蛋白质变性C. 影化食品中禁止使用含铝的食品添加剂,是因为铝元素会危害人体健康D. 家庭装修时用植物生态涂料代替传统墙面涂料,有利于健康及环境 【答案】A 【解析】【详解】A. 液态二氧化碳灭火剂不能扑灭金属钠着火,因为金属钠着火会产生过氧化钠和二氧化碳反应放出氧气,帮助钠的燃烧,故A 错误;B.医疗器械表面附着有大量的细菌和病毒,构成细菌和病毒的基本成分是蛋白质,蛋白质遇到高温时会变性,失去原有的生理活性,因此能用高温来消毒。

2021学年河北省衡水市某校高二(上)第一次月考化学试卷(9月份)一、选择题)1. 化学与生活密切相关,下列说法错误的是()A.煤的干馏是化学变化过程B.绿色化学要求从源头上消除或减少生产活动对环境的污染C.燃煤中加入CaO可以减少酸雨的形成及温室气体的排放D.天然气和液化石油气是我国目前推广使用的清洁燃料2. 下列说法正确的是()A.当反应物的键能之和大于生成物的键能之和时,反应吸热B.反应HCHO+O2→CO2+H2O为吸热反应C.一个化学反应,当反应物能量大于生成物能量时,反应放热,△H为“+”D.放热反应不需要加热就能反应,吸热反应不加热就不能反应3. 下列说法中正确的是()A.在化学反应过程中,发生物质变化的同时不一定发生能量变化B.煤、石油、天然气均为化石能源,是非再生能源C.生成物的总焓大于反应物的总焓时,反应吸热,△H<0D.△H的大小与热化学方程式的化学计量数无关4. 根据键能数据估算CH4(g)+4F2(g)=CF4(g)+4HF(g)的反应热△H为()D.+485 kJ/mol5. 下列各原子或离子的电子排列式错误的是()A.Na+:1s22s22p6B.F−:1s22s22p6C.N3+:1s22s22p6D.O2−:1s22s22p66. 一个价电子构型为2s22p5的元素,下列有关它的描述正确的有()A.原子序数为8B.电负性最大C.原子半径最大D.第一电离能最大7. 原子轨道在两核间以“肩并肩”方式重叠的键是()A.σ键B.π键C.氢键D.离子键8. 在容积固定的密闭容器中存在如下反应:N2(g)+3H2(g)⇌2NH3(g);△H<0.某研究小组研究了其他条件不变时,改变某一条件对上述反应的影响,并根据实验数据作出如图关系图:下列叙述正确的是()A.图Ⅰ研究的是温度对反应的影响,且甲的温度比乙高B.图Ⅱ研究的是温度对反应的影响,且甲的温度比乙高C.图Ⅱ研究的是压强对反应的影响,且甲的压强比乙大D.图Ⅲ研究的是不同催化剂对反应的影响,且乙使用的催化剂效率比甲高9. 合成氨所需的氢气可用煤和水作原料经多步反应制得,其中的一步反应为:CO(g)+H2O(g)⇌CO2(g)+ H2(g)△H<0反应达到平衡后,为提高CO的转化率,下列措施中正确的是()A.增加压强B.降低温度C.增大CO的浓度D.更换催化剂10. 反应N2O4(g)⇌2NO2(g)在温度为T1、T2(T2>T1)时,平衡体系中NO2的体积分数随压强变化如图所示。

2020-2021学年河北省石家庄市某校高二下学期第一次月考 (化学)试卷一、选择题1. 提出“杂化轨道理论”的科学家是()A.门捷列夫B.普鲁特C.玻尔D.鲍林2. 下列各组元素中不符合“对角线法则”的是()A.Li、MgB.C、PC.B、SiD.Be、Al3. 下列基态原子或离子的相关电子排布图正确的是()A.Fe3+的价电子:B.Cr原子的价电子:C.N原子的核外电子:D.S2−的L层电子:4. 短周期主族元素W、X、Y、Z的原子序数依次增大,W、X同周期且基态原子均含有2个未成对电子。
Z的单质常温下为气体且价电子数和:W+X=Y+Z,下列有关说法正确的是()A.简单离子半径:X<YB.最高正价:X>WC.Y与Z形成的化合物为非电解质D.W、Z形成的二元化合物中可能同时含有σ键和π键5. 下列关于卤族元素单质及其化合物的结构与性质说法错误的是()A.相对分子质量:CH2Cl2>CH3Cl,因此熔沸点:CH2Cl2>CH3ClB.键长H−Br>H−Cl,因此稳定性:HCl>HBrC.单质氧化性F2>Cl2,因此F2可氧化水溶液中的Cl−D.非金属性:Cl>Br,因此含氧酸酸性:HClO4>HBrO46. 下列关于物质结构和性质的说法正确的是()A.BF3中的键角大于BF4−的键角B.CH3CN中σ键和π键的数目之比为4:3C.含氧酸酸性:HClO>HClO2D.CH3OH易溶于水的原因仅仅是因为CH3OH和水分子都是极性分子7. 反应SiHCl3(g)+H2(g)===Si(s)+3HCl(g)可用于纯硅的制备,下列说法正确的是()A.SiHCl3中Si原子的杂化方式为sp2杂化B.SiHCl3中Si元素的化合价为+2C.键长:Si−Si>C−C,故键能:Si−Si<C−CD.HCl易溶于水是因为HCl和水分子之间能形成氢键8. 已知X、Y元素同周期,且电负性X大于Y,下列说法一定错误的是()A.第一电离能:Y大于XB.气态氢化物的稳定性:Y大于XC.最高价含氧酸的酸性:X强于YD.X和Y形成化合物时,X显负价,Y显正价9. 已知HF沸点为19.5∘C,BF3沸点为−100∘C,HF+BF3===HBF4,下列有关说法错误的是()A.HBF4中B原子为sp3杂化B.BF3和HBF4分子中B最外层均为8e−稳定结构C.HBF4中存在配位键D.HF沸点高于BF3沸点的原因可能为HF分子之间存在氢键10. 根据价层电子对互斥理论,NCl3、SO2、SO3、BF3的气态分子中,中心原子价层电子对数不同于其他分子的是()A.NCl3B.SO2C.SO3D.BF311. 元素的基态气态原子得到一个电子形成气态−1价离子时所放出的能量称作第一电子亲和能(E),−1价阴离子再获得一个电子的能量变化叫做第二电子亲和能,部分元素或离子的电子亲和能数据如表所示。

2023-2024学年河北省石家庄精英中学高二上学期2月月考化学试题1.下列常见的电池中,叙述错误的是锌锰电池铅蓄电池氢氧燃料电池镍镉电池B.铅蓄电池放电时,铅电极质量减少C.氢氧燃料电池中负极通入氢气,发生氧化反应D.镍镉电池为二次电池,放电时为原电池,充电时为电解池2.下列有关电解的说法错误的是A.电解氢氧化钠溶液可以制得氢气和氧气B.电解氯化铜溶液可以制得金属铜和氯气C.电解熔融食盐可以制得钠和氯气D.电解熔融的氯化铝可以制得金属铝和氯气3.利用电解法可将粗铜(含有Ag、Zn、Fe、Pt)提纯,下列叙述正确的是A.电解提纯时,精铜作阳极B.电解提纯时,可用硫酸铜溶液作电解质溶液C.电解提纯时,粗铜连接电源的负极,电极反应为Cu 2+ +2e - =CuD.电解提纯时,溶液中Ag +、Zn 2+、Fe 2+、Pt 2+浓度均增大4.下列说法错误的是A.钠原子的核外电子有11种运动状态B.电子仅从激发态跃迁到基态才产生原子光谱C.1个原子轨道里最多容纳2个电子,且自旋状态相反D.只有基态原子的电子排布才遵循能量最低原理、洪特规则和泡利不相容原理5.下列关于铁元素的几种表达式错误的是A.Fe在周期表中的位置:第四周期第Ⅷ族B.Fe原子结构示意图:C.基态Fe 2+的价电子排布式:3d 5 4s 1D.基态Fe 3+的轨道表示式:6.下列各项中电极反应式与相关描述对应不合理的是7.钢铁闸门的防护方法有多种,下列对于图中的防护方法描述错误的是A.a、b以导线连接,辅助电极发生氧化反应B.a、b分别连接直流电源的负极、正极,该方法是牺牲阳极法C.a、b以电源连接,辅助电极的材料可能含有CuD.a、b分别连接直流电源,通电后外电路电子被强制从辅助电极流向钢铁闸门8.氯碱工业是高能耗产业,一种将电解池与燃料电池相结合的新工艺可以节能30%以上。
在这种工艺设计中,相关物料的传输与转化关系如图所示,下列说法中错误的是A.A池是电解池,B池是燃料电池B.X为Cl 2,Y为H 2C.NaOH溶液的浓度为a%>b%>c%D.该工艺设计的主要节能之处是燃料电池可以补充电解池消耗的电能9.磷酸二氢钙[化学式Ca(H2PO4)2]广泛用于营养增补剂。
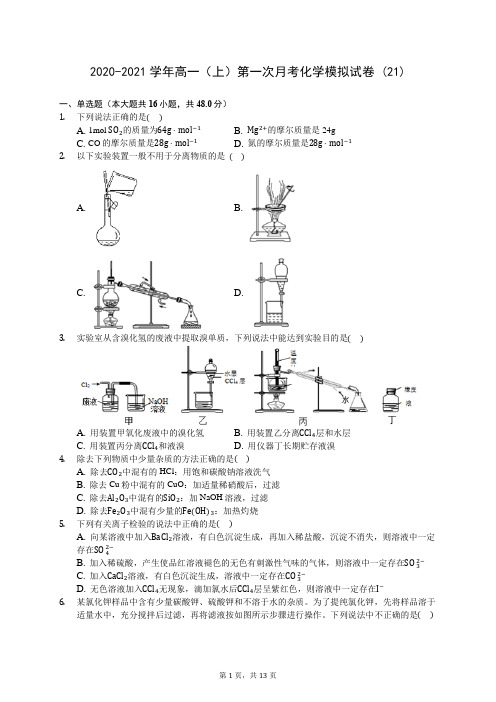
2020-2021学年高一(上)第一次月考化学模拟试卷 (21)一、单选题(本大题共16小题,共48.0分)1.下列说法正确的是()A. 1mol SO2的质量为64g⋅mol−1B. Mg2+的摩尔质量是24gC. CO的摩尔质量是28g⋅mol−1D. 氮的摩尔质量是28g⋅mol−12.以下实验装置一般不用于分离物质的是()A. B.C. D.3.实验室从含溴化氢的废液中提取溴单质,下列说法中能达到实验目的是()A. 用装置甲氧化废液中的溴化氢B. 用装置乙分离CCl4层和水层C. 用装置丙分离CCl4和液溴D. 用仪器丁长期贮存液溴4.除去下列物质中少量杂质的方法正确的是()A. 除去CO2中混有的HCl:用饱和碳酸钠溶液洗气B. 除去Cu粉中混有的CuO:加适量稀硝酸后,过滤C. 除去Al2O3中混有的SiO2:加NaOH溶液,过滤D. 除去Fe2O3中混有少量的Fe(OH)3:加热灼烧5.下列有关离子检验的说法中正确的是()A. 向某溶液中加入BaCl2溶液,有白色沉淀生成,再加入稀盐酸,沉淀不消失,则溶液中一定存在SO 42−B. 加入稀硫酸,产生使品红溶液褪色的无色有刺激性气味的气体,则溶液中一定存在SO 32−C. 加入CaCl2溶液,有白色沉淀生成,溶液中一定存在CO 32−D. 无色溶液加入CCl4无现象,滴加氯水后CCl4层呈紫红色,则溶液中一定存在I−6.某氯化钾样品中含有少量碳酸钾、硫酸钾和不溶于水的杂质。
为了提纯氯化钾,先将样品溶于适量水中,充分搅拌后过滤,再将滤液按如图所示步骤进行操作。
下列说法中不正确的是()A. 试剂Ⅰ可能为BaCl2溶液B. 步骤②中加入试剂Ⅱ的目的是除去Ba2+C. 步骤③包含过滤操作D. 图示步骤中的前两次过滤操作可以合并7.下列提纯方法不正确的是()A. 从碘水中提取碘--用苯萃取后分液B. 除去食盐中的泥沙一一溶解后过滤C. 除去KCl溶液中的K2CO3--加适量盐酸D. 分离油和水--过滤8.某化学活动小组设计提纯NaCl的流程如下,则下列有关说法正确的是()提供的试剂:饱和Na2CO3溶液、饱和K2CO3溶液、NaOH溶液、BaCl2溶液、Ba(NO3)2溶液、75%乙醇、四氯化碳。

2022-2023学年第一学期第一次阶段测试卷高二化学(苏教版)一、选择题:本题共9小题,每小题3分,共27分。
在每小题给出的四个选项中,只有一项是符合题目要求的。
1.下列诗句中涉及吸热反应的是( ) A .日照香炉生紫烟,遥看瀑布挂前川 B .回中烽火人,塞上追兵起 C .千锤万凿出深山,烈火焚烧若等闲 D .煮豆燃豆萁,豆在釜中泣2.下列热化学方程式书写正确的是( ) A .()C s 燃烧的热化学方程式:22C O CO + 1393.5kJ mol H -∆=-⋅B .()4CH g 燃烧的热化学方程式:()()()()4222CH g 2O g CO g 2H O l ++ 1890.3kJ mol H -∆=⋅C .葡萄糖在人体内与氧气反应的热化学方程式:()()()()6126222C H O s 6O g 6CO g 6H O l ++12803kJ mol H -∆=-⋅D .含20.0gNaOH 的稀溶液与足量稀盐酸反应,释放28.7kJ 的热量,则热化学方程式为()()()()2NaOH aq HCl aq NaCl aq H O l ++ 128.7kJ mol H -∆=-⋅3.下列有关说法正确的是( )A .升高温度,使反应物分子中活化分子数增多,但活化分子百分数不变B .()()()223N g 3H g 2NH g +在恒温恒压条件下进行,向容器中通入()Ar g ,化学,反应速率减小C .在化学反应前后,催化剂的质量和化学性质都没有发生变化,故催化剂一定不参与化学反应D .1100mL2mol L -⋅的盐酸与锌反应时,加入适量的NaCl 溶液,生成2H 的速率不变 4.在()()()22H g Br g 2HBr g + 0H ∆<的平衡体系中,下列说法正确的是( )A .从平衡体系中分离出()HBr g ,能加快正反应速率B .降低温度,平衡正向移动,2H 的转化率增大C .增大压强,平衡不移动,混合气体的颜色不变D .若增大2Br 的浓度,平衡正向移动,混合气体的颜色变浅 5.下列说法正确的是( )A .放热反应都能自发进行,吸热反应都不能自发进行B .反应()()()34NH g HCl g NH Cl s +在室温下可自发进行,则该反应的0H ∆<C .合成氨工业中采用高温以提高平衡转化率D .选择不同的催化剂会改变反应H ∆的数值 6.关于下列各装置图的叙述不正确的是( )A .装置①是原电池,可以实现化学能转化为电能B .装置②电解片刻后,阳极附近的pH 变小C .装置③可实现外加电流的阴极保护法D .由装置④的现象可判断电化学腐蚀的类型 7.下列说法正确的是( )A .工业上铝的制取是电解熔融的氯化铝B .电解精炼铜时,阳极为粗铜,阴极为纯铜,电解液中()2Cuc +减小C .惰性电极电解氯化铜溶液,阴极产生的气体可以使湿润的淀粉-KI 试纸变蓝D .钢管表面镀锌可以防止钢管被腐蚀,镀层破损后,钢管反而会加速腐蚀 8.汽车的启动电源常用铅蓄电池,其结构如图所示。

2020-2021学年高二上学期第一次月考化学试题1.本试卷满分为100分,考试时间为90分钟;2.请将答案填写到答题卡上。
可能用到的相对原子质量:H:1 N:14 C:12 O:16 Na:23 S:32 Cl:35.5 Zn:65 Cu:64 Ag:108第Ⅰ卷( 共45分)一、选择题(本题共20个小题,其中1-15题每题2分,16-20题每题3分,每题只有一个答案符合题意)1. 25℃、101 kPa下,碳、氢气、甲烷和葡萄糖的燃烧热依次是393.5 kJ/mol、285.8 kJ/mol、890.3 kJ/mol、2800 kJ/mol,则下列热化学方程式正确的是()A. C(s)+ O2(g)=CO(g) ΔH=―393.5 kJ/molB. 2H2(g)+O2(g)=2H2O(l) ΔH = +571.6 kJ/molC. CH4(g)+2O2(g)=CO2(g)+2H2O(g) ΔH=―890.3 kJ/molD. C6H12O6(s) +6O2(g)=6CO2(g)+6H2O(l) ΔH=―2800 kJ/mol2. 已知两个热化学方程式: C(s)+O2(g) =CO2(g) ΔH=―393.5kJ/mol2H2(g)+O2(g) =2H2O(g) ΔH=―483.6kJ/mol现有炭粉和H2组成的悬浮气共0.2mol,使其在O2中完全燃烧,共放出63.53kJ的热量,则炭粉与H2的物质的量之比是()A. 1︰1B. 1︰2C. 2︰3D. 3︰23. 燃料电池是燃料(例如CO,H2,CH4等)跟氧气或空气起反应,将此反应的化学能转变为电能的装置,电解质通常是KOH溶液。
下列关于甲烷燃料电池的说法不正确的是()A. 负极反应式为CH4+10OH--8e=CO32-+7H2OB. 标准状况下,消耗5.6LO2时,有1mole-发生了转移C. 随着不断放电,电解质溶液碱性不变D. 甲烷燃料电池的能量利用率比甲烷燃烧的能量利用率大4. 高铁电池是一种新型可充电电池,与普通高能电池相比,该电池长时间保持稳定的放电电压。
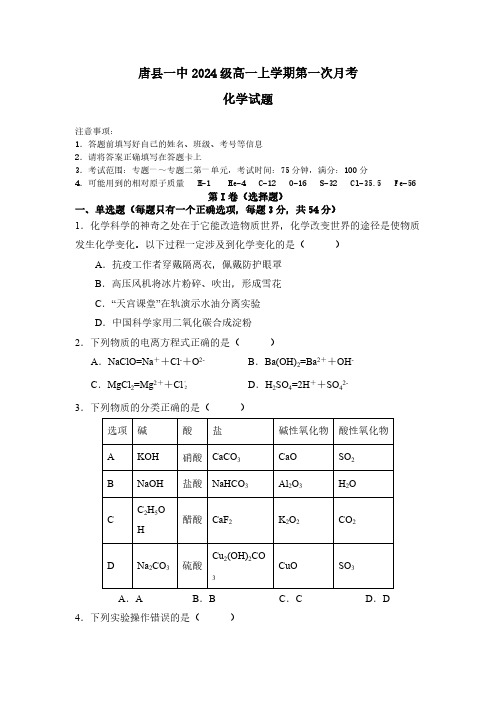
唐县一中2024级高一上学期第一次月考化学试题注意事项:1.答题前填写好自己的姓名、班级、考号等信息2.请将答案正确填写在答题卡上3.考试范围:专题一~专题二第一单元,考试时间:75分钟,满分:100分4.可能用到的相对原子质量 H-1 He-4 C-12 O-16 S-32 Cl-35.5 Fe-56第I 卷(选择题)一、单选题(每题只有一个正确选项,每题3分,共54分)1.化学科学的神奇之处在于它能改造物质世界,化学改变世界的途径是使物质发生化学变化。
以下过程一定涉及到化学变化的是()A .抗疫工作者穿戴隔离衣,佩戴防护眼罩B .高压风机将冰片粉碎、吹出,形成雪花C .“天宫课堂”在轨演示水油分离实验D .中国科学家用二氧化碳合成淀粉2.下列物质的电离方程式正确的是()A .NaClO=Na ++Cl -+O 2-B .Ba(OH)2=Ba 2++OH -C .MgCl 2=Mg 2++ClD .H 2SO 4=2H ++SO 42-3.下列物质的分类正确的是()选项碱酸盐碱性氧化物酸性氧化物A KOH 硝酸CaCO 3CaO SO 2BNaOH 盐酸NaHCO 3Al 2O 3H 2O C C 2H 5O H醋酸CaF 2K 2O 2CO 2D Na 2CO 3硫酸Cu 2(OH)2CO3CuO SO 3A .AB .BC .CD .D4.下列实验操作错误的是()-2A .未用完的金属钠要放回原试剂瓶B .稀释浓硫酸时,应将水沿烧杯壁缓缓加入到浓硫酸中C .组装实验仪器后,先检验装置气密性,再装入药品D .不慎将浓酸沾到皮肤上,可先用大量水冲洗,再用的溶液清洗5.下列叙述正确的是()A .1molH 2SO 4的质量是98g·mol -1B .1molC 约含有6.02×1023个碳原子C .CO 2的摩尔质量等于CO 2的相对分子质量D .在标准状况下,1mol 任何物质的体积都约为22.4L 6.将碘水中的碘萃取出来的实验中,下列说法错误的是 ( )A .分液漏斗使用前要检验它是否漏水B .萃取剂要求不溶于水,且比水更容易使碘溶解C .注入碘水和萃取剂,倒转分液漏斗反复用力振荡后立即分液D .若用苯作萃取剂,则分层后上层液体呈紫红色7.设N A 为阿伏加德罗常数的值,下列叙述正确的是()A .常温常压下,5.6g 铁与足量的盐酸反应,生成H 2的分子数为0.2N AB .标准状况下,11.2L 苯(C 6H 6)中含碳原子数目为3N A C .32g S 8与S 6的混合物中所含S 原子数为N AD .18g H 2O 中含有的H 2数目为N A8.下列各组物质之间可以按下图所示关系直接转化的是()A .Fe →Fe 2O 3→FeSO 4→FeB .HCl →CuCl 2→BaCl 2→HClC .NaOH →NaCl →Na 2CO 3→NaOHD .CO →CO 2→H 2CO 3→CO9.分析下表中三种气体物质的有关数据,下列说法不正确的是()体 积物质质量/g0℃,101kPa20℃,101kPa0℃,202kPa3%~5%3NaHCOH 2222.424.011.2O 23222.424.011.2CO 24422.323.911.2A .物质的量相同的上述三种气体,在相同的条件下,其体积基本相同B .相同的条件下,体积相同的上述三种气体,其质量不同C .质量相同的上述三种气体,在相同的条件下,其体积一定不同D .同温同压,体积相同的上述三种气体,因其质量不同,所以气体分子数目也不同10.磁流体又称磁性液体、铁磁流体或磁液,是一种新型的功能材料,它既具有液体的流动性又具有固体磁性材料的磁性。

河北省石家庄二中2023届高三上学期第一次月考化学试题(时间:75分钟,分值:100分)可能用到的相对原子质量:H-1 O-16 Na-23 S-32 Cl-35.5 Ca-40 Fe-56一、单选题(每题只有一个选项符合题意,1-5题,每题2分,6-10,每题3分,共25分)1.化学作为一门基础学科在生产、生活中起到了重要的作用。
下列有关说法中不正确的是A .中国古代利用明矾溶液清除铜镜表面的铜锈B .我国发射的“北斗组网卫星”所使用的碳纤维,是一种新型无机非金属材料C .加工后具有吸水性的植物纤维、硅胶、P 2O 5可用作食品干燥剂D .市面上的防晒衣通常采用聚酯纤维材料制作,不可以长期用肥皂洗涤2.N A 表示阿伏加德罗常数的值。
下列叙述不正确的是A .1 mol CH 3·所含有的电子数为9N AB .某温度下,1.0 L pH=13的Ba(OH)2溶液中含OH -数目为0.1N AC .5.6 g 铁与足量硫粉反应转移电子数为0.2N AD .120 g NaHSO 4晶体中含有N A 个阳离子3.氟氧酸是较新颖的氧化剂,应用性极强,可用被氮气稀释的氟气在细冰上缓慢通过制得,其反应原理如下:F 2+H 2O = HOF+HF 。
该反应与下列反应中水的作用相同的是A .炭与水蒸气反应制氢气B .过氧化钠与水反应制氧气C .氟单质与水反应制氧气D .氯气与水反应制次氯酸4.下列实验仪器、试剂、操作均正确,且能达到实验目的的是A .制备氢氧化铁胶体B .灼烧海带C .用滴定法测氨水的物质的量浓度D .配制一定物质的量浓度溶液,最终摇匀5.在离子浓度都为0.1 mol·L -1的下列溶液中,加入(或通入)某物质后,发生反应的先后顺序正确的是A .在含Fe 3+、Cu 2+、H +的溶液中加入锌粉:Cu 2+、Fe 3+、H +B .在含I -、SO 32-、Br -的溶液中不断通入氯气:I -、Br -、SO 32-C .在含AlO 2-、SO 32-、OH -的溶液中逐滴加入硫酸氢钠溶液:OH -、AlO 2-、SO 32-D .在含Fe 3+、H +、NH 4+的溶液中逐渐加入烧碱溶液:Fe 3+、NH 4+、H +6.某种化学品的结构如图所示,已知W 、X 、Y 、Z 、M 均为短周期主族元素,其中W 、X 、Y 在同一周期,Z 、M 同处另一周期,M 原子的最外层电子数等于其电子层数,则下列说法中正确的是A .元素对应简单离子半径大小关系为:M>X>WB .与W 的同周期主族元素中,第一电离能比W 大的元素只有1种C .X 、Y 、Z 、W 形成的简单氢化物中,沸点高低顺序为:W>X>Z>YD .W 和M 形成的化合物可以溶解在Y 所形成的最高价氧化物对应水化物中7.下列离子方程式书写正确的是A .NaAl(SO 4)2溶液中滴加Ba(OH)2直至SO 42-沉淀完全:2Al 3+ + 6OH - + 3SO 42-+3Ba 2+ = 2Al(OH)3↓ + 3BaSO 4↓B. 已知:MgCO 3、Mg(OH)2的K sp 分别为6.8×10-6、5.6×10-12,Mg(HCO 3)2中加入足量澄清石灰水:Mg 2+ + 2HCO 3- + 2Ca 2+ + 4OH - = Mg(OH)2↓ + 2CaCO 3↓ + 2H 2OC. 向CuSO 4溶液中滴加氨水,产生难溶物:Cu 2++2OH -=Cu(OH)2↓D .已知硫酸铅难溶于水,也难溶于硝酸,却可溶于醋酸铵溶液,形成无色溶液。

2020-2021学年高一(上)第一次月考化学模拟试卷 (20)一、单选题(本大题共20小题,共60.0分)1.在实验室中,对下列事故或药品的处理正确的是()A. 酒精及其他易燃物小面积失火,应该迅速使用湿抹布扑盖;钠、钾等失火应用泡沫灭火器扑灭B. 用排水法收集气体时,先撤酒精灯后移出导管C. 少量氢氧化钠溶液沾在皮肤上,立即用水冲洗,再涂碳酸氢钠溶液D. 有大量的氯气泄漏时,应用浸有弱碱性溶液的毛巾捂住口鼻向高处跑2.下列实验操作中有错误的是()A. 用蒸馏水润湿的试纸测某溶液的pH,一定会使结果偏低B. 蒸馏操作时,冷却水应从冷凝管的下口通入,上口流出C. 分液时,分液漏斗下层液体从下口放出,上层液体从上口倒出D. 蒸发操作时,当有较多晶体析出时,停止加热3.下列有关过滤和蒸发的操作中,正确的是()A. 过滤时,漏斗的下端管口紧靠烧杯内壁B. 为了加快过滤速度,可用玻璃棒搅动过滤器中的液体C. 当蒸发皿中的固体完全蒸干后,再停止加热D. 实验完毕后,用手直接取走蒸发皿4.下列关于胶体和溶液的叙述正确的是()A. 胶体带电荷,而溶液呈电中性B. 胶体中加入电解质可以产生沉淀,而溶液不能C. 胶体是一种不稳定分散系,而溶液是一种最稳定分散系D. 胶体具有丁达尔效应,而溶液不具有5.分离沸点不同又互溶的液体混合物,常用的方法是()A. 过滤B. 蒸馏C. 萃取D. 分液6.关于酸、碱、盐的下列说法中错误的是()A. 酸在水溶液中电离产生的阳离子全部是氢离子B. 碱在水溶液中电离产生的阴离子全部是氢氧根离子C. 盐在水溶液中电离一定有金属阳离子产生D. 酸和盐在水溶液中电离都可能有含氧酸根离子产生7.下列现象与胶体的性质无关的是()A. 将盐卤或石膏加入豆浆,制成豆腐B. 一支钢笔使用两种不同型号的蓝黑墨水,易出现堵塞C. 向BaCl2溶液中加入稀硫酸,会出现白色沉淀D. 清晨,人们经常看到阳光穿过茂密的树木枝叶产生的美丽景象8.下列状态的物质,既能导电又属于电解质的是()A. KCl溶液B. 气态HClC. 熔融的NaOHD. 酒精溶液9.下列叙述正确的是()A. 一氧化碳的摩尔质量为28gB. 0.5 mol OH−的质量为8.5gC. 镁原子的摩尔质量等于它的相对原子质量D. 一个钠原子的质量等于236.02×102310.下列说法中正确的是()A. 摩尔是物质的量的单位,含有6.02×1023个微粒的物质叫做1摩尔B. 1mol氧含有6.02×1023个氧原子C. 1mol气体的体积随压强增大和温度降低而变小D. 标准状况下,体积相等的CCl4和Cl2,前者含有的氯原子数是后者的两倍11.下列各组反应,前后均可用同一离子方程式表示的是()A. HCl+Na2CO3,HCl+NaHCO3B. HCl+Na2CO3,HNO3+K2CO3C. H2SO4+Ba(OH)2,H2SO4+KOHD. BaCl2+Na2SO4,BaCO3+HCl12.0.5L1mol/L的FeCl3溶液与0.2L1mol/L的KCl溶液中,Cl−浓度比为()A. 15:2B. 1:2C. 3:1D. 1:313.下列反应的离子方程式正确的是()A. 用稀盐酸除水垢中的碳酸钙:Ca2++CO32−+2H+=Ca2++H2O+CO2↑B. 用稀盐酸除水垢中的氢氧化镁:Mg(OH)2+2H+=Mg2++2H2OC. 用碳酸氢钠作为抗酸药中和胃酸:2H++CO32−=H2O+CO2↑D. 用H2SO4中和碱性废水:H2SO4+2OH−=2H2O+SO42−14.证明某未知溶液中含有氯离子(Cl−)的正确方法是()A. 加入AgNO3溶液,有白色沉淀产生B. 加入AgNO3溶液,有白色沉淀产生,再加入稀盐酸,沉淀不消失C. 加入稀盐酸酸化后,再加入AgNO3溶液,有白色沉淀产生D. 加入稀硝酸酸化后,再加入AgNO3溶液,有白色沉淀产生15.已知3.01×1023个X气体分子的质量为16g,则X气体的摩尔质量是()A. 16gB. 32gC. 64g·mol−1D. 32g·mol−116.实验室中需要配制1mol/L的NaCl溶液970mL,配制时应选用的容量瓶的规格是()A. 950mL 容量瓶B. 500mL容量瓶C. 1000mL 容量瓶D. 任意规格的容量瓶17.一个集气瓶的质量为20.0g,在相同状况下,装满O2时质量为21.0g,装满A气体时为22.0g,则A气体的摩尔质量为()A. 16g/molB. 32g/molC. 64g/molD. 128g/mol18.已知98%的浓硫酸的浓度为18.4mol/L,则49%的硫酸溶液的物质的量浓度()A. 等于9.2mol/LB. 小于9.2mol/LC. 大于9.2mol/LD. 无法确定19.BLAl2(SO4)3溶液中含有agAl3+,则SO42−的物质的量浓度为()A. 3a2B mol/L B. a27Bmol/L C. a18Bmol/L D. 2a81Bmol/L20.有BaCl2和NaCl的混合溶液aL,将它均分成两份.一份滴加稀硫酸,使Ba2+离子完全沉淀;另一份滴加AgNO3溶液,使Cl−离子完全沉淀.反应中消耗xmolH2SO4ymol、AgNO3溶液.据此得知原混合液中氯化钠的物质的量浓度(mol/L)为()A. y−2xa B. y−xaC. 2y−2xaD. 2y−4xa二、填空题(本大题共3小题,共26.0分)21.标准状况下,112mL某气体的质量为0.14g,则其摩尔质量为______,相对分子质量为______.22.I.在标准状况下,由CO和CO2组成的混合气体8.96L,质量是16g。

2020-2021学年度高二化学上学期第一次月考试卷可能用到的相对原子质量:H-1 C-12 O-16 N-14 Ca-40 I-127 S-32 Cl-35.5 Na-23一、选择题(本题包括25小题,每小题2分,共50分,每小题一个或两个选项符合题意)1.下列叙述正确的是()A.电能是二次能源 B. 水力是二次能源C.天然气是二次能源 D. 水煤气是一次能源2. 100mL 6mol/L H2SO4与过量锌粉反应,一定温度下,为了减缓反应进行的速率,但又不影响生成氢气的总量,可向反应物中加入适量的()A.Na2SO4(s) B.NaOH (s)C.K2SO4溶液D.(NH4)2SO4(s)3.在2L密闭容器中,盛有2molX和 2molY物质进行如下反应: 2X(s)+3Y(g)Z(g),当反应进行10s后,测得生成0.5molZ,则这期间的平均反应速率为()A.v(Z)=0.025mol/(L·s) B.v(X)=0.025mol/(L·s)C.v(Y)=0.05mol/(L·s) D.v(Y)=0.075mol/(L·s)4.升高温度能加快反应速率的主要原因是()A.活化分子能量明显增加B.降低活化分子的能量C.增加活化分子百分数D.降低反应所需要的能量5.四个试管中都装有5 mL 0.1 mol/LNa2S2O3溶液,分别在不同温度下加入0.1 mol/L硫酸和一定量水,最先出现浑浊的是()A .20℃ 10 mL 硫酸B .20℃ 5 mL 硫酸 5 mL 水C .30℃ 10 mL 硫酸D .30℃ 5 mL 硫酸 5 mL 水6.在真空密闭容器中盛有1 mol PCl 5加热到200℃时发生的如下反应:PCl 5(气) PCl 3(气) +Cl 2(气),反应达平衡后,PCl 5所占体积分数为M%。
若在同一温度和同一容器中,最初投入的是2 mol PCl 5(气),反应达平衡时,PCl 5所占体积分数为 N%。
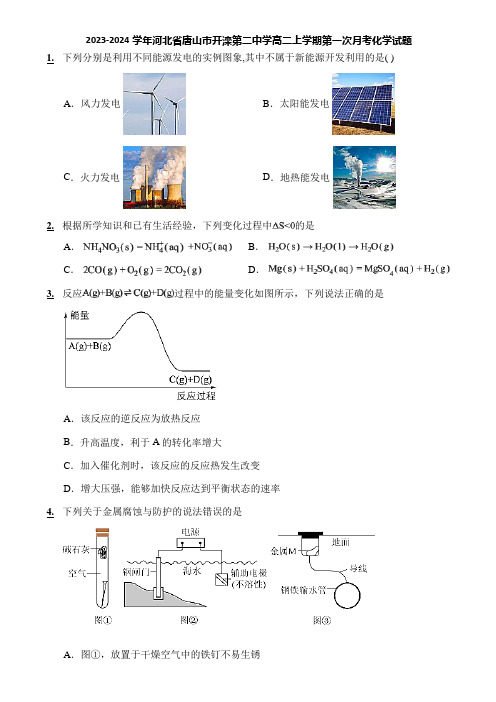
2023-2024学年河北省唐山市开滦第二中学高二上学期第一次月考化学试题1.下列分别是利用不同能源发电的实例图象,其中不属于新能源开发利用的是( )A.风力发电B.太阳能发电C.火力发电D.地热能发电2.根据所学知识和已有生活经验,下列变化过程中的是A.B.C.D.3.反应过程中的能量变化如图所示,下列说法正确的是A.该反应的逆反应为放热反应B.升高温度,利于A的转化率增大C.加入催化剂时,该反应的反应热发生改变D.增大压强,能够加快反应达到平衡状态的速率4.下列关于金属腐蚀与防护的说法错误的是A.图①,放置于干燥空气中的铁钉不易生锈B.图②,若将钢闸门与电源的正极相连,可防止钢闸门腐蚀C.图②,若断开电源,钢闸门将发生吸氧腐蚀D.图③,若金属M比Fe活泼,可防止输水管腐蚀5.某原电池总反应为Cu+2Fe3+=Cu2++2Fe2+,下列能实现该反应的原电池是6.在25℃时,密闭容器中X、Y、Z三种气体的初始浓度和平衡浓度如表所示,下列说法正确的是B.反应可表示为X(g)+3Y(g) 2Z(g),其平衡常数为16C.反应前后压强之比为2:3D.增大压强,该反应平衡会正向移动,此反应的平衡常数增大7.下列关于反应的描述正确的是A.使用催化剂,的平衡转化率增大B.增大浓度,平衡常数K减小C.当时,反应达到平衡状态D.降低反应温度,反应物中活化分子百分数减少,反应速率减慢8.可充电氟镁动力电池比锂电池具有更高的能量密度和安全性,其电池反应为。
下列有关说法不正确的是A.镁为负极材料B.正极的电极反应式为C.电子从镁极流出,经电解质流向正极D.每生成1molMnF 2时转移1mol电子9.下列用来表示物质变化的化学用语中,正确的是A.碱性氢氧燃料电池的负极反应式:B.粗铜精炼时,与电源正极相连的是纯铜,电极反应式为:Cu-2e - =Cu 2+C.用惰性电极电解饱和食盐水时,阴极的电极反应式为:D.在铁制品上镀银时,铁制品与电源正极相连,发生电极反应:Fe-2e - =Fe 2+10.用如图所示装置(X、Y是直流电源的两极)分别进行下列各组实验,则下表中各项所列对应关系均正确的一项是b管中电极反应式是D.D11.某同学设计如图所示实验,探究反应中的能量变化。

河北省石家庄市第二十四中学2023-2024高三上学期第一次月考化学试题1.化学与材料密切相关。
下列关于材料的说法错误的是A.储氢合金是一类储氢材料,可用于解决氢能储存和运输的难题B.“天和”核心舱使用的氮化硼陶瓷属于新型无机非金属材料C.钢是用量最大的合金材料,钢中加入稀土元素可改善钢的性能D.“歼-20”飞机上使用的碳纳米材料是一种新型有机高分子材料2.下列说法不正确的是A.二氧化硫、亚硫酸钠、苯甲酸钠都是食品中常用的脱氧剂B.燕麦粉中添加微量、颗粒极细小铁粉,饮食后可暂时缓解缺铁性贫血C.纯碱不仅是生产玻璃的原料,还可以去除玻璃表面的油污D.硫酸钡不仅可以作白色颜料,还可用于医疗内服药剂“钡餐”3.下列说法不正确的是A.工业制备硫酸的主要设备为沸腾炉、接触室和吸收塔B.工业上制备达98%的粗硅可直接用来生产卫星芯片C.硬度大的新型陶瓷材料碳化硅可用作砂纸的耐磨材料D.某些胶态金属氧化物分散于玻璃中可制造有色玻璃4.下列操作中正确的是A.用水扑灭金属Na、K的燃烧B.焰色试验中用过的铂丝可以用稀硫酸洗净C.丁达尔效应可被用来区分食盐水和淀粉溶液D.若不慎将酸沾到皮肤上,用3%-5%的NaOH溶液冲洗5.下列物质的分类判断正确的是A.汽油属于纯净物B.纯碱晶体属于碱C.漂白粉属于混合物D.NO、为酸性氧化物6.实验室用和浓盐酸制取并回收,下列装置不能达到实验目的的是A.制备氯气B.收集氯气C.过滤除MnO 2D.浓缩滤液7.代表阿伏加德罗常数的值。
下列说法正确的是A.2.4g镁条在空气中充分燃烧,转移的电子数目为B.5.6g铁粉与的HCl的溶液充分反应,产生的气体分子数目为C.标准状况下,与充分反应,生成的分子数目为D.完全溶于所得溶液,微粒数目为8.下列各组离子在相应条件下一定能大量共存的是A.含有较多OH -离子的溶液:、、、B.能使紫色石蕊变红的溶液:Fe 2+、、ClO -、C.澄清透明的溶液:、、、D.能与金属铝反应生成H 2的溶液:、、、9.下列说法不正确...的是A.实验室未用完的钠、钾、白磷需要放回原试剂瓶B.强氧化剂高锰酸钾、氯酸钾、过氧化钠等固体不能随意丢弃,可配成溶液或者通过化学方法将其转化成一般化学品后,再进行常规处理C.如果不慎将酸液滴到皮肤,应该立刻用大量清水冲洗,然后涂上1%的硼酸D.轻微烫伤或者烧伤,可先用洁净的冷水处理,然后涂上烫伤膏药10.用下列装置能达到实验目的的是A.用甲装置灼烧碎海带B.用乙装置蒸发溶液制备无水C.用丙装置制备氧气并控制反应的发生和停止D.用丁装置分离和11.(NH4)2SO4是一种常见的化肥,其溶解度随着温度的升高而增大,某工厂用石膏、NH3、H2O和CO2制备(NH4)2SO4的工艺流程如图:下列说法正确的是A.通入NH 3和CO 2的顺序可以互换B.操作2为将滤液蒸发浓缩、冷却结晶、过滤、洗涤、干燥,可得 (NH 4 ) 2 SO 4C.步骤②中反应的离子方程式为Ca 2+ +2NH 3 +2H 2 O=Ca(OH) 2↓+2NHD.通入的NH 3和CO 2均应过量,且工艺流程中CO 2可循环利用12.下列离子方程式与所给事实不相符的是A.制备84消毒液(主要成分是 ):B.食醋去除水垢中的:C.利用覆铜板制作印刷电路板:D.去除废水中的:13.一种利用有机胺(TBA)参与联合生产碳酸氢钠和二氯乙烷的工艺流程如图所示。
河北省2020-2021年高二上学期化学第一次月考试卷(I)卷姓名:________ 班级:________ 成绩:________一、单选题 (共20题;共40分)1. (2分)下列关于某些社会热点问题的说法中,错误的是()A . 甲醛是某些劣质装饰板材释放的常见污染物之一B . 光化学烟雾的产生与人为排放氮氧化物有关C . 臭氧空洞的形成与氟氯烃或氮氧化物泄漏到大气中有关D . 禁止使用含铅汽油是为了提高汽油的燃烧效率2. (2分) CO(g)与H2O(g)反应生成CO2(g)与H2(g)过程的能量变化如图所示,有关两者反应的说法正确的是()A . 1mol CO2(g)和1mol H2(g)反应生成1molCO(g)和1mol H2O(g)要放出41kJ热量B . 该反应为放热反应C . 反应的热化学方程式是:CO(g)+H2O (g)=CO2(g)+H2(g)△H=+41kJ/molD . CO(g)与H2O(g)所具有的总能量小于CO2(g)与H2(g)所具有的总能量3. (2分)下表中列出了25℃、101kPa时一些物质的燃烧热数据已知键能:C—H键:413.4 kJ/mol、H—H键:436.0 kJ/mol。
则下列叙述正确的是()物质CH4C2H2H2A . C≡C键能为796.0 kJ/molB . C—H键键长小于H—H键C . 2H2(g)+O2(g)=2H2O(g) △H=﹣571.6 kJ/molD . 2CH4(g)=C2H2(g) +3H2(g) △H=﹣376.4 kJ/mol4. (2分) (2016高三上·河北期中) 一定条件下,用甲烷可以消除氮氧化物(NOx)的污染.已知:①CH4(g)+4NO2(g)=4NO(g)+CO2 (g)+2H2O(g)△H1=﹣574kJ•mol﹣1②CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g)△H2=﹣1160kJ•mol﹣1下列选项正确的是()A . CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g)△H=﹣867kJ•mol﹣1B . CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(l)的反应热为△H3 ,则△H3>△H1C . 若用0.2molCH4还原NO2至N2 ,则反应中放出的热量一定为173.4kJD . 若用标准状况下2.24LCH4还原NO2至N2 ,整个过程中转移的电子为1.6mol5. (2分) (2016高一下·眉山期中) 下列各物质中,所有原子或离子都满足最外层8电子结构的是()A . PCl5B . BF3C . BeCl2D . NaClO6. (2分) (2016高一下·右玉月考) 已知下列元素的原子半径为根据以上数据,磷原子的半径可能是()A . 0.08×10﹣10mB . 1.10×10﹣10mC . 1.20×10﹣10mD . 0.70×10﹣10m7. (2分) (2016高二上·厦门期中) 下列叙述正确的是()A . 分子晶体中的每个分子内一定含有共价键B . 原子晶体中的相邻原子间只存在非极性共价键C . 离子晶体中可能含有共价键D . 金属晶体的熔点和沸点都很高8. (2分)(2015·米易模拟) 25℃时,在含有Pb2+、Sn2+的某溶液中,加入过量金属锡(Sn),发生反应:Sn(S )+Pb2+(aq)⇌Sn2+(aq)+Pb(s),体系中c(Pb2+)和c(Sn2+)变化关系如图所示.下列判断正确的是()A . 往平衡体系中加入金属铅后,c(Pb2+)增大B . 往平衡体系中加入少量Sn(NO3)2固体后,c(Pb2+)变小C . 升高温度,平衡体系中c(Pb2+)增大,说明该反应△H>0D . 当溶液中固体质量不再变化时达到平衡状态9. (2分) (2016高二上·赣州期中) 在某2L恒容密闭容器中充入2mol X(g)和1mol Y(g)发生反应:2X(g)+Y(g)⇌3Z(g)△H,反应过程中持续升高温度,测得混合体系中X的体积分数与温度的关系如图所示.下列推断正确的是()A . 升高温度,平衡常数减小B . W,M两点Y的正反应速率相等C . 平衡后充入Z达到新平衡时Z的体积分数增大D . M点时,Y的转化率最大10. (2分) (2016高二上·吉安期中) 下图曲线a表示放热反应X(g)+Y(g)⇌Z(g)+M(g)+N(s)进行过程中X的转化率随时间变化的关系,若要改变起始条件,使反应过程按b曲线进行,可采取的措施是()A . 减压B . 加大X的投入量C . 升高温度D . 减小体积11. (2分) (2018高二上·兰州期中) 在燃烧2.24L(标准状况)CO与O2的混合气体时,放出11.32kJ的热量,最后产物的密度为原来气体密度的1.25倍,则CO的燃烧热为()A . 283 kJ·mol-1B . -283 kJ·mol-1C . -566 kJ·mol-1D . 566kJ·mol-112. (2分) (2016高二上·蕲春期中) 下列热化学方程式正确的是(注:△H的数值均正确)()A . C2H5OH(l)+3O2(g)═2CO2(g)+3H2O(g);△H=﹣1367.0 kJ/mol(燃烧热)B . NaOH(aq)+CH3COOH(aq)═CH3COONa(aq)+H2O(l);△H=﹣57.3kJ/mol(中和热)C . S(s)+O2(g)═SO2(g);△H=﹣269.8kJ/mol(反应热)D . 2NO2═O2+2NO;△H=+116.2kJ/mol(反应热)13. (2分) (2018高一下·广东期末) 分别向2L 0.5mol·L-1的KOH的溶液中加入适量的①浓硫酸、②稀醋酸、③稀盐酸,恰好完全反应的热效应分别为△H1、△H2、△H3 ,下列关系正确的是()A . ΔH1<ΔH3<ΔH2B . ΔH1>ΔH2>ΔH3C . ΔH1>ΔH2=ΔH3D . ΔH1<ΔH2<ΔH314. (2分) (2018高二上·广安期末) 下列说法中正确的是()A . 饱和石灰水中加入一定量生石灰,溶液温度明显升高,pH增大B . AgCl悬浊液中存在平衡:AgCl(s) Ag+(aq)+Cl- (aq),往其中加入少量NaCl粉末,平衡向左移动,溶液中离子的总浓度减小C . AgCl悬浊液中加入KI溶液,白色沉淀变为黄色,证明此条件下Ksp(AgCl)>Ksp(AgI)D . Na2CO3溶液中:2c(Na+)=c(HCO3-)+c(H2CO3)+c(CO32-)15. (2分) (2019高三上·虹口期末) 下列实验操作或现象不能用勒沙特列原理解释的是()A.卤化银沉淀的转化B.配制FeCl3溶液A . AB . BC . CD . D16. (2分) (2017高二上·徐州期末) 对于在一定条件下的密闭容器中进行的反应:A(g)+3B(g)⇌2C(g).下列说法正确的是()A . 压强能够增大反应速率B . 升高温度不能影响反应速率C . 物质A的浓度增大,会减慢反应速率D . 在高温,高压和有催化剂的条件下,A与B能100%转化为C17. (2分) (2017高一下·沭阳期中) 在一定条件下的定容密闭容器中,发生反应2SO2(g)+O2(g)⇌2SO3(g),下列哪种情况,能表明反应达到平衡状态()A . SO3的体积百分含量保持不变B . SO2速率是O2速率的2倍C . SO3的浓度是O2浓度的2倍D . 单位时间内SO2消耗的浓度等于SO3生成的浓度18. (2分) (2016高二上·泰州期中) 下列有关影响化学反应速率的因素的说法错误的是()A . 影响化学反应速率的主要因素是内因,即反应物本身的性质B . 增大反应物浓度,活化分子百分数不变,单位体积内活化分子数增多C . 升高温度,活化分子百分数增大,分子有效碰撞的频率增大,化学反应速率加快D . 使用正催化剂,活化分子百分数不变,但是反应速率加快19. (2分) (2016高一下·襄阳期中) 还原沉淀法是处理含铬(含Cr2O72﹣和CrO42﹣)工业废水的常用方法,过程如下:CrO42﹣ Cr2O72﹣ Cr3+ Cr(OH)3↓己知转化过程中的反应为:2CrO42﹣(aq)+2H+(aq)═Cr2O72﹣(aq)+H2O(1).转化后所得溶液中铬元素含量为28.6g/L,CrO42﹣有10/11转化为Cr2O72﹣.下列说法不正确的是()A . 转化过程中,增大c(H+),平衡向正反应方向移动,CrO42﹣的转化率提高B . 常温下Ksp[Cr(OH)3]=1×10﹣32 ,要使处理后废水中c(Cr3+)降至1×10﹣5mol/L,应调溶液的pH=5C . 若用绿矾(FeSO4•7H2O)(M=278)作还原剂,处理1L废水,至少需要917.4gD . 常温下转化反应的平衡常数K=104 ,则转化后所得溶液的pH=120. (2分) (2016高二上·株洲期中) 各可逆反应达平衡后,改变反应条件,其变化趋势正确的是()A . 向100mL 0.1mol/L醋酸溶液中逐渐加入醋酸钠晶体过程中溶液pH的变化趋势图B . 向FeCl3溶液和KSCN溶液混合后反应达平衡后,向混合液中逐渐加入固体KCl过程中c(Fe3+)的变化趋势图C . 密闭容器中进行N2(g)+3H2(g)⇌2NH3(g)反应达到平衡后,保持恒温恒压条件下,逐渐通入稀有气体Ar的过程中H2的转化率变化趋势图D . 密闭容器中进行CH3OCH3(g)+3H2O(g)⇌6H2(g)+2CO2(g)△H>0达到平衡后,保持恒压条件下,逐渐升高温度过程中CH3OCH3的转化率变化趋势图二、实验题 (共1题;共3分)21. (3分) (2016高二上·铜仁期中) 在一定体积的密闭容器中,进行如下化学反应:CO(g)+H2O (g)⇌CO2(g)+H2(g),其化学平衡常数K和温度t的关系如表:回答下列问题:(1)该反应的化学平衡常数表达式为K=________,该反应为________反应(填吸热或放热).若改变条件使平衡向正反应方向移动,则平衡常数________(填序号)①一定不变②一定减小③可能增大④增大、减小、不变皆有可能(2)能判断该反应是否达到化学平衡状态的依据是________.(a)容器中压强不变(b)混合气体中c(CO)不变(c)v逆(H2)=v正(H2O)(d)c(CO)=c(CO2)(3)将不同量的CO (g)和H2O (g)分别通入到体积为2L的恒容密闭容器中,进行反应CO (g)+H2O (g)⇌CO2(g)+H2(g),得到如表三组数据:①实验B中平衡时H2O (g)的物质的量是________.②通过计算可知,CO的转化率实验A________ 实验B(填“大于”、“等于”或“小于”).③若实验C中达到平衡所需时间 t________3(填“大于”、“等于”或“小于”)三、填空题 (共3题;共11分)22. (5分) (2018高三上·临川期末) 黄铜矿是一种重要的化工原料,主要成分是CuFeS2 ,另外还有少量的氧化铝、二氧化硅及水分,通过化学工艺可获得许多化工产品。