中考化学培优专题练习 构成物质的基本粒子(分子、原子和离子)
- 格式:doc
- 大小:676.50 KB
- 文档页数:10

构成物质的微粒一、选择题1.以下对分子、原子、离子的认识,正确的选项是()A.原子是最小的粒子,不行再分B.温度越高,分子运动速率越快C.分子是保持物质性质的一种粒子D.铝原子与铝离子的化学性质同样2.原子的构成表示图如图,以下表达正确的选项是()A.原子是实心球体B.质子、中子、电子平均散布在原子中C.质子与电子质量相等D.整个原子的质量主要集中在原子核上3.对于原子、分子、离子的说法中,错误的选项是()A.原子不可以直接构成物质B.分子能够保持物质的化学性质C.原子的质量主要集中在原子核上D.金属原子失掉电子会形成阳离子4.氚是氢的一种同位素,氚原子含有 1 个质子和 2 此中子.以下表示图能正确表示氚原子构造的是()A .A B.B C.C D. D5.汤姆森和卢瑟福都对现代原子构造理论做出了巨大贡献.以下对于原子构造的阐述中,不属于他们两人共同看法的是()A.原子很小,但能够分B.原子是构成物质的基本粒子C.原子的电子带负电荷D.原子由原子核和核外电子构成6.以下对分子、原子、离子的认识,正确的选项是()A.原子是全部变化中最小粒子,不行再分B.在化学变化中分子不改变C.温度越高,分子运动越快D.钠原子和钠离子的化学性质同样7.原子核中必定含有的粒子是()A .中子B .质子C.电子D.质子和中子8.以下各样粒子,不带电的是()A .原子核B .质子C.中子D.电子9.碳﹣ 12、碳﹣ 13、碳﹣ 14 都是碳元素的原子,它们的主要差异在于()A .电子数量不一样B .中子数量不一样C.质子数量不一样D.化学性质不一样10.以下说法中正确的选项是()A.原子的质量几乎都集中在原子核中B .生活中常接触到的“高钙牛奶”、“碘盐”中的“钙”、“碘”指的是离子C.往常把PH< 7 的降水称为酸雨D.氯化铵能够与草木灰(含碳酸钾)混淆施用11.跟着经济的发展,汽车已进入我市一般家庭,汽车尾气造成的空气污染日趋严重.为解“”决该问题,一般用尾气催化变换器将汽车尾气中的有毒气体转变为无毒气体,如图表示治理汽车尾气所波及的微观过程.以下说法正确的选项是()A.该反响属于置换反响B .该反响的化学方程式为: 2NO+2CO2CO2+N 2C.该反响前后所有元素的化合价都没有改变D .“”表示的物质溶于雨水能形成酸雨12.在催化剂的作用下,尾气变换器可将汽车中的有毒气体变换成无毒气体,其微观过程如图所示(不一样圆球代表不一样原子).以下说法正确的选项是()A.生成物所有是化合物B.参加反响的两种分子个数比为3: 2C.反响后分子个数变少了D.反响后原子个数变少了13.微粒观是化学基本看法的重要构成部分,从微粒视角认识物质世界是学习化学的重要方法.以下描绘正确的选项是()A.原子是最小的粒子,不行再分B.自然界中全部物质都是由分子构成的C.元素的种类是由原子核内的质子数决定的D.原子最外层电子数的多少决定了原子质量的大小14.某反响的微观表示图(一种小球代表一种元素的原子),则以下说法中正确的选项是()A.参加反响的元素有四种B.反响物和生成物都属于化合物D.该反响属于复分解反响15.如图为某化学反响的微观表示图,此中“ ”和“”表示不一样元素的原子.以下说法错误的是()A.生成物是化合物B.化学反响前后原子个数不变C.生成物的每个分子由三个原子构成D .参加反响的和的个数比为1: 116.雅安“ 4?20地”震造成了部分地域的水污染.以下对水消毒的微观过程剖析正确的选项是()A.参加反响的单质是氧气B.经消毒后的水呈碱性C.反响中,只有一种元素的化合价发生了变化D.该反响的基本种类是置换反响二、填空题17.考古学上经过碳﹣ 14 原子测定文物年月.碳﹣ 14和碳﹣ 12 原子在原子构造上的不一样之处是,它们的原子质量比是.18.如图为某化学反响的微观表示图.(1) X 、 Y 、 Z 中属于化合物的是(选填字母).(2)反响生成 Y 和 Z 的分子个数比是.19.如图是某反响的表示图,请回答以下问题:( 1)图示中属于单质分子的有种;( 2)该反响的基本反响种类为;( 3)化学反响恪守质量守恒定律的原由是反响前后种类和数量不变.20.( 1)在点燃条件下, A 和 B 反响生成 C 和 D.反响前后分子种类变化的微观表示图如图①所示,由此可知:四种物质中属于化合物的是(填图中字母),该反响的基本反响种类为反响.( 2)t℃时,两个装有 100g 水的烧杯中,分别加入不带结晶水的甲、乙物质各 80g,充足搅拌.依据如图②溶解度曲线判断,此时溶液是饱和溶液,甲溶液的溶质质量分数是.( 3)如图③所示a、b、 c、 d 四个点,表示可燃物简单着火的点是点(填字母序号).三、解答题21.历史上相关合成氨的研究成就曾 3 次获诺贝尔奖,如图是与氨气相关的反响微观表示图,请回答以下问题.( 1)该反响属于哪一种基本反响种类?( 2)生成物中氮元素的化合价为价;( 3)经过察看此微观表示图,你还可以获取哪些信息(答出两点即可)?22.据腾讯科技报导:科学家近期研发的“人工树叶”在光照条件下放入水中就能不停产生气泡,将水转变为氢气和氧气.“”如图是人工树叶工作时化学原理的微观表示图.( 1)从能量转变的角度剖析,水分解过程中需要的能量来自于;( 2)从物质分类角度剖析,反响物和产物中属于氧化物的有(填化学式);( 3)“人工树叶”工作时的化学反响方程式;( 4)构成物质的微粒有分子、原子和离子等,水由构成;( 5)水是可贵的自然资源,自来水厂净水时加入明矾的作用是;( 6)划分硬水和软水可用的方法是,生活中降低水的硬度常采纳的方法是.23.制造洁净、环保、便宜的能源也是化学研究的范围之一,近来科学家们研制出了一种氮化镓﹣锑合金,利用它能促使水在太阳光下就能分解获取氢气,且该合金可重复使用.( 1)如图是水分解为氢气和氧气过程中出现的微粒表示图,请按它们在化学变化过程中出现的次序摆列(用图中甲乙丙表示).( 2)氮化镓﹣锑合金在利用太阳光分解水的反响中起作用.参照答案一、选择题1. B ;2. D; 3. A ; 4.A ; 5. B ; 6. C;7. B; 8. C; 9. B; 10.A ; 11. B ;12. C;13. C; 14. C; 15.D ; 16. C二、填空题17.中子数不一样; 7:6;18.X ;1:2;19.2;化合反响;原子; 20.AD ;置换;乙; 44.4%;d;三、解答题21.﹣ 3;22.光; H 2O; 2H 2O2H 2↑+O 2↑;水分子;吸附悬浮杂质,加快沉降;加入肥皂水,遇肥皂水产生泡沫少的是硬水,遇肥皂水产生泡沫多的是软水;煮沸;23.丙甲乙;催化;。

主题三物质的组成与结构第六讲构成物质的几种粒子——分子、原子、离子考情分析导航学业要求年份题型、题序考查内容分值1.能说明分子、原子、离子的区别和联系,能用分子的观点解释生活中的某些变化或现象;能依据化学反应过程中元素不变的规律,推断反应物或生成物的元素组成。
2.能基于真实情境,从元素、原子、分子的视角分析有关物质及其变化的简单问题,并作出合理的解释和判断2023贵州选择4题非选择8题物质的构成分子的特征2分3分2022贵阳选择4题非选择7题物质的构成分子的特征2分1分2021贵阳非选择8题非选择9题物质的构成分子的特征2分1分核心脑图整合知识清单必备【考点一】核外电子排布1.电子层:核外电子运动的特点。
在含有多个电子的原子里,有的电子能量较低,通常在离核较近的区域运动,有的电子能量较高,通常在离核较远的区域运动,为了形象说明,通常用电子层表示。
2.核外电子分层排布原子核外电子最少的有1层,最多有7层,它们按离核的远近分别用K L M N O P Q1 2 3 4 5 6 7表示,第1层离核最近。
3.原子结构示意图:原子结构示意图可以表示出核外电子分层排布的情况。
以氧原子的结构示意图为例:【考点二】离子和原子团1.离子:带电荷的原子或原子团叫做离子,如Mg2+、Cl-等。
2.离子的分类离子{阳离子——带正电荷的原子,如Na+阴离子——带负电荷的原子,如Cl-3.离子符号的意义离子符号前面的化学计量数表示离子个数。
【考点三】相对原子质量(A r)1.定义:以一种碳原子质量的112为标准,其他原子的质量跟它相比较所得到的比,符号为A r。
2.表达式相对原子质量(A r)=一个原子的实际质量一种碳原子的质量×1 123.近似计算相对原子质量≈质子数+中子数。
4.我国科学院院士张青莲为相对原子质量的测定作出了卓越贡献。
【特别提醒】①等质量的不同物质中,其相对原子质量越大的物质中所含原子个数就越少。

初三化学同步与培优辅导分子、原子、离子专题一、知识点过关:1、由分子构成的物质有两类:①共价化合物(非金属与非金属元素组成),如:水[H2O]、甲烷[CH4]、二氧化碳[CO2]等;②有角码的单质,如:氧气[O2]、氮气[N2]、氢气[H2]等2、由原子构成的物质有三类:(没有角码的单质)①金属单质,如:铁[Fe]、铜[Cu]、金[Au]等;②稀有气体单质,如:氦气[He]、氖气[Ne]、氩气[Ar]等③大多数固态非金属单质(碘I2除外),如:碳[C]、硫[S]、磷[P]、硅[Si]等3、由离子构成的物质为离子化合物,如氯化钠、氢氧化钠、硫酸等。
4、构成原子的粒子有:()、()和(),其中()和()构成原子核。
5、在原子里:()数=()数=()数= 原子序数6、以()为标准,其他原子的质量跟他相比较所得的比,叫相对原子质量。
其中基准相当于一个()或一个()或一个()的质量。
7、具有相同()即()的一类原子的总称叫元素。
决定元素种类的是()或(),决定元素化学性质的是()。
8、在分子、原子、质子、中子、电子、原子核等粒子中:①能直接构成物质的粒子有。
②能保持物质化学性质的粒子是。
③显中性的粒子有。
④带正电的粒子有。
⑤带负电的粒子有。
⑥质量最小的粒子有。
⑦参加化学反应一定发生变化的粒子有。
⑧在同一原子里数目相等的是。
⑨质量与氢原子质量相近的是。
9、()叫离子。
()叫阴离子,()叫阳离子。
10、下列物质归类:①水②铁③二氧化碳④臭氧⑤氦气⑥硫粉⑦氯化钠⑧碘⑨硫酸铜⑩C60(1)由原子构成的有:(2)由分子构成的有:(3)由离子构成的有:11、(1)若某元素对应的单质由原子构成,则其元素符号的含义有三种,如:元素符号Na的意义有:①()②()③();(2)若某元素对应的单质由分子构成,则其元素符号的含义有两种,如:元素符号H的意义有:①()②()12、由同种元素组成的物质不一定是纯净物,如()和()、()和()等的混合物。

2024年中考化学专题训练——构成物质的微粒一、选择题1.下列关于原子的叙述中,正确的是A.原子的质量主要集中在原子核上B.原子中质子数一定等于中子数C.原子一定是由质子、中子、电子三种微粒构成D.原子核带正电荷,电子带负电荷,因此原子是显电性的2.下列各图中“”和“”分别表示不同元素的原子,其中表示混合物的是A.B.C.D.3.“结构决定性质”是化学的核心观念。
如图是硫原子结构示意图,下列说法正确的是A.X的值为8B.硫原子的核电荷数为16C.硫原子在化学反中易得到电子,变成阳离子D.硫原子和硫离子的性质完全相同4.化学教会我们从微观角度去认识宏观现象。
下列对生活中现象的解释不合理的是A.春天公园里柳絮纷飞,因为分子在不停地运动B.氮气不如氯气活泼,说明不同分子化学性质不同C.水烧开后易把壶盖顶起,因为温度升高,分子间间隔增大D.一滴水大约有1.6×1021个水分子,说明分子的体积很小5.下列说法中正确的是A.气体的溶解度都随温度的升高而增大B.置换反应中一定有元素的化合价发生改变C.有盐和水生成的反应都属于中和反应D.带电的粒子都是离子6.宏观辨识与微观探析是化学学科的核心素养之一、下列宏观事实的微观解释错误的是A.一滴水中大约含有1.67×1021个水分子—水分子很小B.酒精温度计放入热水中,液柱升高—分子的大小随温度的升高而增大C.将氧气压缩贮存于钢瓶中—分子之间有间隔D.瓜果飘香—分子在不停运动7.液氮可用于制冷。
在氮气由液态变为气态的过程中,下列微观说法正确的是A.分子间间隔变大B.分子的质量变大C.分子的数目增多D.分子的种类改变8.某粒子的结构示意图如图,下列有关说法正确的是A.该粒子在化学反应中容易失去2个电子B.该粒子表示的元素符号是MGC.该粒子表示离子的结构示意图D.该粒子表示的元素位于元素周期表的第二周期9.下列对于宏观事实的微观解释正确的是A.花香四溢的现象说明分子是由原子构成的B.水银温度计放入热水中,水银柱升高,因为原子体积受热变大C.四氧化三铁和二氧化锰物理性质不同,因为不同种分子的化学性质不同D.品红在热水中比在冷水中扩散得更快,说明温度越高分子运动速率越快10.对于图示的理解错误的是(下列物质对应的化学符号:氧化汞HgO、汞Hg、氧气O2)A.原子可构成分子B.分子可以构成物质C.分子是化学变化中的最小粒子D.可用表示氧分子的形成过程二、实验题11.某兴趣小组探究分子的特性时做了以下实验。

构成物质的基本微粒命题分析:中考这样考:1.(2015平凉)斯里兰卡的一家报社由于在油墨里添加了香茅精油,而使印出的报纸散发出一股淡淡的清香,同时又能驱走蚊虫,这说明【D】A.分子很小B.分子之间有间隔C. 分子可以再分D. 分子在不断运动2. (2014平凉)2014年4月14日,科学家约翰·帕特森向人们展示了一款真正意义上曲原子手表,它内置了一个芯片级的铯原子钟,每1000年仅有1秒的误差。
已知这种铯原子核内质子数为55,相对原子质量为133,则其核外电子数为【C】A.188 B.78 C.55 D.233. (2013平凉) 保持水的化学性质的微粒是(填名称)水分子;知识点击:基础梳理考点一:分子与原子考点二、原子与离子微粒 原子离子 阳离子阴离子 结构 质子数=电子数 质子数<,电子数 质子数<电子数 电性 不显电性 带正电 带负电 符号 HNa +、H +Cl - O 2-联系原子可以得到或失去电子转化为离子,离子也可以得到或失去电子转化为原子【记一记】物质的构成考点三:原子的构成由于原子核内质子所带电荷和核外电子的电荷电量相等、且电性相反,因此,整个原子不显电性。
重点解读一:原子结构示意图 以镁原子结构示意图为例二:离子符号表示的意义三、 相对原子质量1.国际上以一种碳原子(碳—12)质量的1/12作为标准,其他原子的质量跟它相比所得的数值,就是这种原子的相对原子质量。
一个镁离子带两个单位的正电荷 两个镁离子2.计算公式:某原子的相对原子质量=该原子的实际质量/(碳—12原子质量的1/12)3.相对原子质量=质子数+中子数典型例题:1.下列关于原子、分子的说法错误的是(A)A.分子可以构成物质,而原子只能构成分子B.在化学变化中,分子可以分成原子,而原子不能再分C.在原子中,质子等于核外电子数D.分子是保持物质化学性质的最小粒子【解析】明确原子和分子的概念最为重要。


人教版2020年中考专项训练-构成物质的几种粒子——分子、原子、离子(1)一.选择题1.下列对一些事实的解释中,不合理的是()选项事实解释A 食盐是咸的,白糖是甜的不同种物质的分子性质不同B 盐酸、稀硫酸都能使紫色石蕊试液变红它们所含的阳离子全部都是H+C 将墨汁滴入一杯清水中,清水很快变黑分子在不断运动D 25 m3的氧气可以装入0.024 m3的钢瓶中氧分子的体积变小2.用分子观点解释“干冰升华”,下列说法错误的是()A.分子不停地运动B.分子间间隔变大C.分子质量变小 D.分子本身不变3.下列有关分子、原子、离子的说法正确的是()A.分子是保持物质性质的最小粒子B.物质都是由分子构成的C.原子是由原子核、中子、电子构成的D.原子得失电子后形成离子4.取一滤纸条,等间距滴紫色石蕊试液,然后装入玻璃管中(如图所示),两端管口同时放入分别蘸有浓氨水和浓盐酸的棉球,几秒后观察到图示现象。
下列说法不正确的是()A.氨水的pH大于7 B.酸、碱能使酸碱指示剂显示不同颜色C.氨分子和氯化氢分子在不断运动 D.所有分子的运动速率都相等5.以下事实,不能说明分子间有间隔的是()A.海绵能吸水B.用打气筒能将气体压缩C.物体有热胀冷缩的现象D.酒精和水混合后,总体积小于两者的体积之和6.对分子和原子两种微粒的叙述正确的是()A.原子构成分子,物质只能由分子构成B.同种原子可能构成不同的分子C.化学变化中分子数目一定发生变化D.分子质量一定大于原子质量7.甲、乙是两种粒子的结构示意图,下列说法正确的是()A.甲是阳离子B.乙是阴离子C.甲、乙属于不同种元素D.甲、乙都属于金属元素8.水电解的过程可用下图表示,微粒运动变化的先后顺序是()A.①②③④ B.④①③② C.①②④③ D.①④③②9.下列关于原子结构的叙述,正确的是()A.一切原子的原子核都由质子和中子构成B.在原子中,核电荷数一定等于质子数或核外电子数C.原子核内质子数一定等于中子数12.如图是元素周期表中第三周期部分元素的微粒结构示意图,依照此示意图,下列描述正确的是()A.示意图①、②、③、④表示的全部是原子结构B.示意图②的核电荷数x=12C.示意图④若表示的是离子结构,则它的最外层电子数y=7D.示意图①的最外层电子数为8,所以它是稀有气体元素二、填空题13.用微粒的观点解释下列现象:(1)今年我国要求“公共场所全面禁烟”非吸烟者往往因别人吸烟而造成被动吸烟,这是因为;(2)夏天钢轨间的缝隙变小:。

6.构成物质的基本粒子【考点梳理】1.了解构成物质的三种基本粒子:分子、原子和离子。
2.会用分子、原子的观点解释物理变化、化学变化和常见的生活现象。
3.会进行微观粒子组成的相关判断。
【考点精析】例1.下列关于分子、原子、离子的说法正确的是()A.分子是保持物质性质的一种离子B.物体有热胀冷缩现象,主要是因为物体中粒子大小随温度的改变而改变C.分子的质量总比原子的质量大D.分子、原子、离子都可以直接构成物质【答案】D【解析】本题考查的是学生对分子、原子、离子的了解。
分子是保持物质化学性质的一种粒子,A错误。
物体有热胀冷缩现象,主要是因为物体中粒子间间隔随温度的改变而改变。
B 错误。
分子的质量不一定比原子的质量大,分子由原子构成,分子一定比构成它的原子的质量大,C错误。
分子、原子、离子都可以直接构成物质,D正确。
【考点精炼】基础达标1.在H2、H2SO4、H2O、H2O2四种物质的分子中都含有()A.2个氢元素B.氢原子C.1个氢分子D.氢气2.从分子和原子的角度分析并解释下列事实,其中不正确的是()A.20mL酒精和20mL水混合后体积小于40mL—分子间存在间隔B.物体的热胀冷缩—分子的大小发生变化C.氧化汞分解成汞和氧气—分子还可以再分D.一滴水中大约有1.67×1021个水分子--分子很小3.不能决定元素种类的是()A.质子数B.核电荷数C.原子序数D.核外电子数4.下列说法中正确的是()A.原子不能再分B.汞分子聚集成金属汞C.原子得或失电子可以变成离子D.元素的化学性质主要由核外电子数决定5.硒的是人体必需的一种微量元素,严重时缺硒有可能诱发皮肤疾病。
已知硒的原子序数为34,质子数与中子数之和为79。
下列有关硒原子的说法中不正确的是()A.核外电子数为34 B.核电荷数为79 C.质子数为34 D.中子数为456.下列化学符号中只表示微观意义的是()A.H2B.H C.2H2D.Fe能力提升7.下列对化学符号中数字“2”所表示的意义,描述不正确的是()A.2CO表示2个一氧化碳分子B.Mg2+表示镁元素的化合价为+2价C.H2O表示一个水分子中含2个氢原子D.2SO42-中前面的2表示2个硫酸根离子8.下列关于四种粒子的结构示意图的说法中正确的是()A.①③是不同种元素B.②表示的是非金属元素C.②③的化学性质相似D.①④表示的是离子9.朝核问题引发了国际关注,核问题的关键是如何利用核能.已知某种核原料的原子核中含有1个质子和2个中子,下列说法错误的是()A.该原子是一种氢原子B.该原子核外有3个电子C.该原子的核电荷数为1 D.该原子的相对原子质量为310.下列微粒中,质子数与电子数相等的是()A.Na+B.Cl-C.OH- D.CO211.现有某粒子的结构示意图为,请根据下列几种情况回答问题.(1)如果其中y=1,则x= ;(2)如果该粒子是一个带2个单位负电荷的阴离子,则该粒子的化学符号为;(3)如果该粒子是一个带2个单位正电荷的阳离子,则该粒子的化学符号为;(4)如果该粒子是一个原子,则x与y的关系是;(5)若该粒子为电中性,则y的最大值为;(6)若x=12,则该粒子对应的元素在化合物中的化合价为;(7)若x=17,且该粒子为食盐的一种组成微粒,则该粒子的化学符号为;(8)若x=16,则y= ,微粒的化学符号为。

总复习:构成物质的几种粒子——分子、原子、离子【考纲要求】1.理解分子、原子、离子的概念,知道分子、原子、离子等都是构成物质的微粒;了解微粒的基本性质,能用微粒观点解释某些常见的现象。
2.知道原子的构成,理解原子结构示意图和离子结构示意图的关系和含义;知道同一元素的原子和离子可以互相转化。
【知识网络】概念:保持物质化学性质的最小微粒分子体积和质量都很小特征分子间有一定的间隔构构分子在不停的运动成成概念:化学变化中的最小微粒特征:同分子的特征相似物质原子质子(带正电)构成原子核(带正电)结构中子(不带电)构核外电子(带负电)成概念:带电的原子或原子团阳离子离子分类阴离子【考点梳理】考点一、分子(专题课堂《物质构成的奥秘》一、2)1.概念:分子是保持物质化学性质的最小粒子(由分子构成的物质)。
“性质”是指化学性质。
分子有什么化学性质,由这种分子聚集成的物质就有什么化学性质。
如一氧化碳分子能与氧分子反应生成二氧化碳分子,所以一氧化碳有可燃性。
分子不能保持物质的物理性质,因为物质的物理性质是由分子的聚集状态决定的,单个分子不能表现物质的物理性质。
如水分子间距离很小时水呈液态,水分子间的距离较大时水呈气态,水分子规则排列,不能自由移动时水呈固态(冰)。
分子是构成物质的一种粒子,有些物质直接由原子或原子团构成。
2.分子基本性质:(1)分子在不停地运动。
(2)质量和体积都很小。
1个水分子的质量大约是3×10-26kg,一滴水(约0.05 g)中约有1.7×1021个水分子。
(3)分子间有间隙,且不断运动,运动速率与温度有关。
用此性质可解释一些物理现象,如热胀冷缩、分子扩散、蒸发等。
(4)同种物质的分子化学性质相同,不同种物质的分子化学性质不同。
如氢分子能与氧分子反应,而水分子不能与氧分子反应。
【要点诠释】用分子理论解释物理、化学现象:1.物理变化和化学变化:由分子构成的物质在发生物理变化时,分子本身没有变化,如水加热变成水蒸气,水分子本身没变;通电氢气+氧气,在此反在发生化学变化时,分子本身发生了变化,变成了其他物质的分子,如水−−−→应中,水分子变成了氢气分子和氧气分子。

微专题一分子、原子、离子和元素角度1 构成物质的微粒1.下列物质,由原子直接构成的是(B)A.水 B.铜 C.氢气 D.氯化钠【解析】水、氢气是由分子构成的;铜属于金属单质,是由铜原子直接构成的;氯化钠是由钠离子和氯离子构成的。
2.保持过氧化氢化学性质的最小粒子是(D)A.氧原子 B.氢原子C.氧分子 D.过氧化氢分子【解析】由分子构成的物质,分子是保持物质化学性质的最小微粒;因此保持过氧化氢化学性质的最小粒子是过氧化氢分子。
3.下列关于分子、原子、离子的说法错误的是(D)A.同种原子可能构成不同种分子B.水和酒精的化学性质不同,是因为它们的分子构成不同C.在化学变化中,分子可以改变为其他物质的分子D.核电荷数少于核外电子数的一定是阳离子【解析】同种原子可能构成不同种分子,例如氧原子可以构成氧分子和臭氧分子,A正确;水是由水分子构成的,酒精是由酒精分子构成的,同种分子化学性质相同,不同种分子化学性质不同,所以水和酒精的化学性质不同,是因为它们的分子构成不同,B正确;在化学变化中,分子分为原子,原子再组合成其他物质的分子,C正确;电子带负电,核电荷数少于核外电子数的一定是阴离子,D错误。
4.(2021·丹东中考改编)对下列事实的微观解释错误的是(A)A.干冰升华——分子的体积变大B.氧气支持燃烧,氮气不支持燃烧——构成物质的分子不同C.中药房里弥漫着中药味——分子是不断运动的D.氮气可压缩储存于钢瓶中——分子间有间隔【解析】干冰升华是因为分子间隔变大造成的,故A错误;由分子构成的物质,分子是保持物质化学性质的最小粒子,氧气和氮气的化学性质不同,是因为构成氧气和氮气的分子不同,故B正确;中药房里弥漫着中药味是因为中药气味中的分子运动到空气中去,四处扩散,故C正确;分子间存在着间隔,压强增大,分子间隔变小,所以氮气可压缩储存于钢瓶中,故D正确。
5.(2021·深圳期中)一定条件下,水在密闭容器里的冷却过程中,温度和时间的关系如图所示。

中考化学专题训练《分子、原子、离子》一选择1.以下有关分子、原子、离子和元素的说法正确的选项是() A.原子不可以直接构成物质B.分子是化学变化中最小的微粒C.决定元素化学性质的是原子的电子数D.原子获得或失掉电子形成离子2.从分子、原子角度对以下现象和变化的解说中,合理的是() A.花香四溢——分子很小,质量也很小B.热胀冷缩——温度变化,分子或原子大小发生变化C.滴水成冰——温度降低,分子间隔变小、运动停止D.食品变质——分子发生变化,物质性质发生变化3.以下有关微粒的表达错误的选项是()A.金刚石由碳原子构成B.水蒸发为气体后分子间隔增大C.氯化钠晶体由分子构成D.化学反响前后,原子个数必定不变4.元素周期表是按以下哪一项对元素进行编号的()A.按元素原子质量的大小进行编号B.按元素原子的核电荷数递加的次序编号C.按元素发现的先后次序编号D.按元素原子核内中子数递加的次序编号5.碳 12、碳 13、碳 14 都是碳元素的原子,它们的主要差异在于 () A.电子数不一样B.中子数不一样C.质子数不一样D.化学性质不一样6、用分子的有关知识解说以下生活中的现象,此中错误的选项是()A.“酒香不怕小巷深”,说明分子在不断运动B.热胀冷缩,说明分子的大小随温度起落而改变C.10mL 酒精和 10mL 水混淆后体积小于20mL,说明分子间有缝隙D.湿衣服在夏季比冬季简单晾干,说明分子的运动速率随温度高升而加速7、分子与原子的实质差异在于()A.分子是构成物质的一种粒子B.分子在不断地运动着C.分子之间有缝隙D.在化学变化中,分子可分,原子不行分8室温时将少许干冰放入塑料袋中并密封,塑料袋会迅速鼓起,其原因是()A.分子的体积变大B.分子分解变为了原子C.分子的间隔变大D.分子由静止变为运动9、以下对于如图两种原子构造表示图的说法中不正确的选项是()A.①②都拥有三个电子层B.②表示的元素属于非金属元素C.①在化学变化中简单失掉电子形成阴离子D.①和②能够形成一种化合物MgCl210、以下粒子中属于原子,且拥有稳固构造的是()A.B.C.D.11、以下图是钙原子的构造表示图,以下有关钙原子的表达中不正确的是()A.该原子第三电子层有8 个电子,因此化学性质比较稳固B.该原子在化学反响中易失掉 2 个电子,进而该元素在化合物中常显+2 价C.该原子核外电子数、核电荷数、质子数均为20D.该原子形成的离子符号为Ca2+12、由 X、Y 两种元素构成的化合物,其相对分子质量为76,已知 Y 元素核内有 8 个质子和 8 此中子,X 元素核内质子数和中子数分别比Y 元素少 1 个,则该化合物化学式为()A. X2Y5B.X2Y3C.XY2 D.X2Y13、以下物质中由原子构成的是()A.汞 B.水 C.氯化钠D.氢气14、以下物质由离子构成的是()A. Cu B.NaCl C.CO2D.金刚石15、以下表达中不正确的选项是()①原子是化学变化中的最小粒子②原子是不可以再分的粒子③全部物质都是由原子直接构成的④全部原子核都是由质子和中子构成的⑤原子不显电性⑥原子之间有间隔A.①和②B.②③和④C.③和⑤D.③和⑥)16 以下对于Na、Na+两种粒子的判断中,正确的选项是(①核电荷数同样;②核外电子数相等;③Na+比 Na 稳固;④质量几乎相等;⑤质子数相等。
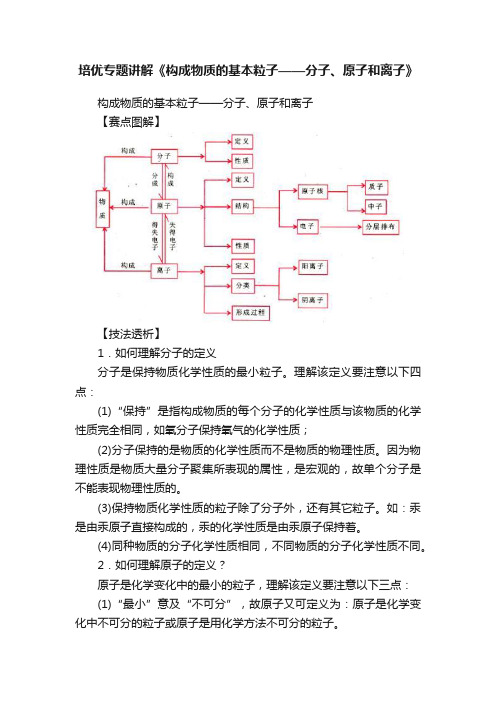
培优专题讲解《构成物质的基本粒子——分子、原子和离子》构成物质的基本粒子——分子、原子和离子【赛点图解】【技法透析】1.如何理解分子的定义分子是保持物质化学性质的最小粒子。
理解该定义要注意以下四点:(1)“保持”是指构成物质的每个分子的化学性质与该物质的化学性质完全相同,如氧分子保持氧气的化学性质;(2)分子保持的是物质的化学性质而不是物质的物理性质。
因为物理性质是物质大量分子聚集所表现的属性,是宏观的,故单个分子是不能表现物理性质的。
(3)保持物质化学性质的粒子除了分子外,还有其它粒子。
如:汞是由汞原子直接构成的,汞的化学性质是由汞原子保持着。
(4)同种物质的分子化学性质相同,不同物质的分子化学性质不同。
2.如何理解原子的定义?原子是化学变化中的最小的粒子,理解该定义要注意以下三点:(1)“最小”意及“不可分”,故原子又可定义为:原子是化学变化中不可分的粒子或原子是用化学方法不可分的粒子。
(2)“最小”、“不可分”是有条件的,即“在化学变化中”这个条件,也就是说:原子的“最小”和“不可分”是相对于化学变化而言的,因为从结构上看,原子可分成原子核和核外电子。
(3)原子在化学反应中不可分,不是说原子在化学反应中不发生任何变化。
在化学变化中,原子的核外电子,尤其是最外层电子数会发生变化。
3.怎样认识原子的结构(1)原子的结构(2)在原子中,由于原子核带正电,带的正电荷数(即核电荷数)与核外电子带的负电荷数(数值上等于核外电子数)相等,电性相反,所以原子不显电性。
由此得出,质子数一核电荷数一电子数。
(3)不同种类的原子,核内的质子数不相同,核外电子数也不相同。
(4)相对来说,原子里有很大的空间,电子在其中作高速运动。
(5)原子的质量主要集中在原子核上。
4.相对原子质量的计算方法(1)相对原子质量=某原子的质量碳原子质量的1/12(2)相对原子质量与原子核内微粒的关系:相对原子质量(近似值)=质子数+中子数5.如何区分原子结构示意图和离子结构示意图?(1)原子或离子结构示意图的画法:画圆圈,标核电,划弧线,中间数字一条线。

二、物质科学(化学)第18讲构成物质的微观粒子知识梳理【复习重点】一、构成物质的微观粒子1.原子、离子、分子、电子、质子等微观粒子,既可表示种类又可表示个数。
原子、离子、分子都是构成物质的粒子。
金属单质、稀有气体等物质由原子直接构成;多数非金属单质、非金属与非金属形成的化合物由分子构成,既有金属元素又有非金属元素的离子化合物由离子构成。
2.原子是化学变化中的最小粒子。
原子由带负电荷的核外电子和带正电荷的原子核构成。
原子核由带正电荷的质子和不带电荷的中子构成。
普通氢原子的原子核中只有质子而无中子,即氢原子的原子核就是一个质子。
在不显电性的粒子(原子、分子)中:核电荷数=质子数=核外电子数。
3.由分子构成的物质,其分子是保持物质化学性质的最小粒子。
注意:有些物质是由原子直接构成的(如金刚石以及各种金属等),这类物质的化学性质是由原子来保持的。
分子是由原子构成的。
如:1个水分子由2个氢原子和1个氧原子构成。
在化学变化中,分子可分为更小的粒子——原子,原子不可再分。
物质发生物理变化时,只是分子间的间隔发生变化,而分子本身没有发生变化;物质发生化学变化时,分子被破坏,分子本身发生变化。
在一切化学反应中,反应前后的元素的种类、原子的种类、原子的数目和原子的质量都不变,反应前后的各物质的质量总和必然相等。
4.原子团:由两种或两种以上元素的原子构成,在化学反应中通常以整体参加反应而不再拆分的原子集团。
原子团只是化合物中的一部分,不能脱离物质单独存在,因此含原子团的物质必定有三种或三种以上的元素,两种元素组成的物质不含原子团。
原子团在化学反应中可再分为更小的粒子——原子。
5.离子:带电的原子或原子团叫离子。
带正电的叫阳离子,带负电的叫阴离子。
对于一个离子:质子总数=核电荷总数=电子总数±带电量离子符号的写法:离子的电荷数标在右上角,电荷的数值等于该离子对应的化合价。
二、核外电子排布的规律和原子结构示意图1.核外电子排布的规律:原子序数1~18的元素,核外电子从里往外排,第一层最多排2个电子,第二、三层最多容纳8个电子。


初三化学构成物质的基本微粒基础练习4 单元知识网络1.构成物质的差不多微粒有分子、原子离子。
2.原子的构成4.相对原子质量:以一种碳原子质量的1/12作为标准,其他原子的质量与这一基准的比值,称为这种原子的相对原子质量。
某原子的相对原子质量运算方法如下121⨯=碳原子质量某原子质量相对原子质量5.相对分子质量等于构成分子的各原子的相对原子质量的总和。
指点迷津已知某原子中共有82个粒子,其中有30个粒子不带电,则该原子的核电荷数是多少?相对原子质量是多少?该原子是什么原子?⎪⎩⎪⎨⎧⎩⎨⎧核外电子中子质子原子核原子⎩⎨⎧+===中子数质子数相对原子质量核外电子数质子数核电荷数原子中思路分析:因为原子是由质子、中子、核外电子三种微粒构成的,其中中子不带电,因此30个粒子明显是中子,余下的粒子共52个是质子数与电子数之和,又因为在原子中质子数等于电子数,故质子数与电子数差不多上26,即该原子的核电荷数为26。
相对原子质量约为质子数与中子数之和,因此相对原子质量是56,该原子为铁原子。
基础评判1.以下生活、学习体会,不能讲明分子之间有间隔的是()A.打气筒能把空气压入自行车胎内B.酒精和水混合,总体积变小C.物体有热胀冷缩现象D.海绵吸取水分2.据报道,上海某医院正研究用放射性碘治疗肿瘤,这种碘原子的核电荷数是53,相对原子质量是125,下列关于这种原子的讲法错误的是()A.质子数是53 B.核外电子数是53C.中子数是53 D.质子数与中子数之和是1253.下列讲法中,不正确的是()A.原子分子和离子差不多上构成物质的微粒B.原子差不多上由原子核和核外电子构成的C.分子和原子差不多上持续运动的D.任何原子核差不多上由质子和中子构成的4.能讲明分子在化学变化中可再分的事实是()A.湿衣服放在不处晒干B.水通电生成氢气和氧气C.硫加热变成硫蒸气D.大块冰糖变成小块冰糖5.下列物质由分子构成的是()A.二氧化碳气体B.铁C.氯化钠晶体D.氩气6.下列各种物质中只含有一种分子的是()A.空气B.液化气C.冰水D.糖水7.某原子失去电子后,关于该原子的讲法正确的是()A.该原子带了正电B.该原子的质子数发生了变化C.该原子带了负电D.该原子的相对质量有了较大的改变正电子、负质子等差不多上反粒子。

1.[2018•兰州] 下列关于分子和原子的说法错误的是 ( )A.分子和原子都能直接构成物质B.相同的原子可以构成不同的分子C.气体可以压缩是由于分子之间存在间隙D.分子可分,原子不可分2.[2017•温州] 5月9日,相关机构发布等四种元素的中文名称, 元素的核电荷数为118,相对原子质量为294,则其原子核外电子数为 ( )A.118B.176C.294D.4123.[2018•济宁] 从分子、原子角度对下面一些现象和变化的解释,合理的是 ( )A.花香四溢——分子很小,质量也很小B.热胀冷缩——温度变化,分子或原子大小发生变化C.滴水成冰——温度降低,分子间隔变小,停止运动D.食品变质——分子发生变化,分子性质发生变化4.[2018•十堰改编] 有关分子和原子的说法中错误的是 ( )A.分子的质量和体积不一定比原子大B.电解水过程中最小的粒子是氢原子和氧原子C.同种分子构成纯净物,不同种分子构成混合物D.发生物理变化时,分子间的距离一定保持不变5.[2018•淮安] 化学的特征是在原子、分子水平上研究物质和创造物质。
请从微观角度回答:(1)“遥知不是雪,为有暗香来”。
花香入鼻的原因是。
图Z6-1(2)由图Z6-1甲推知水和过氧化氢化学性质不同的原因是。
(3)由图乙可知,水分解过程中,没有发生变化的微粒是(填微粒符号)。
(4)N(NO2)3是一种新型火箭燃料,N(NO2)3中N、O原子个数比是。
|能力提升|6.同一原子中,下列说法错误的是 ( )A.质子和电子的数目相同B.原子和中子的电性不同C.原子核和电子的质量不同D.原子核和原子的体积不同7.[2018•新疆] 如图Z6-2是探究分子运动的实验。
下列现象与结论错误的是 ( )图Z6-2A.浓盐酸具有挥发性B.分子在不断运动C.乙烧杯溶液的颜色会改变D.乙、丙烧杯内溶液的颜色会改变8.[2018•滨州] 电解水的过程可用图Z6-3表示,粒子运动变化的先后顺序是 ( )图Z6-3A.①②③④B.①②④③C.④③①②D.④①②③9.[2017•桂林] 请用微粒的知识回答下列问题。

专题05 构成物质的微粒一、新课标的要求:1.认识物质的微粒性,知道分子、原子、离子等都是构成物质的微粒。
2.能用微粒的观点解释某些常见的现象。
3.知道原子是由原子核和核外电子构成的。
4.知道原子可以结合成分子、同一元素的原子和离子可以互相转化,初步认识核外电子在化学反应中的作用。
二、考情分析:1、考查情况:化学是在分子、原子的基础上研究物质的组成、结构、性质及其变化规律的一门基础的自然学科。
从此可以看出构成物质的微粒在化学学科中的重要地位。
构成物质的微粒是各地中考必考的一个知识点,也是中考化学的热点内容。
2、考查形式:纵观近几年的各地中考试题,不难发现该知识点考查形式有:物质的微粒性、微粒基本性质、原子的构成、三种微粒的联系与区别等。
从题型上来说,可主要有选择和填空题。
从题目形式上说,有识记形、理解形、判断正误形和推断推理形。
3、命题方向:该考点的命题方向主要是通过创设相关问题情景或图表信息等,既可以考查学生对相关知识点的理解和掌握情况;还可以去考查学生分析、解答相关的实际问题的能力等。
4、试题难度:由于该知识点涉及微观知识,比较抽象且琐碎,是学生在理解上有一定难度的知识,使得分的难度增加。
试题难度一般为中等或难等的题目。
☆知识梳理☆一、:构成物质的微粒构成物质的基本微粒有三种:分子、原子和离子。
1、由原子构成的物质有:种类示例构成微粒物质符号符号书写特点①金属单质铜铁铜原子铁原子CuFe元素符号②大多数的固态非金属单质(常温)石墨红磷碳原子磷原子CP③稀有气体氦气氩气氦原子氩原子HeAr2、由分子构成的物质有:种类示例构成微粒物质符号①大多数的气态单质(常温)氧气氧分子O23、由离子构成的物质:注意:1、上述规律对初中的大多数物质起作用。
2、混合物的构成微粒要按其中所含物质的成分来分析。
二、微粒的基本性质:构成物质的微粒有以下性质:1、微粒很小(质量小、体积小)2、微粒时刻不停地做规则运动(运动速率与温度成正比)3、微粒间有间隔(间隔与温度成正比,与压强成反比)4、同种微粒,化学性质相同注意:1、微粒时刻不停地做规则运动,温度高时运动速率快;温度低时运动速率慢,但不是不运动。
《构成物质的基本粒子——分子、原子和离子》1.小华用凉开水养鱼,不久鱼儿全死了。
下列解释合理的是 ( )A.凉开水中几乎不含氧元素B.凉开水中几乎不含氧原子C.凉开水中几乎不含水分子D.凉开水中几乎不舍氧分子2.用分子的观点对下列常见现象的解释,错误的是 ( )A.花香四溢——分子在不停运动B.热胀冷缩——分子的大小随温度变化而改变C.酒精挥发——分子间距增大D.氢气和氧气反应生成水——分子发生了变化3.下列粒子中属于阴离子的是 ( )A B C D4.能证明分子在化学变化中可分的是 ( )A.打开汽水瓶,有气体逸出B.10 mL水与10mL酒精混合,体积小于20mLC.加热氧化汞得银白色汞与氧气D.水蒸发为水蒸气5.下列关于分子和原子的说法中,正确的是()A.原子由质子与中子构成,原子呈电中性B.保持水的化学性质的粒子是氢原子和氧原子C.分子的质量总比原子的质量大D.原子可以构成分子6.有一种粒子的结构示意图为,下列说法不正确的是 ( ) A.该粒子具有稳定结构B.该元素是一种金属元素C.该粒子是一种阳离子D.该元素的原子核外有两个电子层7.下列叙述错误的是 ( )A.分子、原子和离子都能直接构成物质B.原子中原子核与核外电子的电量相等,电性相反,因而原子不显电性C.决定原子质量大小的主要是质子和电子D.原子如果得到或失去电子就变成离子8.甲原子与乙原子的质量比为a:b,而乙原子与碳12原子的质量比为c:d,则甲原子的相对原子质量为 ( )A.12ac/bd B.bc/12ac C.12bd/ac D.ab/12beA .通过化学变化一定能改变物质的性质B .改变物质的性质一定要通过化学变化C .在化学变化中原子的电子数不会发生改变D .在任何变化中原子的核都不会发生改变10.1999年度诺贝尔化学奖授予了开创“飞秒(10-15s )化学”新领域的科学家,使运用激光光谱技术观测化学反应时分子中原子运动成为可能。
你认为该技术不能观测到的是( )A .原子中原子核的内部结构B .化学反应中原子的运动C .化学反应中生成物分子的形成D .化学反应中反应物分子的分解11.如图所示,在钠与氯气的反应中,每个钠原子失去1个电子,成为1个钠离子;每个氯原子得到1个电子,成为1个氯离子;钠离子与氯离子结合形成氯化钠。
因为1个电子的质量大约为1个质子或中子质量的11836,故原子的质量几乎都集中 在原子核上。
若用r 、m 分别表示微粒的半径和质量,以“<”或“>”或“≈”填空。
(1)m(Na)_______m(Na +) (2)r(Cl)_______r(Cl -)(3)r(Na)_______r(Cl) (3)r(Na +)_______r(Cl -)12.某元素原子结构示意图如图所示:X 的数值是_______ ,根据元素原子结构示意图,不能直接获得的信息是_______(填编号)。
①核电荷数 ②相对原子质量 ③电子层数 ④最外层电子数13.我国科学家在1993年首次利用超真空扫描隧道显微镜技术,在一块晶体硅(由硅原子构成)的表面直接移动硅原子写下了“中国”两字。
下列说法中,正确的是 ( )A .在上述操作中没有任何变化B .这两个汉字是当时世界上最小的汉字C .此技术说明在化学变化中原子可以再分D .这标志着我国科学家已进入了操纵原子的阶段14.两位美国科学家彼得·阿格雷和罗德里克·麦金农,因为发现细胞膜水通道,以及对离子通道结构和机理研究作出的开创性贡献而获得2003年诺贝尔化学奖。
他们之所以获得诺贝尔化学奖而不是生理学或医学奖是因为( )A .他们的研究和化学物质水有关B .他们的研究有利于研制一些神经系统疾病和心血管疾病的药物C .他们的研究深入到分子、原子的层次D .他们的研究深入到细胞的层次15.已知R 元素的相对原子质量m 与其原子核内的质子数和中子数之和在数值上相等。
若R 2+核外有x 个电子,则其原子核内的中子数为 ( )A.m-x+2 B.m+x-2 C.m-x-2 D.m+x-216.质子和中子都是由U夸克和d夸克组成,U夸克带电量为(2/3)e,d夸克带电量为(-1/3)e,e为基元电荷。
下列论断可能正确的是 ( )A.质子由1个U夸克和1个d夸克组成,中子由1个U夸克和2个d夸克组成B.质子由1个U夸克和2个d夸克组成,中子由2个U夸克和1个d夸克组成C.质子由2个U夸克和1个d夸克组成,中子由1个U夸克和2个d夸克组成D.质子由2个U夸克和1个d夸克组成,中子由1个U夸克和1个d夸克组成17.1911年著名物理学家卢瑟福等人为探索原子的内部结构进行了下面的实验。
他们用一束带正电的、质量比电子大得多的高速运动的a粒子轰击金箔,发现:①大多数a粒子能穿透金箔而不改变原来的运动方向;②一小部分a粒子改变了原来的运动方向;③有极少数a粒子被弹了回来。
由此你能推测出关于原子内部结构的信息是(任写三点):(1)_____________________;(2)_____________________;(3)_____________________.18.根据如下2005年十大科技进展的报道,回答问题:材料1:法国科学家利用特种显微仪器,让一个分子做出了各种动作,这一成果使人类能精确控制单个分子运动,进而开发出分子机器人。
材料2:中科院上海硅酸盐研究所研制出了“药物分子运输车”,这种分子装载满药物后,被引导到疾病靶点释放药物,对疾病进行高效治疗。
(1)材料1和2研究的粒子是_______;构成物质的粒子还有______________.(2)分析上述材料,谈谈你对“分子总是在不断运动着”的新认识:_______.(3)在阿西莫夫所写的科幻小说《梦幻航行》中,人被缩小到细胞般大小,在人体内经历了梦幻般的体验。
试想,如果你被缩小到一个原子般大小,把你放到水里,你会看到的景象是(请至少写两点)___________________________________.19.1803年10月,在曼彻斯特的文学和哲学学会的一次集会上,英国科学家道尔顿讲述了他的原子论,主要论点如下:(1)一切物质都由不可再分的微粒构成,这种微粒叫做原子。
原子在一切化学变化中都保持它的不可再分性;(2)同一元素的原子,各方面的性质,特别是质量,都完全相同;不同元素的原子重量不同。
原子的相对重量(原子量)是每一种元素的特征性质。
(3)不同元素的原子是以简单的整数比相化合。
请利用所学知识判断,道尔顿的上述论点中有哪些错误。
_____________________.20.反物质是由反粒子组成的物质。
所有的粒子都有相应的反粒子,反粒子的特点是其质量、寿命等与相应的粒子相同,但电荷、磁矩等与之相反,如反氢原子的结构示意图为反粒子一旦与相应的粒子碰撞,如电子碰到反电子,就会立即“湮灭”为其他物质。
据最新报导,欧洲核子研究中心近日已成功地制造出约5万个低能量状态的反氢原子,这是人类首次在受控条件下大量制造的反物质。
试回答下列问题:(1)质子与反质子相碰撞而“湮灭”是化学变化吗?____________________________,理由是__________________________________________.(2)请你描述一下反氧原子的构成__________________________________________.【2013年试题】1.(2013.湘潭市)五月初五,粽叶飘香,你能闻到香味是因为()A.分子在不断运动 B.分子的质量很小C.分子之间有间隔 D.分子可以再分2.(2013.福州市)打开盛有浓氨水的试剂瓶,可闻到刺激性气味,其原因是()A.氨分子在不断运动B. 氨分子中原子种类发生变化C. 氨分子的体积变大D. 氨分子转变为氮分子和氢分子阳光下暴晒而炸裂4.(2013.兰州市)下列对分子、原子、离子的认识,正确的是()A. 原子是最小的粒子,不可再分B. 温度越高,分子运动速率越快C. 离子不能直接构成物质D. 固体难压缩,说明固体分子间无间隔5.(2013.荆门市)造成非吸烟者在公共场所吸食“二手烟”的主要原因是()A.分子很小B.分子在不断运动C.分子之间有间隙D.分子由原子构成6.(2013.内江市)春天的公园,百花盛开,阵阵花香,沁人心脾。
花香四溢的现象说明()A.分子是不断运动的 B.分子是由原子构成的C.分子具有一定的质量 D.分子之间有一定的间隙8.(2013.泰安市)下列有关原子的说法正确的是()A.原子能构成分子,但不能直接构成物质B.原子在化学变化中不能再分,只能重新组合C.碳- 12原子和碳一13原子的中子数相同D.原子中一定含有质子、中子、电子三种粒子9.(2013.上海市)关于分子和原子两种微粒的叙述正确的是()A. 物质只能由分子构成B.相同原子可能构成不同的分子C. 分子质量一定大于原子质量D. 化学变化中分子数目一定发生变化11.(2013•长沙)用分子、原子的观点分析下列生活中的现象,其解释不合理的是()A. 50mL水与50mL酒精混合后,总体积小于100mL﹣﹣﹣分子之间有间隔B. 八月桂花飘香﹣﹣﹣分子在不断运动C. 1滴水中约含1.67×1021个水分子﹣﹣﹣分子很小D.水结成冰﹣﹣﹣分子停止运动12.13.(2013.黄冈市)下列有关说法正确的是()A.“春色满园,花香四溢”说明分子在不停地运动B.空气是由空气分子构成的C.组成CO、CO2的元素种类相同,所以它们的化学性质相同D.气体受热膨胀是因为温度升高气体分子变大14.(2013.昆明市)从分子的角度分析并解释下列现象,不正确...的是() A.端午时节粽飘香——分子在不停地运动B.干冰升华变为气体,所占体积变大——气体分子变大C.晴天湿衣服比阴天干得快——晴天气温高,分子运动速率快D.6000L氧气加压后可装入容积为40L的钢瓶中——分子间有间隔15.(2013.苏州市)下列有关微粒的说法错误的是()A.原子、分子、离子都是构成物质的微粒B.钠原子失去1个电子形成钠离子C.过氧化氢分子由氢分子和氧分子组成D.构成物质的微粒是在不停地运动16.(2013.黄石市)下列因素的改变,能显著改变气体体积的是()A.分子间的间隔 B.分子的大小C.分子的质量D.分子的种类17.(2013.北京市)固体碘受热升华,下列关于此过程的说法正确的是()A.碘分子质量变大B.碘分子间的间隔变大C.碘分子体积变小 D.碘分子运动速率不变18.(2013.莱芜市)原子是构成物质的基本粒子。
下列有关原子的叙述不正确...的是()A.原子的质子数等于核外电子数 B.原子质量主要集中在原子核上C.原子在化学变化中能够再分 D.符号“O”可以代表一个氧原子19.(2013.南宁市)下列有关构成物质粒子的说法,正确的是()A.分子一定比原子大B.分子、原子都是保持物质性质的粒子C.分子、原子、离子都是构成物质的粒子D.物质状态发生变化,是因为粒子大小发生变化20.(2013.荆州市)某粒子核内所含的质子数多于其核外电子数,该粒子一定是()A. 原子B. 分子C.阳离子D. 阴离子21.(2013.南宁市)下列说法正确的是()A. 所有原子的原子核都是由质子和中子构成B. 在同一种物质中同种元素的化合价可能不相同C. 由同一种元素组成的物质一定是单质,不可能是化合物D. 分子、原子都是不带电的粒子,所以不带电的粒子一定是分子或原子22.(2013.泸州市)我国南海海底蕴藏着丰富的锰结核——含有锰、铁、铜等金属的矿物。