初中化学除杂专题含答案
- 格式:doc
- 大小:36.37 KB
- 文档页数:8


除杂专题【常考题型】1、选择题,根据除杂原则,利用物质间相互反应除去2、填空题:往往根据物质间的相互反应,将物质或离子除去【易错点】1、违背除杂原则,引入新的杂质2、物理方法跟化学方法都可以3、所加试剂的量根据题意进行判断【解法】①确定题型,强调除杂原则:不增(不引入新杂质)、不减(不除去要提纯的物质)、易还原(还原到初始状态)、易分离。
②分析样品、杂质的性质,确定除杂方法。
a.物理方法,如用磁铁吸引。
b.化学方法注意:不能引入新杂质;所加试剂需过量;还原到原始状态。
③分别分析选项【精选题目】一.选择题(共4小题)1.除去食盐水中CaCl2和Na2SO4杂质的操作有:①加过量BaCl2溶液;②过滤;③加过量Na2CO3溶液;④蒸发结晶;⑤加适量盐酸.(提示:BaSO4、BaCO3难溶于水)下列操作顺序正确的是()A.③①②⑤④B.①⑤③②④C.①③②⑤④D.①③⑤④②2.下列选用的除杂试剂括号内为杂质)和实验操作都正确的是(()选项物质除杂试剂操作方法A KCl(KClO3)MnO2加入适量MnO2,加热使其充分反应B NH3(H2O)浓硫酸将气体通过盛有足量浓硫酸的洗气瓶C CaCl2溶液(HCl)Ca(OH)2溶液向溶液中加入过量的Ca(OH)2溶液D NaCl溶液(BaCl2)Na2SO4溶液向溶液中加入适量的Na2SO4溶液,过滤3.下列除杂方法正确的是()A.用冷却热饱和溶液的方法去除硝酸钾中混有的氯化钠B.用硫酸铜溶液除去铁粉中混有的铜粉C.用稀盐酸去除铁粉中混有的氧化铁D.用点燃的方法除去二氧化碳中混有的一氧化碳4.临近中考,小明将学过的化学知识整理如下。
你认为完全正确的一组是()A除杂(括号内为杂质)B鉴别Ba(NO3)2(KNO3)﹣加适量K2SO4溶液后过滤NaCl(Na2CO3)﹣﹣加适量盐酸后蒸发KNO3(NaCl)﹣﹣降温结晶后过滤磷肥和钾肥﹣﹣观察颜色小苏打和苏打﹣﹣加热后通石灰水硬水和软水﹣﹣用肥皂水C检验D干燥氧气﹣﹣用带火星的木条检验二氧化碳﹣﹣用点燃的木条检验铵盐﹣﹣加熟石灰混合研磨氨气﹣﹣用氢氧化钠固体干燥二氧化硫﹣﹣用生石灰干燥氢气﹣﹣用浓硫酸干燥二.填空题(共5小题)5.以粗盐(含杂质Na2SO4、MgCl2、CaCl2、泥沙)为原料制备精盐.(1)加水溶解后,用如图装置除去粗盐中的泥沙,玻璃棒的作用是.(2)为除去Na2SO4、MgCl2、CaCl2,并得到中性的食盐溶液,下列所加试剂和操作:①加过量的Na2CO3溶液,②过滤,③加过量的NaOH溶液,④加适量的稀HCl,⑤加过量的BaCl2溶液,能达到目的顺序是.A.⑤③②①④B.③⑤①④②C.③⑤①②④(3)用pH试纸检验溶液是否呈中性的操作是.6.除去NaCl溶液中的CaCl2、MgCl2、Na2SO4杂质的操作是①加过量的Na2CO3溶液;②加过量的BaCl2溶液;③向滤液中适量的稀盐酸;④过滤;⑤加过量的NaOH溶液.(1)以上操作合理的先后顺序为(数字符号不能重复使用).(2)操作中加入过量Na2CO3溶液的目的是除去溶液中的(用离子符号表示).7.除杂和推断是初中化学一种常见的题型。

一、中考初中化学除杂分离和提纯1.下列实验方案能达到实验目的的是()A.A B.B C.C D.D【答案】D【解析】【详解】A、除去KCl溶液中的K2CO3,加入适量的硝酸钙溶液,硝酸钙与碳酸钾反应生成硝酸钾和碳酸钙沉淀,过滤可除去碳酸钙,但引入了新的杂质硝酸钾,故A不正确;B、除去BaCl2溶液中的HCl,加入过量Ba(OH)2溶液,除去了杂质但引入了新杂质Ba(OH)2(过量的),故B不正确;C、稀盐酸和稀硫酸都属于强酸,不能通过比较溶液的pH来区分,故C不正确;D、氢氧化钠固体加水溶解会放出大量的热,溶液温度升高;硝酸铵固体加水溶解会吸收热量,溶液温度降低,可鉴别二者,故D正确。
故选D。
2.下表中,除去物质所含少量杂质的方法和反应类型归类均正确的是A.A B.B C.C D.D【答案】A【解析】【分析】【详解】A、铜和氧气加热生成氧化铜,反应为化合反应,氧化铜和氧气加热不反应,可以除去铜粉,故A正确;B、一氧化碳和氧化铜反应生成铜和二氧化碳,反应不属于置换反应,故B不正确;C、盐酸和氢氧化钠反应生成氯化钠和水,反应类型为复分解反应,故C不正确;D、硫酸钾和硝酸钡反应生成硫酸钡和硝酸钾,引进新杂质硝酸钾,故D不正确。
故选A。
3.下列依据实验目的所设计的实验方案正确的是()A.A B.B C.C D.D【答案】C【解析】【分析】【详解】A、除去CO2中的HCl气体,将混合气体通入足量NaOH溶液中,NaOH不仅与杂质氯化氢反应,还与原物质二氧化碳反应,不符合除杂的“原物质不减少”原则,不能用于除氯化氢杂质,选项说法错误,故不符合题意;B、区分尿素CO(NH2)2、NH4Cl和NH4NO3,加熟石灰研磨闻气味,只能区分出尿素,NH4Cl 和NH4NO3都与熟石灰反应产生刺激性气味的氨气,无法区分,选项说法错误,故不符合题意;C、区分稀HCl( 酸性)、Na2CO3溶液(碱性)、NaCl溶液(中性),滴加紫色石蕊溶液,紫色石蕊遇稀HCl显红色,遇Na2CO3溶液显蓝色,遇NaCl溶液显紫色,可以通过观察颜色区分开,选项说法正确,故符合题意;D、除去KNO3溶液中的KCl,加入过量的AgNO3溶液,AgNO3只与KCl生成硝酸钾和沉淀氯化银,但AgNO3溶液是过量的,引入了新杂质,不符合除杂的“不引入新杂质”原则,不能用于除去KCl,选项说法错误,故不符合题意,故选C。

【化学】初中化学化学除杂分离和提纯解题技巧及经典题型及练习题(含答案)一、中考化学除杂分离和提纯1.下列除杂(括号内为杂质)的试剂选用正确的是( )A .AB .BC .CD .D【答案】B 【解析】 【分析】 【详解】A 、CaCl 2溶液(盐酸)加入过量的Na 2CO 3溶液发生反应;2322Na CO 2HCl=2NaCl CO H O ++↑+ 2323Na CO CaCl =2NaCl CaCO ++↓会生成新杂质NaCl ,Na 2CO 3,被提纯CaCl 2会减少,不符合题意; B 、NaOH 溶液(Na 2CO 3溶液)加入适量的Ca(OH)2溶液发生反应;2323Na CO Ca(OH)=CaCO 2NaOH +↓+ 可以去除Na 2CO 3,符合题意;C 、CuO(Cu) 加入足量的稀H 2SO 4,CuO 会和稀H 2SO 4反应生成硫酸铜和水CuO 减少,不符合题意;D 、KCl 溶液(K 2SO 4溶液)加入适量的Ba(NO 3)2溶液发生反应;243234K SO Ba(NO )=2KNO BaSO ++↓ 虽然去除了K 2SO 4但是会产生新杂质KNO 3不符合题意; 故选:B 。
2.下列除杂质的方法正确的是( )A.A B.B C.C D.D【答案】D【解析】【分析】除杂(提纯),是指除去杂质,同时被提纯物质不得改变。
【详解】A、氧化铜和盐酸反应生成氯化铜和水,把原物质除去了,故A不正确;B、硫酸钠和硝酸钡反应生成硫酸钡沉淀和硝酸钠,引入新杂质硝酸钠,故B不正确;C、盐酸和碳酸钠反应生成氯化钠、水和二氧化碳,把原物质除去了,故C不正确;D、铁和氯化铜反应生成氯化亚铁和铜,可以除去氯化亚铁溶液中的氯化铜杂质,没有引入新的杂质,故D正确。
故选D。
【点睛】除杂条件:①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质。
3.下列方法不能达到除杂目的的是A.A B.B C.C D.D【答案】A【解析】【分析】【详解】A、CO能与灼热的氧化铜反应生成铜和二氧化碳,反而会把原物质除去,不符合除杂原则,故选项所采取的方法错误。

中考化学化学除杂分离和提纯解题技巧(超强)及练习题(含答案)一、中考化学除杂分离和提纯1.为除去下列物质中的少量杂质(括号内为杂质),下列操作方法能达到目的的是A.A B.B C.C D.D【答案】A【解析】【分析】【详解】A、铜在空气中充分灼烧能产生氧化铜,而氧化铜不能反应,可以用于除杂;故选项正确;B、生石灰与水反应产氢氧化钙,氢氧化钙能与二氧化碳反应产生碳酸钙,不能用于除杂;故选项错误;C、硝酸钡能与硫酸钠反应产生硫酸钡沉淀和硝酸钠,引入新的杂质硝酸根离子,不能用于除杂;故选项错误;D、氧化钙能与水反应产生氢氧化钙,不能用于除杂;故选项错误;故选:A。
2.下列各组括号内除杂的方法或试剂错误的是( )A.Cu粉中混有Fe粉(用磁铁吸引) B.Cu粉中混有CuO(稀硫酸)C.CO中混有CO2(氢氧化钙溶液) D.CO2中混有CO(点燃)【答案】D【解析】【分析】【详解】A、铁粉能被磁铁吸引,铜粉不能磁铁吸引,能除去杂质且没有引入新的杂质,符合除杂原则。
B、CuO能与稀硫酸反应生成硫酸铜和水,铜不与稀硫酸反应,能除去杂质且没有引入新的杂质,符合除杂原则。
C、二氧化碳能与氢氧化钙溶液反应生成碳酸钙和水,CO不与氢氧化钙溶液反应,能除去杂质且没有引入新的杂质,符合除杂原则。
D、除去二氧化碳中的一氧化碳不能够点燃,这是因为当二氧化碳(不能燃烧、不能支持燃烧)大量存在时,少量的一氧化碳是不会燃烧的,不符合除杂原则。
故选:D。
【点睛】物质的分离与除杂是中考的重点,也是难点,解决除杂问题时,抓住除杂质的必需条件(加入的试剂只与杂质反应,反应后不能引入新的杂质)是正确解题的关键。
3.如表中除去物质中少量杂质的方法正确的是A.A B.B C.C D.D【答案】A【解析】试题分析:除杂质的原则:所加的物质只与杂质反应,不能引入新的杂质,A、除去氯化钙溶液中的稀盐酸,加入过量的碳酸钙,发生反应:CaCO3+2HCl==CaCl2+H2O+CO2↑,然后再过滤,即可得到氯化钙溶液,正确,B、除去硫酸钾溶中的氢氧化钾,加入适量的稀盐酸,发生反应:KOH+HCl==KCl+H2O,引入了新的杂质KCl,错误,C、除去二氧化碳中氯化氢,通过足量的氢氧化钠溶液,两者都会发生反应,错误,D、除去二氧化锰中的氯化钾,根据二氧化锰不溶于水,氯化钾溶于水,故加水溶解、过滤、洗涤、烘干即可,不需要蒸发、结晶,错误,故选A考点:物质的除杂4.除去下列各组物质中的杂质(括号内为杂质),所选用的试剂(足量)及操作方法均正确的是()A.A B.B C.C D.D【答案】B【解析】【详解】A、Fe和Fe2O3均能与稀盐酸反应,不但能把杂质除去,也会把原物质除去,不符合除杂原则,采取的方法错误,故不符合题意;B、CO2能与氢氧化钠溶液反应生成碳酸钠和水,CO不与氢氧化钠溶液反应,再通过浓硫酸进行干燥,能除去杂质且没有引入新的杂质,符合除杂原则,采取的方法正确,故符合题意;C、CaO能与水反应生成氢氧化钙,碳酸钙难溶于水,反而会把原物质除去,不符合除杂原则,采取的方法错误,故不符合题意;D、Na2CO3能与Ca(NO3)2溶液反应生成碳酸钙沉淀和硝酸钠,能除去杂质但引入了新的杂质硝酸钠,不符合除杂原则,采取的方法错误,故不符合题意;故选B。
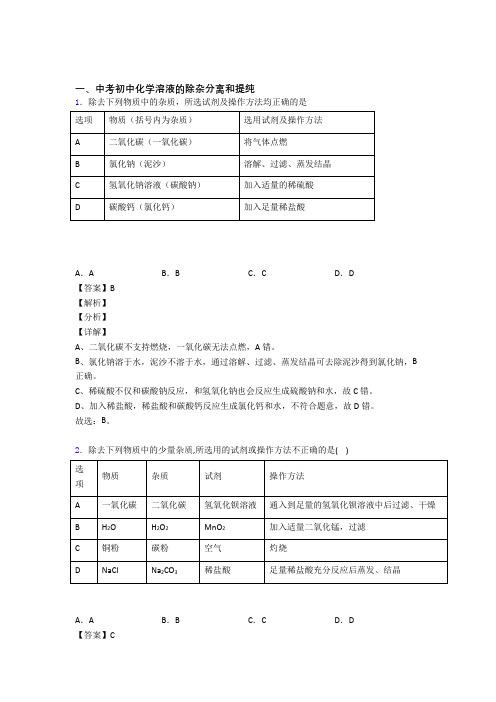
一、中考初中化学溶液的除杂分离和提纯1.除去下列物质中的杂质,所选试剂及操作方法均正确的是A.A B.B C.C D.D【答案】B【解析】【分析】【详解】A、二氧化碳不支持燃烧,一氧化碳无法点燃,A错。
B、氯化钠溶于水,泥沙不溶于水,通过溶解、过滤、蒸发结晶可去除泥沙得到氯化钠,B 正确。
C、稀硫酸不仅和碳酸钠反应,和氢氧化钠也会反应生成硫酸钠和水,故C错。
D、加入稀盐酸,稀盐酸和碳酸钙反应生成氯化钙和水,不符合题意,故D错。
故选:B。
2.除去下列物质中的少量杂质,所选用的试剂或操作方法不正确的是( )A.A B.B C.C D.D【答案】C【解析】【分析】根据原物质和杂质的性质选择适当的除杂剂和分离方法,所谓除杂(提纯),是指除去杂质,同时被提纯物质不得改变。
除杂质题至少要满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质。
【详解】A、将混合气体通入氢氧化钡溶液,二氧化碳和氢氧化钡反应生成碳酸钡沉淀和水,一氧化碳不反应,然后通过干燥除掉溶液中带入的水分,可得一氧化碳,选项正确;B、过氧化氢在二氧化锰的作用下生成水和氧气,过滤后液体只有水,选项正确;C、在空气中灼烧时,铜和碳都会与氧气发生反应,选项错误;D、碳酸钠能与过量的稀盐酸反应生成氯化钠、水和二氧化碳,所得溶液是氯化钠和氯化氢的混合溶液,蒸发结晶,可得氯化钠晶体,选项正确。
故选C。
3.为除去下列各物质中混有的少量杂质,采用的相应除杂方案正确的是A.A B.B C.C D.D【答案】C【解析】【分析】【详解】A、铜粉中含有氧化铜杂质,在空气中充分灼烧,铜与氧气在加热条件下反应生成氧化铜,不能除去杂质,反而将铜粉反应了。
故A不符合题意;B、NaCl溶液中含有Na2CO3杂质,加入适量稀硫酸,碳酸钠与稀硫酸反应生成硫酸钠、二氧化碳和水,可以除去碳酸钠,但是引入了新的杂质硫酸钠。
故B不符合题意;C、H2中含有CO2气体,通过足量NaOH溶液,氢氧化钠与二氧化碳反应生成碳酸钠和水,除去了二氧化碳,再对出来的氢气进行干燥,可以除去从氢氧化钠溶液中带出的水蒸气,从而得到纯净的氢气。

初三化学化学除杂分离和提纯试题(有答案和解析)一、中考化学除杂分离和提纯1.除去下列物质中的少量杂质,所选用的试剂和操作方法都正确的是()A.A B.B C.C D.D【答案】B【解析】【分析】【详解】A、将混合气体通过足量的铜网,铜与氮气不反应,铜与氧气能在加热的条件下反应生成氧化铜,但是常温下铜与氧气不反应,常温下,通过足量的铜网,不能除去混合气体中的氧气,不符合题意;B、氯化钾能溶于水,二氧化锰不溶于水,加水溶解、过滤,除去二氧化锰,蒸发、结晶得到氯化钾,符合题意;C、活性炭具有吸附性,能吸附水中的色素和异味,故加活性炭可除去水中的臭味,过滤,除去活性炭,才能得到水,需加过滤步骤,不符合题意;D、将混合气体通过适量的氢氧化钠溶液,氢氧化钠与二氧化碳反应生成碳酸钠和水,虽然除去了杂质二氧化碳,但是一氧化碳通过氢氧化钠溶液会携带上水蒸气,引入了新的杂质水蒸气,不符合题意。
故选B。
2.除去CO气体中少量CO2,可采用的方法是()A.把混合气体点燃B.把混合气体通过水中C.把混合气体通过灼热的CuO粉末D.把混合气体通过足量的澄清石灰水【答案】D【解析】【分析】【详解】A、一氧化碳能与氧气反应生成二氧化碳,反而会把原物质除去,不符合除杂原则,故选项错误。
B、二氧化碳能与水反应生成碳酸,但是碳酸不稳定会分解成二氧化碳和水,不能彻底除去杂质,故选项出错误。
C、一氧化碳能与灼热的氧化铜反应生成铜和二氧化碳,二氧化碳不能与灼热的氧化铜反应,反而会把原物质除去,不符合除杂原则,故选项错误。
D、CO2能与足量澄清石灰水反应生成碳酸钙和水,CO不与足量澄清石灰水反应,能除去杂质且没有引入新的杂质,符合除杂原则,故选项正确。
故选:D。
【点睛】根据原物质和杂质的性质选择适当的除杂剂和分离方法,所谓除杂(提纯),是指除去杂质,同时被提纯物质不得改变.除杂质题至少要满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质.3.为除去粗盐中的泥沙、Ca2+、Mg2+、SO42-等杂质,可将粗盐溶于水,再进行下列五步操作:①过滤②加过量的氢氧化钠溶液③加稍过量的盐酸④加过量的碳酸钠溶液⑤加过量的氯化钡溶液⑥蒸发结晶。


一、中考初中化学除杂分离和提纯1.下列实验方案不能达到实验目的的是()A.A B.B C.C D.D【答案】D【解析】【分析】【详解】A、Na2CO3+2HCl=2NaCl+H2O+CO2↑,选项A正确;B、NaCl溶于水溶液温度不变,NaOH固体溶于水溶液温度升高,选项B正确;C、CO2可以使澄清石灰水变浑浊,CO则不能,选项C正确;D、CaO和CaCO3都与稀盐酸反应,选项D不正确。
故选D。
2.除去下列物质中的杂质,所选用的试剂和操作方法均正确的是A.A B.B C.C D.D【答案】A【解析】【详解】A、碱石灰中的火碱是氢氧化钠,生石灰是氧化钙。
氢氧化钠易潮解,生石灰能和水反应。
可以除去氢气中混有的水蒸气。
A正确;B、氢氧化钾和硫酸反应生成硫酸钾和水。
该反应中会引入新的杂质硫酸钾,不符合除杂的要求。
B错误;C、二氧化锰难溶于水,氯化钠易溶于水。
加水溶解后,过滤,烘干,即可得到二氧化锰。
蒸发结晶会得到溶于水的氯化钠,不符合除杂的要求。
C错误;D、稀硫酸和铁、氧化铁均能发生化学反应。
对原物质造成影响,不符合除杂的要求。
D 错误。
故选A。
3.下列实验操作中不能达到实验目的的是A.A B.B C.C D.D【答案】A【解析】【详解】A、溶解后过滤得到氯化钠溶液,再蒸发才能够得到氯化钠固体,该选项不能达到实验目的;B、加入氯化钡溶液和稀硝酸后,产生白色沉淀的是稀硫酸,无明显现象的是盐酸,该选项能够达到实验目的;C、高温条件下碳酸钙分解生成氧化钙和二氧化碳,该选项能够达到实验目的;D、加入熟石灰研磨,能够产生刺激性气味的是氯化铵,无明显现象的是硫酸钾,该选项能够达到实验目的。
故选:A。
4.下列根据实验目的所设计的实验方案中,不正确的是A.分离CO2和CO混合气体----先通入NaOH溶液再加稀硫酸B.区分铁粉、碳粉、氧化铜粉末 ---- 加入稀盐酸C.除去部分变质的NaOH中的杂质----加水溶解,滴加适量的CaCl2溶液D.除去CuSO4溶液中少量的H2SO4----加过量的氧化铜,再过滤【答案】C【解析】【详解】A、二氧化碳能与氢氧化钠溶液反应生成碳酸钠和水,一氧化碳不能,先通入NaOH溶液,能分离出一氧化碳;再加稀硫酸,碳酸钠能与稀硫酸反应生成二氧化碳,能分离出二氧化碳,故选项实验方案正确。

化学除杂分离和提纯练习题(含答案)经典一、中考化学除杂分离和提纯1.下列哪种试剂最适合用来除去NaCl 溶液中混有的少量NaOH ( ) A .23Na CO 溶液 B .24H SO 溶液C .HCl 溶液D .2Ca(OH)溶液【答案】C 【解析】 【分析】 【详解】A 、23Na CO 溶液和NaOH 不反应,不能用于除去NaCl 溶液中混有的少量NaOH ,故A 错;B 、24H SO 溶液和NaOH 发生反应生成硫酸钠和水,会引入新杂质硫酸钠,故B 错;C 、HCl 溶液和NaOH 发生反应生成氯化钠和水,不会引入新杂质,符合题意故C 正确;D 、2Ca(OH)溶液和NaOH 不反应,不能用于除去NaCl 溶液中混有的少量NaOH ,故D 错; 故选:C 。
【点睛】除杂的原则不引入新杂质,被提纯物质不能减少,杂质容易分离。
2.下列除杂(括号内为杂质)选用的试剂或方法错误的是( ) A .Cu (CuO ):加入足量的稀盐酸,过滤,洗涤、烘干 B .NaCl 溶液(HCl ):加入过量碳酸钠,充分反应后过滤 C .CO 2 气体(CO ):将气体通过灼热的氧化铜层后收集气体 D .NaCl (泥沙):加适量水充分溶解,过滤、蒸发结晶 【答案】B 【解析】 【分析】 【详解】A 、在金属活动性顺序里,铜位于氢之前,不与稀盐酸反应,氧化铜能与稀盐酸反应生成氯化铜和水,加入足量稀盐酸,过滤、洗涤、干燥可得铜,不符合题意;B 、加入过量的碳酸钠,碳酸钠能与稀盐酸反应生成氯化钠、二氧化碳和水,碳酸钠过量,虽然除去了杂质,但是引入了新的杂质碳酸钠,符合题意;C 、将混合气体通过灼热的氧化铜,氧化铜能与一氧化碳在加热的条件下反应生成铜和二氧化碳,收集气体可得纯净的二氧化碳,不符合题意;D 、氯化钠溶于水,泥沙不溶于水,加适量水充分溶解,过滤、蒸发结晶,可得氯化钠,不符合题意。
故选B 。
【点睛】除杂选择试剂的原则是:不增(不引入新的杂质)、不减(不能将原物质反应掉)、不繁(整个过程不繁琐)。



除杂题除杂题 解法指导(1)原则:认准目的、统观全局,互不矛盾、能易则易。
)原则:认准目的、统观全局,互不矛盾、能易则易。
①量对性质的影响。
如CO 2 ( 杂有少量CO ) 。
(2)注意)注意②不同状态(气液固)的物质不易混杂;同种状态的物质易混杂。
不同状态(气液固)的物质不易混杂;同种状态的物质易混杂。
要除杂,啥办法?除杂、留用性兼挂,加剂序量细咂吧,要除杂,啥办法?除杂、留用性兼挂,加剂序量细咂吧, 除 杂 (3)思路)思路 改除啥,定除啥,不该除的莫除它,改除啥,定除啥,不该除的莫除它,改除啥,定除啥,不该除的莫除它,题除老杂,莫生新杂,最好生成有用哒,经济方便才顶呱呱,顶呱呱!除老杂,莫生新杂,最好生成有用哒,经济方便才顶呱呱,顶呱呱!除杂常用有五法:沉淀、置换和气化,还有溶解、把热加除杂常用有五法:沉淀、置换和气化,还有溶解、把热加 。
(4)解释)解释①Na 2CO 3 须在BaCl 2之后之后 ; 粗盐提纯:NaCl (杂有杂有CaCl 2、Na 2SO 4、MgCl 2、少量泥沙) ②都沉淀完后再过滤;都沉淀完后再过滤; ③滤液加入过量酸,最后一步是蒸干。
(5)两例)两例(1)例题:N 2 [ 可能杂有H 2、H 2O(气)、CO 、CO 2 ] 验杂净气验杂净气转化①H 2 、CO H 2O(气)、CO 、CO 2 ,然后再验除。
,然后再验除。
(2)思路)思路 ②先验后除须牢记,水是典型的一例。
先验后除须牢记,水是典型的一例。
③先验除H 2O(气)、CO 2 ,后验除H 2 、CO 。
启导学案设计人:化学辅导启导学案设计人:化学辅导 聂老师聂老师除杂题 专项训练1.下列除去混合物中少量杂质的方法或加入试剂合理的是.下列除去混合物中少量杂质的方法或加入试剂合理的是 ( )选项选项 物质物质 所含杂质所含杂质 除去杂质的方法或加入试剂除去杂质的方法或加入试剂 A KCl K 2SO 4 Ba(NO 3) 2 B CuO Cu 空气中灼烧空气中灼烧 C CO 2 N 2 澄清石灰水澄清石灰水 D Ca(OH)2CaCO 3盐酸盐酸2.下列实验操作中,不能达到实验目的是(下列实验操作中,不能达到实验目的是( )3.除去下列物质中含有的杂质所选用试剂或操作方法不正确...的一组是的一组是 物 质 所含杂质所含杂质 除去杂质的试剂或方法除去杂质的试剂或方法 A NaCl 溶液 Na 2CO 3 过量盐酸,加热过量盐酸,加热 B CuO Cu 灼烧灼烧 C KCl KClO 3 MnO 2,加热,加热 D O 2 H 2O 浓硫酸,干燥浓硫酸,干燥4.为提纯下列物质,所选用的除杂试剂和分离方法都正确的是为提纯下列物质,所选用的除杂试剂和分离方法都正确的是 ( ) 序号序号 物质(括号内为杂质)物质(括号内为杂质) 除杂试剂除杂试剂 分离方法分离方法 A 氯化钠固体(碳酸钠)氯化钠固体(碳酸钠) 稀盐酸稀盐酸 蒸发结晶蒸发结晶 B 氯化铜溶液(氯化锌)氯化铜溶液(氯化锌) 金属铜金属铜 过滤过滤 C 二氧化碳(一氧化碳)二氧化碳(一氧化碳)氢氧化钠溶液氢氧化钠溶液洗气洗气D 二氧化锰粉末(碳粉)二氧化锰粉末(碳粉) 水 过滤过滤5.下列选项中括号内物质为杂质,右边为除杂试剂,其中不合理...的是的是 A .氯化钠固体(碳酸钙).氯化钠固体(碳酸钙) 水 B .氧气(水蒸气).氧气(水蒸气) 浓硫酸浓硫酸 C .硫酸亚铁溶液(硫酸铜).硫酸亚铁溶液(硫酸铜) 铁粉铁粉实验目的实验目的实验操作实验操作A 鉴别涤纶和羊毛面料鉴别涤纶和羊毛面料 分别取样灼烧、闻气味分别取样灼烧、闻气味B 提纯粗盐(含少量泥沙)提纯粗盐(含少量泥沙) 将粗盐加适量水溶解、过滤、蒸发结晶将粗盐加适量水溶解、过滤、蒸发结晶 C 除去氯化钙溶液中少量盐酸除去氯化钙溶液中少量盐酸加入过量的碳酸钙粉末、充分反应后过滤加入过量的碳酸钙粉末、充分反应后过滤D 分离硫酸钠和硫酸铜的混合溶液分离硫酸钠和硫酸铜的混合溶液 加入过量氢氧化钠溶液后过滤,将滤渣溶于稀硫酸加入过量氢氧化钠溶液后过滤,将滤渣溶于稀硫酸6.为除去下表样品中的少量杂质(括号内为杂质),所选试剂及操作方法均正确的是,所选试剂及操作方法均正确的是 ( )序号序号样品成分样品成分所选试剂所选试剂操作方法操作方法A KCl (MnO 2)水溶解、过滤、洗涤干燥溶解、过滤、洗涤干燥B Na 2CO 3(NH 4HCO 3)加热至质量不再减少加热至质量不再减少 C NaCl (KNO 3) 水溶解、降温结晶、过滤溶解、降温结晶、过滤D NaCl (MgCl 2)过量NaOH 溶液溶液过滤、蒸发结晶过滤、蒸发结晶7.为除去下列物质中的杂质(括号内是杂质),下列操作方法正确的是(,下列操作方法正确的是( ) 选项选项 物质物质 操作方法操作方法A Fe (Fe 2O 3)加入过量稀盐酸,充分反应后过滤加入过量稀盐酸,充分反应后过滤 B CaO 粉末(CaCO 3粉末)粉末) 加足量的水,充分搅拌后过滤加足量的水,充分搅拌后过滤 C NaOH 溶液[Ca(OH)2溶液] 通入过量CO 2气体,充分反应后过滤气体,充分反应后过滤 D CuSO 4溶液(硫酸)溶液(硫酸)加入过量CuO 粉末,加热,充分反应后过滤粉末,加热,充分反应后过滤8.除去下列物质中的少量杂质(括号内为杂质)的方法错误的是(.除去下列物质中的少量杂质(括号内为杂质)的方法错误的是( ) A .O 2(H 2O )﹣用生石灰)﹣用生石灰 B .NaCl 溶液(KNO 3)﹣降温结晶)﹣降温结晶 C .CaCO 3粉末(Na 2CO 3)﹣加水过滤)﹣加水过滤D .KCl 溶液(K 2CO 3)﹣加适量盐酸)﹣加适量盐酸 9. 除去下列物质中的杂质,选用试剂或操作方法不正确是( ) 物质物质所含杂质所含杂质除去杂质的试剂或方法除去杂质的试剂或方法A Na 2CO 3固体固体NaHCO 3固体固体加热加热 B Cu Fe 加过量稀盐酸后过滤、洗涤、干燥加过量稀盐酸后过滤、洗涤、干燥 C O 2 H 2O 通人盛有过量浓H 2SO 4的洗气瓶的洗气瓶 D CO 2HC1 通入盛有NaOH 溶液的洗气瓶,然后干燥溶液的洗气瓶,然后干燥10.为除去物质中的杂质(括号内为杂质),所选试剂(过量)及操作方法均正确的是,所选试剂(过量)及操作方法均正确的是 ( ) 物质物质 选用试剂选用试剂 操作方法操作方法 A Cu(CuO) 氧气氧气 通入氧气并加热通入氧气并加热B CO 2(HCl) 氢氧化钠溶液氢氧化钠溶液 通过盛有氢氧化钠溶液的洗气瓶通过盛有氢氧化钠溶液的洗气瓶 C CaCl 2溶液(盐酸)溶液(盐酸) 碳酸钙粉末碳酸钙粉末 加入碳酸钙粉末充分反应后过滤加入碳酸钙粉末充分反应后过滤 D KCl 溶液(K 2CO 3) 氯化钙溶液氯化钙溶液加入氯化钙溶液充分反应后过滤加入氯化钙溶液充分反应后过滤11.除去下列物质中所含的少量杂质,下表中除杂方法正确的是除去下列物质中所含的少量杂质,下表中除杂方法正确的是 选项选项 物 质 所含杂质所含杂质 除杂质的方法除杂质的方法 A 氧化铜氧化铜 氯化钠氯化钠 加水溶解、过滤、蒸发结晶加水溶解、过滤、蒸发结晶 B 氧气氧气 水蒸气水蒸气 通过盛有浓硫酸的洗气瓶通过盛有浓硫酸的洗气瓶 C 硫酸钠溶液硫酸钠溶液 稀硫酸稀硫酸 加入过量碳酸钠溶液,过滤过滤D 二氧化碳二氧化碳一氧化碳一氧化碳点燃点燃12.除去下列各组物质中的少量杂质,所用方法不正确...的是的是 ( ) 选项选项 物质物质 杂质杂质 除去杂质的方法除去杂质的方法 A NaCl 泥沙泥沙 加入水溶解,过滤,蒸发加入水溶解,过滤,蒸发B O 2 水蒸气水蒸气 通过足量的浓硫酸通过足量的浓硫酸C NaOH 溶液溶液Na 2CO 3 滴入足量稀盐酸至不再产生气体滴入足量稀盐酸至不再产生气体 D H 2HCl 气体气体先通过NaOH 溶液,再通过浓硫酸溶液,再通过浓硫酸13. 下列除去杂质的方法中正确的是下列除去杂质的方法中正确的是 ( ) 选项选项 物质物质 杂质杂质 除杂质的方法除杂质的方法 A CaCl 2溶液溶液 稀盐酸稀盐酸 过量碳酸钙、过滤过量碳酸钙、过滤B KOH 溶液溶液 KCl 适量稀盐酸适量稀盐酸 C NaCl 溶液溶液Na 2CO 3 适量硝酸钙溶液、过滤适量硝酸钙溶液、过滤 D O 2CO 通过灼热的氧化铜通过灼热的氧化铜14.除去下列物质中的杂质(括号中的为杂质),所用试剂错误..的是的是 ( ) 选项选项 A B C D 物质物质 CO 2(CO) CO 2(HCl) Cu(CuO) KCl(MnO 2) 除杂试剂除杂试剂CuO NaOH 溶液溶液稀盐酸稀盐酸H 2O 15.下表列出了除去物质中所含少量杂质的方法,其中错误的是下表列出了除去物质中所含少量杂质的方法,其中错误的是 ( ) 选项选项 物质物质 杂质杂质 除杂方法除杂方法 A CO 2 CO 点燃B Cu 粉 Fe 粉 磁铁吸引磁铁吸引 C CaO CaCO 3 高温高温D CaCl 2溶液溶液稀盐酸稀盐酸加入足量的CaCO 3 ,过滤,过滤16.除去下列物质中的少量杂质所选用的试剂或方法正确的是(除去下列物质中的少量杂质所选用的试剂或方法正确的是( ) 选项选项 物质物质 所含杂质所含杂质 所选用试剂或方法所选用试剂或方法A NaOH 溶液溶液Na 2CO 3 溶液溶液 稀盐酸稀盐酸 B CaO CaCO 3高温灼烧高温灼烧C CO 2 CO 点燃点燃D 稀盐酸稀盐酸稀硫酸稀硫酸加适量Ba(NO 3)2溶液,再过滤溶液,再过滤17.除去下列物质中混有的少量杂质(括号内为杂质),所用方法正确的是,所用方法正确的是 ( )A .CO 2气体(CO 气体)——通入氧气通入氧气B .CaO 固体(CaCO 3固体)——加水充分溶解,过滤加水充分溶解,过滤C .KCl 固体(MnO 2固体)——加水充分溶解,过滤,蒸发结晶加水充分溶解,过滤,蒸发结晶D .NaCl 溶液(CaCl 2溶液)——滴加碳酸钾溶液至恰好完全反应,过滤滴加碳酸钾溶液至恰好完全反应,过滤 18.除去下列物质中混有的少量杂质(括号内为杂质)所用方法正确的是除去下列物质中混有的少量杂质(括号内为杂质)所用方法正确的是 ( ) A.CO 2( CO )──通入氧气点燃通入氧气点燃B.SO 2( HCl )──通过足量的氢氧化钠溶液通过足量的氢氧化钠溶液C.KCl 固体(固体( KClO 3 )── 加少量二氧化锰固体并加热加少量二氧化锰固体并加热D.NaCl 溶液( NaHCO 3 )──滴加稀盐酸至恰好完全反应滴加稀盐酸至恰好完全反应 19.下列鉴别物质的方法错误..的是的是 ( ) A.用水鉴别无水硫酸铜和氯化钠晶体用水鉴别无水硫酸铜和氯化钠晶体 B.用熟石灰鉴别硫酸铵和氯化铵用熟石灰鉴别硫酸铵和氯化铵C.用燃烧的木条鉴别氧气和二氧化碳用燃烧的木条鉴别氧气和二氧化碳D.用小木条鉴别浓硫酸和稀硫酸用小木条鉴别浓硫酸和稀硫酸20、下面除去混合物中少量杂质(括号内为杂质)的方案中,不合理的是( ) 混合物混合物 思路方法思路方法 选用物质选用物质 A .CO 2(CO) 点燃点燃 空气空气B .NaOH(Na 2CO 3) 沉淀、过滤沉淀、过滤 石灰乳[Ca(OH)2] C .FeCl 2(CuCl 2) 置换、过滤置换、过滤 铁粉铁粉D .NaCl(MgCl 2) 沉淀、过滤沉淀、过滤 NaOH 21、除去下列物质中的少量杂质,所用试剂或方法不正确的是( ) 选项选项 物质物质 杂质杂质 试剂或方法试剂或方法A NaCl 固体固体 泥沙泥沙 加水溶解、过滤、蒸发加水溶解、过滤、蒸发 B NaCl 溶液溶液 Na 2CO 3 滴加硫酸溶液至不再产生气泡滴加硫酸溶液至不再产生气泡 C KNO 3 溶液溶液 Ba(NO 3)2 滴加适量K 2SO 4溶液、过滤溶液、过滤 D N 2O 2通过红热的铜丝通过红热的铜丝22、除去下列物质中的杂质所选用的试剂或操作方法不正确的一组是(、除去下列物质中的杂质所选用的试剂或操作方法不正确的一组是( ) 物质物质 所含杂质所含杂质 除去杂质的试剂或方法除去杂质的试剂或方法 A CaO CaCO3 HCl B CuO Cu 灼烧灼烧C NaOH 溶液溶液 Na 2CO 3 适量Ca(OH)2溶液、过滤过滤 D O 2H 2O 干燥干燥23、(2011济南)济南) 除去下列各物质中混有的少量杂质,所用试剂和操作方法均正确的是( ) 序号序号 物质物质 杂质杂质 所用试剂和操作方法所用试剂和操作方法A H 2HCl 通过足量的NaOH 溶液、干燥溶液、干燥 B Na 2CO 3溶液溶液 Na 2SO 4溶液溶液 加入过量的Ba(NO 3)2溶液,过滤溶液,过滤 C NaCl 固体固体 细沙细沙 加入足量的水溶解,过滤加入足量的水溶解,过滤 D 铁粉铁粉Fe 2O 3加入适量的稀盐酸,过滤加入适量的稀盐酸,过滤24、下列做法正确的是(、下列做法正确的是( )A .加入适量的氢氧化钡溶液以除去NaCl 溶液中的少量Na 2SO 4B .加入适量的碳酸钙粉末以除去盐酸溶液中的少量CaCl 2C .用点燃的方法除去CO 2中混有的少量CO D .用氢氧化钠溶液处理硫在氧气中燃烧产生的气体.用氢氧化钠溶液处理硫在氧气中燃烧产生的气体25、除去下列物质中括号内少量杂质的方法,合理的是(、除去下列物质中括号内少量杂质的方法,合理的是( )A .CaO(CaCO 3):加入足量的稀盐酸B .CO 2(CO):在氧气中点燃:在氧气中点燃C .H 2 (HCl 、H 2O):把混合气体通过盛有足量生石灰和烧碱混合固体的干燥管D .KNO 3(K 2SO 4):溶解,加入过量的硝酸钡溶液,过滤:溶解,加入过量的硝酸钡溶液,过滤26、除去下列各物质中的少量杂质(括号内为杂质),其中方法错误的是(,其中方法错误的是( ) A .Cu 粉(Fe 粉):用磁铁吸:用磁铁吸 B .NaOH (NaNO 3):加稀盐酸:加稀盐酸 C. NaCl (泥沙)(泥沙):溶解、过滤、蒸发:溶解、过滤、蒸发 D. O 2(水蒸气):用浓H 2SO 4干燥干燥 27、除去下表所列物质中含有的杂质,所选试剂及操作方法均正确的是(、除去下表所列物质中含有的杂质,所选试剂及操作方法均正确的是( ) 选项选项 物质物质 杂质杂质 除去杂质所选试剂除去杂质所选试剂 操作方法操作方法 A 二氧化碳二氧化碳 一氧化碳一氧化碳 氧气氧气 点燃点燃 B 氯化钾氯化钾 碳酸钾碳酸钾 稀盐酸稀盐酸 蒸发蒸发 C 锌 铁 稀硫酸稀硫酸 过滤过滤 D 氧化钙氧化钙碳酸钙碳酸钙稀盐酸稀盐酸蒸发蒸发28、下列除去杂质所选择的试剂错误的是(、下列除去杂质所选择的试剂错误的是( )29、除去下列物质中混有的少量杂质(括号中的物质为杂质)所设计的试验方案或操作中,合理的是(、除去下列物质中混有的少量杂质(括号中的物质为杂质)所设计的试验方案或操作中,合理的是( ) A、KNO 3晶体(NaCl ):将固体溶于水,配置成热的饱和溶液,采用降温结晶的方法 B、CO 2气体(HCl ):将气体通过装有NaOH 溶液的洗气瓶溶液的洗气瓶 C、BaCl 2溶液(Ba(OH)2):加入适量得稀硫酸,过滤加入适量得稀硫酸,过滤 D、O 2 ( N 2):将混合气体通过炽热得铜网。

初中化学除杂试题及答案1. 在实验室中,为了除去氯化钠溶液中的少量碳酸钠,可以采取的方法是:A. 加入盐酸B. 加热C. 加入氯化钙D. 加入水答案:A2. 某学生在进行实验时,不小心将硫酸铜溶液与硫酸亚铁溶液混合,为了分离出纯净的硫酸铜溶液,应该采取的措施是:A. 加入铁粉B. 加入铜粉C. 加入氢氧化钠D. 加入硫酸答案:A3. 为了除去铜粉中的少量铁粉,可以采取以下哪种方法?A. 加入盐酸B. 加入硫酸铜溶液C. 加入硫酸D. 加入水答案:B4. 在实验室中,为了除去氢氧化钠溶液中的少量碳酸钠,可以采取的方法是:A. 加入氢氧化钙B. 加入氢氧化钠C. 加入二氧化碳D. 加入盐酸答案:A5. 实验室中,为了除去铜片表面的氧化铜,可以采取的方法是:A. 加热B. 加入稀硫酸C. 加入盐酸D. 加入水答案:B6. 为了除去硝酸钾溶液中的少量氯化钠,可以采取的方法是:A. 蒸发结晶B. 加热C. 加入硝酸D. 加入水答案:A7. 在实验室中,为了除去酒精中的少量水,可以采取的方法是:A. 加入生石灰B. 加热蒸馏C. 加入硫酸铜D. 加入水答案:B8. 为了除去铁粉中的少量铜粉,可以采取以下哪种方法?A. 加入盐酸B. 加入硫酸铜溶液C. 加入硫酸D. 加入水答案:A9. 在实验室中,为了除去硝酸银溶液中的少量氯化银,可以采取的方法是:A. 加入硝酸B. 加热C. 加入水D. 加入盐酸答案:A10. 实验室中,为了除去硫酸铜溶液中的少量硫酸,可以采取的方法是:A. 加入铜粉B. 加入氧化铜C. 加入氢氧化铜D. 加入水答案:A。

【化学】初中化学化学除杂分离和提纯的基本方法技巧及练习题及练习题(含答案)及解析一、中考化学除杂分离和提纯1.除去下列各物质中混有的少量杂质,所用试剂和操作方法均正确的是()A.A B.B C.C D.D【答案】C【解析】【分析】根据原物质和杂质的性质选择适当的除杂剂和分离方法,所谓除杂(提纯),是指除去杂质,同时被提纯物质不得改变。
除杂质题至少要满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质。
【详解】A、CaO能与水反应生成氢氧化钙,碳酸钙难溶于水,反而会把原物质除去,不符合除杂原则,故选项所采取的方法错误。
B、Na2CO3能与过量的CaCl2溶液反应生成碳酸钙沉淀和氯化钠,能除去杂质但引入了新的杂质氯化钙(过量的),不符合除杂原则,故选项所采取的方法错误。
C、CuO能与稀硫酸反应生成硫酸铜和水,铜不与稀硫酸反应,再过滤、洗涤、干燥,能除去杂质且没有引入新的杂质,符合除杂原则,故选项所采取的方法正确。
D、H2SO4能与适量BaCl2溶液反应生成硫酸钡沉淀和盐酸,能除去杂质但引入了新的杂质盐酸,不符合除杂原则,故选项所采取的方法错误。
故选:C。
【点睛】物质的分离与除杂是中考的重点,也是难点,解决除杂问题时,抓住除杂质的必需条件(加入的试剂只与杂质反应,反应后不能引入新的杂质)是正确解题的关键。
2.稀硝酸中混有少量的硫酸,为了除去硫酸,可加入适量的物质是()A.Ba(NO3)2B.AgNO3C.NaCl D.CuO【答案】A【解析】【分析】除杂(提纯),是指除去杂质,同时被提纯物质不得改变。
【详解】A、硫酸能与硝酸钡溶液反应生成硫酸钡沉淀和硝酸,能除去杂质且没有引入新的杂质,符合除杂原则,故A正确;B、硫酸能与硝酸银溶液反应生成微溶于水的硫酸银沉淀和硝酸,能除去杂质但引入了新的杂质硫酸银(微溶于水),不符合除杂原则,故B不正确;C、硫酸与氯化钠不反应,加入氯化钠,引入了氯化钠杂质,不符合除杂原则,故C不正确;D、稀硝酸和硫酸均能与氧化铜反应,不但能把杂质除去,也会把原物质除去,不符合除杂原则,故D不正确。

初中除杂实验题精选一.解答题(共15小题)1.(2015•攸县校级模拟)雷利是英国物理学家,他曾用下列两种方法测定氮气的密度.方法一:将除去水蒸气和二氧化碳的空气通过烧红的装有铜屑的玻璃管,使空气中的氧气全部除去,测得氮气的密度为1.2572kg/L.方法二:将氨气(NH3)通过赤热的装有氧化铜的玻璃管,生成氮气和水蒸气,除去水蒸气后测得氮气的密度为1.2508g/L.若两次测定的状况相同,请问:(1)方法二中发生反应的化学方程式为;(2)欲除去空气中的水蒸气和二氧化碳,可供选择的装置如下图所示(不可重复使用),在你选择的装置中,用相应的字母表示导管口的连接顺序,瓶中应盛放什么物质.(3)请分析两种方法所测定的氮气密度数值不同的原因.2.(2014春•泰州校级月考)一气体混合物中含有CO2、CO、H2O和N2四种气体.现将其分别通过如下试剂(均足量),请判断所得气体的组成情况(假设每步反应都进行完全).(1)依次通过NaOH溶液、浓H2SO4,最后得到的气体有:(填化学式下同).(2)依次通过灼热的氧化铜粉末、浓H2SO4,最后得到的气体有:.(3)依次通过灼热的氧化铜粉末、NaOH溶液、浓H2SO4,最后得到的气体有:.3.(2011•姜堰市校级模拟)如图是利用CO、CO2混合气体中的CO还原CuO的实验示意图.①仪器a的名称是.乙装置中应该用酒精灯的焰加热.②写出甲中反应的化学方程式:;乙装置的仪器b中黑色粉末变红时发生反应的化学方程式:.③反应过程中,丙中可观察到的实验现象是.④该装置存在的主要问题是.4.(2011•济南模拟)某化学课外小组的同学想要用含有杂质二氧化碳和水蒸气的一氧化碳气体测定样品中氧化铁的质量分数,装置如图所示.回答下列问题:根据上图回答:(1)甲装置的作用是.(2)乙装置的作用是.(3)丙装置中反应的化学方程式是.(4)丁装置中的现象是.(5)在装置丙中放入12克该氧化铁样品,待完全反应后冷却至室温,再称量剩余固体的总质量为9.6g.则该样品中氧化铁的质量分数为.(6)戊装置的作用.5.(2014秋•揭西县校级期中)蒸馏可降低水的硬度.在实验室可用如图装置制取蒸馏水.回答下列问题:(1)写出下列仪器的名称.a.;b.;c.;d..(2)得到的蒸馏水在中(填仪器名称).(3)仔细观察d仪器,它起到作用.冷水进入d仪器的方向如图所示,如果改为从上端流入,下端流出行不行?(填“行”或“不行”).(4)水在(填序号,下同)中由液态变为气态,在中由气态变为液态.6.(2014春•昌都县校级月考)下图所示为实验室制取蒸馏水的装置.根据此图回答下列问题:(1)写出下列仪器的名称:a、,b、,c、;(2)水在中由液态变为气态,在中由气态变为液态.在制取蒸馏水的过程中发生的是(填“物理”或“化学”)变化.(3)得到的蒸馏水在中.(4)仔细观察b仪器,它起作用,冷水进入b仪器的方向如图所示,如果改为从上端流入,下端流出(填“行”或“不行”).其原因是:.7.(2015•遵义)用如图实验方法分离NaCl和CaCl2两种固体的混合物A,根据操作流程完成下列问题:(1)B物质是CaCO3.(2)过滤操作中玻璃棒的作用是引流.(3)经分析上述方法分离出的F含杂质,请对该设计方案加以完善加入过量的Hcl.(4)若用原操作方法,要测出混合物A中NaCl和CaCl2的质量比,不称量D,可通过称量和的质量求解.8.(2015•扬州模拟)实验室可用草酸(H2C2O4)在浓硫酸的作用下分解制得一氧化碳和二氧化碳(化学方程式为:H2C2O4CO2↑+CO↑+H2O).所用的实验装置见图:若分别得到一氧化碳和二氧化碳,请回答:①装置A中,盛放浓硫酸的仪器名称是;②收集一氧化碳时,打开a、b,关闭c,装置B的作用是.由于一氧化碳有毒,多余的气体应(填写具体处理办法);③关闭、打开,释放出二氧化碳,并通过装置可收集到干燥的二氧化碳气体.9.(2015•南开区一模)某兴趣小组用NaCl溶液、NaOH溶液和稀H2SO4三种试剂,将含有Cu2+、Ba2+、Ag+、NO混合液中的三种阳离子逐一除去(每次只除一种离子).步骤如下(所加试剂均过量);步骤一:混合液中加入试剂A,过滤得到沉淀1和滤液1;步骤二:滤液1中加入试剂B,过滤得到沉淀2和滤液2;步骤三:滤液2中加入试剂C,过滤得到沉淀3和滤液3.(1)同学们选择的试剂A是溶液(填化学式),写出步骤一中反应的化学方程式.(2)三种沉淀中,能溶于稀盐酸的是(填物质名称).(3)滤液3中,除NaNO3外还含有的溶质是.10.(2015•河南校级模拟)化工生产中需要对原料提纯,以利于提高产品质量,经测定某氯化钠样品中混有硫酸钠,为了除去杂质并制得纯净的氯化钠固体,在实验室研究中某学生设计方案如下:回答下列问题.(1)过滤操作中玻璃棒的作用是引流,蒸发结晶操作中待出现较多固体停止加热.(2)操作②能否用硝酸钡溶液?说明理由不能,产生硝酸钠;进行操作②后,如何判断硫酸钠已除尽,方法是;(3)操作③的目的是除去过量的氯化钡,③、④操作顺序能否交换,其理由是不能,得不到滤液;此设计方案是否严密,说明理由不严密,没有用盐酸除去过量的碳酸钠.(4)实验中学化学兴趣小组为测定某石灰石样品(杂质不溶于水,也不与酸反应)中碳酸钙的质量分数,进行如图所示的实验.请根据以上信息计算:样品中碳酸钙的质量分数?11.(2012•长沙模拟)废干电池内的黑色固体含有MnO2、ZnCl2、NH4Cl、C(少量)等物质.化学小组欲通过以下流程,分离并回收部分物质.回答相关问题.(1)固体B常用作催化剂,则B是啦啦啦啦(填化学式),(2)写出在空气中灼烧A时发生反应的化学方程式:.12.(2011•维扬区校级一模)如图表示从固体混合物中分离X物质的2种方案,请回答有关问题.(1)选用方案I时,X物质应该具有的性质是,残留物应该具有的性质是;(2)选用方案Ⅱ从Fe和Cu的混合物中分离出Cu,加入的试剂是,有关反应的化学方程式为,该反应所属反应类型为;(3)为从大理石样品中提纯CaCO3(主要杂质SiO2,已知SiO2不溶于水、不与酸、碱反应,受热不分解),参照方案I和Ⅱ,请设计一种以框图形式表示的实验方案(注明物质和操作).13.(2009•海陵区校级模拟)食盐是日常生活的必需品,也是重要的化工原料.一同学用某种粗盐进行提纯实验,步骤如图所示.请回答:(1)步骤①和②的操作名称是.(2)步骤②中为得到纯净的固体A,需将沉淀A用水洗涤干净,请设计实验检验沉淀A 是否洗净.的钙元素含量,取10g这种盐溶于水,加入足量盐酸,生成0.132g二氧化碳.请计算此加钙食盐中钙元素的质量分数.14.(2014•安徽模拟)某同学设计的“从含铜电缆废料中提取铜”的实验方案如下:(1)过滤用到的玻璃仪器除了漏斗、烧杯还有.(2)写出步骤③发生反应的化学方程式及反应类型:步骤③:;.(3)图是实验室一氧化碳还原氧化铜的装置图,该装置存大一个主要的问题是;你认为改进的方法是.(4)在实验过程中,图中A处能看到的现象是.15.(2009•茂名)废干电池内的黑色固体含有MnO2、ZnCl2、NH4Cl、C(少量)等物质.化学小组欲通过以下流程,分离并回收部分物质.回答相关问题;(1)玻璃棒在操作I中的作用:.(2)过滤后,滤液C仍然浑浊,则造成浑浊的原因可能是(填编号)A.滤纸破损B.过滤过程中滤液的液面超过了滤纸的边缘C.烧杯不干净D.滤液C中的物质相互反应(3)固体B常用作催化剂,则B是(填化学式),写出在空气中灼烧A时发生反应的化学方程式:.(4)仅用硝酸银溶液(填“能”或“不能”)区分E和F.某同学认为固体E是NH4Cl,则检验方法是:.(5)NH4Cl属于化学肥料中的肥.初中除杂解答题参考答案一.解答题(共15小题)1.2NH3+3CuO3Cu+N2+3H2OBAGH或者GHBA氢氧化钠溶液和浓硫酸2.CO、N2CO2、N2N2.铁架台外CO2+2NaOH═Na2CO3+H2OCuO+CO Cu+CO2澄清石灰水变浑浊缺少尾气处理装置4.吸收气体中的二氧化碳吸收水蒸气3CO+Fe2O32Fe+3CO2石灰水变浑浊66.7%处理尾气.酒精灯蒸馏烧瓶铁架台冷凝管锥形瓶使水蒸气冷却得到水不行bc6.蒸馏瓶冷凝管锥形瓶ab物理c冷凝不行冷凝效果不好7.碳酸钙(或CaCO3)引流蒸发前先加适量的盐酸至不再产生气泡AB 8.分液漏斗吸收混合气中的二氧化碳点燃处理bcC、D 9.NaClNaCl+AgNO3=NaNO3+AgCl↓氢氧化铜HNO3、H2SO4、NaCl、Na2SO410.引流蒸发皿中出现较多固体不能用硝酸钡溶液,会引入新的硝酸钠杂质无法除去取清液少许,滴加氯化钡溶液,看是否有沉淀生成使钡离子完全沉淀不能,得不到滤液不严密,过量的碳酸钠没有除去11.MnO2C+O2CO212.受热易挥发受热不易挥发也不易分解稀盐酸Fe+2HCl=FeCl2+H2↑置换反应.过滤将少量固体A加入试管内,向试管内倒入少量水,再向试管内滴加无色酚酞试液,如果酚酞试液变红,说明没洗干净,如果不变红,就证明已经洗干净了14.玻璃棒CuSO4+2NaOH=Cu(OH)2↓+Na2SO4(复分解反应)没有尾气处理装置在右端导管口处加一个燃着的酒精灯,或加一个气球;黑色固体变成红色15.搅拌ABCMnO2C+O2CO2不能取少量E加入适量熟石灰(或其他强碱),并加热,若闻到刺激性气味的气体,则E为NH4Cl,氮。

化学化学除杂分离和提纯练习题及答案一、中考化学除杂分离和提纯1.除去下列物质中混有的少量杂质所选试剂的操作方法正确的是()A.A B.B C.C D.D【答案】D【解析】【分析】【详解】A、将气体通过足量NaOH溶液,NaOH能与HCl反应生成NaCl和水,氢氧化钠也能与二氧化碳反应生成碳酸钠和水,虽然除去了杂质,也除去了原物质,不符合题意;B、加入适量稀盐酸,氧化铜能与稀盐酸反应生成氯化铜和水,碳不与稀盐酸反应,过滤、洗涤、干燥可得碳,不但没有除去杂质,反而除去了原物质,不符合题意;C、加入适量K2CO3溶液,氯化钙能与碳酸钾反应生成碳酸钙和氯化钾,过滤,除去碳酸钙,虽然除去了杂质,但是引入了新的杂质氯化钾,不符合题意;D、加入适量AgNO3溶液,氯化铜能与硝酸银反应生成硝酸铜和氯化银,过滤,除去氯化银,可得硝酸铜,符合题意。
故选D。
【点睛】除杂选择试剂的原则是:不增(不引入新的杂质)、不减(不能将原物质反应掉)、不繁(整个过程不繁琐)。
2.下列除去杂质的方法不正确的是()A.A B.B C.C D.D【答案】B【解析】【分析】【详解】A、氧气通过灼热的铜网时,可与铜发生反应生成氧化铜,而氮气不与铜反应,能除去杂质且没有引入新的杂质,故选项所采取的方法正确;B、氧化钙与水反应生成氢氧化钙,混合物加入水,会消耗主要物质,故选项所采取的方法错误;C、浓硫酸具有吸水性,且不与二氧化碳反应,能除去杂质且没有引入新的杂质,故选项所采取的方法正确。
D,AgNO3能与适量的氯化钾溶液反应生成氯化银沉淀和硝酸钾,能除去杂质且不引入了新的杂质,故选项所采取的方法正确。
故选B。
【点睛】除杂(提纯),是指除去杂质,同时被提纯物质不得改变。
加入试剂除杂时至少要满足两个条件:①加入的试剂只能与杂质反应,不能与主要物质反应;②反应后不能引入新的杂质。
3.除去下列物质中的少量杂质,所用试剂和操作方法都正确的是()A.A B.B C.C D.D【答案】A【解析】【分析】【详解】A、氧气通过灼热的铜网时可与铜发生反应生成氧化铜,而氮气不与铜反应,能除去杂质且没有引入新的杂质,符合除杂原则,故选项所采取的方法正确。

【化学】九年级化学化学除杂分离和提纯题20套(带答案)及解析一、中考化学除杂分离和提纯1.下列除去杂质的试剂和方法可行的是选项物质(括号内为杂质)除杂试剂和方法A Mg(NO3)2溶液(AgNO3)加入过量铁粉,过滤B NaCl溶液(Na2SO4)加入适量BaCl2溶液,过滤C CO2(CO)通过足量澄清石灰水D N2(O2)通过灼热的氧化铜A.A B.B C.C D.D【答案】B【解析】试题分析:A、铁粉与硝酸银反应,生成银和硝酸亚铁,引来新的杂质,错误;B、硫酸钠与适量氯化钡反应,生成硫酸钡和氯化钠,正确;C、CO与澄清石灰水不发生反应,错误;D、氧化铜与氧气不发生化学反应,错误。
故选B考点:除杂质问题。
2.除去下列物质中的杂质,所选方法正确的是()选项物质杂质除去杂质的方法A C CuO加入足量稀硫酸,过滤、洗涤、干燥B NaCl Na2CO3加入足量稀硫酸,蒸发结晶C CO2CO点燃D MnO2KCl加水溶解、过滤、蒸发A.A B.B C.C D.D【答案】A【解析】【分析】【详解】A、碳不与稀硫酸反应,氧化铜能与稀硫酸反应生成硫酸铜和水,待完全反应后,过滤、洗涤、干燥可得碳,符合题意;B、加入足量稀硫酸,碳酸钠能与稀硫酸反应生成硫酸钠、二氧化碳和水,氯化钠与稀硫酸不反应,虽然除去了碳酸钠,但是引入了新的杂质硫酸钠,硫酸,不符合题意;C、二氧化碳不燃烧,也不支持燃烧,二氧化碳中混有少量一氧化碳,无法点燃,不符合题意;D、二氧化锰不溶于水,氯化钾溶于水,加水溶解、过滤,洗涤、干燥可得二氧化锰,不符合题意。
故选A。
【点睛】除杂选择试剂的原则是:不增(不引入新的杂质)、不减(不能将原物质反应掉)、不繁(整个过程不繁琐)。
3.如表中除去物质中少量杂质的方法正确的是A.A B.B C.C D.D【答案】A【解析】试题分析:除杂质的原则:所加的物质只与杂质反应,不能引入新的杂质,A、除去氯化钙溶液中的稀盐酸,加入过量的碳酸钙,发生反应:CaCO3+2HCl==CaCl2+H2O+CO2↑,然后再过滤,即可得到氯化钙溶液,正确,B、除去硫酸钾溶中的氢氧化钾,加入适量的稀盐酸,发生反应:KOH+HCl==KCl+H2O,引入了新的杂质KCl,错误,C、除去二氧化碳中氯化氢,通过足量的氢氧化钠溶液,两者都会发生反应,错误,D、除去二氧化锰中的氯化钾,根据二氧化锰不溶于水,氯化钾溶于水,故加水溶解、过滤、洗涤、烘干即可,不需要蒸发、结晶,错误,故选A考点:物质的除杂4.下列实验操作不可以达到实验目的的是()A.A B.B C.C D.D【答案】C【解析】【分析】【详解】A、氧化铜能与稀硫酸反应,木炭粉不与稀硫酸反应,故取样、加稀硫酸,能与稀硫酸反应的是氧化铜,可以用稀硫酸鉴别,不符合题意;B、氢氧化钠能与二氧化碳反应生成碳酸钠和水,干燥,可得一氧化碳,不符合题意;C、氯化铵和硫酸铵都属于铵态氮肥,和熟石灰混合研磨,均能产生有刺激性气味的气体,无法用加熟石灰、研磨,鉴别,符合题意;D、加入过量的铁粉,铁能与氯化铜反应生成氯化亚铁和铜,过滤,除去过量的铁和铜,可得氯化铜,不符合题意。
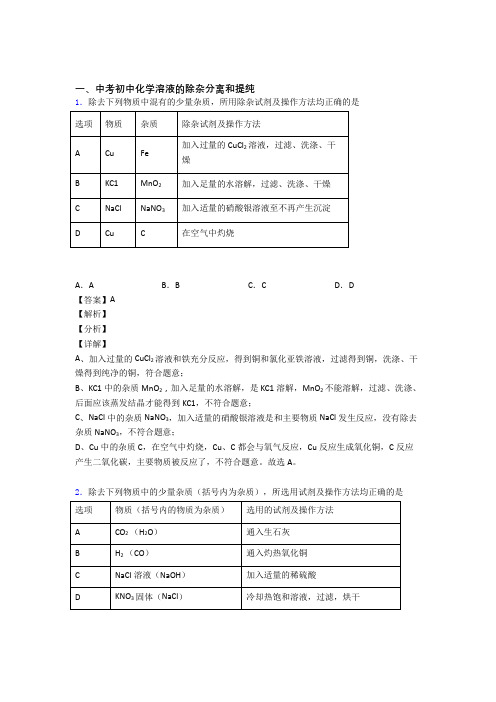
一、中考初中化学溶液的除杂分离和提纯1.除去下列物质中混有的少量杂质,所用除杂试剂及操作方法均正确的是A.A B.B C.C D.D【答案】A【解析】【分析】【详解】A、加入过量的CuCl2溶液和铁充分反应,得到铜和氯化亚铁溶液,过滤得到铜,洗涤、干燥得到纯净的铜,符合题意;B、KC1中的杂质MnO2,加入足量的水溶解,是KC1溶解,MnO2不能溶解,过滤、洗涤、后面应该蒸发结晶才能得到KC1,不符合题意;C、NaCl中的杂质NaNO3,加入适量的硝酸银溶液是和主要物质NaCl发生反应,没有除去杂质NaNO3,不符合题意;D、Cu中的杂质C,在空气中灼烧,Cu、C都会与氧气反应,Cu反应生成氧化铜,C反应产生二氧化碳,主要物质被反应了,不符合题意。
故选A。
2.除去下列物质中的少量杂质(括号内为杂质),所选用试剂及操作方法均正确的是A.A B.B C.C D.D【答案】D【解析】【分析】除杂质至少要满足两个条件:①一般加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质。
【详解】A、生石灰能与水反应生成氢氧化钙,但生成的氢氧化钙能与二氧化碳反应生成碳酸钙和水,不但能把杂质除去,也会把原物质除去,不符合除杂原则,故选项错误;B、氢气、CO均能与灼热的氧化铜反应,不但能把杂质除去,也会把原物质除去,不符合除杂原则,故选项错误;C、NaOH能与硫酸反应生成硫酸钠和水,能除去杂质但引入了新的杂质硫酸钠,不符合除杂原则,故选项错误;D、KNO3和NaCl的溶解度受温度的影响不同,硝酸钾溶解度受温度影响较大,而氯化钠受温度影响较小,所以可采取加热水溶解配成饱和溶液、冷却热饱和溶液使KNO3先结晶出来、再过滤、烘干的方法,故选项正确。
故选D。
3.去下列各物质中混有的少量杂质,所用试剂及操作方法均正确的是()A.A B.B C.C D.D【答案】A【解析】【分析】【详解】A、硝酸银和氯化钠反应生成氯化银沉淀和硝酸钠,过滤得到硝酸钠溶液,该选项正确;B、碳酸钠和氯化钡反应生成碳酸钡沉淀和氯化钠,除去碳酸钠后引入氯化钡(过量)新杂质,该选项不正确;C、高温条件下铜和氧气反应生成氧化铜,该选项不正确;D、氧化钙和盐酸反应生成氯化钙和水,过量的氧化钙和水反应生成氢氧化钙,除去盐酸后引入新杂质氢氧化钙,该选项不正确。
) (2012.宁波市)为提纯下列物质,所选用的除杂试剂和分离方法都正确的是( 4.初中化学除杂专题分离方法除杂试剂序号物质(括号内为杂质)
A 蒸发结晶稀盐酸氯化钠固体(碳酸钠))德阳)下列除去混合物中少量杂质的方法或加入试剂合理的是(1.(2012·
B 金属铜过滤氯化铜溶液(氯化锌)所含杂质除去杂质的方法或加入试剂选项物质
C 二氧化碳(一氧化碳)氢氧化钠溶液洗气)A KCl KSOBa(NO 2 4 32D
二氧化锰粉末(碳粉)水过滤Cu CuO B 空气中灼烧5.(2012.株洲市)下列选项中括号内物质为杂质,右边为除杂试剂,其中不合理的是...NC CO 澄清石灰水2 2
A.氯化钠固体(碳酸钙)水 D
Ca(OH)CaCO 盐酸32
B.氧气(水蒸气)浓硫酸)淮安市)下列实验操作中,不能达到实验目的是((2.2012.C.硫酸亚铁溶液(硫酸铜)铁粉
,所选试剂及操作方法均泰州市)为除去下表样品中的少量杂质(括号内为杂质)6.(2012. )正确的是(
操作方法样品成分所选试剂序 A 溶解、过滤、洗涤干燥水)KCl(MnO2 3.的一组是菏泽市)除去下列物质中含有的杂质所选用试剂或操作方法不正确(2012.... B
加热至质量不再减少)(NaCONH HCO
3234
C
NaCl(KNO)水溶解、降温结晶、过滤3D
NaCl(MgCl)过量NaOH溶液过滤、蒸发结晶2
7.(2012?绍兴)为除去下列物质中的杂质(括号内是杂质),下列操作方法正确的是()11.(2012.鸡西市)除去下列物质中所含的少量杂质,下表中除杂方法正确的是
)苏州)除去下列物质中的少量杂质(括号内为杂质)的方法错误的是()8.(2012?...)﹣降温结晶B.NaCl溶液(KNO )﹣用生石灰(A.OHO322除去杂质的方法选项物质杂质
COCaCOC.粉末(Na)﹣加水过滤D.COK)﹣加适量盐酸KCl溶液(32233NaCl A 加入水溶解,过滤,蒸发泥沙
)
(2012.眉山市)除去下列物质中的杂质,选用试剂或操作方法不正确是( 9 OB 水蒸气通过足量的浓硫酸2
C NaCO 滴入足量稀盐酸至不再产生气体溶液NaOH32 HD
溶液,再通过浓硫酸先通过NaOHHCl气体2)(13.(2012.兰州市)下列除去杂质的方法中正确的是物质选项杂质除杂质的方法A 过量碳酸钙、过滤稀盐酸溶液CaCl2,所选试剂(过量)及操作方法均日照市)为除去物质中的杂质(括号内为杂质)2012.10.(KCl B 适量稀盐酸KOH溶液
正确的是()NaC
32
D
O 通过灼热的氧化铜2
14.(2012.桂林市)除去下列物质中的杂质(括号中的为杂质),所用试剂错误的是()
H
( ) ( CO )──通入氧气点燃 A.CO2( HCl )──通过足量的氢氧化钠溶液 B.SO2C.KCl固体(KClO)──加少量二氧化锰固体并加热)其中错误的是(下表列出了除去物质中所含少量杂质的方法,(15.2012.武汉市)3
)──滴加稀盐酸至恰好完全反应( NaHCO溶液D.NaCl3
19.(2012.桂林市)下列鉴别物质的方法错误的是()..CO A CO 点燃2[ A.用水鉴别无水硫酸铜和氯化钠晶体 B.用熟石灰鉴别硫酸铵和氯化铵 B Fe粉磁铁吸引粉Cu C.用燃烧的木条鉴别氧气和二氧化碳 D.用小木条鉴别浓硫酸和稀硫酸CaO C CaCO 高温320、
(2011济宁)下面除去混合物中少量杂质(括号内为杂质)的方案中,不合理的是混合物 D 溶液CaCl 稀盐酸CaCO,过滤加入足量的3 2混合物思路方法选用物质A.CO(CO) 点燃空气2)(16.2012.达州市)除去下列物质中的少量杂质所选用的试剂或方法正确的是
(
B.NaOH(NaCO)沉淀、过滤石灰乳[Ca(OH)] 223所选用试剂或方法所含杂质物质选项C.FeCl(CuCl) 置换、过滤铁粉22A 稀盐酸溶液Na溶液NaOH CO3 2D.NaCl(MgCl) 沉淀、过滤NaOH
2 B CaO CaCO 高温灼烧321、(2011滨州)除去下列物质中的少量杂质,所用试剂或方法不正确的是CO COC 点燃2
(.南京市)除去下列物质中混有的少量杂质201217.(括号内为杂质),所用方法正确的是)(——)(CO气体气体.A CO通入氧气2——(CaCO固体CaO.B )固体加水充分溶解,过滤3KCl.C )固体——(MnO固体加水充分溶解,过滤,蒸发结晶2溶液NaCl.D 滴加碳酸钾溶液至恰好完全反应,过滤——(CaCl)溶液2.
22、(2011宜宾)除去下列物质中的杂质所选用的试剂或操作方法不正确的一组是()26、(2011邵阳,)除去下列各物质中的少量杂质(括号内为杂质),其中方法错误的是()
A .Cu粉(Fe粉):用磁铁吸
B .NaOH(NaNO):加稀盐酸3C. NaCl(泥沙):溶解、过滤、蒸发 D. O(水蒸气):用浓HSO干燥42227、(2011无锡)除去下表所列物质中含有的杂质,所选试剂及操作方法均正确的是
B CaCO 盐酸CaCl溶液32
C Cu CuO 稀盐酸)下列做法正确的是南昌,2011、24(
D NaCl溶液NaOH溶液BaCl溶液A.加入适量的氢氧化钡溶液以除去Na溶液中的少量SONaCl24229、.加入适量的碳酸钙粉末以除去盐酸溶液中的少量BCaCl(2011兰州)除去下列物质中混有的少量杂质(括号中的物质为杂质)所设计的试验2方案或操作中,合理的是
(中混有的少量CO.用点燃的方法除去CCO )2A、KNO晶体(NaCl D.用氢氧化钠溶液处理硫在氧气中燃烧产生的气体):将固体溶于水,配置成热的饱和溶液,采用降温结晶的方法3B、CO气体(HCl): 泰州)除去下列物质中括号内少量杂质的方法,合理的是2011、25(将气体通过装有NaOH溶液得洗气瓶2C、BaCl溶液(Ba(OH) :加入足量的稀盐酸))CaO(CaCO.A:加入适量得稀硫酸,过滤232D、O(N :在氧气中点燃(CO)):COB.将混合气体通过炽热得铜网。
222O)H、(HCl:把混合气体通过盛有足量生石灰和烧碱混合固体的干燥管.CH22KNO.D:溶解,加入过量的硝酸钡溶液,过滤(KSO)423.
30、(2011湛江)下列选用的除杂试剂和实验操作都正确的是(括号内为杂质)初中化学除杂专题
答案 1.B 2.D 3.C 4.A 5.D 6. B 7. D 8. B 9.D 10.C 11.B 12.C 13.A 14. B 15. A 16. B 17. C 18. D 19. B 20. 21. B 22.A 23.A 24.D 25.C 26.B 27.B 28.D 29.A 30.BC 31B32D )31、下列除杂的实验过程中都正确的是(括号内为杂质)((KCl)加水溶解、过滤、蒸发、结晶A.MnO2 )BaSO(BaCO 加足量稀盐酸、过滤、洗涤、干燥B.34.CuO(Cu) 加足量稀盐酸、过滤、洗涤、干燥C ) 加足量稀盐酸、过滤、蒸发、结晶D.KCl(KCO32)32、下列除去杂质的方法正确的是(
除去N中的少量OCuO粉末,收集气体:通过灼热的A.22 CaCOCaO中的少量:加入足量稀盐酸,充分反应B.除去3溶液,过滤MgClC.除去KCl溶液中的少量:加入适量NaOH2除去溶液中的少量)Cu(NOAgNO:加入足量铜粉,充分反应后过滤D.332。