总糖含量的测定—3, 5-二硝基水杨酸法
- 格式:docx
- 大小:19.00 KB
- 文档页数:1

3,5-二硝基水杨酸比色法-还原糖和总糖的测定3,5-二硝基水杨酸比色法是一种常用的测定还原糖和总糖含量的方法。
本文将介绍该方法的操作步骤、原理及注意事项。
一、操作步骤1. 样品制备:精确称取适量糖样品,加入足量去离子水稀释至1 mL,摇匀。
2. 试剂制备:(1) Na2CO3试液:称取0.5 g Na2CO3加入50 mL去离子水中,溶解并稀释至1 L。
(2) 3,5-二硝基水杨酸(DNS)重量浓度为1 g/L的甲醛溶液:按比例称取适量DNS和甲醛,在去离子水中稀释制成重量浓度为1 g/L的甲醛溶液。
3. 测定步骤:(1) 取3个试管,编号为A、B、C,并进行空白对照。
将A、B、C试管分别加入0.1 mL 样品,每个试管中加入相同量的0.9 mL去离子水。
在空白试管中加入相同量的去离子水代替样品。
(2) 在A试管中加入0.5 mL Na2CO3试液,摇匀。
(3) 将B试管浸于沸水中加热3-5分钟,使其中的还原糖完全还原。
(4) 在A、B两样品试管中加入0.5 mL甲醛溶液,摇匀并置于60℃水浴上加热10分钟。
(6) 加入1.5 mL水后,在空白对照试管和样品试管中均加入0.5 mL DNS溶液,摇匀。
(7) 在95℃水浴加热10分钟,并立即冷却至室温。
(8) 测量吸光度值,通过标准曲线计算样品中还原糖或总糖含量。
二、原理还原糖或总糖与Na2CO3在典型的碱性条件下发生醛基反应,把碳水化合物中的亲电基转化为醛基,再将其还原为对应的醇,生成糖醇和尿素等。
然后,在碱性条件下,醛基与3,5-二硝基水杨酸(DNS)反应,发生环化,生成糖醛酸化合物,这些化合物在pH9.0以下表现为桥形分子,具有紫色的吸收峰。
在高温条件下,DNS与糖醛酸化合物相结合,形成柿子色化合物,进一步增加吸收光的强度。
还原糖或总糖的含量可以通过比较样品的吸光度值和标准曲线来测定。
三、注意事项1. 避免试管附着并确保试管内部表面干净。

3,5-二硝基水杨酸法测定山楂片中还原糖和总糖含量3,5-二硝基水杨酸法是一种常用的测定还原糖和总糖含量的方法,其原理基于还原糖在酸性条件下与3,5-二硝基水杨酸反应生成红色化合物,而总糖则在强硫酸存在下加热分解,生成由葡萄糖和六碳糖等组成的还原糖,在酸性条件下与3,5-二硝基水杨酸反应生成红色化合物。
具体操作步骤如下:1. 取一定质量的山楂片粉末,加入适量的蒸馏水,加热水浴至沸腾,过滤,将过滤液冷却至室温。
2. 取0.2 ml 过滤液,加入2 ml 3,5-二硝基水杨酸溶液,摇匀后在60摄氏度恒温水浴中反应10分钟,然后放冷。
3. 吸收液的吸光度在515 nm处测定,还原糖含量的计算公式为:还原糖含量(%)= (As–A0)/(有效光程×C×0.88)×100,其中As为样品吸光度,A0为空白试剂吸光度,有效光程为1 cm,C为样品初始体积,0.88为还原糖的摩尔吸光系数。
4. 取剩余过滤液,加入相当于5倍于样品初始体积的浓硫酸,浸于沸水中煮2小时,浸于水中冷却,并用蒸馏水将瓶口水洗入容量瓶,摇匀。
5. 取0.1ml 还原糖水样稀释液加入容量瓶,加入相当于5倍于样品初始体积的浓硫酸,摇匀后加入适量的蒸馏水到刻度线,摇匀后离心。
6. 取0.1 ml 离心上清液,加入2 ml 3,5-二硝基水杨酸溶液,摇匀后在60摄氏度恒温水浴中反应10分钟,然后放冷。
7. 吸收液的吸光度在515 nm处测定,总糖含量的计算公式为:总糖含量(%)= (As–A0)/(有效光程×C×0.88)×100,其中As为样品吸光度,A0为空白试剂吸光度,有效光程为1 cm,C为样品初始体积,0.88为还原糖的摩尔吸光系数。
总之,3,5-二硝基水杨酸法是一种稳定可靠的方法,能够准确测定山楂片中的还原糖和总糖含量,为山楂片的质量控制提供了重要的参考。
实验二十还原糖和总糖含量的测定—3、5-二硝基水杨酸比色定糖法目的要求1、掌握3,5-二硝基水杨酸比色法定糖的原理及方法。
2、用3,5-二硝基水杨酸定糖法测定山芋粉中的总糖及还原糖。
3、熟悉721型光电比色计的原理及使用方法。
实验原理3,5-二硝基水杨酸在强碱溶液中与还原糖在沸水浴中共热后被还原成棕红色的氨基化合物,在一定范围内,还原糖的量和反应液的颜色强度呈比例关系,利用比色法可测知样品的含糖量。
该方法是半微量定糖法,操作简便,快速,杂质干扰较少。
试剂和器材1.试剂(1)6mol/L盐酸溶液、10%氢氧化钠溶液、碘化钾-碘溶液(碘试剂)、酚酞指示剂、85%乙醇。
(2)3,5-二硝基水杨酸试剂(又称DNS试剂):甲液——溶解6.9g结晶酚于15.2ml 10%氢氧化钠中,并稀释至69ml,在此溶液中加入6.9g亚硫酸氢钠。
乙液——称取255g酒石酸钾钠,加到300ml 10%氢氧化钠中,再加入880ml 1%的3,5-二硝基水杨酸溶液。
将甲液与乙液相混合即得到黄色试剂,贮于棕色试剂瓶中,在室温下,放置7~10d以后使用。
(3)0.2%葡萄糖标准液:准确称取200mg分析纯的葡萄糖(预先在70℃干燥至恒重),用少量蒸馏水溶解后定容至100ml,冰箱保存备用。
2.器材试管和试管架、碱滴定管(50ml)、铁架台、滴定管夹、移液管(1ml,2ml)、移液管架、容量瓶(100ml)、铜水浴锅、玻璃漏斗、烧杯、铁三脚架、量筒(10ml、100ml)、电热恒温水浴、煤气灯、玻璃棒、白瓷板、721型分光光度计。
操作方法1.葡萄糖标准曲线的制定取9支刻度试管(25ml)或血糖管,分别按下表顺序加入各种试剂:DNS试剂1.5 1.5 1.5 1.5 1.5 1.5 1.5 1.5 1.5(ml)加热均在沸水浴中加热5min冷却立即用流动冷水冷却蒸馏水(ml)21.5 21.5 21.521.521.521.521.521.5 21.5 将上述各管溶液混匀后,在721型分光光度计上进行比色测定,用空白管溶液调零点,记录光密度值,以葡萄糖浓度为横座标,光密度值为纵座标绘制出标准曲线。
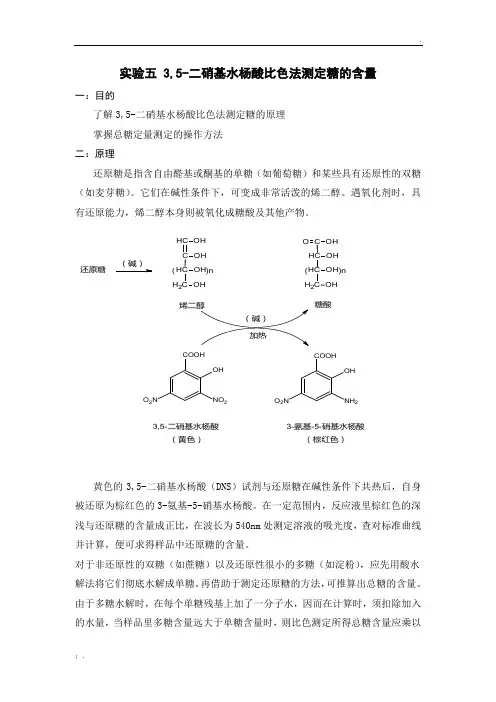
实验五 3,5-二硝基水杨酸比色法测定糖的含量一:目的了解3,5-二硝基水杨酸比色法测定糖的原理 掌握总糖定量测定的操作方法 二:原理还原糖是指含自由醛基或酮基的单糖(如葡萄糖)和某些具有还原性的双糖(如麦芽糖)。
它们在碱性条件下,可变成非常活泼的烯二醇。
遇氧化剂时,具有还原能力,烯二醇本身则被氧化成糖酸及其他产物。
黄色的3,5-二硝基水杨酸(DNS )试剂与还原糖在碱性条件下共热后,自身被还原为棕红色的3-氨基-5-硝基水杨酸。
在一定范围内,反应液里棕红色的深浅与还原糖的含量成正比,在波长为540nm 处测定溶液的吸光度,查对标准曲线并计算,便可求得样品中还原糖的含量。
对于非还原性的双糖(如蔗糖)以及还原性很小的多糖(如淀粉),应先用酸水解法将它们彻底水解成单糖。
再借助于测定还原糖的方法,可推算出总糖的含量。
由于多糖水解时,在每个单糖残基上加了一分子水,因而在计算时,须扣除加入的水量,当样品里多糖含量远大于单糖含量时,则比色测定所得总糖含量应乘以COOHOHNO 2O 2N 还原糖COOHOHO 2N NH 23,5-二硝基水杨酸(黄色)3-氨基-5-硝基水杨酸(棕红色)C C H O OH OH C H C H 2OH OH( )n ( )n C H C OH OHC H H 2OH OH糖酸折算系数(1-18018= 0.9),即得比较接近实际的样品中总糖含量。
三:实验材料及设备 1、材料:面粉2、仪器:分光光度计 电子天平 沸水浴3、器材:刻度试管: 25mL ×8 容 量 瓶: 100mL ×2 锥 形 瓶: 100mL ×1移 液 管: 1mL ×2 2mL ×2 10mL ×2 烧 杯: 250mL ×1 50mL ×1 滴 管: 2 洗 耳 球: 2 滤 纸: 11cm 坐 标 纸漏斗、洗瓶、白瓷板、试管架、移液管架、试管夹、玻棒:各1 四:试剂的配制1、葡萄糖标准液(1mg/mL )预先将分析纯葡萄糖置80℃烘箱内约12小时。

实验一还原糖和总糖的测定——3,5-二硝基水杨酸比色法一、实验目的掌握还原糖和总糖测定的基本原理,学习比色法测定还原糖的操作方法和分光光度计的使用。
二、实验原理还原糖的测定是糖定量测定的基本方法。
还原糖是指含有自由醛基或酮基的糖类,单糖都是还原糖,双糖和多糖不一定是还原糖,其中乳糖和麦芽糖是还原糖,蔗糖和淀粉是非还原糖。
利用糖的溶解度不同,可将植物样品中的单糖、双糖和多糖分别提取出来,对没有还原性的双糖和多糖,可用酸水解法使其降解成有还原性的单糖进行测定,再分别求出样品中还原糖和总糖的含量(还原糖以葡萄糖含量计)。
还原糖在碱性条件下加热被氧化成糖酸及其它产物,3,5-二硝基水杨酸则被还原为棕红色的3-氨基-5-硝基水杨酸。
在一定范围内,还原糖的量与棕红色物质颜色的深浅成正比关系,利用分光光度计,在540nm波长下测定光密度值,查对标准曲线并计算,便可求出样品中还原糖和总糖的含量。
由于多糖水解为单糖时,每断裂一个糖苷键需加入一分子水,所以在计算多糖含量时应乘以0.9。
三、实验材料、主要仪器和试剂1.实验材料小麦面粉;广范pH试纸。
2.主要仪器(1)大试管:2×20cm×14(2)烧杯:100mL×3(3)三角瓶:100mL×1(4)容量瓶:100mL×3(5)移液管:1mL×3;2mL×2;10mL×4(6)吸耳球、玻璃棒(7)恒温水浴锅(8)漏斗、滤纸(9)白瓷缸、电炉(10)精度天平(11)分光光度计3.试剂(已制备)(1)1mg/mL葡萄糖标准液准确称取90℃烘至恒重的分析纯葡萄糖100mg,置于小烧杯中,加少量蒸馏水溶解后,转移到100mL容量瓶中,用蒸馏水定容至100mL,混匀,4℃冰箱中保存备用。
(2)3,5-二硝基水杨酸(DNS)试剂将6.3g 3,5-二硝基水杨酸(DNS)和2mol\L NaOH溶液262mL,加到500mL含有185g酒石酸钾钠的热水溶液中,再加5g重蒸酚和5g亚硫酸钠,搅拌溶解,冷却后加蒸馏水定容至1000mL,贮于棕色瓶中,7-10天后才能使用。

总糖和还原糖的测定─3,5-二硝基水杨酸法思考题
1.为什么3,5-二硝基水杨酸法能够测定总糖和还原糖?
答:3,5-二硝基水杨酸法是一种常用的测定还原糖和总糖的方法,其
原理是将还原糖还原成相应的葡萄糖,在酸性条件下,葡萄糖与3,5-二
硝基水杨酸反应生成黄色化合物,通过比色法测定吸光度,即可计算出样
品中还原糖的含量。
同时,总糖中还包括非还原糖,这些非还原糖无法被3,5-二硝基水杨酸还原成葡萄糖,因此测得的是总糖含量,再用还原糖含
量去减即可计算出非还原糖含量。
2.3,5-二硝基水杨酸法测定还原糖会受到哪些因素的影响?
答:3,5-二硝基水杨酸法测定还原糖会受到以下因素的影响:
(1)反应时间:反应时间过短会导致还原糖没有充分被还原为葡萄糖,反应时间过长则会使吸光度值趋于平台,使测定结果不准确。
(2)反应温度:反应温度过高则会使试剂发生非特异性反应,导致
误差增大;反应温度过低则会使反应速率降低,反应不充分,测定结果不
准确。
(3)试剂的浓度:试剂浓度过高或过低均会影响反应结果的准确性,因此应当根据样品的含量调整试剂浓度。
(4)样品颜色:样品的颜色会影响吸光度的测定结果,因此应将样
品与试剂充分混合并进行比色。
(5)其他因素:例如样品中存在着色物质、杂质等都会影响到反应
的准确性。

DNS法测定发酵液中总糖含量3,5-二硝基水杨酸与还原糖共热后被还原成棕红色的氨基化合物,在一定范围内,还原糖的量和反应液的颜色强度呈现比例关系,利用比色法可测知样品的含糖量。
DNS试剂的配方(3,5-二硝基水杨酸试剂):称取酒石酸钾钠18.2g,溶于50ml蒸馏水中,加热(不超过50℃),于热溶液中依次加入3,5-二硝基水杨酸0.63g,NaOH 2.1g(先配成溶液),苯酚0.5g,无水亚硫酸钠0.5 g, 搅拌至溶解完全,冷却后用蒸馏水定容至100ml,贮于棕色瓶中,室温保存。
0.1%葡萄糖标准液:准确称取100 mg分析纯的葡萄糖(预先在105℃干燥至恒重),用少量蒸馏水溶解后定容至100 ml,冰箱保存备用。
注意事项:1. 在配制的过程中,如果操作不合理,会出现溶液变黑,或者有鸡蛋花一样的絮状沉淀出现。
2.称取DNS(具体重量,按照你的配方来,下同),加水溶解,水浴45℃;3.逐步加入氢氧化钠溶液,同时不断搅拌,直到溶液清澈透明;(a.药品中的氢氧化钠要配制成溶液;直接加颗粒,可能产生鸡蛋花;b.加入氢氧化钠溶液时,溶液的温度会上升,所以要慢慢加,不停地搅拌,同时溶液的温度不能超过48度;温度高了,溶液颜色变黑。
)4. 逐步加入四水酒石酸钾钠、苯酚和无水亚硫酸钠;(顺序最好不要更改!)5.继续45度水浴,同时补水,不断搅拌,直到加入的物质完全溶解;(一定要有耐心地搅拌!)6. 停止加热,冷却至室温,用水定容。
7. 储存在棕色瓶中,避光保存。
室温下存放7天后使用。
有效期为6个月。
(时间不忙的话,最好按照时间来操作,时间紧迫了,时间提前个几天,推后几天,也可以用的)【操作方法】一、葡萄糖标准曲线的绘制取9支大试管,分别按下表顺序加入各种试剂:将上述各管溶液混匀后,用72型分光光度计(520nm)进行比色测定,用空白管溶液调零点,记录光密度值。
以葡萄糖浓度为横坐标,光密度值为纵坐标绘制出标准曲线。

3,5-二硝基水杨酸比色法测定废烟草中总糖第21卷第6期V0I.21NO.6湖北工业大学JournalofHubeiUniversityofTechnology2006年12月Dec.2006[文章编号]1003—4684(2006)12—0062—043,5一二硝基水杨酸比色法测定废烟草中总糖赵春玲,王秀霞,李琼(1湖北工业大学化学与环境工程学院,湖北武汉430068;2莱阳农学院理学院,山东青岛266109)[摘要]对3,5-二硝基水杨酸比色法测定总糖含量的条件进行了研究,结果表明:最佳比色波长为540nm,显色剂的最佳用量为2.5mL,沸水浴时间为5min.对废烟草样品进行测定,试验表明:该方法在2~240/zg?mL浓度范围内遵循比耳定律,呈线性关系(R一0.9993),变异系数为0.46,平均回收率为98.9,该法的准确性和精密度均较好.与经典的斐林试剂法相比,具有操作简便,快速,测定成本低等特点.尤其适合于低浓度糖样的测定.[关键词]废烟草;总糖;3,5-二硝基水杨酸比色法;斐林试剂法[中图分类号]$572.01[文献标识码]:A烟草的综合利用是烟草行业21世纪的重要研究方向.废烟草是卷烟生产过程中产生的烟梗,碎叶,碎末等的总称.如果将这些废料经济合理地利用起来,对于减少原料消耗以实现烟草行业的清洁生产具有重要的现实意义.其中,将烟草下脚料通过工艺处理,如采用造纸法生产来制造所谓"烟草薄片"并将之回用于卷烟生产过程,可以说是实现废烟料综合利用的有效途径之一[】].造纸法烟草薄片生产是指采用造纸工艺的基本原理,辅以化工工艺技术,把烟梗,烟末,碎烟片以及低次等烟叶经过一定的工艺技术处理,制造出符合卷烟配方需要的一种生产工艺.而在烟草薄片的生产过程中如何控制糖类和其他物质的比例以制成高档香烟,是一个新的课题.含糖量是衡量烟草品质好坏的重要指标之一[2].因此,准确地测定废烟草中的总糖含量对回收废料中的含糖物质并用于卷烟再生产过程具有指导作用.废烟草中的主要成分与正常烟草中所含有效成分基本相似但含量有差异,而目前有关废烟草中的总糖含量测定尚未见报道.笔者采用了3,5-二硝基水杨酸(DNS)比色法对废烟草中的总糖进行了测定.其测定原理是利用还原糖能使DNS还原为棕红色的3一氨基一5一硝基水杨酸,在一定范围内,还原糖. 的量和棕红色物质的颜色深浅的程度成一定比例关系[3].笔者对影响测定的多种因素进行了探讨,以期得到最佳测定条件.1材料与方法1.1仪器,材料与试剂紫外可见分光光度计:755S;废烟草:许昌卷烟厂;1mg?mL葡萄糖标准液:准确称取105℃烘至恒重的分析纯葡萄糖100mg溶于少量蒸馏水中,溶解后移入100mL容量瓶中,用蒸馏水定容至100mL,混匀,4℃冰箱中保存备用.DNS试剂:称取6.5gDNS溶于少量热蒸馏水中,加入2mol?L氢氧化钠溶液325mL,再加入45g丙三醇,摇匀,冷却后加水至总体积1000mL,贮于棕色瓶中备用.斐林试剂:A液,称取69.82g硫酸铜,溶于蒸馏水,并稀释至1000mL;B液,称取346g酒石酸钾钠与100g氢氧化钠,溶于蒸馏水,完全溶解后,用水稀释至1000mL,贮存于橡胶塞玻璃瓶内.氢氧化钠溶液(20),Pb(Ac).溶液(20),NaSO溶液(10).浓盐酸(以上试剂均为分析纯).1.2样品预处理称取100g废烟草于2000mL的烧杯内,加入1000mL的热水,在80℃的水浴加热2h,然后再过滤,得到浸提糖液.取糖液100mL(视含糖量而定)于250mL容量瓶内,加入20mL的20Pb(Ac)2溶液,至沉淀完全为止.并加入20mL109/6NazSO[收稿日期]2006—07—03[作者简介]赵春玲(1971一),女,山东齐河人,湖北工业大学讲师,研究方向:分析化学.第21卷第6期赵春玲等3,5一二硝基水杨酸比色法测定废烟草中总糖63溶液,至不再产生沉淀为止.加水至刻度,摇匀,过滤得上清液.取上清液5OmL于100mL容量瓶内,加入5mL的37浓盐酸.并在68℃水浴加热15min.取出后流水冷却.然后用2ONaOH溶液调节pH值至7.5左右,加水至刻度,摇匀并静置.1.3试验方法1.3.1最佳比色波长的测定分别取1mL蒸馏水及2mL的DNS试剂,在沸水浴里加热5min进行显色,取出后用流动水迅速冷却,用蒸馏水定容至25.OOmL,摇匀.以蒸馏水作参比溶液,在440~800 nm波长范围内,用分光光度计测定各个波长处的光吸收值,得到DNS显色剂的吸收曲线.取1mL的1mg?mL葡萄糖标准溶液,1mL的蒸馏水与2mL的DNS试剂,其它步骤同上. 以空白溶液作参比,在440~800nm波长范围内测定吸收值,得到葡萄糖的吸收曲线.1.3.2显色剂用量的选择分别取一定量的显色剂,1mL蒸馏水和1mL1mg?mL葡萄糖标液显色测定.以1.0mL蒸馏水代替葡萄糖标准液为空白.1.3.3沸水浴时间的影响将其它条件固定,改变沸水浴时间,测定反应体系的吸光度.1.3.4稳定性试验测定反应体系随时间变化的吸光度.1.3.5标准曲线的制作分别取一定量的1.0mgmL葡萄糖标准液和蒸馏水.再分别加入DNS试剂2.5mL,进行显色测定.1.3.6干扰性试验取制备的供试液1.0mL,加入2.5mLDNS试剂和1.0mL蒸馏水,用蒸馏水定容至25.OOmL,摇匀,以蒸馏水作参比溶液测定吸光度.1.3.7样品测定取制备的试液稀释适当倍数后各5份,每份1.0mL,按1_3.2项操作.所测样品吸光度值从标准曲线中求出还原糖含量,再计算出废烟草中总糖含量.1.3.8斐林试剂法测定总糖].2结果与分析2.1吸收光谱测定显色剂和葡萄糖标准液在440~800nm范围内的吸收光谱,实验表明两者在低于480nm 以下所测的吸光度都十分不稳定,所以对于测定无实际意义.DNS试剂在480nm处达到最大吸收(图1),葡萄糖标准液在500nm处达到最大吸收(图2).理论应该选择500nm作为测定波长,而在500 nm,520nm处的DNS试剂干扰较大(吸光度值为0.374和0.109),并且吸收值较不稳定.因此,选用540nm作为测定波长(此处DNS的吸光度值为0. 055),显色反应的灵敏度虽有所下降,却消除了干扰,提高了测定的准确度和选择性,因而比较合适. ::图1/nm图2葡萄糖标液的吸收曲线2.2显色剂用量图3为显色剂用量与吸光度关系曲线,在a~b范围内,曲线平直,吸光度出现稳定值,因此可在n ~6范围内选择合适的显色剂用量.在此范围内选择DNS试剂的用量为2.5mL.v/mL图3显色剂用量与吸光度关系曲线2.3沸水浴时间的影晌由图4可知,沸水浴时间在3min内,显色液的吸光度随显色时间的延长而增加较快,3min之后, 吸光度随时间变化不大.尤其在5min之后,显色后的吸光度已基本趋于稳定.因此,取DNS试剂与还原糖反应的显色时间为5min.O51O152O沸水浴时间/rain图4吸光度一沸水浴时间曲线2.4稳定性试验由图5可知,吸光度在3O~60min内稳定,随着时间的推移,吸光度缓慢减小.因此要保证显色后的60min内测定吸光度,以减少误差.32l0O0O32lO0O64湖jb工业大学2006年第6期图5吸光度与稳定时间的关系曲线2.5标准曲线实验得到回归方程为Y一0.0066X一0.0246, R:0.9993,在2~240/lg?mL范围内呈良好线性关系.2.6干扰性试验按1.2项中方法除蛋白后烟草浸提液仍带有颜色,为考察颜色对测定的影响,按1.3.6做干扰试验得到烟草浸提液的吸光度值为0.021.说明糖液的颜色的干扰不大,无需进行进一步脱色处理,但需要选不加热的样品糖液和DNS试剂作参比,以消除色素影响.2.7方法的精密度与重复性表1和表2分别表示精密度和重复性实验结果.从表1中可以看取同一均匀样品5份,测得废烟草浸提液中的总糖含量为0.656,变异系数为0.30%,说明该方法具有较好的精密度.从表2可以看出该方法的重复性实验结果较为理想.表1精密度实验结果2.8回收率回收率实验结果见表3.由表3可知,采用DNS比色法测定废烟草中的总糖含量,方法的回收率在97~101%之间,说明该方法准确度较高.表3回收实验结果样品加入量/ug回收量/ug回收率/500.0500.o500.0500.0500.05O2.3487.1498.5494.7490.9100.597.499.798.998.22.9DNS比色法和斐林试剂法的比较两种方法的测定结果比较见表4.表4DNS比色法与斐林试剂法结果比较样品号DNS比色法/斐林试剂法/0.6560.6590.6560.6600.660O.655O.672O.6690.668O.668O.665O.672由表4知,DNS比色法与经典的斐林试剂法所得的总糖含量的差异性不显着.斐林试剂法是经典的测糖方法,以其试剂稳定,需用仪器设备少等优点而被广为采用.然而,由于各种内外因素的影响,即使是熟练的技术人员,在实际操作过程中,须多次平行测定才能满足误差要求,实验过程比较费时,而且对于含量低的样品测定误差较大,需要对样品进行浓缩处理.DNS比色法与之相比,具有快速省时,操作简单,试剂消耗少等优点.3结论与展望笔者研究了DNS比色法测定废烟草水提取物中的总糖含量.通过单因素实验确定:样品量和显色剂用量为1:2.5,煮沸5min后,以不煮沸的样品液与DNS试剂作为测定时的参比液,在540nm处测定吸光度.在最佳实验条件下所得的葡萄糖标准曲线,其回归方程为Y一0.0066X一0.0246,R一0.9993,在2~240#g?mL-1范围内呈良好线性关系.试验证实,此法与经典的斐林试剂法测定结果差异性不显着.并且DNS比色法测定总糖稳定性好, 重现性好,测定结果的精密度,准确度高.这是因为DNS比色法消除了斐林试剂法测定过程中的加热温度,滴定速度等很难控制的参数,操作简单,测定快速准确,测试成本低.笔者已将膜分离等高新技术应用于制造烟草薄片的最新工艺,该工艺中,废烟草水提液中糖类物质O655O34443●●●●●OOOOO96OO55566566666●●●●●OOOOO27O376566566666●●●●●OOOOO6O6845655566666●●●●●OOOOOO23676565566666●●●●●OOOOO847325556566666●●●●●OOOOO782O65566566666●●●●●OOOOO第21卷第6期赵春玲等3,5一二硝基水杨酸比色法测定废烟草中总糖65的检测并回用是重要一环,尤其是在检测低浓度的[2]含糖提取液方面,DNS比色法显示出明显的优势.[参考文献][1]韩卿,张美云,吴养育.造纸法烟草薄片制造工艺的研究[J].西北轻工业学院,2002,1(20):19—22.[3][4]施剑,张怀壁.对测定烟草中水溶性总糖含量使用萃取剂的探讨[J].烟草科技,1993,102(5):21—22.宋占午,王莱,刘艳玲,等.3,5一二硝基水杨酸测定还原糖含量的条件探讨[J].西北师范大学(自然科学版),1997,33(2):52—55.刘福岭,戴行钧.食品物理与化学分析方法[M].北京:轻工业出版社,1978:50—64. OnDeterminingtheTotalSugarinTobaccoResidueswith3,5-DinitrosalicyliCAcidColorimetryZHAOChu-ling,W ANGXiu—xia,LIQong(1SchoolofChemicalandEnvironmentalEngin.,HubeiUniv.ofTechnology,Wuhan430068,China;2TheCollegeofScience,LaiyangAgricultureUniv.Qingdao,266109,China) Abstract:Factorsaffectingthe3,5一Dinitrosa1icy1icacidticle.Itissuggestedthatthebestsuitablewavelengths(DNS)determinationhavebeenstudiedinthisar—fordeterminationiS540nm,andthebestsuitableamountofcolorreagentis2.5mL.Theboilingtimefordevelopingshouldbeabout5min.Whe ntobaccoresiduessamplesaredetermined.Beefs1awisobeyedinaconcentrationrangeof2~240gmLf or540nmwithagoodcorrelationcoefficient(R===0.9993).Theproposedmethodhasagoodprecision withaRSDof0.46%paredwiththeclassicalFehlingmethod,DNScolor imetryissimpler,morerapidandcheaper.Thismethodespeciallyissuitablefordetermining1owercon c'entrationto—ta1sugarofsamples.Inaword,DNScolorimetrywil1bebenefitonreusingoftobaccoresidues .Keywords:tobaccoresidues;totalsugar;3,5一Dinitrosalicylicacidcolorimetry;fehlingmethod[责任编辑:张培炼]。

实验⼀还原糖和总糖的测定——3,5⼆硝基⽔杨酸⽐⾊法《⽣物化学》实验指导书适⽤专业:⽣物科学、⾷品科学、⽣物⼯程、农学、园艺、环境科学孝感学院⽣命科学与技术学院⽣物化学实验细则为了保证⽣物化学实验的顺利进⾏,培养同学们掌握良好、规范的⽣物化学基本实验技能,特制定以下实验细则,请同学们严格遵守。
1. 实验前应提前预习实验指导书并复习相关知识。
2. 严格按照⽣物化学实验分组,分批进⼊实验室,不得迟到。
⾮本实验组的同学不准进⼊实验室。
3. 进⼊实验室必须穿实验服。
各位同学进⼊各⾃实验⼩组实验台后,保持安静,不得⼤声喧哗和嬉戏,不得⽆故离开本实验台随便⾛动。
绝对禁⽌⽤实验仪器或药物嬉耍。
4. 实验中应保持实验台的整洁,废液倒⼊废液桶中,⽤过的滤纸放⼊垃圾桶中,禁⽌直接倒⼊⽔槽中或随地乱丢。
5. 实验中要注意节约药品与试剂,爱护仪器,使⽤前应了解使⽤⽅法,使⽤时要严格遵守操作规程,不得擅⾃移动实验仪器。
否则,因⾮实验性损坏,由损坏者赔还。
6. 使⽤⽔、⽕、电时,要做到⼈在使⽤,⼈⾛关⽔、断电、熄⽕。
7. 做完实验要清洗仪器、器⽫,并放回原位,擦净桌⾯。
8. 实验后,要及时完成实验报告。
⽬录实验⼀还原糖和总糖的测定——3,5-⼆硝基⽔杨酸⽐⾊法...............................1实验⼆油脂酸价的测定............................................................5实验三蛋⽩质的提取及浓度测定?(紫外吸收法)........................................7实验四淀粉酶活⼒的测定...........................................................9实验五酶的激活和抑制作⽤......................................................13实验六氨基酸的分离鉴定――纸层析法............................................14实验七基因组DNA的快速提取---碘化钾法........................................16实验⼋琼脂糖凝胶电泳技术――DNA样品检测.....................................18实验⼀还原糖和总糖的测定——3,5-⼆硝基⽔杨酸⽐⾊法⼀、⽬的与要求掌握还原糖和总糖测定的基本原理,学习⽐⾊法测定还原糖的操作⽅法和分光光度计的使⽤。

收稿日期:2018-12-21作者简介:宋娇娇(1986-),女,助理工程师,硕士研究生,主要从事酿酒工艺与微生物研究工作。
优先数字出版时间:2019-01-25;地址:/kcms/detail/52.1051.TS.20190125.1246.003.html 。
DOI :10.13746/j.njkj.20183633,5-二硝基水杨酸法测定黄水中总糖的含量宋娇娇,裴斐,马勇,朱青,赵祥(江苏洋河酒厂股份有限公司,江苏宿迁223800)摘要:建立3,5-二硝基水杨酸(DNS )测定黄水中总糖含量的方法,对检测条件和黄水总糖水解条件进行优化,并进行方法学考查。
结果表明,最佳检测条件:显色剂添加量5mL ,显色时间7min ,显色温度90℃;黄水总糖水解条件为:水解时间30min ,盐酸浓度12mol/L ,盐酸添加量15mL ;精密度、重复性和稳定性试验结果的相对标准偏差(RSD )均小于2%,加标回收率94.60%~97.60%,RSD 值均小于2%。
该方法准确、可靠、重现性好,可用于黄水中总糖含量的测定。
关键词:3,5-二硝基水杨酸法;黄水;总糖;测定中图分类号:TS262.3;TS261.7;TS261.9文献标识码:A文章编号:1001-9286(2019)04-0113-05Determination of Total Sugar Content in YellowWater by 3,5-Dinitrosalicylic Acid MethodSONG Jiaojiao,PEI Fei,MA Yong,ZHU Qing and ZHAO Xiang(Yanghe Distillery Co.Ltd.,Suqian,Jiangsu 223800,China)Abstract :The determination of total sugar content in yellow water by 3,5-dinitrosalicylic acid (DNS)method had been developed.The optimum hydrolysis conditions of total sugar were summed up as follows:hydrolysis time was 30min,hydrochloric acid concen-tration was 12mol/L,and the addition level of hydrochloric acid was 15mL.The optimum detection conditions were summed up as follows:DNS amount was 5mL,coloration time was 7min,and reaction temperature was at 90℃.The relative standard deviation (RSD)of precision,repeatability and stability were less than 2%,the adding standard recovery rate were 94.60%to 97.60%,and RSD was below 2%.This method was reliable,accurate and reproducible,and it could be used for the determination of total sugar content in yellow water.Key words :3,5-dinitrosalicylic acid (DNS)method;yellow water;total sugar;determination黄水是浓香型白酒主要的副产物,黄水中含有丰富的酸类、酯类、醇类等呈香呈味物质[1],同时含有大量的糖和蛋白质等大分子物质,限制了黄水的应用[2],通常将黄水经预处理后再利用,总糖含量是评价处理效果的标准之一。
一、概述还原糖是一类可溶于水的碳水化合物,通常具有甜味。
在食品加工和生产中,还原糖的含量是一个重要的指标。
测定食品中还原糖的含量对于保障产品质量和食品安全具有重要意义。
而3,5-二硝基水杨酸比色法是一种常用的方法来测定还原糖的含量。
二、3,5-二硝基水杨酸比色法原理3,5-二硝基水杨酸比色法是利用还原糖与3,5-二硝基水杨酸在酸性溶液中发生还原反应,生成带有黄色的还原糖-3,5-二硝基水杨酸络合物。
通过比色测定络合物的吸光度,可以间接测定还原糖的含量。
这种方法的优点是操作简便、灵敏度高、准确性较好,因此被广泛用于食品、医药等领域的还原糖含量测定。
三、实验步骤1. 样品制备:将待测食品样品制成均匀的糊状。
2. 提取还原糖:将制好的样品用水提取,得到含有还原糖的提取液。
3. 混合试剂:将3,5-二硝基水杨酸试剂与提取液进行混合,使其发生化学反应生成还原糖-3,5-二硝基水杨酸络合物。
4. 比色测定:用比色计测定络合物的吸光度,据此计算出还原糖的含量。
四、实验注意事项1. 实验操作中需注意安全,避免接触到有毒化学品。
2. 实验操作要严格按照步骤进行,避免操作失误。
3. 比色计要保持清洁,以确保测定结果的准确性。
五、实验结果分析通过3,5-二硝基水杨酸比色法测定出的还原糖含量可以作为食品加工和质量控制的重要数据。
实验结果的准确性和稳定性对于保障产品质量和食品安全具有重要意义。
六、实验应用3,5-二硝基水杨酸比色法不仅在食品加工领域有重要应用,还在医药、化工等领域具有广泛的应用。
对该方法的研究和实际应用具有重要价值。
七、结论3,5-二硝基水杨酸比色法是一种简便、灵敏度高的测定还原糖含量的方法,具有较好的准确性和实用性。
在食品加工和生产中,该方法有着重要的应用价值,能够为保障产品质量和食品安全提供重要数据支持。
八、参考文献1. Zhang, Y.; Wu, X.; Chen, Z. A. M. Determination of Reducing Sugars in Low Concentrations by 3,5- dinitrosalicylic Acid Method in Tapered Microfluidic Channels. Anal. Chem. 2017, 89, 9750-9756.2. Miller, G. L. Use of Dinitrosalicylic Acid Reagent for Determination of Reducing Sugar. Anal. Chem. 1959, 31, 426-428.以上就是3,5-二硝基水杨酸比色法测定还原糖含量的一些基本内容,该方法的简便性和高灵敏度使其成为食品加工和生产中常用的一种检测手段。
实验二3,5-二硝基水杨酸比色定糖法定制葡萄糖标准曲线马铃薯总糖含量测定实验目的1. 熟悉并掌握7200型分光光度仪的结构及工作原理和操作使用方法;2. 掌握分光光度法测定物质含量的基本操作步骤及微机绘制标准曲线的操作方法;3.掌握3,5-二硝基水杨酸比色定糖法测定还原糖(葡萄糖)的原理及方法;4.掌握3,5-二硝基水杨酸比色定糖法测定马铃薯总糖含量测定的原理与方法。
实验原理1. 3,5-二硝基水杨酸比色定糖法测定还原糖(葡萄糖)的及标准曲线定制原理3,5-二硝基水杨酸在强碱溶液中与还原糖在沸水浴中加热反应后被还原成棕红色的氨基化合物,该有色物质在540nm 处有最大吸光度,且在一定浓度范围内(一般OD值在0.2~0.8范围内线性较好),还原糖的量与反应液的颜色强度(吸光度OD值)呈线性关系,利用分光光度仪,以分析纯葡萄糖为还原糖测定的标准品,在540nm处按梯度依次测定各葡萄糖浓度对应的反应液的吸光度(OD值)大小,通过微机处理数据,定制葡萄糖标准曲线,确定出3,5-二硝基水杨酸比色定糖法测定还原糖的线性回归方程;2. 3,5-二硝基水杨酸比色定糖法测定马铃薯总糖含量测定的原理先将马铃薯去皮,经机械粉碎,过滤和清水漂洗,烘干制成马铃薯淀粉;再精确称取干燥恒重后的马铃薯淀粉加酸水解为还原糖,经中和定容,配制成马铃薯总糖含量测定的待测液(即样品液);再以标准曲线测定的加样操作方法,测定出样品待测液的吸光度大小,将测定的吸光度大小代入其回归方程,即可计算出样品待测液的显色浓度,根据稀释倍数关系,计算出以还原糖的量表示的马铃薯总糖的量,并测定出马铃薯总糖百分含量。
该方法是半微量定糖法,操作简便,快速,杂质干扰较少。
实验操作1. 3,5-二硝基水杨酸比色定糖法定制葡萄糖标准曲线(1)葡萄糖标准溶液的配制:(2mg/mL)准确称取2000mg分析纯的葡萄糖(预先在105℃干燥至恒重),用少量蒸馏水溶解后定容至1000mL,冰箱保存备用(2)葡萄糖标准曲线定制加样操作及测定结果纪录(详见表1)按表1进行实验操作,在沸水浴中准确反应20min,取出后立即用冷水冷却,加蒸馏水定容至25mL,摇匀,用lcm的比色杯于540nm处测光密度值。
3,5-二硝基水杨酸比色法测定糖含量
3,5-二硝基水杨酸比色法是一种常用于测定糖含量的方法。
该方法基于糖的还原性,利用糖与3,5-二硝基水杨酸反应生成一个特定的有色产物,通过测量这个有色产物的吸光度,可以确定糖的含量。
下面是该方法的步骤:
1. 准备一定浓度的3,5-二硝基水杨酸溶液。
可以将一定量的3,5-二硝基水杨酸粉末溶解在适量的溶剂(如醇)中,制备出一定浓度的3,5-二硝基水杨酸溶液。
2. 准备样品溶液。
将待测糖溶解在适量的溶剂中,制备出合适浓度的糖溶液。
3. 反应。
将一定量的样品溶液与一定量的3,5-二硝基水杨酸溶液混合,在适当的温度下进行反应。
4. 吸收测量。
将反应后的溶液用比色皿装入分光光度计中,设置波长(通常为540 nm),测量吸光度。
5. 构建标准曲线。
根据已知浓度的糖溶液,按照上述步骤测量吸光度,并绘制出吸光度与糖浓度之间的关系图。
可以根据标准曲线来确定未知样品中糖的含量。
需要注意的是,该方法只适用于对还原性糖进行测定,不适用
于非还原性糖的测定。
同时,实验过程中要注意操作规范和安全,避免接触有毒物质。
3,5-二硝基水杨酸法测定发酵型果露酒中总糖含量杨宁;王伟明;姚琳;董坤【摘要】The detection method of total sugar in fermented fruit wine was established by 3,5-dinitrosalicylic acid (DNS) method,and the hydrolysis conditions of total sugar and the detection conditions of reducing sugar were optimized.The results showed that the reducing sugar content in fruit wine were as follows:absorption wavelength 540 nm,DNS color developing agent 3 ml,boiling water bath 9 min,color developing time 20 min;the hydrolysis conditions of total sugar were as follows:1∶1 (Ⅴ/Ⅴ) hydrochloric acid addition 7 ml,80 ℃ water bath heating 20 min.Glucose content in the range of 0.2-1.0 mg/ml had good linear relation with the absorbance value (R2=0.999 8).The relative standard deviation (RSD) of precision,repeata bility and stability tests results were all less than 2%.The average adding standard recovery rate was 98.53%,RSD was 0.50%,which indicated that the method was reliable,accurate and good reproducible,and could be used for the determination of total sugar content in fermented fruit wine.%通过3,5-二硝基水杨酸(DNS)法建立发酵型果露酒中总糖的检测方法,并对总糖的水解条件和还原糖的检测条件进行了优化.结果表明,果露酒中还原糖的检测条件为:吸收波长540 nm,DNS显色剂3mL,沸水浴加热9min,显色20 min;总糖的水解条件为:1∶1 (Ⅴ/Ⅴ)盐酸添加量7mL,80 ℃水浴加热20 min.葡萄糖质量浓度在0.2~1.0 mg/mL范围内与吸光度值呈良好的线性关系(相关系数R2=0.999 8),精密度、重复性和稳定性试验结果的相对标准偏差(RSD)均<2%,平均加标回收率为98.53%,RSD值为0.50%,表明该方法可靠、准确、重现性好,可用于发酵型果露酒中总糖含量的测定.【期刊名称】《中国酿造》【年(卷),期】2018(037)001【总页数】4页(P181-184)【关键词】3,5-二硝基水杨酸法;发酵型果露酒;总糖含量;测定【作者】杨宁;王伟明;姚琳;董坤【作者单位】黑龙江省中医药科学院中药研究所,黑龙江哈尔滨150036;黑龙江省中医药科学院中药研究所,黑龙江哈尔滨150036;黑龙江省中医药科学院中药研究所,黑龙江哈尔滨150036;黑龙江省中医药科学院中药研究所,黑龙江哈尔滨150036【正文语种】中文【中图分类】TS262.7果露酒是果酒和露酒的统称。
基于3,5-二硝基水杨酸比色法建立一种快速测定总糖含量的方法任婧;李景富;张佳;刘俊芳;许向阳;姜景彬【摘要】本实验利用3,5-二硝基水杨酸(DNS)比色法对番茄果实总糖含量进行了测定,并初步建立了微型化DNS比色法测定总糖含量的实验方法和DNS比色法测定番茄总糖含量的最佳条件,对影响测定结果的因素:测定波长、显色剂用量、显色时间进行了单因素试验.结果表明,540 nm波长、0.2 mL DNS、沸水浴4 min为最佳测定条件.该最佳测定条件下,葡萄糖含量在20~200 μg与吸光值呈良好的线性关系.利用得到优化方法对4个番茄品种的总糖含量进行了测定,结果表明测定样品在1.5 h内的吸光值较为稳定,RSD为2.19%~2.88%.本研究得到番茄果实总糖含量测定的优化方法,是一种稳定、高效可行的测定方法,为番茄高糖品种的鉴定和筛选提供了依据.【期刊名称】《黑龙江科学》【年(卷),期】2017(008)010【总页数】4页(P66-69)【关键词】番茄;DNS;酶标仪【作者】任婧;李景富;张佳;刘俊芳;许向阳;姜景彬【作者单位】东北农业大学园艺园林学院,哈尔滨 150036;东北农业大学园艺园林学院,哈尔滨 150036;东北农业大学园艺园林学院,哈尔滨 150036;东北农业大学园艺园林学院,哈尔滨 150036;东北农业大学园艺园林学院,哈尔滨 150036;东北农业大学园艺园林学院,哈尔滨 150036【正文语种】中文【中图分类】TS255.7番茄(Lycopersicon esculentum Mill),原产于南美洲的秘鲁和墨西哥,营养丰富,是人们餐桌上不可缺少的蔬菜。
番茄也是全世界种植最为普遍的蔬菜作物之一。
番茄含有VA、VC、叶酸、钾等主要的营养元素,其中富含的番茄红素可以清除人体内的活性氧自由基,延缓衰老,同时具有预防癌症、心血管疾病等功能[1]。
因此,近些年番茄果实的风味品质和营养含量也越来越受到人们的关注[2]。
总糖含量的测定——3, 5-二硝基水杨酸法
原理:在氢氧化钠或丙三醇的的存在下, 还原糖能将3, 5-二硝基水杨酸(DNS) 中的硝基还原成氨基, 生成氨基化合物, 此化合物在过量的氢氧化钠碱性溶液中呈橘红色。
试剂:葡萄糖;3, 5-二硝基水杨酸(化学纯) ;酒石酸钾钠、苯酚、盐酸、氢氧化钠、无水亚硫酸钠(均为分析纯);超纯水。
仪器和设备:紫外可见分光光度计;电子天平(感量为0.0001g);电热鼓风干燥箱;电热恒温水浴锅。
溶液的配制
(1)DNS试剂的配制:称取18.2 g酒石酸钾钠、0.63 g3,5-二硝基水杨酸、2.1 g Na OH、0.5 g苯酚、0.5 g无水Na2SO3,分别加少量超纯水溶解,将酒石酸钾钠溶液放于45℃水浴锅,然后依次加入上述溶解好的试剂,边加边搅拌,取出后冷却至室温,加超纯水定容至100 m L,贮存于棕色瓶内,暗处保存,一周后使用。
(2)葡萄糖标准溶液的配制:将葡萄糖置于105℃中干燥至恒重,精密称取0.100g 葡萄糖于100mL烧杯中,加水溶解,定容至1000mL,即得浓度为0.1mg/mL的葡萄糖标准溶液。
样品溶液的制备:准确称取样品0.2g~1.0g,精确到0.0001g,于50 mL试管中,加入20 m L蒸馏水,在沸水浴中煮沸20 min,取出冷却,过滤入100 mL容量瓶中,用蒸馏水冲洗残渣数次,定容至刻度,即为样品测定液。
标准曲线的制作:
精密量取0.1mg/mL的葡萄糖标溶液0mL,0.2mL,0.4mL,0.6mL,0.8mL,1.0mL 置于25mL具塞比色管中,加入蒸馏水补充至2.0mL。
向试液中分别加入3 mL DNS显色剂,于沸水浴中加热9 min,立即冷却至室温,定容至刻度,显色20 min后于波长540 nm处,用可见分光光度计测定不同浓度葡萄糖混合溶液的吸光度,并以葡萄糖质量浓度 (x)为横坐标,吸光度 (y)为纵坐标,绘制葡萄糖溶液标准曲线。
比色测定:吸取1.00mL样品测定液于25mL比色管中,向试液中分别加入3 mL DNS 显色剂,于沸水浴中加热9 min,立即冷却至室温,定容至刻度,显色20 min后于波长540 nm处,用可见分光光度计测定不同浓度葡萄糖混合溶样品溶液的吸光度,每个样品重复3次,取平均值。
样品中总糖含量,按式(3)进行计算
(3)
式中:
X3——样品中总糖含量(以葡萄糖计),单位以克每百克(g/100g);
C——从标准曲线上查得样品测定液中葡萄糖的质量浓度,单位为毫克每毫升(mg/mL );
V1——样品定容体积,单位为毫升(mL);
V2——比色测定时所移取样品测定液的体积,单位为毫升(mL);
m——样品的质量,单位为克(g);
0.9——以葡萄糖计算总糖含量的换算系数。
[1]杨宁, 王伟明, 姚琳, 董坤. 3,5-二硝基水杨酸法测定发酵型果露酒中总糖含量[J]. 中国酿造, 2018, 37(01): 181-184.。