高中化学铁及其化合物专题练习
- 格式:doc
- 大小:126.00 KB
- 文档页数:6

人教版(2019)高中化学必修第一册《3.1 铁及其化合物》练习卷(1)一、单选题(本大题共10小题,共30.0分)1.下列关于铁的说法正确的是()A. 纯铁为灰黑色,所以铁属于黑色金属B. 铁在硫蒸气中燃烧生成Fe2S3C. 纯铁的抗腐蚀能力非常强,铁在干燥的空气里不易被氧化D. 铁的化学性质比较活泼,所以铁在自然界中全部以化合态存在2.下列有关实验的说法正确的是()A. 为测定熔融氢氧化钠的导电性,可在石英坩埚中熔化氢氧化钠固体后进行测量B. 除去铁粉中混有的少量铝粉,可加入过量的氢氧化钠溶液,完全反应后过滤C. 制备Fe(OH)3胶体,通常是将NaOH加入FeCl3溶液中D. 某溶液中加入盐酸产生使澄清石灰水变浑浊的气体,则该溶液中一定含有CO32−3.铁的常见化合价有+2价和+3价。
据研究,铁在浓HNO3中发生钝化时,可生成一种化学式为Fe8O11的化合物,它可以看作由FeO和Fe2O3组成的复杂氧化物。
该化合物可以表示为()A. FeO·3Fe2O3B. FeO·2Fe2O3 C. 2FeO·3Fe2O3D. 2FeO·Fe2O34.下列关于铁的氧化物说法不正确的是()A. 铁的氧化物通常状况下都是有色固体B. 四氧化三铁是一种复杂的铁的氧化物,它与盐酸反应后的溶液中同时存在Fe2+和Fe3+C. 氧化铁是铁锈的主要成分,因此氧化铁俗称为铁锈D. 工业上常使用铁的氧化物作原料冶炼铁5.为了验证Fe3+的性质,某化学兴趣小组设计了如图所示的一组实验,其中实验方案设计错误的是()A. 只有④B. 只有③C. ③和④均错D. 全部错误6.要证明某溶液中不含Fe3+而含有Fe2+,所采用的最佳方法是()A. 加入适量的氯水,再加入少量KSCN溶液B. 加入少量KSCN溶液,再加入适量的氯水C. 加入少量KSCN溶液,再加入适量的铁粉D. 加入适量的氢氧化钠溶液,观察颜色的变化7.向FeCl3、CuCl2的混合溶液中加入一定量的铁粉,充分反应后仍有固体存在,则下列判断不正确的是()A. 剩余固体中一定含CuB. 充分反应后的溶液中一定含Fe2+C. 向充分反应后的溶液中加入KSCN,溶液一定不为红色D. 充分反应后的溶液中一定含有Cu2+8.检验用硫酸亚铁制得的硫酸铁中是否含有硫酸亚铁,可选用的试剂是()A. NaOHB. KMnO4C. KSCND. 苯酚9.已知下列三组实验:①向KMnO4晶体上滴加浓盐酸,产生氯气;②向FeCl2溶液中通入少量氯气,溶液变黄色;③取实验②中生成的溶液滴在淀粉KI试纸上,试纸变蓝色.则下列判断不正确的是()A. 实验①能够证明Cl−具有还原性B. 上述实验不能证明Fe2+具有氧化性C. 上述实验能够证明氧化性:MnO4−>Cl2>Fe3+>I2D. 由上述实验不能判断氯气能使湿润的淀粉KI试纸变蓝10.下列实验操作正确的是()A. 用图1示装置制备Cl2B. 将混合气体通过装有NaOH溶液的洗气瓶除去Cl2中混有的HClC. 用图2示装置分离CH3COOC2H5与饱和Na2CO3溶液D. 称取1.06 g Na2CO3固体,置于100 mL容量瓶中,加水稀释,配制0.10mol⋅L−1的Na2CO3溶液二、实验题(本大题共4小题,共40.0分)11.某同学欲在实验室中完成Fe与水蒸气反应的实验,实验装置如图甲、乙所示。

高中化学《铁及其化合物》练习题学校:___________姓名:___________班级:_________________一、单选题1.珊瑚是由无数珊瑚虫分泌出的石灰质长期积淀而形成的。
红珊瑚之所以是红色,最有可能的是含有 ( )A .NO 2B .Fe 3O 4C .Fe 2O 3D .Al 2O 32.下列关于物质用途的叙述中不正确的是( )A .Na 2O 2可用作呼吸面具中的供氧剂B .硅胶多孔,吸水能力强,可做食品干燥剂C .Al(OH) 3可作治疗胃酸过多的一种药剂D .四氧化三铁俗称铁红,可用于作油漆、红色涂料3.化学与生产、生活、环境密切相关,下列有关说法错误的是( )A .氧化铁可用于红色油漆和涂料B .明矾可用于自来水的杀菌消毒C .N95活性炭口罩可用于防霾,其原理是吸附原理D .氨气易液化,汽化时会吸收大量热,可做制冷剂4.下列试剂的保存方法错误..的是( ) A .实验室少量的钠保存在煤油中B .浓硝酸保存在无色细口玻璃瓶中C .存放FeSO 4溶液时加入少量铁粉D .NaOH 溶液保存在橡皮塞的试剂瓶中5.将m g 铁和氧化铁的混合物加入100mL 浓度为11mol L -⋅盐酸中,恰好完全反应,放出标准状况下的气体0.448L 。
滴加KSCN 溶液,溶液不变色。
则下列判断正确的是( )A .原混合物中()23Fe O :(Fe)3:1n n =B .无法计算原混合物的质量C .收集产生的气体刚好能与20.224L Cl 完全反应D .向溶液中通入20.025mol Cl ,可以将2Fe +完全转化为3Fe +6.1.12克铁粉加入25mL 2mol/L 的氯化铁溶液中,正确的是( )A .溶液中[Fe 2+]<[Fe 3+]B .溶液中[Fe 2+]>[Fe 3+]C .部分Fe 3+被氧化D .在反应后的溶液中加入KSCN 溶液,会出现血红色沉淀7.下列有关溶液组成的描述合理的是()+、Cl-、I-A.无色溶液中可能大量存在Fe3+、NH4-、Cl-B.酸性溶液中可能大量存在Na+、ClO-、SO24-C.弱碱性溶液中可能大量存在Na+、K+、Cl-、HCO3-、SCN-D.FeCl3溶液中可能大量存在Mg2+、Al3+、MnO48.N A代表阿伏加德罗常数的值。

高考化学铁及其化合物综合练习题附答案一、高中化学铁及其化合物1.有一种埋在地下的矿物X(仅含四种元素),挖出后在空气中容易发黄,现探究其组成和性质,设计完成如下实验:请回答:(1)X的化学式_________________,挖出后在空气中容易发黄的原因______________。
(2)写出溶液分二等份,加KSCN无明显现象后,滴加双氧水的两个离子方程式:___________________,_________________。
【答案】Fe2(OH)2CO3或Fe(OH)2·FeCO3 +2价铁元素被空气氧化为+3价铁元素2Fe2++H2O2+2H+=2Fe3++2H2O Fe3++3SCN-= Fe(SCN)3【解析】【分析】⑴先计算分解生成的水的物质的量,再计算CO2的物质的量,根据现象得出含有亚铁离子并计算物质的量,根据比例关系得出化学式。
⑵滴加双氧水是Fe2+与H2O2反应生成Fe3+,Fe3+与3SCN-反应生成血红色。
【详解】⑴分解生成的水是1.8g,物质的量是0.1mol;无色无味气体是CO2,物质的量是0.1mol;黑色固体用稀硫酸溶解后分为两等分,滴加KSCN溶液没有实验现象,然后滴加双氧水变为血红色,则含有亚铁离子;另一份加入足量的氢氧化钠溶液得到沉淀,过滤洗涤并充分灼烧后得到8g固体,该固体是氧化铁,物质的量是0.05mol,其中铁元素的物质的量是0.1mol,则黑色固体中亚铁离子的物质的量是0.2mol,所以氧化亚铁是0.2mol,X中相当于含有0.1氢氧化亚铁和0.1mol碳酸亚铁,所以化学式为Fe2(OH)2CO3或Fe(OH)2·FeCO3,挖出后在空气中容易发黄的原因是+2价铁元素被空气氧化为+3价铁元素;故答案为:Fe2(OH)2CO3或Fe(OH)2·FeCO3;挖出后在空气中容易发黄的原因是+2价铁元素被空气氧化为+3价铁元素。

铁及其化合物一、选择题(本题包括10小题,每小题5分,共50分)1.下列反应,其产物的颜色按红色、红褐色、淡黄色、蓝色顺序排列的是()①金属钠在纯氧中燃烧②FeSO4溶液中滴入NaOH溶液,并在空气中放置一段时间③FeCl3溶液中滴入KSCN溶液④无水硫酸铜放入医用酒精中A.②③①④B.③②①④C.③①②④D.①②③④2.已知下述三个实验中均有化学反应发生。
下列判断正确的是()A.实验①中铁钉只做还原剂B.实验②中Fe2+既显氧化性又显还原性C.实验③中发生的是置换反应D.上述实验证明氧化性:Fe3+>Fe2+〉Cu2+3.在含有FeCl3和BaCl2的酸性溶液中,通入足量的SO2后有白色沉淀生成,过滤后,向溶液中滴加KSCN 溶液,无明显现象,下列叙述不.正确的是()A.白色沉淀是BaSO4和BaSO3B.溶液的酸性增强C.白色沉淀是BaSO4D.FeCl3全部被还原为FeCl24.某溶液中有Fe3+、Mg2+、Fe2+和Al3+四种阳离子,若向其中加入过量的氢氧化钠溶液,搅拌后,再加入过量的盐酸,溶液中大量减少的阳离子是()A.Fe3+B.Mg2+C.Fe2+D.Al3+5.下列离子方程式书写正确的是()A.FeO固体放入稀硝酸溶液中:FeO+2H+===Fe2++H2OB.过量的铁粉与稀硝酸溶液反应:Fe+4H++NO错误!===Fe3++NO↑+2H2OC.向氢氧化亚铁中加入足量的稀硝酸:Fe(OH)2+2H+===Fe2++2H2OD.向Fe(OH)3中加入氢碘酸:2Fe(OH)3+6H++2I-===2Fe2++I2+6H2O6.某学生设计了如图所示的方法,鉴定盐A的组成成分。
由此分析,下列结论中正确的是( )A.A中一定有Fe3+B.C中一定有Fe3+C.B为AgI沉淀D.A一定为FeBr2溶液7.高铁酸钠(Na2FeO4)是一种新型、高效、多功能的水处理剂。
湿法制备的主要反应方程式为2Fe(OH)3+3ClO -+4OH-===2FeO2-,4+3Cl-+5H2O。

垫江中学高2018级化学练习题铁及其化合物一、铁单质1.将铁屑溶于过量盐酸后,再加入下列物质,会有三价铁生成的是()A.硫酸B.硫酸铜C.氯水D.氯化铜2.硫酸亚铁溶液含有杂质硫酸铜和硫酸铁,为除去杂质,提纯硫酸亚铁,应该加入下列哪种物质()A.锌粉B.镁粉C.铁粉D.铝粉3.下列有关铁及其化合物的说法中正确的是()A.赤铁矿的主要成分是Fe3O4B.铁与水蒸气在高温下的反应产物为Fe2O3和H2C.除去FeCl2溶液中的FeCl3杂质可以向溶液中加过量铁粉,然后过滤D. 3Fe与KSCN反应产生红色沉淀4.将Fe、Cu、FeCl2、FeCl3、CuCl2盛于同一容器中充分反应,如Fe有剩余,则容器中只能有的金属或金属离子是()A.Cu、Fe3+B.Fe2+、Fe3+C.Cu、Cu2+、FeD.Cu、Fe2+、Fe5.在FeCl3、CuCl2混合溶液中,加入一定量的铁屑,反应完全后将固体滤出,下列说法中正确的是()A.若滤出的固体中只有铜,则溶液中一定含有的阳离子是Fe2+,一定不含Cu2+B.若滤出的固体中只有铜,则溶液中一定含有的阳离子是Fe2+,可能含Cu2+和Fe3+C.若滤出的固体中只有铜,则溶液中一定含有的阳离子是Fe3+和Fe2+,一定不含Cu2+D.若滤出的固体中含有铁和铜,则溶液中一定含有的阳离子是Fe2+,一定不含Cu2+和Fe3+6.已知硝酸能将Fe2+氧化为Fe3+。
下列物质反应后能使KSCN溶液变红的是()①过量的Fe与Cl2反应②Fe与过量稀硫酸反应③FeCl2溶液中通入少量Cl2 ④Fe和Fe2O3的混合物溶于盐酸中A.只有①B.只有①③C.只有①②③D.全部6.金属单质A可发生以下反应。
试推断:(1)A、B、C、D、E分别是(写化学式,B写主要成分):A________、B________、C________、D________、E________。
(2)写出反应③和⑤的离子方程式:③_____________________________;⑤______________________。
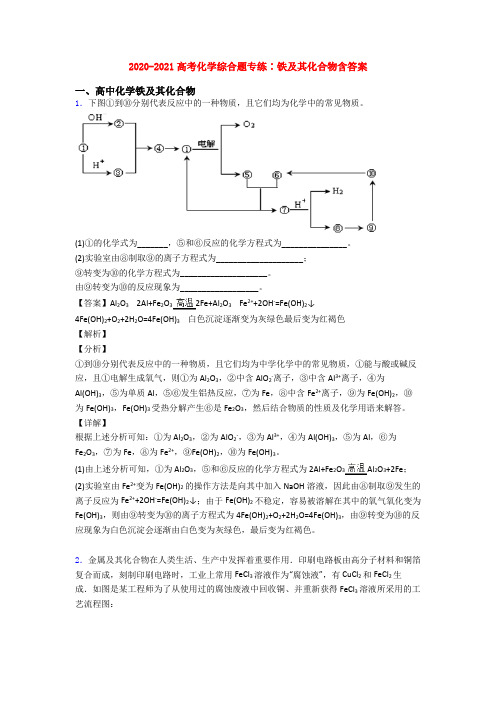
2020-2021高考化学综合题专练∶铁及其化合物含答案一、高中化学铁及其化合物1.下图①到⑩分别代表反应中的一种物质,且它们均为化学中的常见物质。
(1)①的化学式为_______,⑤和⑥反应的化学方程式为_______________。
(2)实验室由⑧制取⑨的离子方程式为____________________;⑨转变为⑩的化学方程式为____________________。
由⑨转变为⑩的反应现象为__________________。
【答案】Al2O3 2Al+Fe2O32Fe+Al2O3 Fe2++2OH-=Fe(OH)2↓4Fe(OH)2+O2+2H2O=4Fe(OH)3白色沉淀逐渐变为灰绿色最后变为红褐色【解析】【分析】①到⑩分别代表反应中的一种物质,且它们均为中学化学中的常见物质,①能与酸或碱反应,且①电解生成氧气,则①为Al2O3,②中含AlO2-离子,③中含Al3+离子,④为Al(OH)3,⑤为单质Al,⑤⑥发生铝热反应,⑦为Fe,⑧中含Fe2+离子,⑨为Fe(OH)2,⑩为Fe(OH)3,Fe(OH)3受热分解产生⑥是Fe2O3,然后结合物质的性质及化学用语来解答。
【详解】根据上述分析可知:①为Al2O3,②为AlO2-,③为Al3+,④为Al(OH)3,⑤为Al,⑥为Fe2O3,⑦为Fe,⑧为Fe2+,⑨Fe(OH)2,⑩为Fe(OH)3。
(1)由上述分析可知,①为Al2O3,⑤和⑥反应的化学方程式为2Al+Fe2O3Al2O3+2Fe;(2)实验室由Fe2+变为Fe(OH)2的操作方法是向其中加入NaOH溶液,因此由⑧制取⑨发生的离子反应为Fe2++2OH-=Fe(OH)2↓;由于Fe(OH)2不稳定,容易被溶解在其中的氧气氧化变为Fe(OH)3,则由⑨转变为⑩的离子方程式为4Fe(OH)2+O2+2H2O=4Fe(OH)3,由⑨转变为⑩的反应现象为白色沉淀会逐渐由白色变为灰绿色,最后变为红褐色。

高一化学必修一铁及其化合物课时练习1 .我国宋代《开宝木草》中记载了中药材铁华粉的制作方法:“取钢煅作叶如笏或团,平面磨错令光净,以盐水酒之,于醋瓮中阴处埋之一百日,铁上衣生,铁华成矣。
”中药材铁华粉是指( )A .铁粉B .氯化铁C .冰醋酸D .醋酸亚铁2 .下列离子的检验方法合理的是()A .向某溶液中滴入KSCN 溶液呈红色,说明溶液中一定不含Fe 2+B .向某溶液中加入NaOH 溶液,有红褐色沉淀生成,说明溶液中一定含有Fe 3+C .向某溶液中通入Cl 2,然后再加入KSCN 溶液变红色,说明原溶液中一定含有Fe 2+D .向某溶液中加入NaOH 溶液得白色沉淀,迅速变为灰绿色,最终变为红褐色,说明该溶液中只含有Fe 2+,不含有 Mg 2+3 .以下物质之间的每步转化中,都能通过一步实现的是() ① FeTFeCl 2-Fe(OH)2TFe(OH)3 ② Na-Naq —Na 2cO 3TNaHCO 3-NaOH③ MgTMgCl 2-Mg(OH)2 ④ Al-A1203TAl(OH)3 ⑤ Al —NaAlO 2-Na 2cO 3A .②③④B .①③④⑤C .①②③⑤D .①②③④⑤4 .常温下氯化铁为棕黑色固体,易升华。
实验室欲证明H 2能在加热的条件下还原FeCl 3,设计如下实验。
下列说法错 误的是()A .装置A 的优点是随开随用,随关随停B .导管m 的作用是平衡压强,观察是否堵塞C .装置D 中产生白色沉淀即可证明H 2能还原FeCl 3D .实验结束后,应先熄灭C 处酒精灯,待硬质玻璃管冷却后关闭K5 .制取Fe (OH )2并使之能久存,可采取的操作有:①加入一些植物油;②溶解FeSO 4配成溶液;③把蒸馏水加热煮沸, 并密封冷却;④加入少量铁屑;⑤向FeSO 4溶液中滴加足量氨水;⑥把盛有氨水的胶头滴管伸入FeSO 4溶液中后再挤 出氨水。
进行操作的正确顺序是()A .③②⑤④B .③②④①⑥C .③②④⑥D .②④①⑥6 .将铁粉、铜粉混合物加入FeCl 3溶液,充分反应后仍有固体存在,则下列判断不正确的是()A .溶液中一定含Cu 2+B .溶液中一定含有Fe 2+。

高考化学铁及其化合物综合练习题及详细答案一、高中化学铁及其化合物练习题(含详细答案解析)1.某固体化合物A,按图所示发生系列变化,已知E溶液中加入氨水后产生的白色沉淀很快变为灰绿色,最后变为红褐色。
回答下列问题:(1)物质A是___(填化学式)。
(2)反应②的离子反应方程式为___。
(3)反应④的化学反应方程式为___。
【答案】Fe(OH)3 Fe2O3+6H+=2Fe3++3H2O 4Fe(OH)2+O2+2H2O=4Fe(OH)3【解析】【分析】已知E溶液中加入氨水后产生的白色沉淀很快变为灰绿色,最后变为红褐色说明A为氢氧化铁,Fe(OH)3,A加热分解生成B为Fe2O3,C为H2O,依据流程分析判断D为FeCl3,X为Fe,E为FeCl2 溶液,据此分析。
【详解】已知E溶液中加入氨水后产生的白色沉淀很快变为灰绿色,最后变为红褐色说明A为氢氧化铁,Fe(OH)3,A加热分解生成B为Fe2O3,C为H2O,依据流程分析判断D为FeCl3,X为Fe,E为FeCl2 溶液。
(1)依据推断可知A为Fe(OH)3;(2)反应②是盐酸和氧化铁发生的复分解反应,反应的离子反应方程式为Fe2O3+6H+=2Fe3++3H2O;(3)反应④是氢氧化亚铁和氧气水发生反应生成氢氧化铁的也还原反应,反应的化学反应方程式为4Fe(OH)2+O2+2H2O=4Fe(OH)3。
2.现有金属单质A、B、C和气体甲、乙、丙以及物质D、E、F、G、H,它们之间的相互转化关系如图所示(图中有些反应的生成物和反应的条件没有标出)。
请根据以上信息完成下列各题:(1)写出下列物质的化学式:B_______、丙__________。
(2)写出黄绿色气体乙的一种用途___________,反应过程⑦可能观察到的实验现象是______。
对应的化学方程式是_______。
(3)反应③中的离子方程式是_________。
【答案】Al HCl 杀菌消毒、强氧化剂、漂白白色沉淀迅速变成灰绿色,最终变成红褐色 4Fe(OH)2+O2+2H2O=4Fe(OH)3 2Al+2OH- +2H2O=2AlO2-+3H2↑【解析】【分析】金属A颜色反应为黄色证明A为金属Na,Na与水反应生成气体甲为H2,D为NaOH;金属B和氢氧化钠溶液反应产生H2,说明B为金属Al,黄绿色气体乙为Cl2,气体甲是H2,H2和Cl2反应生成丙为HCl,HCl溶于水得到的物质E为盐酸溶液,盐酸与金属C反应产生F溶液是金属氯化物,该氯化物与Cl2还可以反应产生G,G与NaOH溶液反应生成红褐色沉淀H为Fe(OH)3,则G为FeCl3,推断物质F为FeCl2;判断C为Fe,以此解答该题。

3.1 铁及其化合物基础知识点练习知识点1 铁单质1.常温下,下列物质可以用铁制容器盛装的是( )A. 浓硫酸B. 浓盐酸C. 硫酸铜溶液D. 硝酸银溶液答案 A2.下列叙述正确的是( ) A.纯铁为灰黑色B.铁锈的主要成分是34Fe O ,不能保护内层金属C.铁在干燥的空气里不易被氧化D.在加热条件下铁与氯气反应生成2FeCl 和3FeCl答案 C3.下列关于铁与水反应的描述错误的是( ) A.铁与水蒸气反应的产物是黑色的23Fe OB.红热的铁能与水蒸气反应,产生的气体可在空气中燃烧C.铁与水蒸气的反应是氧化还原反应D.常温下,Fe 与2H O 不反应,但能与空气中的22O H O 、共同作用发生反应答案 A4.把铁片投入到下列溶液中,铁片质量减少,且没有气体产生,此溶液是( ) A.4FeSO 溶液 B.24H SO 溶液 C.()243Fe SO 溶液D.3AgNO 溶液答案C知识点2 铁的氧化物4.司南是中国古代劳动人民在长期的实践中对磁石磁性认识的发明,《论衡》中记载有“司南之杓,投之于地,其柢指南”。
下列说法正确的是( )A.“杓”的主要成分是四氧化三铁B.纯净的铁在常温下与水反应可得到磁性氧化铁C.磁性氧化铁为23Fe O 和FeO 的混合物 D .Fe 、23Fe O 、34Fe O 均具有磁性答案 A5.下列关于铁的氧化物说法不正确的是( ) A.铁的氧化物通常状况下都是有色固体B.四氧化三铁是一种复杂的铁的氧化物,它与盐酸反应后的溶液中同时存在2+Fe 和3+FeC.氧化铁是铁镑的主要成分,因此氧化铁俗称为铁锈D.工业上常使用铁的氧化物作原料冶炼铁答案 C6.铁的常见化合价有+2价和+3价。
据研究,铁在浓HNO 3中发生钝化时,可生成一种化学式为Fe 8O 11的化合物,它可以看作由FeO 和Fe 2O 3组成的复杂氧化物。
该化合物可以表示为( )A .FeO·3Fe 2O 3B .FeO·2Fe 2O 3C .2FeO·3Fe 2O 3D .2FeO·Fe 2O 3答案 C知识点3 铁的氢氧化物7. 某同学欲利用下图装置制取能较长时间存在的Fe (OH )2,其中实验所用溶液现配现用且蒸馏水先加热煮沸。

铁及其化合物1. 【易】将铁片放到下列溶液中,铁片溶解,溶液质量减轻的是( )A .稀硫酸B .硫酸铜溶液C .氢氧化钠溶液D .氯化铝溶液 【答案】B【解析】铁不与NaOH 溶液和AlCl 3溶液发生反应,C 、D 两项错误;铁与H 2SO 4反应:Fe +H 2SO 4===FeSO 4+H 2↑,溶液质量增加,A 选项错误;Fe 与CuSO 4溶液反应,Fe +CuSO 4===FeSO 4+Cu ,溶液质量减轻,故应选B 。
2. 【易】下列有关铁及其化合物的说法中正确的是( )A .赤铁矿的主要成分是Fe 3O 4B .铁与水蒸气在高温下的反应产物为Fe 2O 3和H 2C .除去FeCl 2溶液中的FeCl 3杂质可以向溶液中加过量铁粉,然后过滤D .Fe 3+与KSCN 反应产生红色沉淀【答案】C【解析】赤铁矿的主要成分是Fe 2O 3,A 错误;铁与水蒸气高温条件下反应生成Fe 3O 4和H 2,B 错误;C项中2FeCl 3+Fe===== 3FeCl 2,过滤可除去过量的铁粉,C 正确;Fe 3+与SCN -反应形成红色溶液而不是红色沉淀,D 错误。
3. 【易】(2012·佛山市高一教学质量检测)下列变化能发生且不.属于氧化还原反应的是( ) A .Fe ――→盐酸FeCl 2 B .Na ―——―→空气中燃烧Na 2O 2C .CuSO 4溶液――→铁CuD .Fe(OH)3――→加热Fe 2O 3 【答案】D【解析】2Fe(OH)3===== △Fe 2O 3+3H 2O 的过程是非氧化还原反应。
4. 【易】下列离子方程式正确的是( )A .铁跟FeCl 3溶液反应:Fe +Fe 3+===== 2Fe 2+B .Fe 跟稀盐酸反应:2Fe +6H +===== 2Fe 3++3H 2↑C .FeCl 2溶液跟Cl 2反应:Fe 2++Cl 2===== Fe 3++2Cl -D .Fe(OH)3跟盐酸反应:Fe(OH)3+3H +===== Fe 3++3H 2O【答案】D【解析】A 中电荷不守恒,应为:Fe +2Fe 3+===== 3Fe 2+;B 中违反反应事实,应为:Fe +2H +===== Fe 2++H 2↑;C 中得失电子、电荷均不守恒,应为:2Fe 2++Cl 2===== 2Fe 3++2Cl -。

高考化学易错题精选-铁及其化合物练习题含答案一、高中化学铁及其化合物练习题(含详细答案解析)1.已知A、B、C、D四种物质均含有铁元素,彼此转化关系如下:请回答:(1)反应①称为铝热反应(属于置换反应),写出该反应的化学方程式:__、其中Al作__剂。
(2)反应④的离子方程式为:__。
(3)新配制的C溶液中应加入__,以防止其转化为D。
检验D溶液中阳离子的常用试剂是__(填化学式),实验现象为__。
【答案】2Al+Fe2O3高温2Fe+Al2O3还原剂 2Fe2++H2O2+2H+=2Fe3++2H2O 铁粉(屑) KSCN (或NH4SCN)溶液变红(或呈现血红色)【解析】【分析】氧化铁与铝单质在高温下发生铝热反应,生成A,则A为Fe,铁和水蒸气在高温下反应生成B,B为黑色磁性氧化物,则B为Fe3O4,Fe3O4中铁元素的化合价含有+2、+3价,与盐酸反应生成FeCl3和FeCl2,铁与过量盐酸反应生成FeCl2,则C为FeCl2,FeCl2与双氧水反应生成FeCl3,则D为FeCl3,据此分析解答。
【详解】(1)反应①称为铝热反应(属于置换反应),该反应的化学方程式:2Al+Fe2O3高温2Fe+Al2O3,反应中Al有0价变为+3价,化合价升高,失电子,被氧化,作还原剂;(2)反应④为FeCl2与双氧水反应生成FeCl3,离子方程式为:2Fe2++H2O2+2H+=2Fe3++2H2O;(3)C为FeCl2,D为FeCl3,亚铁离子具有还原性,易被氧化,新配制的FeCl2溶液中应加入铁粉(屑),以防止其转化为FeCl3。
检验三价铁离子常用试剂是KSCN(或NH4SCN),三价铁离子遇SCN-变为血红色溶液。
2.A、B、C均为中学化学常见的纯净物,它们之间存在如下转化关系:其中①②③均为有单质参与的反应。
(1)若A是常见的金属,①③中均有同一种黄绿色气体参与反应,B溶液遇KSCN显血红色,且②为化合反应,写出反应②的离子方程式_________________________。

第7讲铁及其化合物【练基础】1.春秋初年,我国已掌握了冶铁技术。
下列有关铁的化学反应的叙述正确的是A.室温下,过量Fe与浓硫酸反应生成FeSO4B.加热时,过量Fe与氯气反应生成FeCl2C.高温下,铁与水蒸气反应有Fe3O4生成D.高温下,铁粉与氧化铝粉末反应生成单质铝【答案】C【解析】室温下,Fe在浓硫酸中钝化,无法持续反应,A错误;氯气氧化性较强,无论Fe是否过量与氯气加热反应都只生成FeCl3,B错误;高温条件下,Fe与水蒸气反应得到Fe3O4和氢气,C正确;Fe的活动性不如Al,不能从氧化铝中置换出Al单质,D错误;综上所述答案为C。
2.我国清代《本草纲目拾遗》中叙述了“铁线粉”:“粤中洋行有舶上铁丝,……日久起销,用刀刮其销,……,所刮下之销末,名铁线粉”。
这里的“铁线粉”是指()A.Fe B.FeCl3C.FeO D.Fe2O3【答案】D【解析】铁在空气中容易发生吸氧腐蚀,根据题意“舶上铁丝,……日久起销”,说明销是铁锈,铁锈的主要成分为Fe2O3,D项正确。
3.将铁钉投入热的浓硝酸中,一段时间后,下列说法错误的是A.铁钉表面形成致密的氧化膜B.溶液可能呈棕黄色C.铁钉会溶解D.产生红棕色的气体【答案】A【解析】常温下铁钉在浓硝酸中会发生钝化现象,在铁钉表面形成致密的氧化膜阻碍反应进行,但在热的浓硝酸中不会产生钝化,故A错误;铁钉与过量的热浓硝酸反应生成棕黄色的硝酸铁,则溶液可能呈棕黄色,故B正确;铁钉在浓硝酸中会钝化,但在热的浓硝酸中不会钝化,会发生反应而溶解,故C正确;铁钉能与热的浓硝酸反应,反应中浓硝酸被还原为红棕色的二氧化氮气体,故D正确;故选A。
4.下列物质的用途与氧化还原反应无关..的是A.浓盐酸用于实验室制备氯气B.铁粉用作暖贴发热剂C.干冰用作制冷剂D.镁粉用于炼铁脱硫【答案】C【解析】浓盐酸和二氧化锰发生氧化还原反应,可用于实验室制备氯气,与氧化还原反应有关,A不符合;铁粉用作暖贴发热剂过程中发生铁的腐蚀,铁被氧化,与氧化还原反应有关,B不符合;干冰易升华,升华过程中吸收大量的热,因此可以做制冷剂,与氧化还原反应没有关系,C符合;镁粉用于炼铁脱硫,过程中镁被氧化,与氧化还原反应有关,D不符合;答案选C。

高考化学铁及其化合物(大题培优易错难题)含详细答案一、高中化学铁及其化合物练习题(含详细答案解析)1.某兴趣活动小组利用物质间的互变,设计成一个平面魔方,如下图所示:已知①A、B、C、D、G含有同种元素。
②纯A(单质)B溶液D固体G溶液颜色银白色黄色红棕色浅绿色③E是通常情况下密度最小的气体;B与硝酸银溶液反应生成不溶于稀硝酸的白色沉淀,也能将一种氧化物氧化为F,F是含有三种元素的化合物,与A反应生成E、G。
依据以上信息填空:(1)写出D的化学式:___________________________________________。
(2)G生成C的过程中所出现的现象为_________________________。
(3)写出反应A→B的化学方程式:_________________________________。
(4)B→F的离子方程式为________;G与次氯酸反应的离子方程式为________________________________。
【答案】Fe2O3先产生白色沉淀,迅速变为灰绿色,最后变为红褐色 2Fe+3Cl22FeCl3 2Fe3++SO2+2H2O=2Fe2++SO42-+4H+ H++2Fe2++HClO=2Fe3++Cl-+H2O【解析】【分析】结合框图,D固体呈红棕色,则其为Fe2O3;A、B、C、D、G含有同种元素,B与硝酸银溶液反应生成不溶于稀硝酸的白色沉淀,则B为FeCl3,G中含有Fe2+,A为Fe。
由“B与硝酸银溶液反应生成不溶于稀硝酸的白色沉淀,也能将一种氧化物氧化为F,F是含有三种元素的化合物,与A反应生成E、G”,则F为H2SO4,G为FeSO4;E是通常情况下密度最小的气体,则E为H2。
由B→C→D的转化可推知,C为Fe(OH)3。
【详解】(1)由以上分析可知,D为氧化铁,其化学式:Fe2O3。
答案为:Fe2O3;(2)FeSO4生成Fe(OH)3,可先加碱、后氧化,所出现的现象为先产生白色沉淀,迅速变为灰绿色,最后变为红褐色。

高考化学知识点复习《铁及其化合物》真题练习含答案一、单选题1.(2023年7月黑龙江省普通高中学业水平合格性考试)长江以南的低山丘陵区普遍存在着红色土壤,有人说主要因其含铁质(三价铁)相对较多。
某研究小组设计简单实验验证该说法是否正确,应选择的试剂是 A .KClB .KNO 3C .K 2SO 4D .KSCN 【答案】D【解析】验证土壤中是否含有Fe 3+,可以使用KSCN 溶液检验,向蒸馏水中加入少量的土壤后搅拌,土壤中的离子可以进入到蒸馏水中,过滤后得到澄清溶液,向溶液中滴加KSCN 溶液,若溶液变成红色,则说明土壤中含有Fe 3+,故答案选D 。
2.(2023年黑龙江省春季普通高中学业合格考试)向盛有()43Fe SO 溶液的试管中,滴入几滴KSCN 溶液,溶液呈A .无色B .红色C .白色D .蓝色 【答案】B【解析】向盛有()43Fe SO 溶液的试管中,滴入几滴KSCN 溶液,溶液中的反应为:3+-3Fe 3SCN Fe(SCN)+=,生成血红色溶液。
答案选B 。
3.(2023年1月辽宁省普通高中学业水平合格性考试)下列关于铁及其化合物的叙述错误的是 A .铁具有导电、导热、延展性B .氧化铁常用作涂料、油漆的红色颜料C .用铜粉除去2FeCl 溶液中含有的少量3FeCl 杂质D .实验室制备氢氧化亚铁的关键是防止氧气的干扰【答案】C【解析】A .铁是一种金属单质,具有导电、导热、延展性,A 正确;B . 氧化铁是红棕色粉末,常用作涂料、油漆的红色颜料,B 正确;C .氯化铁溶液和铜反应得到氯化亚铁和氯化铜,用铜粉除去2FeCl 溶液中含有的少量3FeCl 杂质时会引入新杂质氯化铜,C 不正确;D .氢氧化亚铁具有还原性,易发生:22234Fe(OH)+O +2H O=4Fe(OH) ,实验室制备氢氧化亚铁的关键是防止氧气的干扰,D 正确;答案选C 。
4.(2023年1月辽宁省普通高中学业水平合格性考试)下列可用于检验3Fe +的试剂是A .稀盐酸B .KCl 溶液C .4CuSO 溶液D .KSCN 溶液 【答案】D【解析】铁离子与稀盐酸、KCl 溶液和4CuSO 溶液均不反应,铁离子能发生特征反应:3-3Fe 3SCN Fe(SCN)++,所得溶液呈血红色,故可以用KSCN 溶液检验3Fe +,故选D 。

专题7:铁及其化合物一、单选题(共10题;共20分)1.下列有关铁及其化合物的说法中正确的是()A. 赤铁矿的主要成分是Fe3O4B. 铁与水蒸气在高温下的反应产物为Fe2O3和H2C. 除去FeCl2溶液中的FeCl3杂质可以向溶液中加入铁粉,然后过滤D. Fe3+与KSCN溶液产生红色沉淀2.下列说法错误的是()A. 钠在空气燃烧时先熔化,再燃烧,最后所得的产物是Na2O2B. 铝因在空气中形成了一薄层致密的氧化膜,保护内层金属,故铝不需特殊保护C. 铁因在潮湿的空气中形成的氧化物薄膜疏松,不能保护内层金属D. SiO2是酸性氧化物,不与任何酸发生反应3.下列变化不能通过一步反应直接完成的是()A. Fe→Fe3+B. Fe→Fe3O4C. Al(OH)3→Al2O3D. Al→Al(OH)34.一定条件下A、B、C的如图所示的转化关系,且△H=△H1+△H2.则A、C可能是()①Fe、FeCl3②C、CO2③AlCl3、NaAlO2④NaOH、NaHCO3⑤S、SO3⑥Na2CO3、CO2.A. ②③④⑥B. ②③④⑤⑥C. ①②③④⑥D. ①②③④⑤⑥5.一定条件下,下列各组物质能一步实现如图所示转化关系的是()A. AB. BC. CD. D6.常温下,将一定量的铁粉加入到50 mL10mol/L硝酸(①)中,待其充分反应后,收集到的气体换算成标准状况下的体积为4.2L(②),所得溶液能够使淀粉碘化钾溶液变蓝(③),该溶液也能使酸性高锰酸钾褪色(④)。
下列说法正确的是()A. ①中数据表明,硝酸是浓硝酸,因此Fe已经钝化B. ②中数据表明,生成的气体中只有NO2C. ③中现象表明,硝酸一定有剩余D. ④中现象表明,溶液中一定含有Fe2+7.FeCl3、CuCl2的混合溶液中加入铁粉,充分反应后仍有固体存在,则下列判断正确的是()A. 溶液中一定含Cu2+B. 溶液中不一定含Fe2+C. 剩余固体一定含Cu和FeD. 加入KSCN溶液一定不变红色8.铜片和铁片(均少部分被氧化)一起放入足量的盐酸中充分反应。

高考化学提高题专题复习铁及其化合物练习题附详细答案一、高中化学铁及其化合物练习题(含详细答案解析)1.在一定条件下,A、B、C、D、E物质相互转化关系如图所示(反应条件和部分产物略),其中A、B、C为单质。
(1)若A为金属,B、C常温下均为气体,D为黑色晶体,E为一种生活中必不可少的物质,则这五种物质的化学式为:A为__,B为__,C为__,D为__,E为__。
(2)A和E在一定条件下反应生成D的化学方程式为__。
【答案】Fe O2 H2 Fe3O4 H2O 3Fe+4H2O(g)Fe3O4+4H2【解析】【分析】A、B、C为单质,若A为金属,B、C常温下均为气体,D为黑色晶体,Fe和H2O反应生成黑色的Fe3O4,Fe和O2反应生成黑色的Fe3O4,氢气和氧气反应生成H2O,符合转化关系,则A是Fe、B是O2、C是H2、E是H2O、D是Fe3O4,据此分析解答。
【详解】A、B、C为单质,若A为金属,B、C常温下均为气体,D为黑色晶体,Fe和H2O反应生成黑色的Fe3O4,Fe和O2反应生成黑色的Fe3O4,氢气和氧气反应生成H2O,符合转化关系,则A是Fe、B是O2、C是H2、E是H2O、D是Fe3O4;(1)通过以上分析知,这五种物质的化学式为:A为Fe,B为O2,C为H2,D为Fe3O4,E为H2O;(2)在高温条件下,Fe和水蒸气反应生成四氧化三铁和氢气,所以A和E在一定条件下反应生成D的化学方程式为3Fe+4H2O(g)Fe3O4+4H2。
2.A、B、C、D四种化合物,其中A、C、D焰色反应均为黄色,而B的焰色反应为紫色,A、C和盐酸反应均得到D,将固体C加热可得到A,若在A的溶液中通入一种无色无味气体,又可制得C,若B的溶液滴加到硫酸亚铁溶液会先后出现白色沉淀→灰绿色沉淀→红褐色沉淀E。
试推断:(1)A:__、B:__、C:__、D:__、E:__;(2)固体C加热得到A的化学反应方程式__;(3)得到红褐色沉淀E的化学反应方程式__。
铁及其化合物一、选择题(本题包括10小题,每小题5分,共50分)1.下列反应,其产物的颜色按红色、红褐色、淡黄色、蓝色顺序排列的是( )①金属钠在纯氧中燃烧②FeSO4溶液中滴入NaOH溶液,并在空气中放置一段时间③FeCl3溶液中滴入KSCN溶液④无水硫酸铜放入医用酒精中A.②③①④B.③②①④C.③①②④D.①②③④2.已知下述三个实验中均有化学反应发生。
下列判断正确的是( )A.实验①中铁钉只做还原剂B.实验②中Fe2+既显氧化性又显还原性C.实验③中发生的是置换反应D.上述实验证明氧化性:Fe3+>Fe2+>Cu2+3.在含有FeCl3和BaCl2的酸性溶液中,通入足量的SO2后有白色沉淀生成,过滤后,向溶液中滴加KSCN溶液,无明显现象,下列叙述不.正确的是( )A.白色沉淀是BaSO4和BaSO3B.溶液的酸性增强C.白色沉淀是BaSO4D.FeCl3全部被还原为FeCl24.某溶液中有Fe3+、Mg2+、Fe2+和Al3+四种阳离子,若向其中加入过量的氢氧化钠溶液,搅拌后,再加入过量的盐酸,溶液中大量减少的阳离子是( )A.Fe3+B.Mg2+C.Fe2+D.Al3+5.下列离子方程式书写正确的是( )A.FeO固体放入稀硝酸溶液中:FeO+2H+===Fe2++H2OB.过量的铁粉与稀硝酸溶液反应:Fe+4H++NO-3===Fe3++NO↑+2H2OC.向氢氧化亚铁中加入足量的稀硝酸:Fe(OH)2+2H+===Fe2++2H2OD.向Fe(OH)3中加入氢碘酸:2Fe(OH)3+6H++2I-===2Fe2++I2+6H2O6.某学生设计了如图所示的方法,鉴定盐A的组成成分。
由此分析,下列结论中正确的是( )A.A中一定有Fe3+B.C中一定有Fe3+C.B为AgI沉淀D.A一定为FeBr2溶液7.高铁酸钠(Na2FeO4)是一种新型、高效、多功能的水处理剂。
湿法制备的主要反应方程式为2Fe(OH)3+3ClO-+4OH-===2FeO2-4+3Cl-+5H2O。
干法制备的主要反应方程式为2FeSO4+4Na2O2===2Na2FeO4+2Na2SO4。
下列有关说法不.正确的是( )A.高铁酸钠中铁显+3价B.湿法中氢氧化铁被氧化C.干法中每生成1 mol Na2FeO4转移4 mol电子D.Na2FeO4处理水的能力优于次氯酸的能力8.在含有FeBr2和FeI2的混合溶液中,通入一定量的Cl2,再滴加KSCN溶液后,溶液变为红色,则溶液中一定不存在的离子是( )A.Cl-B.Fe2+C.I-D.Br-9.将a g铁和氧化铁的混合物加入足量的盐酸中充分反应后,固体无剩余,测得参加反应的HCl为0.08 mol,放出标准状况下的气体0.224 L。
则下列判断中正确的是( ) A.原混合物中n(Fe)∶n(Fe2O3)=2∶1B.向溶液中滴入KSCN溶液,显血红色C.无法计算原混合物的质量D.此时溶液中Fe2+和Fe3+的物质的量之比为3∶110.某反应混合物中有下列物质:N2O、FeSO4、Fe(NO3)3、HNO3、Fe2(SO4)3和H2O,下列叙述错误的是( )A.HNO3与FeSO4的计量数之比为5∶4B.FeSO4是还原剂,HNO3是氧化剂C.每生成1 mol Fe(NO3)3转移电子为1 molD.Fe(NO3)3、Fe2(SO4)3是氧化产物二、非选择题(本题包括4小题,共50分)11.(12分)下图表示某种盐的制备步骤:已知:水合盐B含有45.3%的水;无水盐C焙烧分解,放出两种无色刺激性气体E和F,并生成红棕色固体D。
请写出物质的化学式或名称:A________,B________,C________,D________,E________,F________。
12.(12分)粉末状试样A是由等物质的量的MgO和Fe2O3组成的混合物。
进行如下实验:①取适量A进行铝热反应,产物中有单质B生成;②另取20 g A全部溶于0.15 L 6.0 mol·L-1盐酸中,得溶液C;③将①中得到的单质B和溶液C反应,放出1.12 L(标准状况)气体,同时生成溶液D,还残留有固体物质B;④用KSCN溶液检验时,溶液D不变色。
请填空:(1)产物中的单质B是________。
(2)②中所发生的各反应的化学方程式是:________________________________________________________________________,________________________________________________________________________。
(3)③中所发生的各反应的离子方程式是:________________________________________________________________________,________________________________________________________________________。
(4)若溶液D的体积仍视为0.15 L,则该溶液中c(Mg2+)为________,c(Fe2+)为________。
13.(12分)某厂的酸性工业废水中含有一定量的Fe3+、Cu2+、Au3+等。
有人设计了如图所示的工艺流程,利用常用的酸、碱和工业生产中的废铁屑从废水中回收金,并生成一定量的铁红和氧化铜。
请回答下列问题:(1)图中标号处需加入的相应物质:①_________、②_________、③_________、④_________、⑤_________。
(2)写出①处发生反应的所有离子方程式:________________________________________________________________________;________________________________________________________________________;________________________________________________________________________;________________________________________________________________________。
写出③处发生反应的化学方程式:______________________________________________________________________________________________________________。
(3)铁红的化学式为________。
14.(14分)Fe2+、SO2-3和I-都具有还原性。
为了比较其还原性强弱,进行以下探究并回答:(1)已知:①还原性:SO2-3>Fe2+;②FeSO3难溶于水。
(2)在(1)的基础上,完成下列假设。
假设1,还原性:I->SO2-3>Fe2+;假设2,还原性:SO2-3>I->Fe2+;假设3,还原性:___________________________________________________。
(3)实验探究:现对假设2进行探究,完成实验步骤以及预期的现象和结论。
限选以下试剂:0.1 mol·L-1Na2SO3溶液、0.1 mol·L-1KI溶液、 0.1 mol·L-1FeCl2溶液、10% KSCN溶液、新制饱和氯水、淀粉溶液、稀HNO3溶液、1 mol·L-1HCl溶液、1 mol·L -1 BaCl2溶液。
铁及其化合物参考答案 1 2 3 4 5 6 7 8 9 10 BAACDBACAC11.解析:根据最终得到的固体D 为红棕色固体,且水合盐B ――→300℃氮气保护无水盐C 可推知A 为变价金属铁,依次推出无水盐C 为FeSO 4,水合盐B 为FeSO 4·7H 2O 。
盐C 灼烧的反应式为:2FeSO 4=====高温 Fe 2O 3+SO 2↑+SO 3↑答案:Fe FeSO 4·7H 2O FeSO 4 Fe 2O 3 SO 2(或SO 3) SO 3(或SO 2)12.解析:根据题意,各步发生的化学反应如下: ①Fe 2O 3+2Al=====高温2Fe +Al 2O 3MgO 与Al 不发生铝热反应,故单质B 为Fe ; ②MgO +2HCl===MgCl 2+H 2O , Fe 2O 3+6HCl===2FeCl 3+3H 2O ; ③Fe +2FeCl 3===3FeCl 2, Fe +2HCl===FeCl 2+H 2↑;④说明:Fe 3+无剩余,溶液D 为MgCl 2、FeCl 2的混合液。
设20 g A 中MgO 和Fe 2O 3的物质的量均为x ,则有40 g ·mol -1x +160 g ·mol -1x =20 g , 解得x =0.1 mol ,则溶液D 中c (Mg 2+)=0.1 mol 0.15 L =0.67 mol ·L -1,据Cl -守恒得溶液D 中Fe 2+的浓度为:c (Fe 2+)= 6.0 mol ·L -1×0.15 L -0.1 mol ×2×120.15 L=2.3 mol ·L -1。
答案:(1)Fe(2)Fe 2O 3+6HCl===2FeCl 3+3H 2O MgO +2HCl===MgCl 2+H 2O(3)Fe +2H +===Fe 2++H 2↑ Fe +2Fe 3+===3Fe 2+(4)0.67 mol ·L -12.3 mol ·L -113.解析:从题中给出的信息可知,首先分离出来的应是铁元素,所加最佳试剂应是废铁屑,E 溶液含Fe 2+,铁红的成分为Fe 2O 3,可联想到反应2Fe(OH)3=====△Fe 2O 3+3H 2O ,试剂⑤应为可溶性碱(NaOH 溶液或氨水),当加入过量铁粉后,所得A 应为Fe 、Cu 、Au 的混合物,此时只需加入稀硫酸(试剂②)后过滤可得Cu 、Au 的混合物B ,再向混合物B 中加入稀硝酸(试剂③)可使Cu 、Au 分离,向反应得到的C[Cu(NO 3)2]溶液中加NaOH 溶液(试剂④)得到D[Cu(OH)2]后,再加热得到CuO 。
答案:(1)①废铁屑 ②稀硫酸 ③稀硝酸 ④氢氧化钠 ⑤氢氧化钠(其他合理答案均可)(2)Fe +2H +===Fe2++H 2↑ 2Fe3++Fe===3Fe2+Cu2++Fe===Cu +Fe2+2Au3++3Fe===2Au +3Fe 2+ 3Cu +8HNO 3(稀)===3Cu(NO 3)2+2NO ↑+4H 2O(3)Fe 2O 314.解析:(3)步骤1、2是比较SO 2-3、I -还原性大小。