肾功能不全抗生素选择完整版本
- 格式:ppt
- 大小:1.54 MB
- 文档页数:35


肾功能不全时,哪些抗菌药要调整剂量?4张表格帮你轻松搞定4张表格告诉你!我们知道,肾脏在药物代谢、排泄方面起着不可或缺的作用,但随着病程的变化,药物的给药次数增加、用药剂量加大、用药时间过长等会加重肾脏的负担,产生“肾毒性”。
对于老人和肾功能不全患者,用药更应谨慎。
但肾功能不全时就不能使用抗生素了吗?或者该怎么使用抗生素较为合理?通过4个案例和4张表格,我们来总结常用抗菌药(青霉素类、头孢菌素类、大环内酯类、喹诺酮类抗菌药)的剂量调整。
青霉素类抗菌药怎么调?案例1:患者,男,86岁,身高168cm、体重62.8kg,血肌酐155μmol/L↑(正常值59-104μmo l/L,不同检测方法参考范围略有出入)。
临床医师给予替卡西林克拉维酸钾3.2g,静脉滴注,每8h给药一次。
这个用药剂量是否合理?需要调整吗?▎用药分析首先我们根据案例中的信息,按照血肌酐计算公式进行计算:肌酐清除率=[(140-年龄)×体重(kg)]/[0.818×血肌酐(umol/L)] 可以和小编简单计算一下,肌酐清除率约为26.7ml/min。
要知道当患者的肌酐清除率为10-30ml/min时,应该减少替卡西林克拉维酸钾的剂量。
因此,将替卡西林克拉维酸钾的剂量可调整为1.6g ,给药间隔时间不变。
若患者的肌酐清除率为>30ml/min时,可以考虑上面案例中提到的剂量。
▎给药建议对于肾功能不全的患者,给予青霉素类抗菌药应该注意调整剂量:对轻中度肾功能不全患者,无需调整剂量;对重度肾功能不全的患者,应该调整药物剂量或者延长用药时间间隔。
这些需要调整剂量的药物详见表1。
(点击查看大图)头孢菌素类抗菌药怎么调?案例2:患者,女,85岁,身高156cm,体重56kg,血肌酐236μmol/L↑(正常值45-84μmol/L,不同检测方法参考范围略有出入)。
临床医师给予头孢哌酮-舒巴坦(1.0g:0.5g)3.0g,静脉滴注,每12h给药一次。



肝功能减退时抗菌药物的应用分为以下几种情况:1)药物主要经肝脏清除:包括大环内酯类药物(不包括红霉素酯化物)、林可霉素、克林霉素、麦迪霉素、罗红霉素及阿奇霉素等药,主要经胆汁排泄,在胆汁中浓度较高、相当量药物可能在肝脏内代谢灭活,少量随尿排出。
肝功能减退时,药物排泄较慢,但无明显肝毒性发生,因此可谨慎应用,按原治疗量或减量。
克林霉素与林可霉素在肝内代谢,随胆汁及粪便排出,肝功能减退时其清除半衰期明显延长,血药浓度升高,可引起血清转氨酶升高,但转氨酶的升高和高胆红素血症可能由药物干扰比色测定所致,并非肝毒性反应,故应慎用,并需减量给药。
2)主要经肝或相当量经肝清除的抗生素:包括氯霉素、氨苄西林酯化物、红霉素酯化物、利福平、异烟肼、两性霉素B、四环素类、磺胺药及酮康唑、咪康唑等,肝功能减退时药物清除及代谢减少,可导致毒性反应发生,应避免使用。
3)药物经肝、肾两途径清除:肝功能减退时血药浓度略升高,如同时有肾功能损害时,则血药浓度升高尤为明显。
严重肝病时应减量应用,属此类的有青霉素族中的美洛西林、哌拉西林、头孢哌酮、头孢曲松、头孢噻肟、头孢噻吩等。
此外头孢哌酮、头孢曲松、头孢孟多在肝病时易引起凝血功能障碍,主要抑制维生素K合成,从而使凝血因子合成不足及血小板减少,应予注意。
4)药物主要经肾排泄:肝功能减退时不需要调整剂量,包括青霉素、头孢唑林、头孢他啶、亚胺培南等药物,氨曲南、磷霉素、万古霉素、多粘菌素及喹诺酮类药物(不包括培氟沙星),肝功能减退时,选用这类药物最安全。
对氨基糖甙类药物,尽管主要经肾脏排泄,但肝病患者肾毒性发生率明显增高,因此肝功能减退患者应注意慎用。
肝功能减退者细菌感染,一般根据感染部位及病原菌类型,选用适宜抗菌药物,避免应用肝毒性药物,除败血症外,一般不采用两种抗菌药物联合应用。
其疗程根据临床情况而定,症状好转后,仍应延长疗程,以免感染复发,一般极重感染的有效抗菌素疗程应不短于3周。

慢性肾功能不全患者抗菌药物的合理应用大理市第一人民医院临床药学室:杨伟君时间:2019.12.26一、慢性肾功能不全慢性肾功能不全是指各种原发病或继发性慢性肾脏疾病导致进行性肾功能损害所出现的一系列症状和(或)代谢紊乱的临床综合征。
(一) 慢性肾功能不全对抗菌药物 PK/ PD 的影响表现为药物或其代谢产物经肾脏排泄减少,半衰期延长,导致血药浓度升高。
肾功能不全时药物由肾小管重吸收速率及吸收程度均降低,因水肿、血浆白蛋白降低使药物与蛋白的结合量减少,药物游离部分增多,影响血药浓度。
(二)、优化给药方案的推荐意见1.慢性肾功能不全时抗菌药物选择原则:肾功能不全时,需根据以下因素调整抗菌药物的剂量:(1)肾功能减退程度;(2)抗菌药物对肾毒性的大小;(3)药物的体内过程,即PK特点;(4)抗菌药物经血液透析或腹膜透析后可清除的程度。
主要经肾脏排泄的药物,其半衰期可因肾功能减退而延长,因此,半衰期可作为调整用药的重要依据。
但同一药物在不同患者的血半衰期差异较大,如有条件应进行血药浓度监测,进行个体化给药。
2、慢性肾功能不全时抗菌药物剂量调整原则 :(1)正常应用或剂量略减:包括主要经肝胆系统代谢或排泄的抗菌药物,如大环内酯类、青霉素类和头孢菌素类的部分品种(氨苄西林和头孢哌酮)、多数抗真菌药物、抗分枝杆菌的多数品种及利奈唑胺等。
(2)可选用,但剂量需适当减少:主要经肾脏排泄,药物本身并无肾毒性或仅有轻度肾毒性的抗菌药物,需按照肾功能减退程度调整给药方案,包括青霉素类、头孢菌素、碳青霉烯类的多数品种、左氧氟沙星及磺胺甲噁唑等。
(3) 应避免应用,确有指征使用时,需在监测治疗药物浓度的情况下减量应用:药物本身或其代谢产物主要经肾脏排出,且有较大毒性,包括氨基糖甙类、多黏菌素类及糖肽类等。
(4)不宜应用:包括四环素类(多西环素除外)、呋喃类及萘啶酸等,四环素可加重氮质血症,如有指征应用时需慎重考虑,并肾功能损害程度减量应用;呋喃妥因、萘啶酸:可在体内明显积集,产生神经系统毒性。

肾功能不全患者抗生素用量
万古霉素肌酐清除率
常规用量>80ml/min
每1~3日1000mg 50~80
每3~7日1000mg 10~50
每7~14日1000mg <10
美罗培南
每12小时1g 26~50
每12小时0.5g 10~25
每24小时0.5g <10
泰能
常规用量>70ml/min
每6~8小时0.5g 30~70 ml/min
每8~12小时0.25~0.5g 20~30 ml/min
每12小时0.25g <20 ml/min
舒巴坦
最大量每12小时1g 15~30 ml/min
每12小时0.5g <15 ml/min
氟康唑
常规剂量每24小时1次>40 ml/min
常规剂量的1/2或每48小时1次21~40 ml/min
常规剂量的1/3或72小时1次10~20 ml/min
头孢他啶
每12小时1g 31~50 ml/min
每24小时1g 16~30 ml/min
每24小时0.5g 6~15 ml/min
每48小时0.5g <6 ml/min
每12小时0.2g >30 ml/min
每18~24小时0.2g 5~29 ml/min
左氧氟沙星
重症细菌感染、慢支、社区获得性肺炎:
首剂500mg,每24小时250mg维持20~49 ml/min 首剂500mg,每48小时250mg维持10~19 ml/min 院内获得性肺炎:
首剂750mg,每48小时750mg维持20~49 ml/min 首剂750mg,每48小时500mg维持10~19 ml/min 莫西沙星不用调整剂量。

肝肾功能不全患者抗菌药物的应用考试
肝肾功能不全患者抗菌药物的应用考试,需要掌握以下几个方面:
抗菌药物分类:了解各类抗菌药物的性质、特点、适应症和不良反应,如青霉素类、头孢菌素类、大环内酯类、氟喹诺酮类、磺胺类等。
肝肾功能不全患者抗菌药物的应用原则:肝肾功能不全患者应避免使用对肝肾功能有损害的抗菌药物,尽量选择对肝肾功能影响较小的药物。
同时,根据患者的肝肾功能情况,调整药物剂量和给药间隔。
各类抗菌药物在肝肾功能不全患者中的应用:了解各类抗菌药物在肝肾功能不全患者中的使用方法和注意事项,如青霉素类和头孢菌素类在肝功能减退患者中可正常使用,但需注意剂量调整;氟喹诺酮类药物在肾功能减退患者中需减量使用;磺胺类药物在肾功能减退患者中需避免使用等。
肝肾功能不全患者抗菌药物的剂量调整:根据患者的肝肾功能情况,调整抗菌药物的剂量和给药间隔,避免药物蓄积和毒性反应。
肝肾功能不全患者抗菌药物的监测:在治疗过程中,需密切监测患者的肝肾功能,及时发现并处理药物不良反应。
总之,肝肾功能不全患者抗菌药物的应用考试需要掌握抗菌药物的分类、应用原则、各类抗菌药物在肝肾功能不全患者中的应用、剂量调整和监测等方面的知识。
在实际临床工作中,应根据患者的具体病情,综合考虑各方面因素,合理选用抗菌药物。

临床特殊情况下抗菌药物应用的注意事项1、肾功能不全患者应用抗菌药物注意(1)选择药物和设计给药方案时,必须考虑:药物的肾毒性、患者肾功能损害程度及对药物动力学的影响.如正在进行血液或腹膜透析治疗时,应估测对药物清除率的膨响。
(2)根据肾功能不全程度应调整药物给药剂量及给药时间.2、肝功能不全应用抗菌药物注意:在选用抗菌药物时应考虑药物对肝脏毒性反应及肝功能减退对药代动力学的膨响,避免使用肝毒性明显的药物.3、新生儿患者应用抗菌药物注意:一般应选用青毒素类、头胞菌素类等β-内酰胺类抗生素。
避免使用或慎用氯卷素、横胺药等抗菌药物,避免应用氨基糖昔类、万古霉素、去甲万古霉素等,确有应用指征时,必须进行血药浓度监测,个体化给药,不能迸行血药浓度监测者,不可选用上述药物.禁止使用四环素类、喳诺酮类药物.新生儿不宜肌肉注射.4、小儿患者抗菌药物应用注意:避免应用氨基糖昔类药物,确有应用指征时,必须进行血药浓度监测,个体化给药.8岁以下儿童不用四环素类药物,18岁以下未成年人避免使用瞳诺酮类药物.5、妊娠妇女应用抗箧药物注意:必须考虑药物对胎儿的影响及妊娠期妇女药代动力学的改变,避免不必要的用药。
在必须用药时,应选择风险效果之比最小的药物,并告知患者药物对继续妊娠可能引起的风险。
6、哺乳妇女应用抗菌药物注意:必须使用抗菌药物时,应尽可能选择在乳汁中浓度低、安全性高的药物,如青霉素类、头抱菌素类.并按药代动力学原理调整给药与哺学时间,如哺乳结束后立即用药,或在婴J由长睡眠前用药,使婴儿从乳汁中摄取的药物降至最低.7、老年患者应用抗图药物注意:老年人因组织器官生理功能减退,药代动力学过程有明显变化,特别是由于肾功能减退而致药物血浓度增加,不良反应也增加,应尽量使用不良反应小的药物,并依据肾功能调整剂量和用药方案,以达到安全、有效的目的。

肾功能不全时,4类抗菌药物如何调整?一文掌握!许多抗菌药物在人体内主要经肾脏排出,由于某些抗菌药物具有肾毒性,因此肾功能不全患者用药与肾功能正常者相比,需兼顾保证疗效和防止副作用两个方面。
在治疗感染导致的肾盂肾炎时,应用抗菌药更需要慎重。
那么临床上肾功能不全患者到底该如何使用抗生素呢?我们一起来复习一下吧!对于肾功能不全患者选用抗菌药物的原则是什么?抗菌药物的选择原则1.尽量避免使用肾毒性抗菌药物,确有应用指征时,严密监测肾功能情况。
2.根据感染的严重程度、病原菌种类及药敏试验结果等选用无肾毒性或肾毒性较低的抗菌药物。
3.根据肾功能轻、中、重度损害,每日剂量分别减为原正常剂量的1/3-1/2,1/2-1/5和1/5-1/10。
4.使用主要经肾排泄的药物,必须根据患者肾功能减退程度及抗菌药物在人体内清除途径,调整给药剂量及方法[1]。
如何选用抗菌药物?肾毒性抗菌药物,确有应用指征时,须调整给药方案。
根据感染的严重程度,病原菌种类及药敏试验结果等,选用肾毒性低的抗菌药物;根据患者肾功能减退程度,及抗菌药物在人体内代谢途径调整给药剂量及强度。
1青霉素类抗菌药物绝大部分青霉素类抗菌药物主要以原型和(或)代谢物形式经肾脏排泄,仅少量经胆汁排泄。
其中,肝功能正常者应用哌拉西林后,约10%~20%经胆汁排泄,而氯唑西林和苯唑西林约有10%经胆汁排泄,以上药物的胆汁排泄量均高于其他青霉素类抗菌药物。
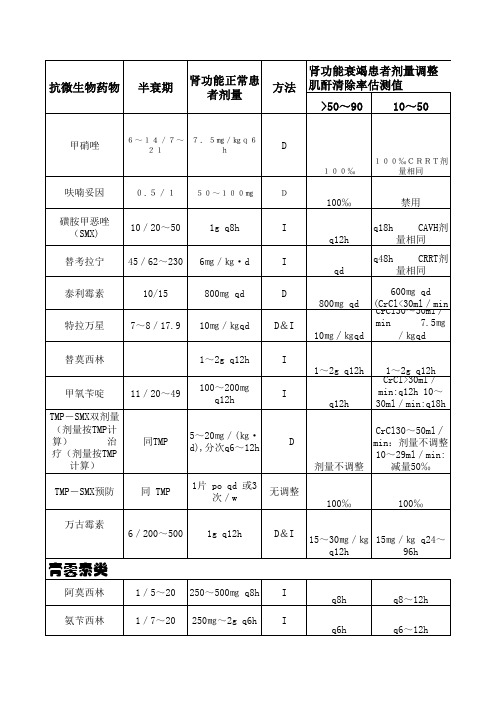
总之,绝大部分青霉素类抗菌药物应用于轻、中度肾功能不全患者时,无需调整剂量,重度肾功能不全者需减少剂量和(或)延长给药时间间隔,见表1。
表1:青霉素类抗菌药剂量调整分类及具体药品2头孢菌素类抗菌药物绝大部分头孢菌素类抗菌药物主要以原型和(或)代谢物形式经肾脏排泄,少量经胆汁排泄。
其中,头孢哌酮几乎不在体内代谢,主要经胆汁排泄(胆汁中药物回收量≥40%),约25%经尿液排泄,严重肝功能不全或胆道梗阻者,尿液中排泄量可达90%。

肾功能不全患者抗生素使用注意事项一、左氧氟沙星注射液1、如果存在肾功能不全,慎用左氧氟沙星。
2、对于肌酐清除率大于等于50ml/min患者没有必要进行剂量调整.3、肾功能正常:250mg或500毫克缓慢静滴,时间大于60分钟,24小时一次。
或750mg缓慢静滴,时间大于90分钟,24小时一次。
4、肌酐清除率20~40ml/min:每48小时750mg或首剂500mg,此后每24小时250mg。
或者250mg每24小时一次缓慢静滴.5、肌酐清除率10~19ml/min:第一次给予750mg,此后每48小时500mg;或第一次给予500mg,此后每48小时250mg;或每48小时给予250mg.6、血液透析或腹膜透析患者:第一次给予750mg,此后每48小时500mg;或第一次给予500mg,此后每48小时250mg.7、分子量:415。
85 蛋白结合率24%~38% 87%由肾脏排出。
8、血液透析和腹膜透析均不能有效清除体内的左氧氟沙星,故透析后不用补充。
二、注射用阿奇霉素1、分子量:1465。
59 蛋白结合率为7%~15%。
2、肾功能不全者慎用。
3、主要经过胆汁排泄。
三、头孢曲松钠1、分子量661.59 蛋白结合率95%60%经尿排出.2、肾功能不全患者肌酐清除率大于5ml/min,每日剂量应少于2g。
3、血液透析对本品清除率不高,透析后不需要补充剂量.四、头孢西丁1、分子量449.43蛋白结合率80.7% 85%经肾排泄。
2、肌酐清除率50-30ml/min:1~2g,8-12小时一次。
肌酐清除率29-30ml/min:1—2g,12—24小时一次。
肌酐清除率9—5ml/min:0.5—1g12-24小时一次。
肌酐清除率小于5ml/min:0.5-1.0g24—48小时一次五、头孢哌酮舒巴坦1、头孢哌酮约25%经过肾脏排泄。
舒巴坦84%经肾脏排泄2、肌酐清除率15—30ml/min时:舒巴坦每日最高2g,分12小时一次。


一.肾功能不全患者抗生素使用抗菌药物导致肾损害的类型及机制药物导致的肾损害大多损害肾小管和肾间质。
抗菌素导致肾损害的主要机制包括两个方面,一是抗菌素的直接毒性,二是药物诱发的免疫损伤。
此外,抗菌素和肾脏的关系还表现在,肾功能下降后,某些抗菌素通过肾脏的排泄障碍而在体内蓄积,引发其他问题。
1. 氨基糖苷类常用的有阿米卡星、妥布霉素、庆大霉素、奈替米星、西索米星及链霉素等,可导致急性肾小管坏死。
2. 多肽类包括多粘菌素B,多粘菌素E,万古霉素,去甲万古霉素等。
多粘菌素B和多粘菌素E主要从肾脏排泄,在肾功能下降时,两药的消除半衰期明显延长。
全身给药剂量过大或时间过长可出现肾脏毒性,尤其是原已有肾脏疾患则更易产生。
主要表现蛋白尿、管型尿、血尿及尿素氮上升,及时停药一般可恢复。
万古霉素80%-90%以原形从肾脏排泄。
清除半衰期成人为5-11小时,当肾功能衰竭时,半衰期将延至7天以上,故肾功能衰竭患者用药需增大间隔时间,并进行血药浓度监测。
3. β-内酰胺类青霉素类:包括青霉素G,双氯青霉素,阿莫西林,哌拉西林,阿洛西林、美洛西林等。
青霉素在体内存留的时间短,通过肾脏后随尿液排泄出去,一般不会在身体蓄积而产生直接肾毒性。
青霉素类导致的肾损伤类似于过敏反应,绝大部分患者发生在用药后2~3周,也可在1~2 月不等,容易误诊。
头孢菌素类:第一代头孢菌素类(头孢噻吩,头孢氨苄,头孢唑林,头孢拉定等)肾毒性最大,其中头孢拉定因为经常引起血尿而被国家药品不良反应监测中心通报多次。
第二代(头孢他啶除外)及以上头孢菌素肾毒性明显减少。
4. 磺胺类磺胺类药物的乙酰化代谢产物容易在肾小管形成结晶而堵塞肾小管,导致肾小管坏死。
多发生在血容量不足、原有肾脏病变、药物过量或特定的尿pH值情况下。
5.喹诺酮类左氧氟沙星主要是以原形经肾脏排出,可在肾小管产生结晶,尤其在碱性尿中更易发生,肾功能不全患者慎用或减量使用。
二.肾功能不全患者抗生素使用尽量避免使用经肝或有相当量药物经肝清除,肝功能减退时清除减少,有毒性反应发生。

抗生素与肝肾功能不全肝肾功能不全患者的抗生素选择与剂量调整抗生素在医学上扮演着重要的角色,可用于治疗感染性疾病,但在肝肾功能不全的患者中,抗生素的选择和剂量调整需谨慎进行。
本文将就此话题进行探讨,以指导临床实践。
一、影响抗生素处理的肝肾功能不全肝肾功能不全可能导致药物的代谢和排泄发生异常,从而影响抗生素在体内的药动学。
因此,在确定抗生素的选择和剂量时,必须充分考虑患者的肝肾功能状态。
肝功能不全会导致药物的代谢能力下降,进而延长抗生素的半衰期,增加患者暴露在药物的时间上。
而肾功能不全则会影响药物的排泄,导致药物的蓄积。
二、抗生素的选择与剂量调整2.1 抗生素的选择- 肝肾功能不全患者的抗生素选择首先要遵循病原学指导原则。
即明确病原体后,根据病原体的药物敏感性测定选择敏感的抗生素进行治疗。
- 同时,应尽可能选择具有较低肝肾毒性的抗生素。
例如,万古霉素和四环素类抗生素对肝肾的损伤较小,可优先考虑使用。
2.2 抗生素的剂量调整- 对于肝功能不全患者,需要降低需要通过肝脏代谢的抗生素的剂量。
一般来说,肝功能受损的患者,抗生素的剂量要进行相应减少。
可以根据患者的肝功能状态,调整剂量,并密切监测药物血药浓度。
- 对于肾功能不全患者,抗生素的剂量调整常取决于肾小球滤过率(GFR)。
通常,抗生素经肾脏排泄的剂量需要根据GFR的降低程度进行调整。
医生可以根据肾功能不全的严重程度调整剂量,并适时监测药物浓度与疗效。
三、常用抗生素的肝肾功能不全剂量调整策略举例3.1 青霉素类抗生素- 氨苄青霉素:肝肾功能不全剂量需减半。
- 青霉素G:肝肾功能不全需减少剂量和延长给药间隔。
3.2 大环内酯类抗生素- 红霉素:肝功能不全明显时需减少剂量和增加给药间隔。
- 克拉霉素:剂量仅需参考肾功能不全情况进行调整。
3.3 链霉素类抗生素- 阿奇霉素:肾功能不全时剂量需减半。
- 克林霉素:肝肾功能不全时剂量需减半。
以上仅为举例,具体剂量调整应根据患者具体情况而定。

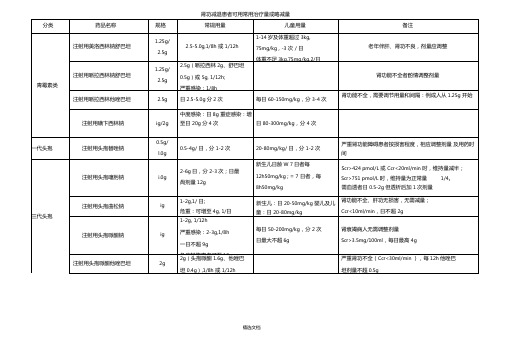
肾功减退患者可用常用治疗量或略减量
可选用,但剂量需减少
注射用美罗培南每8h 一次
肺炎、尿路感染、妇科感染、皮肤软组织感染:0.5g, 院内获得性肺炎、腹膜炎等:
ig,
脑膜炎:2g
碳青霉烯类
注射用亚胺培南西司他丁钠0.5g
日1-2g,分3-4次
中度感染:1g/次,日2次不敏
感病原菌:最多日4g
儿童体重》40kg,按成
人量
体重<40kg,按
15mg/kg,每6h 一
次,总剂量w 2g
单环B- 内酰胺类注射用氨曲南 1.0g
尿路感染:0.5或1g,每8或
12h 一次。
中重度感染:1或2g,每8或
12h 一次。
危及生命或铜绿严重感染:2g, 每6
或8h 一次
Ccr: 26-50ml/min,原剂量,每12h 一次
Ccr: 10-25ml/min , 1/2 原剂量,每12h 一次
Ccr<10ml/min , 1/2 原剂量,每24h 一次
2
体重<70kg , Ccr:6-20,用0.5g,弓I起癫痫可能性增加
Ccr:w 5,除非病人在48h内透析,否则不给于本品
Ccr<10-30ml/(min*1.73m 2)首次1g 或2g,以后减半;
Ccr<10ml/(min*1.73m 2),首次0.5、1或2g维持持量为首次1/4,间隔6、8
或12h;
对严重或危及生命的感染者,每次血透后,在维持量上增加首次
1/8
避免应用,根据血药浓度减量或延长给药间隔。