土壤有机质的测定2.0
- 格式:doc
- 大小:76.00 KB
- 文档页数:7

土壤有机质含量标准,沙质土、黏质土、壤土各有什么特点在土壤学中,一般把耕作层中含有机质20%以上的土壤称为有机质土壤,含有机质在20%以下的土壤称为矿质土壤。
土壤有机质含量指的是单位体积的土壤中含有的各种动植物残体与微生物及其分解合成的有机物质的数量,是衡量土壤肥力的重要指标之一。
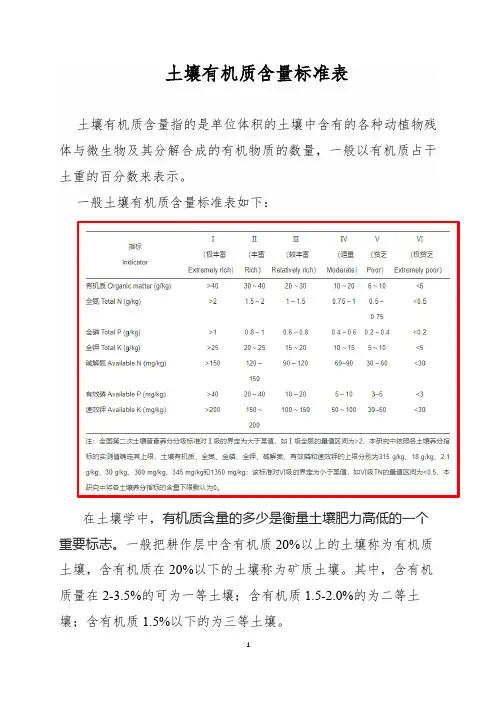
一、土壤有机质含量标准1、土壤有机质含量指的是单位体积的土壤中含有的各种动植物残体与微生物及其分解合成的有机物质的数量,一般以有机质占干土重的百分数来表示,是衡量土壤肥力的重要指标之一。
2、在土壤学中,一般把耕作层中含有机质20%以上的土壤称为有机质土壤,含有机质在20%以下的土壤称为矿质土壤。
其中,含有机质量在2-3.5%的可为一等土壤;含有机质1.5-2.0%的为二等土壤;含有机质1.5%以下的为三等土壤。
3、一般情况下,耕作层土壤有机质含量通常在5%以上;褐土在自然植被下,有机质含量为1-3%,但由于褐土适于耕作,大部分已辟为农地,致使土壤中的有机质含量减少到了1%左右。
4、娄土中的土壤有机质含量一般在1%左右;黄绵土中的土壤有机质含量一般在0.5%左右;黑垆土中的土壤腐殖质含量一般为0.5-1%左右;灰褐土中的表层土壤有机质含量一般在6-13%左右;灰钙土中的土壤有机质含量一般在0.7-1.5%左右。
5、棕钙土中的表层土壤有机质含量一般在0.6-2%左右;栗钙土中的表层土壤有机质含量一般在2-5%左右;风沙土中的土壤有机质含量一般在0.012-0.233%左右;棕钙土中的土壤有机质含量一般在1%左右。
二、沙质土、黏质土、壤土各有什么特点1、沙质土(1)砂粒含量高,颗粒粗,组成的粒间大孔隙数量多,所以土壤通气透水性比较好,不易产生积水。
(2)保水、保肥性能弱(土壤含砂粒较多,粘粒少,颗粒间空隙比较大,导致蓄水力弱;缺乏粘粒和有机质胶体导致保肥能力差),雨后容易造成水肥流失,水分蒸发速率快,失熵多易引起土壤干旱。
(3)土温变幅大,白昼土壤升温快,晚上降温也快;早春土温低,但随气温回升,土温上升也快,对喜温作物花生、棉花、瓜类、块茎、块根作物生长有利,称之为热性土,但晚秋也容易造成霜冻。


实验报告课程名称: 土壤学实验 指导老师: 廖敏 成绩:__________________实验名称: 土壤有机质的测定 同组学生姓名: 张逸涵一、实验目的和要求 二、实验内容和原理三、实验材料与试剂 四、实验器材与仪器五、操作方法和实验步骤 六、实验数据记录和处理七、实验结果与分析 八、讨论、心得一、 实验目的和要求1. 了解土壤有机质测定对于农业生产的意义;2. 掌握土壤有机质含量的测定方法。
二、 实验内容和原理有机质是土壤中重要组成成分,其含量水平是衡量土壤肥力的重要指标之一。
本实验采用外加热法重铬酸钾氧化有机质,利用浓硫酸和重铬酸钾混合,在外加热源下氧化有机质中的碳。
通过滴定消耗的氧化剂的量来计算得出土壤有机质含量,从而分析该土壤肥力水平,并对此提出改良措施。
重铬酸钾外加热法过程的化学反应式:氧化过程:K 2Cr 2O 7+C+H 2SO 4→K 2SO 4+Cr 2(SO 4)3+CO 2+H 2O滴定过程:K 2Cr 2O 7+FeSO 4+H 2SO 4→K 2SO 4+Cr 2(SO 4)3+Fe 2(SO 4)3+H 2O土壤有机碳与有机质换算公式:土壤有机质(g/Kg)=10001.10.310)(5300⨯⨯⨯⨯⨯-⨯⨯-km V V V c 其中:c ——0.8000 mol·L -1 (1/6K 2Cr 2O 7)标准溶液的浓度; 5——重铬酸钾标准溶液加入的体积(mL );V0——空白滴定用去FeSO4体积(mL);V——样品滴定用去FeSO4体积(mL);3.0——1/4碳原子的摩尔质量(g·mol-1);10-3——将mL换算为L;1.1——氧化校正系数;m——风干土样质量(g);k——将风干土样换算成烘干土的系数;k=1(1+1/含水量) 土壤有机质(g/Kg)=土壤有机碳(g/Kg)×1.724三、实验器材与仪器土样(取于钟楼北,风干研磨细后过100目筛);油浴锅,三角瓶、5mL移液管、5.00mL移液枪,棕色酸式滴定管;0.8000mol/L 1/6 K2Cr2O7标准溶液、浓硫酸、领啡啰啉指示剂、0.2mol/L FeSO4标准溶液。

实训六土壤有机质含量的测定一、目的要求土壤有机质含量是衡量土壤肥力的重要指标,对了解土壤肥力状况,进行培肥、改土有一定的指导意义。
通过实验了解土壤有机质测定原理,初步掌握测定有机质含量的方法既注意事项。
能比较准确地测出土壤有机质含量。
二、方法原理在加热条件下,用稍过量得标准重铬酸钾—硫酸溶液,氧化土壤有机碳,剩余的重铬酸钾用标准硫酸亚铁(或硫酸亚铁铵)滴定,由所消耗标准硫酸亚铁的量计算出有机碳量,从而推算出有机质的含量,其反应式如下:2K2Cr2O7+3C+8H2SO4→K2SO4+2Cr2(SO4)3+3CO2+8H2OK2Cr2O7+6FeSO4+7H2SO4→K2SO4+ Cr2(SO4)3+3Fe2(SO4)3+8H2O 用Fe2+滴定剩余的K2Cr2O72-时,以邻啡罗啉(C2H8N2)为氧化还原指示剂,在滴定过程中指示剂的变色过程如下:开始时溶液以重铬酸钾的橙色为主,此时指示剂在氧化条件下,呈淡蓝色,被重铬酸钾的橙色掩盖,滴定时溶液逐渐呈绿色(Cr3+),至接近终点时变为灰绿色。
当Fe2+溶液过量半滴时,溶液则变成棕红色,表示颜色已到终点。
三、仪器试剂1. 仪器用具硬质试管(18mm×180mm)、油浴锅、铁丝笼、电炉、温度计(0~200℃)、分析天平(感量0.0001g)、滴定管(25ml)、移液管(5ml)、漏斗(3~4cm),三角瓶(250ml)、量筒(10ml,100ml)、草纸或卫生纸。
2. 试剂配制1.0.1333mol/L重铬酸钾标准溶液称取经过130℃烘烧3~4h的分析纯重铬酸钾39.216g,溶解于400ml蒸馏水中,必要时可加热溶解,冷却后架蒸馏水定容到1000ml,摇匀备用。
2.0.2mol/L硫酸亚铁(FeSO4.7H2O)或硫酸亚铁铵溶液称取化学纯硫酸亚铁55.60g或硫酸亚铁铵78.43g,溶于蒸馏水中,加6mol/L H2SO41.5ml,再加蒸馏水定容到1000ml备用。

土壤有机质的测定(重铬酸钾容量法-外加热法)试剂准备:1.0.8 mol·L-1(1/6K2Cr2O7):称取130℃烘干的重铬酸钾(分析纯)39.2245g溶于水,定容1000mL。
2. 0.2mol·L-1FeSO4溶液:称取硫酸亚铁(FeSO4·7H2O,化学纯)56.0g溶于水中,加入浓硫酸5mL,稀释至1L。
(不稳定,现用现配)3. 邻菲罗啉指示剂:称取邻菲罗啉(分析纯)1.485g与FeSO4·7H2O 0.695g,定容至100mL。
4. 浓硫酸操作步骤:称取通过0.149mm(100目)的风干土样(约0.2g,根据有机质含量确定,有机质含量越高,质量越少)于硬质试管中→加重铬酸钾8mL(根据有机质含量来确定)→浓硫酸5mL→摇匀→弯颈漏斗→消煮炉(设定到220℃~240℃)→试管内液体沸腾发生气泡时开始计时5min→冷却→转移至250mL三角瓶中,并用蒸馏水冲洗漏斗和试管壁,使三角瓶中液体总体积约60~70mL,加邻菲罗啉指示剂2~3滴,用0.2mol·L-1 FeSO4滴定(橙黄→蓝绿→砖红色),记录FeSO4的体积。
每一批样品测定的同时,进行2-3个空白试验,即取少许二氧化硅颗粒代替土样,其他步骤相同。
注:滴定时多滴入一滴,约0.05mL。
土壤有机碳(mg·kg-1)=c×V 重铬酸钾×(V0-V1)×3×1.1/( V0×m)式中:c——0.8 mol·L-1(1/6K2Cr2O7)标准溶液的浓度;V 重铬酸钾——重铬酸钾标准溶液加入的体积,mL;V0——滴定空白样时所消耗的FeSO4体积,mL;V1——滴定样品时所消耗的FeSO4体积,mL;3——1/4C原子的摩尔质量,g/mol;1.1——氧化校正系数;m——为风干土质量,g。
土壤有机质(mg·kg-1)=土壤有机碳×1.724式中:1.724——土壤有机碳换成土壤有机质的平均换算系数。

土壤有机质的测定最常用的是以下办法:1.称土样:用减量法称取0.1~0.5g(精确到0.0001 g)通过0.25mm()的风干土样于硬质大试管中。
再用吸管加入5ml 0.8000mol/L的1/6 K2Cr2O7标准溶液;然后用注射器(或移液管)注入5ml浓硫酸,并小心旋转摇匀。
(本次实验土样称取量:<0.2000 g) 2.消煮:预先将油浴锅加热至185~190℃,将盛土样的大试管插入铁丝笼架中,然后将其放入油浴锅中加热,此时应控制锅内温度在170~180℃之间,并使溶液保持沸腾5min,然后取出铁丝笼架,待试管稍冷,用干净纸擦净试管外部的油液3.滴定:如消煮后的溶液呈橙黄色或黄绿色,则冷却后,将试管内混合物洗入250ml锥形瓶(或三角瓶)中,使瓶内体积在60~80ml左右,加邻啡罗林指示剂3~4滴,用0.2mol/L的硫酸亚铁滴定,溶液由橙黄色或黄绿色经蓝绿色到棕红色为终点;若用N-苯基邻氨基苯甲酸指示剂,则变色过程由棕红色经紫至蓝绿色为终点。
终点时,记录硫酸亚铁的用量(V)。
分析每批土样时,必须做3~5个空白标定,空白标定不加土样,仅加0.1~0.5g粉状石英砂,其它步骤与测定土样时完全相同,记录硫酸亚铁的用量(V),取测定结果的平均值。
最常用的是以下办法:1.称土样:用减量法称取0.1~0.5g(精确到0.0001 g)通过0.25mm ()的风干土样于硬质大试管中。
再用吸管加入5ml 0.8000mol/L的1/6 K2Cr2O7标准溶液;然后用注射器(或移液管)注入5ml浓硫酸,并小心旋转摇匀。
(本次实验土样称取量:<0.2000 g)2.消煮:预先将油浴锅加热至185~190℃,将盛土样的大试管插入铁丝笼架中,然后将其放入油浴锅中加热,此时应控制锅内温度在170~180℃之间,并使溶液保持沸腾5min,然后取出铁丝笼架,待试管稍冷,用干净纸擦净试管外部的油液3.滴定:如消煮后的溶液呈橙黄色或黄绿色,则冷却后,将试管内混合物洗入250ml锥形瓶(或三角瓶)中,使瓶内体积在60~80ml左右,加邻啡罗林指示剂3~4滴,用0.2mol/L的硫酸亚铁滴定,溶液由橙黄色或黄绿色经蓝绿色到棕红色为终点;若用N-苯基邻氨基苯甲酸指示剂,则变色过程由棕红色经紫至蓝绿色为终点。

一、实验目的1. 了解土壤的基本性质和组成;2. 掌握土壤检测的基本方法和原理;3. 分析土壤的酸碱度、有机质含量、养分含量等指标;4. 为农业生产提供科学依据。
二、实验原理土壤是由矿物质、有机质、水分和空气等组成的复杂混合物。
土壤的物理、化学和生物性质对植物的生长发育和农业生产具有重要影响。
本实验主要检测土壤的酸碱度、有机质含量、养分含量等指标。
1. 土壤酸碱度检测:采用pH试纸法,将土壤与水按1:1比例混合,搅拌均匀后静置,取上层清液滴在pH试纸上,与标准色卡对照,得到土壤的酸碱度。
2. 土壤有机质含量检测:采用重铬酸钾氧化法,将土壤与重铬酸钾混合,在高温下加热,使有机质氧化,通过测定剩余重铬酸钾的浓度,计算土壤有机质含量。
3. 土壤养分含量检测:采用原子吸收分光光度法,分别测定土壤中的氮、磷、钾、钙、镁等养分含量。
三、实验材料与仪器1. 实验材料:土壤样品、蒸馏水、重铬酸钾、硫酸、浓硫酸、氢氧化钠、过氧化氢、硫酸铵、硫酸钾、硝酸、盐酸、硝酸银、氯化钡、碳酸钠、硫酸铜、硫酸锌、硫酸铵、氢氧化钠等。
2. 实验仪器:pH试纸、电子天平、振荡器、水浴锅、电热板、离心机、分光光度计、原子吸收分光光度计、锥形瓶、烧杯、滴定管、移液管等。
四、实验步骤1. 土壤酸碱度检测:(1)取土壤样品10g,加入90ml蒸馏水,振荡混合均匀;(2)静置30min,取上层清液;(3)滴取少量清液于pH试纸上,与标准色卡对照,记录pH值。
2. 土壤有机质含量检测:(1)取土壤样品5g,加入10ml重铬酸钾溶液,振荡混合均匀;(2)将混合液转移至锥形瓶中,加入硫酸和浓硫酸,置于电热板上加热;(3)待溶液颜色由橙色变为绿色,继续加热5min;(4)冷却后,用蒸馏水定容至100ml;(5)取适量溶液,用硫酸亚铁铵标准溶液滴定,计算土壤有机质含量。
3. 土壤养分含量检测:(1)分别称取土壤样品0.5g,加入适量的硝酸和盐酸,振荡混合均匀;(2)将混合液转移至锥形瓶中,加入过氧化氢,置于电热板上加热;(3)待溶液颜色由黄色变为无色,继续加热5min;(4)冷却后,用蒸馏水定容至100ml;(5)分别测定溶液中的氮、磷、钾、钙、镁等养分含量。

土壤有机质的测定土壤有机质是鉴别土壤肥力的重要指标,是肥力的标志。
有机质的含量、组成和性质,随气候生物条件呈有规律的变化,所以,在土壤分析中常是必测项目,它对探讨土壤的形成、分布、分类以及肥力等,都重要的理论和实践意义。
一、实验目的1、了解土壤有机质测定的基本原理。
2、初步掌握土壤有机质测定的基本方法。
二、实验原理稀释热法(水合热法)是利用浓硫酸和重铭酸钾迅速混合是所产生的热来氧化有机质,剩余的重辂酸钾以邻菲罗琳为指示剂,用硫酸亚铁标准溶液进行滴定,以氧化耗去重铭酸钾的量来计算出碳的含量。
该法操作方便,但由于产生的热温度较低,所以对有机质氧化程度较低,只有77%。
其反应式如下:IK2Cr2O1+SH2SO4÷3C→2K2SO4+2Cr2(SO4)3+3CO2+SH2OK2Cr2O1+6FeSO4+7H2SO4→K2SO^1Cr2(SO4)y÷3Fe2(SO1)3+7H2O三、实验试剂(1)UZdKao7)溶液:准确称取KgO?(分析纯,105C6烘干)49.04g,溶于水中,稀释至I1。
(2)0.4〃7。
/.1(打℃)的基准溶液:准确称取“码(分析6纯,13OC烘干3∕ι)19.6132g于250/泣烧杯中,以少量水溶解,全部洗入IoOO,泣容量瓶中,加入浓乩5。
4约70m,冷却后用水定容至刻度,充分摇匀备用。
(其中含硫酸浓度约为2.5mo1∙E-1(^H2SO4))。
(3)05mo1∙1FeSO4溶液:称取尸W〃小。
140g溶于水中,加入浓乩SO,15神,冷却稀释至I1。
此溶液的准确浓度以OAmo111(^K2Cr2O7)的基准溶液标定之。
即准确分别吸取3份04〃H11(∖K2Cr2O1)基准溶液各25m1于150m1三角瓶中,加入邻菲罗咻指示剂2~3滴,然后用0∙5∕M∕∙1"eSθ4溶液滴定至终点,并计算出FeSO4的准确浓度。
硫酸亚铁(反SO4)溶液在空气中易被氧化需新鲜配制或以标准的KQaQ溶液每天标定。
一、土壤一般概述土壤养分是指存在于土壤中的植物所必需的营养元素。
包括碳(C)、氢(H)、氧(O)、氮(N)、磷(P)、钾(K)、钙(Ca)、镁(Mg)、硫(S)、铁(Fe)、锰(Mn)、钼(Mo)、锌(Zn)、铜(Cu)、硼(B)、氯(Cl)等16种。
在自然土壤中,除前三种碳(C)、氢(H)、氧(O)三种元素外,其他土壤养分主要来源于土壤矿物质和土壤有机质、其次是大气降水、坡渗水和地下水等。
土壤养分分级标准主要针对有机质、全氮、速效氮、速效磷和速效钾的含量进行分级,每种级别对应不同成分的含量不同。
而在实际工作中,我们可以对照或参考这个标准,对要进行施肥的土地进行测试分析,以了解土壤的真实肥力状况。
一般情况下,耕作层土壤有机质含量通常在5%以上;褐土在自然植被下,有机质含量为1-3%,但由于褐土适于耕作,大部分已辟为农地,致使土壤中的有机质含量减少到了1%左右。
有机质是土壤肥力的标志性物质,其含有丰富的植物所需要的养分,调节土壤的理化性状,是衡量土壤养分的重要指标。
它主要来源于有机肥和植物的根、茎、枝、叶的腐化变质及各种微生物等,基本成分主要为纤维素、木质素、淀粉、糖类、油脂和蛋白质等,为植物提供丰富的C、H、O、S及微量元素,可以直接被植物所吸收利用。
其中有机质的分级可作为土壤养分分级,土壤养分分级标准共六级,且六级为最低,一级为最高。
二、常见土壤分类1.棕壤:棕壤又称棕色森林土,主要分布于半湿润半干旱地区的山地垂直带谱中,如秦岭北坡、吕梁山、中条山、六盘山等高山及洮河流域的密茂针叶林或针阔混交林的林下。
在褐土分布区之上。
具有深达1.5-2m发育良好的剖面,有枯枝落叶层、腐殖质聚积层,粘化过渡层,疏松的母质层等。
表土层厚约15-20cm,质地多为中壤。
其下则为粘化紧实的心土层,粘粒聚集作用明显,厚约30-40,富含胶体物质和粘粒,有明显的核状或棱块状结构,在结构体表面有明显的铁锰胶膜复被。
再下逐渐过渡至轻度粘化的底土层。

土壤有机质测定方法土壤有机质是土壤中最活性和最变化快的部分,对土壤的肥力和生态功能具有重要影响。
土壤有机质含量的测定是土壤学研究中的重要内容之一。
本文将详细介绍几种常用的土壤有机质测定方法。
一、干燥燃烧法干燥燃烧法是一种常用的土壤有机质测定方法。
该方法的基本原理是通过将土壤样品在高温下燃烧,将有机质转化为无机物,从而测定土壤中的有机质含量。
具体操作步骤如下:1. 准备土壤样品:将取样土壤样品经过筛分,去除大颗粒杂质,并尽量避免土壤样品的长时间曝晒,以免有机质含量的变化。
2. 干燥土壤样品:将土壤样品在室温下晾干,然后放入105C的烘箱中进行干燥至恒重。
3. 燃烧土壤样品:将已经干燥的土壤样品放入预先烧热的燃烧瓶中,用隔绝氧气的氮气进行灌注,然后将煤油灯置于样品下方进行燃烧,使土壤样品在高温下完全燃烧。
4. 灰化:将燃烧后的土壤样品进行水洗,然后放入烘箱中干燥至恒重,最后得到土壤样品的干燥灰分,根据土壤样品的质量差和质量变化计算土壤有机质含量。
二、浸提法浸提法是一种常用的土壤有机质测定方法,该方法的基本原理是通过使用一定溶剂提取土壤样品中的有机物质,然后经过蒸发、干燥等处理,最后测定溶液中有机物质的含量。
具体操作步骤如下:1. 准备土壤样品:同样需要进行筛分处理以去除杂质,并尽量避免曝晒,保证土壤样品的有机质含量不发生变化。
2. 提取样品:将土壤样品与一定比例的溶剂(如醇、水等)混合,然后通过振荡或冷却浸提的方法,提取土壤样品中的有机物质。
3. 过滤与蒸发:将浸提液通过滤纸过滤,去除杂质,然后将滤液置于蒸发皿中,进行蒸发浓缩。
4. 干燥与称重:将浓缩后的溶液放入烘箱中干燥至恒重,然后根据质量差和质量变化计算土壤有机质含量。
5. 计算:计算有机质的含量,根据样品的质量、提取溶液的体积和测定结果来计算土壤样品中有机质的含量。
三、颜色比色法颜色比色法是一种简便快速的土壤有机质测定方法。
该方法的基本原理是通过土壤样品中有机质的氧化还原反应,使得有机质转化为可产生颜色的物质,并使用比色法来测定颜色的强度从而计算有机质的含量。

土壤有机质试验标定用的石英砂规格
为了保证土壤有机质试验的准确性,需要使用石英砂进行标定。
石英砂的规格应该符合以下要求:
1. 石英砂应该是纯度高、无杂质的天然石英矿石经过粉碎、筛分而成的细粒度石英砂。
2. 石英砂的粒径应该在0.05mm-2.0mm之间,适合用于土壤有机质试验的标定。
3. 石英砂的比表面积应该在300-400平方米/克之间,能够提供充足的吸附表面,保证标定的准确性。
4. 石英砂应该是无毒、无害的,不会对土壤有机质试验产生干扰。
在进行土壤有机质试验的标定时,应该选择符合以上标准的石英砂,并按照标定方法进行操作,以保证试验结果的准确性和可靠性。
- 1 -。
土壤农化分析常用指标测定方法土壤有机质测定一、原理170~180℃条件下,用一定浓度的K2Cr2O7-H2SO4溶液(过量)氧化土壤有机质,剩余的K2Cr2O7用FeSO4滴定,由消耗的K2Cr2O7量计算出有机碳量,再乘以常数1.724,即为土壤有机质含量。
其反应式如下:K2Cr2O7与有机碳反应K2Cr2O7+8 H2SO4+3C→2Cr2(SO4)3+3CO2+8H2O过量的K2Cr2O7与FeSO4的滴定反应K2Cr2O7+4FeSO4+7 H2SO4→K2SO4+Cr2(SO4)3+3Fe2(SO4)3+7H2O二、试剂1、0.4mol/L(K2Cr2O7-浓H2SO4)标准溶液:称取经130℃烘干的K2Cr2O7(AR)39.2245g61溶于水中,加热溶解后加入1000mL浓H2SO4定容至2000mL。
2、0.2mol/L FeSO4溶液:称取FeSO4(AR)56g溶于水中,加浓硫酸5mL,稀释至1L。
3、石英砂:粉末状。
三、实验步骤称取<0.25mm风干土0.5×××~1.0×××g于干燥试管中。
加入少量水润湿样品,准确沿避缓慢加入10.0mL K2Cr2O7-H2SO4混合液,摇分散土样,加入小漏斗,放入铁丝笼中。
将铁丝笼放入已开启185~190℃油浴锅中(使温度在170~180℃)沸腾准确5分钟;取出稍冷,擦净试管外壁油污(同时做空白实验);冷却后把溶液全部转移到200~250mL三角瓶中(最后体积控制在60~70mL),加入指示剂3滴,用已知浓度的FeSO4滴定。
四、结果计算有机质()100724.11.1100.3%30⨯⨯⨯⨯⨯⨯-=-WcVV式中:V0——滴定空白所用的FeSO4溶液的体积(mL);V——滴定样品所用的FeSO4溶液的体积(mL);c——0.2mol/L FeSO4溶液准确浓度;3.0——1/4碳原子的摩尔质量(g/mol);10-3——将mL换算为L;1.1——氧化校正系数;1.724——土壤有机碳换算成土壤有机质的平均换算系数。
土壤有机质的测定方法土壤指标的测定方法土壤,作为地球生态系统的重要组成部分,其质量和健康状况对于农业生产、环境保护以及生态平衡都具有至关重要的意义。
而土壤有机质含量以及各项土壤指标的测定,是了解土壤特性、评估土壤肥力和制定合理土壤管理措施的关键环节。
一、土壤有机质的测定方法(一)重铬酸钾容量法——外加热法这是测定土壤有机质含量的常用方法之一。
其原理是:在加热的条件下,用过量的重铬酸钾硫酸溶液氧化土壤中的有机碳,剩余的重铬酸钾用硫酸亚铁标准溶液滴定,根据消耗的重铬酸钾量计算出有机碳含量,再乘以常数 1724,即为土壤有机质含量。
具体操作步骤如下:1、准确称取通过 025mm 筛孔的风干土样 01 05g(精确到00001g),放入硬质玻璃试管中。
2、用移液管准确加入 08000mol/L 重铬酸钾标准溶液 500mL,再加入 5mL 浓硫酸,摇匀。
3、将试管插入铁丝笼中,放入预先加热至180 190℃的油浴锅中,保持温度在 170 180℃,使溶液沸腾 5 分钟。
4、取出试管,冷却后将溶液全部转入 250mL 三角瓶中,用水冲洗试管内壁,使总体积约为 60 70mL。
5、加入邻菲啰啉指示剂 3 4 滴,用 02mol/L 硫酸亚铁标准溶液滴定,溶液颜色由橙黄经蓝绿到棕红即为终点。
6、同时做空白试验,即在试管中加入 500mL 重铬酸钾标准溶液和5mL 浓硫酸,按上述步骤进行操作。
(二)灼烧法该方法的原理是通过高温灼烧使土壤中的有机物质氧化分解,以失重的量来计算土壤有机质含量。
操作流程为:1、称取适量的风干土样,放入已知重量的坩埚中。
2、将坩埚置于高温电炉中,逐渐升温至 550 600℃,保持 4 5 小时。
3、取出坩埚,在干燥器中冷却至室温,称重。
4、通过灼烧前后的重量差,计算土壤有机质含量。
二、土壤指标的测定方法(一)土壤酸碱度(pH 值)的测定1、电位法这是较为准确的测定方法。
原理是利用玻璃电极和参比电极组成的原电池,测量其电动势来确定溶液的 pH 值。
土壤有机质、N、P、K测定1、有机质测定测定步骤:常规容量法(标准方法):(1)用长形称量纸在分析天平上用差减法精确称取0.25mm风干土样0.1~0.5克(有机质含量5-40g/kg),放入一干燥的硬质试管当中(20×220mm),用移液管准确加入0.8mol(1/6)·L-1K2Cr2O7溶液5ml,用定量加液器加浓H2SO45ml(酸水比1:1),在试管口加一小漏斗,以冷凝回流水蒸气。
(2)将试管成批的插入铁丝笼中(10-20个),每批一空白试管(不加土,只加K2Cr2O7和浓H2SO4和干净小瓷片,以防爆沸)。
放入已预热控温在180度的远红外消煮器中。
待内容物微沸,记时5分钟,取出。
(3)稍冷,用洗瓶冲洗小漏斗内外,洗涤液无损流入试管。
将试管中的消化液完全转入150ml三角瓶中,再用洗瓶多次洗涤试管内壁,并将洗涤液无损转入三角瓶中,溶液体积达到60-70ml(以控制硫酸浓度在1-1.5 mol·L-1)。
加邻菲罗啉指示剂3-5滴,(用标准低铁盐溶液)用标准FeSO4溶液滴定至溶液由黄―绿―棕红即为终点。
记下低铁用量。
注:采用其它加热器(电热板、电炉、酒精灯等)加热样品时,可直接将土样和K2Cr2O7-H2SO4放入100~150ml三角瓶中,在瓶口插一小漏斗,然后将同一土样平行测定的多个三角瓶一同置于加热器上,待瓶内溶液出现均匀豆大气泡立即记时,降低加热器温度,保持微沸五分钟,立即取下三角瓶(注意:空白的测定条件应与样品相同)。
稍冷,用洗瓶冲洗小漏斗内外,洗液一并入三角瓶中。
加指示剂后即可用低铁滴定。
此法简单易行,快速准确,适于少数样品的分析。
(4)计算。
土壤有机碳g/kg=M(V0-V)×0.003×1.1×1000/W土壤有机质g/kg=土壤有机碳g/kg×1.724式中:M――标准低铁盐溶液的摩尔浓度V0――空白滴定所用的低铁溶液体积(ml)V――样品滴定所用的低铁溶液体积(ml)W――烘干土重=样重×水分系数0.003――1mmol(1/6).L-1 K2Cr2O7所相当的碳的克数1.1――氧化率校正值1.724――每克碳所相当的有机质克数(5)试剂与仪器仪器与器皿:万分之一的天平、硬质玻璃试管、加热器(油浴、电热板、电炉、酒精灯、远红外消煮器)5ml移液管、150ml三角瓶、2~3cm小漏斗、25~50ml酸式滴定管等。
土壤有机质的测定•相关推荐土壤有机质的测定土壤有机质的测定土壤有机质既是植物矿质营养和有机营养的源泉(本身含有氮、磷、钾、钙、镁、有机碳、硫和其他微量元素,以及各种简单的有机化合物),又是土壤中异养型微生物的能源物质,同时也是形成土壤结构的重要因素。
因此,土壤有机质就直接影响着土壤的耐肥性、保墒性、缓冲性、耕性,通气状况和土壤温度等,因此土壤有机质是鉴别土壤肥力的重要标志。
土壤有机质按其分解程度不同分为三类:第一类为粗有机质,包括分解很少但仍保持原形态特征的植物残体;第二类为半分解有机质,包括正在分解中的植物残体(如纤维素等),以及微生物生命活动的各种产物;第三类为腐殖质,主要指与原来有机质性质发生较大变化,复合成为特殊性质的有机物质。
我国除东北-1黑土有机质含量高达40~50g·kg以上外,由此向西北,土壤有机质含量亦逐渐减少。
大量的研究资料表明土壤有机质含量与土壤全氮含量之间呈正相关关系,且其比值(C/N)随着土壤所处的环境因素和利用状况而变化。
我国耕作土壤的C/N介于9-13之间,其比值的高低放映有机质在矿化过程中所释放出有效氮量的多少,其比值越小,释放出的有效氮量就越多。
土壤有机质的测定方法目前,土壤有机质含量的测定使用比较普遍方法是重铬酸钾容量法。
重铬酸钾容量法不宜用于测定含有氯化物的土壤,如样品中氯离子含量不多,可加入Ag2SO4消除部分干扰,如土壤中氯离子含量较高,可考虑用水洗的办法加以克服,经水洗处理后测出的土壤有机质总量中不包括水溶性有机质组分,应加以说明。
新采回的水稻土或长期处于渍水条件下的土壤中,由于其中的低价铁、锰等化合物会影响分析结果的准确性,必须将土壤充分自然风干才可进行分析。
实验原理:在加热并有硫酸存在的条件下,用过量的重铬酸钾溶液氧化土壤中的有机碳,多余的重铬酸钾用标准的硫酸亚铁溶液进行滴定,根据消耗掉的重铬酸钾的量来间接计算土壤中有机碳的含量,进而根据土壤中有机质与有机碳的比例(即换算因数)计算土壤中有机质的含量。
土壤有机质、N、P、K测定1、有机质测定测定步骤:常规容量法(标准方法):(1)用长形称量纸在分析天平上用差减法精确称取0.25mm风干土样~0.5克(有机质含量5-40g/kg),放入一干燥的硬质试管当中(20×220mm),用移液管准确加入(1/6)·L-1K2Cr2O7溶液5ml,用定量加液器加浓H2SO45ml(酸水比1:1),在试管口加一小漏斗,以冷凝回流水蒸气。
(2)将试管成批的插入铁丝笼中(10-20个),每批一空白试管(不加土,只加K2Cr2O7和浓H2SO4和干净小瓷片,以防爆沸)。
放入已预热控温在180度的远红外消煮器中。
待内容物微沸,记时5分钟,取出。
(3)稍冷,用洗瓶冲洗小漏斗内外,洗涤液无损流入试管。
将试管中的消化液完全转入150ml三角瓶中,再用洗瓶多次洗涤试管内壁,并将洗涤液无损转入三角瓶中,溶液体积达到60-70ml(以控制硫酸浓度在mol·L-1)。
加邻菲罗啉指示剂3-5滴,(用标准低铁盐溶液)用标准FeSO4溶液滴定至溶液由黄―绿―棕红即为终点。
记下低铁用量。
注:采用其它加热器(电热板、电炉、酒精灯等)加热样品时,可直接将土样和K2Cr2O7-H2SO4放入100~150ml三角瓶中,在瓶口插一小漏斗,然后将同一土样平行测定的多个三角瓶一同置于加热器上,待瓶内溶液出现均匀豆大气泡立即记时,降低加热器温度,保持微沸五分钟,立即取下三角瓶(注意:空白的测定条件应与样品相同)。
稍冷,用洗瓶冲洗小漏斗内外,洗液一并入三角瓶中。
加指示剂后即可用低铁滴定。
此法简单易行,快速准确,适于少数样品的分析。
(4)计算。
土壤有机碳g/kg=M(V0-V)×××1000/W土壤有机质g/kg=土壤有机碳g/kg×。
式中:M――标准低铁盐溶液的摩尔浓度V0――空白滴定所用的低铁溶液体积(ml)V――样品滴定所用的低铁溶液体积(ml)W――烘干土重=样重×水分系数――1mmol(1/6).L-1 K2Cr2O7所相当的碳的克数――氧化率校正值――每克碳所相当的有机质克数(5)试剂与仪器仪器与器皿:万分之一的天平、硬质玻璃试管、加热器(油浴、电热板、电炉、酒精灯、远红外消煮器)5ml移液管、150ml三角瓶、2~3cm小漏斗、25~50ml酸式滴定管等。
土壤有机质测定方法一、物理方法物理方法主要通过测定土壤中有机质的含量来判断土壤肥力。
常用的物理方法有燃烧法和重量法。
1.燃烧法:将土壤样品加热至500℃以上,使有机质燃烧,通过测定样品质量的损失来计算土壤中有机质的含量。
具体步骤如下:(1)将土壤样品称取,将其放入事先称重好的烧杯中;(2)将烧杯放到燃气或电炉上进行加热,控制温度在500℃以上;(3)加热结束后,取出烧杯,冷却并重新称重,计算样品质量的损失,即可得出有机质的含量。
2.重量法:通过测定土壤样品在干燥条件下的重量,再与样品在水分饱和状态下的重量进行比较,从而计算出有机质的含量。
具体步骤如下:(1)将土壤样品取一定量,放入烘箱中进行干燥,通常温度为105℃;(2)干燥至恒重后,取出样品,重新称重;(3)将干燥后的土壤样品与其在湿润状态下的重量进行比较,计算出有机质的含量。
二、化学方法化学方法主要通过测定土壤中的一些元素或化合物的含量来间接判断土壤有机质的含量,常用的化学方法有酸碱浸提法和蒽酮颜色反应法。
1.酸碱浸提法:通过用酸或碱溶液浸提土壤样品中的有机物质,再以其中一种指示剂作为指示,测定酸碱溶液浸提液中的指示剂变化来判断有机质的含量。
具体步骤如下:(1)将土壤样品取一定量,加入一定体积的酸或碱溶液中;(2)使用其中一种指示剂,测定浸提液的颜色变化,根据颜色变化的程度来判断有机质的含量。
2.蒽酮颜色反应法:通过将土壤样品与蒽酮反应,蒽酮与有机物质发生反应产生颜色,从而测定有机质的含量。
具体步骤如下:(1)将土壤样品取一定量,加入蒽酮溶液中;(2)等待一定时间后,测定溶液的吸光度,在特定的波长下进行测定;(3)根据测定的吸光度值,通过比色计或光度计来计算有机质的含量。
三、生物学方法生物学方法主要通过测定土壤中微生物数量变化或酶活性的变化来判断土壤有机质的含量。
常用的方法有微生物数测定法和酶活性测定法。
1.微生物数测定法:通过将土壤样品加入适当培养基中,培养一段时间后,根据样品上产生的菌落数量来判断有机质的含量。
实验报告课程名称: 土壤学实验 指导老师: 谢晓梅 成绩:__________________实验名称: 土壤有机质的测定 同组学生姓名: 边舒萍一、实验目的和要求 二、实验内容和原理三、实验材料与试剂 四、实验器材与仪器五、操作方法和实验步骤 六、实验数据记录和处理七、实验结果与分析 八、讨论、心得一、 实验目的和要求1. 了解土壤有机质测定对于农业生产的意义;2. 掌握土壤有机质含量的测定方法。
二、 实验内容和原理有机质是土壤中重要组成成分,其含量水平是衡量土壤肥力的重要指标之一。
本实验采用重铬酸钾容量法——稀释热法,利用浓硫酸和重铬酸钾混合时产生的热氧化有机质中的碳,通过测定消耗的氧化剂的量来计算得出土壤有机质含量,从而分析该土壤肥力水平,并对此提出改良措施。
重铬酸钾容量法——稀释热法过程的化学反应式:氧化过程:K 2Cr 2O 7+C+H 2SO 4→K 2SO 4+Cr 2(SO 4)3+CO 2+H 2O滴定过程:K 2Cr 2O 7+FeSO 4+H 2SO 4→K 2SO 4+Cr 2(SO 4)3+Fe 2(SO 4)3+H 2O土壤有机碳与有机质换算公式:土壤有机质(g/Kg )=土壤有机碳(g/Kg )×1.724 三、 实验器材与仪器土样(取于余杭塘路施工旁,风干研磨细后过100目筛);250mL三角瓶×2,10mL量筒,100mL量筒,5mL移液管,5.00mL移液枪,棕色酸式滴定管;1mol/L 1/6 K2Cr2O7标准溶液,浓硫酸,领啡啰啉指示剂,0.5021mol/L FeSO4标准溶液。
四、操作方法和实验步骤1.在500mL三角瓶中加入m=0.5070g土样;2.用移液管加入1mol/L 1/6 K2Cr2O7标准溶液10mL;3.混匀后用移液枪移取浓硫酸20mL,旋转摇动1min,之后放置30mL,加水100mL;4.滴入3滴指示剂后用0.5021mol/L FeSO4标准溶液滴定至溶液由绿色变暗绿色,最终以瞬间变为砖红色为终点;5.用相同方法作空白对照(不加土样)测定。
五、实验数据记录和处理表1 FeSO4标准溶液消耗体积与土壤有机质(碳)含量样品滴定前读数V1/mL 滴定后读数V2/mLFeSO4消耗体积V(V0)/mL土壤有机碳么m1(g/Kg)土壤有机质m2(g/Kg)第一组0.00 18.70 18.705.255 9.060 空白组 3.32 23.35 20.03注:m1={[c(V0-V)×10-3×3.0×1.33]/m}×1000;m2=m1×1.724其中,1.33为氧化校正系数;m为所称量土样重。
六、实验结果与分析本实验中我组取得土样,其土壤有机质为9.060g/Kg,土样有机质含量为9.060%。
依据相关分类标准[1],该土壤属于矿质土壤,超过耕作层土壤有机质含量5%的一般情况。
结合采样地点环境状况,这与采样点地处河流10-15m处,土壤表层有较多草本植物生长,如沿阶草等情况相符合。
该采样土壤能维持草本植物或者低等植物的生长,但很难为农作物和园艺植物的生长提供足够的碳素营养来源,因此也可以理解,为何采样地点旁边区域有青菜种植而采样地点无。
因此,若要使类似采样地点的土壤有机质增加到20%以上,建议采取的措施:①秸秆还田[2]。
秸秆还田能直接为土壤增加有机物,同时也减少了田间焚烧时所产生的环境污染;②增加生物总产量。
在增产的条件下,提高地上植物和地下根系的数量,促进土壤生物的繁殖,致使动植物残体的积累量增加。
③合理增加有机肥用量。
实行有机物和无机肥料混合使用,不断增加有机物残留在土壤中的数量;④减少土壤有机质补益药的消耗。
采用少耕、覆盖等,减少和控制土壤氧气的供应,削弱好氧微生物分解活动,覆盖则能降低土壤有机质随水土流失而减少的可能性。
七、讨论与心得问题1. 比较所列计算公式与书中计算公式,并说明计算公式中各参数的意义?1.计算公式为:土壤有机碳(g/Kg)={[c(V0-V)×10-3×3.0×1.33]/m}×1000土壤有机质(g/Kg)=土壤有机碳(g/Kg)×1.724其中,1.33为氧化校正系数;C为0.5mol/L FeSO4标准溶液的浓度;V0为空白所用的0.5mol/L FeSO4标准溶液的浓度(mL);V为样品所用的0.5mol/L FeSO4标准溶液的浓度(mL);m为所称量土样重(g)。
2.书中公式为:土壤有机碳(g/Kg)={[5c(V0-V)×10-3×3.0×1.1]/mkV0}×1000土壤有机质(g/Kg)=土壤有机碳(g/Kg)×1.724其中,C×5/ V0为0.5mol/L FeSO4标准溶液的浓度;V0为空白所用的0.5mol/L FeSO4标准溶液的浓度(mL);V为样品所用的0.5mol/L FeSO4标准溶液的浓度(mL);m为所称量土样重(g)。
公式1和公式2之间的区别主要在于:硫酸亚铁浓度表示方法不同:1.中c即为硫酸亚铁浓度,已经考虑了氧化还原反应中物质的量的对应(通过调整重铬酸钾溶液浓度)而2.中C×5/ V0才是硫酸亚铁的浓度,C是指空白的重铬酸钾浓度,V0指的是滴定空白消耗硫酸亚铁的毫升数。
因此如果运用公式1,需要运用优级纯试剂配置的0.1000mol/L 1/6 K2Cr2O7做基准试剂标定硫酸亚铁,其浓度较为精准[3];而用公式;2,无需标定硫酸亚铁浓度,但准确度较差。
因此实验室采用第一种公式计算方法。
问题2. 试述测定土壤有机质的各种方法,并进行比较?1.干烧法:运用土壤有机质中的碳经氧化后放出的二氧化碳量。
在无二氧化碳的氧气流或惰性载气流中将土壤样品进行燃烧,完全燃烧后释放出的二氧化碳置于监测,此时检测手段测量实验中形成的二氧化碳实际含量。
具体而言,是在高温下将有机碳加热分解,使其变成二氧化碳后,用碱石灰吸收,由碳酸钙重量换算OM含量。
该方法结果准确,作为标准方法校核;费时且一起设备要求高,一般不用仪器方法:快速灵敏但是一般仪器昂贵。
[4]2.重铬酸钾容量法:在过量的硫酸存在下,借氧化剂重铬酸钾氧化有机碳,剩余的氧化剂用标准硫酸亚铁溶液回滴,通过剩余量算出被土壤有机质消耗的重铬酸钾,计算土壤有机质。
化学反应式参见实验原理。
该方法测定结果准确,土壤中碳酸盐无干扰作用,适用于大量样品分析。
但操作比较复杂,多滴定终点的观察判断要求精准,常常会产生视觉误差。
3.灼烧法:测定土壤有机质中的C经灼烧后造成的土壤失重。
将温度在105℃下出去吸湿水的土壤样品先称重,再将其置于350-1000℃灼烧2h,然后称重。
两次称重之重量差即是测定土壤样品中土壤有机质的重量。
该方法操作简单,但有机碳不完全燃烧会产生误差。
4.比色法:在土壤样品中直接加入重铬酸钾溶液和浓硫酸,利用浓硫酸和重铬酸钾溶液迅速混合时所产生的热(温度在120℃左右)来氧化土壤中的有机碳。
样品氧化液用TFW-1型数字直读式多功能土壤分析仪,选用波长为620nm滤色片,用5cm比色皿直接比色测定,以测出的表头读书来计算有机质的含量。
[5]该方法操作简便,实验步骤容易掌握,测定灵敏度高、准确度高,干扰少,且节约油料、能源。
是最佳的测定方案,但其使用的仪器设备价格较贵。
问题3. 试述土壤有机质对于土壤肥力及土壤生态的意义?1.有机质对于土壤肥力:1)提供植物所需养分:土壤有机质是作物所需的氮、磷、硫、微量元素等各种养分的主要来源。
同时土壤有机质分解合成过程中,产生的多种有机酸和腐殖酸能溶解部分土壤矿质部分,促进矿物风化,有利于养料的有效化。
2)改善土壤肥力特征:在物理性质上,土壤有机质在多糖和腐殖物质在土壤团聚体的形成和稳定方面起着重要作用。
改善土壤的可塑性、粘结性、透水性、通气性。
在化学性质上,腐殖物质对阴阳离子的吸附有重要贡献,显著提高了部分土壤的保肥能力。
在生物性质上,土壤有机质是微生物生命活动所需养分和能量的主要来源,它还可以通过刺激微生物和动物活动来增加土壤酶的活性,从而直接影响土壤养分转化的生物化学过程[5]。
2.有机质对于生态环境:1)有机质能与重金属离子发生络合、吸附和还原作用,对其有较强的络合和富集能力。
2)有机质对农药等有机污染物有极强的亲和力,对有机污染物在土壤中的生物活性、残留、生物降解、迁移和蒸发等过程有重要的影响。
3)有机质是全球碳平衡过程中非常重要的碳库[6],土壤有机质的损失对地球自然环境有重大影响[7]。
参考文献[1] 武天云, 李凤民, 钱佩源, 等. 土壤有机质概念和分组技术研究进展[J]. 应用生态学报, 2004, 15(4): 717-722.[2] 刘天学, 纪秀娥. 焚烧秸杆对土壤有机质和微生物的影响研究[J]. 土壤, 2003, 35(4): 347-348.[3] 马爱生,张英利. 土壤有机质测定的计算公式说明[J]. 高校实验室工作研究. 2001(01).[4] 李静. 土壤有机质测定方法比对分析[J]. 绿色科技, 2012 (5): 203-204.[5] 谢细香. 重铬酸钾稀释热比色法测定土壤有机质的研究[J]. 安徽农业科学, 2005, 33(6): 998-999.[6] 黄昌勇,徐建明. 2010. 土壤学[M]. 北京:中国农业出版社.[7] Eswaran H, Van Den Berg E, Reich P. Organic carbon in soils of the world[J]. Soil science society of America journal, 1993, 57(1): 192-194.。