人教版化学选修四思维导图化学反应进行的方向含答案
- 格式:docx
- 大小:104.33 KB
- 文档页数:4


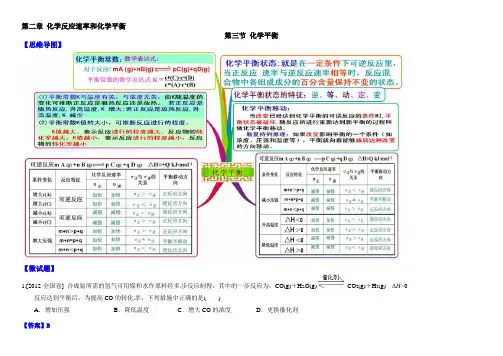
第二章化学反应速率和化学平衡第三节化学平衡【思维导图】【微试题】1.[2012·全国卷] 合成氨所需的氢气可用煤和水作原料经多步反应制得,其中的一步反应为:CO(g)+H2O(g)CO2(g)+H2(g)ΔH<0反应达到平衡后,为提高CO的转化率,下列措施中正确的是()A.增加压强B.降低温度C.增大CO的浓度D.更换催化剂【答案】B2.向绝热恒容密闭容器中通入SO2和NO2,在一定条件下使反应SO2(g)+NO2(g)SO3(g)+NO(g)达到平衡,正反应速率随时间变化的示意图如下所示。
由图可得出的正确结论是()A.反应在c点达到平衡状态B.反应物浓度:a点小于b点C.反应物的总能量低于生成物的总能量D.△t1=△t2时,SO2的转化率:a~b段小于b~c段【答案】D3.(2012·安徽卷)一定条件下,通过下列反应可实现燃煤烟气中硫的回收:SO2(g)+2CO(g)2CO2(g)+S(l)ΔH<0若反应在恒容的密闭容器中进行,下列有关说法正确的是()A.平衡前,随着反应的进行,容器内压强始终不变B.平衡时,其他条件不变,分离出硫,正反应速率加快C.平衡时,其他条件不变,升高温度可提高SO2的转化率D.其他条件不变,使用不同催化剂,该反应的平衡常数不变【答案】D4.(2014山东理综)研究氮氧化物与悬浮在大气中海盐粒子的相互作用时,涉及如下反应:2NO2(g)+NaCl(s)NaNO3(s)+ClNO(g)K1∆H < 0 (I)2NO(g)+Cl2(g )2ClNO(g)K2∆H < 0 (II)(1)4NO2(g)+2NaCl(s )2NaNO3(s)+2NO(g)+Cl2(g)的平衡常数K= (用K1、K2表示)。
(2)为研究不同条件对反应(II)的影响,在恒温条件下,向2L恒容密闭容器中加入0.2mol NO和0.1mol Cl2,10min时反应(II)达到平衡。

第二章化学反应速率和化学平衡第四节化学反应进行的方向【思维导图】【微试题】1.(2010·杭州第一次质量检测)下列说法中正确的是( )A.凡是放热反应都是能自发进行的反应,而吸热反应都是非自发进行的反应B.自发反应一定是熵增大的反应,非自发反应一定是熵减小或不变的反应C.熵增加且放热的反应一定是自发反应D.非自发反应在任何条件下都不能发生【答案】C2.对于反应:4Fe(OH)2(s)+2H2O(l)+O2(g)===4Fe(OH)3(s) ΔH=- kJ·mol-1,且熵减小,在常温常压下该反应能自发进行,对该反应的方向起决定作用的是( ) A.焓变 B.温度 C.压强 D.熵变【答案】A3.高温下,某反应达平衡,平衡常数K=[c(CO)·c(H2O)]/[c(CO2)·c(H2)],恒容时,温度升高,H2浓度减小,下列说法正确的是( )A.该反应的焓变为正值B.恒温恒容下,增大压强,H2浓度一定减小C.升高温度,逆反应速率减小D.该反应的化学方程式为CO+H2OCO2+H2【答案】A4.(2012·海南高考·15) 已知A(g)+B(g)C(g)+D(g)反应的平衡常数和温度的关系如下:回答下列问题:(1)该反应的平衡常数表达式K= ,△H 0(填“<”“ >”“ =”);(2)830℃时,向一个5 L的密闭容器中充入0.20mol的A和的B,如反应初始6s内A的平均反应速率υ(A)= mol·L-1·s-1。
,则6s时c(A)= mol·L-1, C的物质的量为 mol;若反应经一段时间后,达到平衡时A的转化率为,如果这时向该密闭容器中再充入1 mol氩气,平衡时A的转化率为;(3)判断该反应是否达到平衡的依据为 (填正确选项前的字母):a.压强不随时间改变 b.气体的密度不随时间改变c. c(A)不随时间改变 d.单位时间里生成C和D的物质的量相等(4)1200℃时反应C(g)+D(g)A(g)+B(g)的平衡常数的值为。



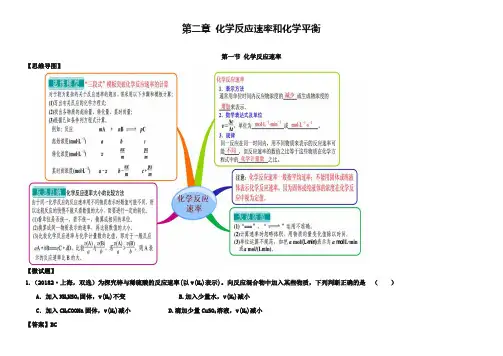
第二章化学反应速率和化学平衡第一节化学反应速率【思维导图】【微试题】1.(20182·上海,双选)为探究锌与稀硫酸的反应速率(以v(H2)表示)。
向反应混合物中加入某些物质,下列判断正确的是()A.加入NH4HSO4固体,v(H2)不变 B.加入少量水,v(H2)减小C.加入CH3COONa固体,v(H2)减小 D.滴加少量CuSO4溶液,v(H2)减小【答案】BC2.(2018海南,双选)对于可逆反应H2(g)+I2(g)2HI(g),在温度一定下由H2(g)和I2(g)开始反应,下列说法正确的是()A. H2(g)的消耗速率与HI(g)的生成速率之比为2:1B. 反应进行的净速率是正、逆反应速率之差C. 正、逆反应速率的比值是恒定的D. 达到平衡时,正、逆反应速率相等【答案】BD[:3.(2018·福建卷)一定条件下,溶液的酸碱性对TiO2光催化染料R降解反应的影响如图所示。
下列判断正确的是( )[:A.在0~50 min之间,pH=2和pH=7时R的降解百分率相等B.溶液酸性越强,R的降解速率越小C.R的起始浓度越小,降解速率越大D.在20~25 min之间,pH=10时R的平均降解速率为0.04 mol·L-1·min-1【答案】D4.臭氧是一种强氧化剂,常用于消毒、灭菌等。
(1)O3与KI溶液反应生成的两种单质是___________和_________。
(填分子式)(2)O3在水中易分解,一定条件下,O3的浓度减少一半所需的时间(t)如题表所示。
已知:O3的起始浓度为0.0216 mol/L。
①pH增大能加速O3分解,表明对O3分解起催化作用的是___________.②在30°C 、pH=4.0条件下,O 3的分解速率为__________ m ol/(L ·min)。
③据表中的递变规律,推测O 3在下列条件下分解速率依次增大的顺序为______.(填字母代号) a. 40°C 、pH=3.0 b. 10°C 、pH=4.0 c. 30°C 、pH=7.0【答案】(1)O 2 I 2 (2)①OH -; ②1.00×10-4 ; ③b 、a 、c 【解析】本题考察化学反应速率的概念、计算、外界条件对反应速率对影响。

人教版化学选修四思维导图化学反应进行的方
向含答案
集团标准化办公室:[VV986T-J682P28-JP266L8-68PNN]
第二章化学反应速率和化学平衡
第四节化学反应进行的方向
【思维导图】
【微试题】
1.(2010·杭州第一次质量检测)下列说法中正确的是( )
A.凡是放热反应都是能自发进行的反应,而吸热反应都是非自发进行的反应
B.自发反应一定是熵增大的反应,非自发反应一定是熵减小或不变的反应
C.熵增加且放热的反应一定是自发反应
D.非自发反应在任何条件下都不能发生
【答案】C
2.对于反应:4Fe(O H)
2(s)+2H
2
O(l)+O
2
(g)===4Fe(OH)
3
(s) ΔH=-444.3kJ·mol-1,且熵减小,在常温常压下该反应能自发进行,对该反应的
方向起决定作用的是()
A.焓变B.温度C.压强D.熵变
【答案】A
3.高温下,某反应达平衡,平衡常数K=[c(CO)·c(H2O)]/[c(CO2)·c(H2)],恒容时,温度升高,H2浓度减小,下列说法正确的是(??)?
A.该反应的焓变为正值?
B.恒温恒容下,增大压强,H2浓度一定减小
C.升高温度,逆反应速率减小?
D.该反应的化学方程式为CO+H2O CO2+H2
【答案】A
4.(2012·海南高考·15)已知A(g)+B(g)C(g)+D(g)反应的平衡常数和温度的关系如下:
温度/℃70080083010001200
平衡常数 1.7 1.1 1.00.60.4
回答下列问题:
(1)该反应的平衡常数表达式K=,△H0(填“<”“>”“=”);
(2)830℃时,向一个5 L的密闭容器中充入0.20m ol的A和0.80mol的B,如反应初始6s内A的平均反应速率υ(A)=0.003mol·L-1·s-1。
,则6s时c(A)=mol·L-1,C的物质的量为mol;若反应经一段时间后,达到平衡时A的转化率为,如果这时向该密闭容器中再充入1mol氩气,平衡时A的转化率为;
(3)判断该反应是否达到平衡的依据为(填正确选项前的字母):
a.压强不随时间改变b.气体的密度不随时间改变
c.c(A)不随时间改变d.单位时间里生成C和D的物质的量相等
(4)1200℃时反应C(g)+D(g)A(g)+B(g)的平衡常数的值为。
【答案】(1)
(C)(D)
(A)(B)
⋅
⋅
c c
c c<(2)0.0220.0980%80%
(3)c(4)2.5
【解析】(1)因反应中的物质都是气体,据平衡常数的定义可知其K=
(C)(D)
(A)(B)
⋅
⋅
c c
c c;由表中数据可知,温度升高,K值减小,故正反应为放热反应,Δ
H<0。
(2)υ(A)=0.003mol ·L -1·s -1,则A 减少的浓度Δc(A)=υ(A)·t=0.018mol ·L -1,故剩余的A 的浓度为0.2mol/5L-0.018mol ·L-1=0.022mol ·L -1;A 减少的物质的量为0.018mol ·L -1×5L=0.09mol ,根据方程式的计量数关系,生成的C 的物质的量也为0.09mol 。
设830℃达平衡时,转化的A 的浓度为x ,则:
A(g)+B(g)C(g)+D(g)
起始浓度(mol ·L -1)0.040.16 0 0
转化浓度(mol ·L -1)x x x x
平衡浓度(mol ·L -1
)0.04-x 0.16-x x x 有:(0.04)(0.16)⋅-⋅-x x x x =1,解得x=0.032,故A 的转化率α(A)=-1
-10.032mol L 0.04mol L ⋅⋅×100%=80%;由于容器的体积是固定的,通入氩气后各组分的浓度不变,反应速率不改变,平衡不移动。
(3)由于该反应是气体分子数不变的反应,容器中压强、气体的密度都永远不变,故a 、b 错;c(A)随反应的进行要减小,故c 可以;不论是否达平衡,单位时间里生成C 和D 的物质的量永远相等,故d 错。
(4)反应“C(g)+D(g)
A(g)+B(g)”与“A(g)+B(g)C(g)+D(g)”互为逆反应,平衡常数互为倒数关系,故1200℃时,C(g)+D(g)A(g)+B(g)的K=1
0.4=2.5。