人表皮生长因子的纯化及浓度在线检测
- 格式:pdf
- 大小:399.14 KB
- 文档页数:7

用Elisa试剂盒检测人血清血浆中VEGF血管内皮生长因子的浓度引言VEGF (Vascular Endothelial Growth Factor,血管内皮生长因子) 是一种重要的血管生成调节因子,在多种生理和病理状态下发挥着重要的作用。
测定血清血浆中VEGF的浓度可以为许多疾病的诊断和治疗提供有价值的参考依据。
本文将介绍如何使用Elisa试剂盒来定量检测人血清血浆中VEGF的浓度。
实验准备材料1.试剂盒:Elisa试剂盒 (VEGF检测)2.样本:人血清血浆样本3.校准曲线标准品:不同浓度的VEGF标准品仪器和设备1.Elisa酶标仪2.微量移液器和相应的移液枪尖3.微量离心机实验步骤1.将试剂盒中的标准品取出并溶解。
2.准备一系列不同浓度的标准品,包括0 pg/mL,10 pg/mL,20pg/mL,50 pg/mL,100 pg/mL,200 pg/mL和400 pg/mL。
标准品的浓度根据试剂盒的说明书进行稀释。
3.将标准品和待测样本加入已涂有VEGF抗体的微孔板中。
4.混合孔板中的标准品和样本,并在37°C的恒温孵育箱中孵育一段时间。
5.将孵育后的孔板倒置,用洗涤缓冲液洗涤孔板,去除未结合的物质。
6.加入带有酶标记的VEGF抗体,并在37°C的恒温孵育箱中孵育一段时间。
7.再次倒置孔板并洗涤,去除未结合的物质。
8.加入底物溶液,并在室温下孵育一段时间。
9.加入停止液,停止反应。
10.使用Elisa酶标仪测量各孔的吸光度。
11.利用标准曲线,根据各孔的吸光度读数来计算出样本中VEGF的浓度。
数据分析根据测得的吸光度读数,通过标准曲线可以计算出待测样本中VEGF的浓度。
将各样本的浓度数据进行统计分析,计算出平均值和标准差,以及样本之间的相关性。
通过使用Elisa试剂盒,我们可以方便、快速地检测人血清血浆中VEGF的浓度。
这对于疾病的诊断和治疗提供了有价值的参考依据,同时也为相关生物学研究提供了重要的数据支持。

人表皮生长因子工艺
人表皮生长因子工艺是一种生物技术,用于生产人表皮生长因子(EGF)。
EGF是一种蛋白质,它在人体中起着重要的生理作用,如促进细胞增殖和修复受损组织。
因此,EGF被广泛应用于医药、化妆品和生物技术等领域。
人表皮生长因子工艺的主要步骤包括:菌种培养、发酵、纯化和结晶。
首先,选择适合生产EGF的菌株,如大肠杆菌或酵母菌等。
然后,将菌株接种到培养基中,提供充足的营养物质和适宜的环境条件,促进菌株生长和繁殖。
接下来,将菌株转移到发酵罐中,进行大规模发酵。
在发酵过程中,EGF被合成并分泌到培养液中。
随着发酵的进行,EGF的浓度逐渐增加,直到达到最高峰。
此时,将培养液进行离心分离,分离出EGF。
最后,通过多种纯化技术,如离子交换层析、凝胶过滤层析和亲和层析等,将EGF纯化并结晶,得到高纯度的EGF。
人表皮生长因子工艺的优点在于,可以大规模生产高纯度的EGF,满足医药和化妆品等领域的需求。
此外,该工艺还可以通过改变菌株和培养条件等因素,调节EGF的产量和质量,提高生产效率和产品质量。
人表皮生长因子工艺是一种重要的生物技术,可以生产高纯度的EGF,为医药和化妆品等领域提供优质的原料。
随着技术的不断发展和完善,相信人表皮生长因子工艺将会得到更广泛的应用和推广。

重组人表皮生长因子体外生物活性的测定
何海琼;李黄金
【期刊名称】《广东医学》
【年(卷),期】1998(019)005
【摘要】探讨适合本实验室用MTT或MTS/PMS检测重组人表皮生长因子的一系列实验参数,包括血清肖度,细胞浓度,细胞培养时间和酶解程度。
方法:利用MTT或MTS/PMS结合示仪分别在多种实验条件下对重组人表皮细胞因子进行生物活性检测,同时绘制细胞生长曲线,对细胞生长状态拍照观察。
【总页数】2页(P324-325)
【作者】何海琼;李黄金
【作者单位】中山大学生命科学学院生物系;中山大学生命科学学院生物系
【正文语种】中文
【中图分类】Q516
【相关文献】
1.重组人表皮生长因子对大鼠宫颈鳞状上皮细胞体外增殖的影响 [J], 张琳;杨静;张晶;詹春
2.重组人表皮生长因子对大鼠宫颈鳞状上皮细胞体外增殖的影响 [J], 张琳;杨静
3.重组人表皮生长因子复方抗菌凝胶生物活性检测方法的建立 [J], 吴培诚;吴园园;潘德顺;卢安根
4.重组人表皮生长因子对体外培养人角质细胞增殖的影响 [J], 郭文平;赵阳;卢小梅;张亚楼;阿孜古丽
5.重组人表皮生长因子生物活性国家标准品的研制 [J], 刘兰;饶春明;丁有学;郭莹;田登安;王军志
因版权原因,仅展示原文概要,查看原文内容请购买。


人表皮生长因子工艺
人表皮生长因子是一种生长因子,它可以促进人的表皮细胞增生和修复,是一种非常有价值的生物制剂。
下面将介绍人表皮生长因子的工艺流程。
一、种植细胞
1.1 种植原料:采用人的表皮细胞作为种植原料。
可以从人的表皮中取下细胞,然后经过培养和筛选,选择性地获得具有较强增殖能力的高质量细胞。
1.2 细胞培养:将选择后的细胞培养在培养基中,将其细胞密度控制在一定范围内,进行细胞增殖、育种和筛选。
在培养过程中,需要注意细胞的微环境,如温度、氧气浓度、营养物质浓度等,以保证细胞具有良好的生长条件。
1.3 细胞扩增:通过细胞培养,可将种植原料扩增成数百万倍,以满足后续的生产需要。
二、生产人表皮生长因子
2.1 细胞刺激:将细胞接种到生长因子培养基中,通过给细胞提供一定的激素和营养物质,刺激其生长,产生人表皮生长因子。
2.2 增殖和筛选:在细胞刺激的过程中,选择具有较高产量的细胞株进
行扩增,同时筛选出人表皮生长因子。
2.3 粗提和纯化:将生产出的人表皮生长因子进行粗提和纯化处理,以
去除杂质和其他细胞成分,得到高纯度的人表皮生长因子。
三、应用人表皮生长因子
人表皮生长因子可用于治疗和预防人体表皮缺损,促进表皮细胞增生
和修复。
常见的应用包括:
3.1 伤口愈合:人表皮生长因子可促进伤口愈合,促进细胞增殖和再生。
3.2 美容修复:人表皮生长因子可用于美容修复,促进皮肤细胞新陈代谢,改善皮肤质量和光泽。
3.3 治疗皮肤病:人表皮生长因子可用于治疗各种皮肤病,如白斑、皮
肤溃疡等。
以上就是人表皮生长因子的工艺流程及应用介绍。

重组人表皮生长因子(rhEGF)品牌:Robustnique®INCI:Rh-Oligopeptide-1 (Human oligopeptide-1)CAS No.:62253-63-8别名:表皮生长因子,表皮细胞生长因子,rh-EGF,EGF概述:重组人类表皮生长因子(rhEGF),是一个含53个氨基酸残基的多肽,大小为6.2 kDa,有三个二硫键。
EGF分布在多种组织和体液中。
EGF对伤口愈合和器官形成有重要作用。
它能刺激各种表皮和上皮细胞增殖,分化和生存;促进角质形成细胞的生长和迁移,以及促进成纤维细胞和胚胎细胞的增殖。
此外,人表皮生长因子与β-尿抑胃素(β-urogastrone)为同一物质,能够抑制胃酸的分泌。
机制:EGF可以高亲和力的与细胞表面的表皮生长因子受体(EGFR)结合,从而激活受体的蛋白酪氨酸激酶活性。
酪氨酸激酶的激活可以启动信号转导级联反应,从而引起细胞内各种生化改变(细胞内钙水平升高,糖酵解和蛋白质的合成,以及某些基因的表达,如EGFR基因增加)并最终导致DNA合成和细胞增殖。
规格:产品重组人表皮生长因子(原液)货号E0021包装100 mL (可定制)性状无色液体浓度 1 mg/mL成分纯化后蛋白溶于10mM磷酸盐缓冲液(pH 6.8)氨基酸序列NSDSECPLSHDGYCLHDGVCMYIEALDKYACNCVVGYIGERCQYRDLKWWELR分子量 6.2 kDa纯度≥ 95% (SDS-PAGE和HPLC)活性 1 × 106 IU/mg (Balb/c 3T3细胞增殖法检测)无菌处理0.22 μm滤膜过滤内毒素≤ 0.5 EU/μg来源大肠杆菌(E. coli)表达的重组蛋白存储-80°C/-20°C保质期36个月(-80°C); 24 个月(-20°C)产地中华人民共和国运输条件干冰运输产品重组人表皮生长因子(冻干粉)货号E0022,E0023包装60 μg,1 mg (可定制)性状白色冻干粉赋形剂磷酸氢二钠/磷酸二氢钠和5%甘露醇氨基酸序列NSDSECPLSHDGYCLHDGVCMYIEALDKYACNCVVGYIGERCQYRDLKWWELR分子量 6.2 kDa纯度≥ 95% (SDS-PAGE 和HPLC)活性 1 × 106 IU/mg (Balb/c 3T3 细胞的增殖法)无菌处理0.22 μm滤膜过滤内毒素≤ 0.5 EU/μg来源大肠杆菌(E. coli)表达的重组蛋白存储室温(25°C)保质期24个月(室温,25°C)复溶无菌去离子水,置于低温状态防止微生物污染产地中华人民共和国运输常温运输高效液相色谱检测(HPLC):重组人表皮生长因子的纯度经反相高效液相色谱(RP-HPLC)的检测结果如下:生物活性检测:不同浓度重组人表皮生长因子对Balb/c 3T3细胞的促增殖能力评估结果如下图所示,对照样品为EGF活性的国际标准品(购自NIBSC,代号91/530,活性1 × 106 IU/mg)。


重组人表皮生长因子iii型
表皮生长因子III型(Epidermal Growth Factor III, EGF III)是一种蛋白质,它与细胞生长、分化和组织修复等生物学过程密切相关。
在一些情况下,可能存在对表皮生长因子III型的基因工程或蛋白重组的研究。
重组表皮生长因子III型通常是通过基因工程技术来制备的,包括以下步骤:
1.基因克隆:从源生物体(通常是人体细胞)中提取表
皮生长因子III型基因,并进行克隆。
这个基因编码了表皮生长
因子III型的氨基酸序列。
2.表达载体构建:将表皮生长因子III型基因插入表达载
体中,以便在宿主细胞中进行表达。
这个表达载体通常包含有
助于基因表达的调控元件,如启动子、激活子等。
3.细胞转染:将构建好的表达载体导入宿主细胞中,通
常采用细胞转染技术,使细胞能够表达表皮生长因子III型基因。
4.蛋白表达:在宿主细胞内,表皮生长因子III型基因被
转录和翻译成蛋白质,即重组表皮生长因子III型。
5.纯化与验证:通过蛋白质纯化技术,将重组表皮生长
因子III型从细胞提取物中纯化出来。
然后通过各种实验手段验
证其结构和功能的一致性。
这样得到的重组表皮生长因子III型可以用于科研、医药研发等领域。
在医学上,表皮生长因子III型可能用于促进伤口愈合、治疗皮肤疾病等。
需要注意的是,这些研究和应用必须符合伦理规范和法规。
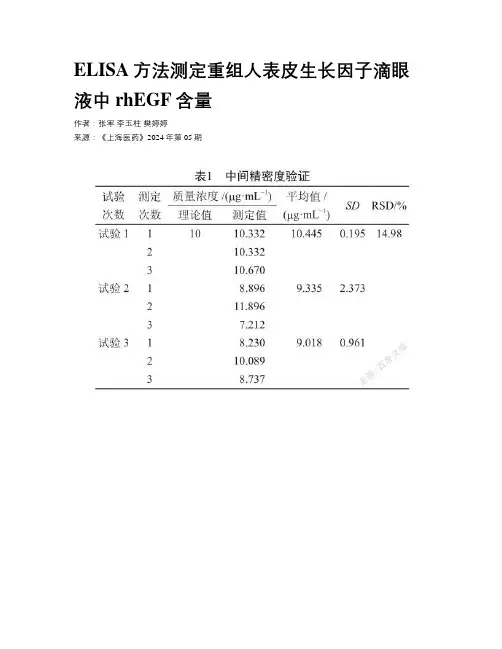
ELISA方法测定重组人表皮生长因子滴眼液中rhEGF含量作者:张军李玉柱樊婷婷来源:《上海医药》2024年第05期摘要目的:建立重组人表皮生长因子(rhEGF)滴眼液中rhEGF含量的检测方法,并进行方法学验证。
方法:应用商品化试剂盒Quantikine ELISA,采用酶联免疫定量测定技术(ELISA)测定样品中的rhEGF含量。
结果:标准曲线的线性范围为20~200 pg/mL;中间精密度所得相对标准偏差RSD为14.98%(n=9)。
低、中、高3个质量浓度的平均回收率分别为94.08%、100.46%、104.89%,相对标准偏差分别为11.03%、9.85%、8.75%(n=3),重复检测10次的相对标准偏差为5.58%。
结论:该研究建立的ELISA方法专属性强,精密度、准确度、稳定性均良好,适用于重组人表皮生长因子滴眼液中rhEGF含量的检测。
关键词重组人表皮生长因子 ELISA 滴眼液中图分类号:R927.2; R988.1 文献标志码:A 文章编号:1006-1533(2024)05-0077-04引用本文张军,李玉柱,樊婷婷. ELISA方法测定重组人表皮生长因子滴眼液中rhEGF 含量[J]. 上海医药, 2024, 45(5): 77-80.Determination of recombinant human epidermal growth factor ( rhEGF) content in rhEGF eye drops by ELISAZHANG Jun1, LI Yuzhu2, FAN Tingting1,2(1. Shanghai Haohai Biotechnology Co., Ltd., Shanghai 201613, China; 2. Shanghai Li Kang Rui Biological Engineering Co., Ltd., Shanghai 201707, China)ABSTRACT Objective: To establish a method for the determination of rhEGF content in rhEGF ( recombinant human epidermal growth factor) eye drops and perform method validation. Methods: The content of rhEGF in eye drops was determined using a commercial kit Quantikine by enzyme-linked immuno sorbent assay (ELISA). Results: The linear range of the standard curve was 20-200 pg/mL. The relative standard deviation (RSD) of intermediate precision was 14.98% (n=9). The average recoveries of low, medium, and high concentrations of samples were94.08%, 100.46% and 104.89% with RSD 11.03%, 9.85%, 8.75% (n=3), respectively. The RSD for 10 replicates was 5.58%. Conclusion: The ELISA method established in this study has a good specificity, precision, accuracy and stability, and is suitable for the determination of the content of rhEGF in rhEGF eye drops.KEY WORDS rhEGF; ELISA; eye drop重组人表皮生长因子(recombinant human epidermal growth factor,rhEGF)是由53个氨基酸组成的活性多肽,具有广泛的生物學效应,能促进各种表皮组织生长,应用广泛。
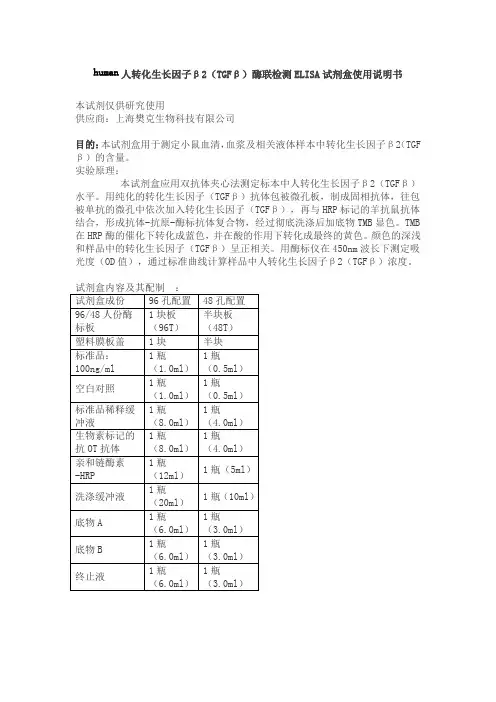
human人转化生长因子β2(TGFβ)酶联检测ELISA试剂盒使用说明书本试剂仅供研究使用供应商:上海樊克生物科技有限公司目的:本试剂盒用于测定小鼠血清,血浆及相关液体样本中转化生长因子β2(TGF β)的含量。
实验原理:本试剂盒应用双抗体夹心法测定标本中人转化生长因子β2(TGFβ)水平。
用纯化的转化生长因子(TGFβ)抗体包被微孔板,制成固相抗体,往包被单抗的微孔中依次加入转化生长因子(TGFβ),再与HRP标记的羊抗鼠抗体结合,形成抗体-抗原-酶标抗体复合物,经过彻底洗涤后加底物TMB显色。
TMB 在HRP酶的催化下转化成蓝色,并在酸的作用下转化成最终的黄色。
颜色的深浅和样品中的转化生长因子(TGFβ)呈正相关。
用酶标仪在450nm波长下测定吸光度(OD值),通过标准曲线计算样品中人转化生长因子β2(TGFβ)浓度。
试剂盒内容及其配制:试剂盒成份96孔配置48孔配置96/48人份酶标板1块板(96T)半块板(48T)塑料膜板盖1块半块标准品:100ng/ml 1瓶(1.0ml)1瓶(0.5ml)空白对照1瓶(1.0ml)1瓶(0.5ml)标准品稀释缓冲液1瓶(8.0ml)1瓶(4.0ml)生物素标记的抗OT抗体1瓶(8.0ml)1瓶(4.0ml)亲和链酶素-HRP 1瓶(12ml)1瓶(5ml)洗涤缓冲液1瓶(20ml)1瓶(10ml)底物A 1瓶(6.0ml)1瓶(3.0ml)底物B 1瓶(6.0ml)1瓶(3.0ml)终止液1瓶(6.0ml)1瓶(3.0ml)试剂盒组成:试剂盒组成48孔配置96孔配置保存说明书1份1份封板膜2片(48)2片(96)密封袋1个1个酶标包被板1×48 1×96 2-8℃保存标准品:45μmol/L0.5ml×1瓶0.5ml×1瓶2-8℃保存标准品稀释液 1.5ml×1瓶 1.5ml×1瓶2-8℃保存酶标试剂 3 ml×1瓶 6 ml×1瓶2-8℃保存样品稀释液 3 ml×1瓶 6 ml×1瓶2-8℃保存显色剂A液 3 ml×1瓶 6 ml×1瓶2-8℃保存显色剂B液 3 ml×1瓶 6 ml×1瓶2-8℃保存终止液3ml×1瓶6ml×1瓶2-8℃保存浓缩洗涤液(20ml×20倍)×1瓶(20ml×30倍)×1瓶2-8℃保存自备材料:1. 蒸馏水。
人表皮生长因子(EGF)ELISA试剂盒分析检测说明书樊克生物专业供应本试剂盒仅供研究使用。
检测范围:48T 25 ng/L -800 ng/L使用目的:本试剂盒用于测定人血清、血浆及相关液体样本表皮生长因子(EGF)含量。
实验原理本试剂盒应用双抗体夹心法测定标本中人表皮生长因子(EGF)水平。
用纯化的人表皮生长因子(EGF)抗体包被微孔板,制成固相抗体,往包被单抗的微孔中依次加入表皮生长因子(EGF),再与HRP标记的表皮生长因子(EGF)抗体结合,形成抗体-抗原-酶标抗体复合物,经过彻底洗涤后加底物TMB显色。
TMB在HRP 酶的催化下转化成蓝色,并在酸的作用下转化成最终的黄色。
颜色的深浅和样品中的表皮生长因子(EGF)呈正相关。
用酶标仪在450nm波长下测定吸光度(OD 值),通过标准曲线计算样品中人表皮生长因子(EGF)浓度。
试剂盒组成1 20倍浓缩洗涤液20ml×1瓶7 终止液3ml×1瓶2 酶标试剂3ml×1瓶 8 标准品(1600ng/L)0.5ml×1瓶3 酶标包被板12孔×4条9 标准品稀释液1.5ml×1瓶4 样品稀释液3ml×1瓶 10 说明书1份5 显色剂A液3ml×1瓶 11 封板膜2张6 显色剂B液3ml×1/瓶12 密封袋1个标本要求1.标本采集后尽早进行提取,提取按相关文献进行,提取后应尽快进行实验。
若不能马上进行试验,可将标本放于-20℃保存,但应避免反复冻融2.不能检测含NaN3的样品,因NaN3抑制辣根过氧化物酶的(HRP)活性。
操作步骤1. 标准品的稀释:本试剂盒提供原倍标准品一支,用户可按照下列图表在小试管中进行稀释。
800 ng/L 5号标准品150μl的原倍标准品加入150μl标准品稀释液400 ng/L 4号标准品150μl的5号标准品加入150μl标准品稀释液200 ng/L l 3号标准品 150μl的4号标准品加入150μl标准品稀释液100 ng/L 2号标准品150μl的3号标准品加入150μl标准品稀释液50 ng/L 1号标准品150μl的2号标准品加入150μl标准品稀释液2. 加样:分别设空白孔(空白对照孔不加样品及酶标试剂,其余各步操作相同)、标准孔、待测样品孔。
基因工程人表皮生长因子的分离纯化及其浓度的在线检测童望宇;姚善泾;关怡新;朱自强【期刊名称】《分析测试学报》【年(卷),期】2004(23)6【摘要】在分离纯化快速开拓系统(AKTA explorer 100)中用凝胶(Sephadex G-50 superfine)纯化人表皮生长因子,并在优化的条件下对人表皮生长因子(hEGF)进行定量测定.与经离子交换柱、SDS-PAGE及凝胶图象扫描分析系统的人表皮生长因子标准品间相互印证.结果表明在优化条件下,在SDS-PAGE上可得到与标准样品hEGF一样清晰的单条带,其产品纯度高于94%,检出限可达1μg/mL.该法不仅对人表皮生长因子的在线检测行之有效,而且对其它蛋白质分离的在线检测也具有参考价值.【总页数】4页(P22-24,28)【作者】童望宇;姚善泾;关怡新;朱自强【作者单位】浙江大学,化学工程与生物工程学系,浙江,杭州,310027;浙江大学,化学工程与生物工程学系,浙江,杭州,310027;浙江大学,化学工程与生物工程学系,浙江,杭州,310027;浙江大学,化学工程与生物工程学系,浙江,杭州,310027【正文语种】中文【中图分类】Q503;TQ033【相关文献】1.以蓝藻为载体重组人表皮生长因子的分离纯化研究 [J], 刘凯2.基质辅助激光解吸飞行时间质谱及毛细管电泳对基因工程产品—重组人表皮生长因子的质量控制研究 [J], 蔡耘3.人表皮生长因子(h—EGF)RIA及国产基因工程制备的h—EGF抗血清的鉴定[J], 陆国钧;黄秉仁4.基因工程人表皮生长因子(rhEGF)单克隆抗体的制备与初步鉴定 [J], 邹岳奇;辛春艳;刘玉翠;陈英珠;籍宝霞5.应用RP-HPLC分析基因工程人表皮生长因子肽谱 [J], 张翊;饶春明;丁锡申因版权原因,仅展示原文概要,查看原文内容请购买。
表皮生长因子受体检测方法
姜晓丹; 侯庆华; 黄来珍
【期刊名称】《《医学信息》》
【年(卷),期】2010(023)005
【摘要】表皮生长因子受体(EGFK)是一种受体型酪氨酸激醇。
在多种肿瘤中都有过表达,并与肿瘤的发生、浸润、转移、预后度患者生存期密切相关。
多种方法可用于检测组织、血液、细胞中EGFR蛋白表达及其酪氨酸激酶活性。
EGFR的检测将有助于肿瘤的靶向治疗。
【总页数】3页(P1515-1517)
【作者】姜晓丹; 侯庆华; 黄来珍
【作者单位】广东海洋大学海洋药物实验室广东湛江 524025
【正文语种】中文
【相关文献】
1.表皮生长因子受体基因突变检测方法及质量评价 [J], 黄杰;高尚先
2.血清人表皮生长因子受体2的临床检测价值与检测方法研究进展 [J], 王璐;沈国栋;胡世莲
3.表皮生长因子受体分子标记物及其检测方法在非小细胞肺癌患者表皮生长因子受体酪氨酸激酶抑制剂疗效预测中的研究进展 [J], 梁乃新;杨华夏;李单青
4.胶质瘤表皮生长因子受体基因突变检测方法的对比研究 [J], 王敏;李兴涛
5.浸润性乳腺癌组织中人表皮生长因子受体2表达的检测方法比较 [J], 李忻;张韫;杨鑫;王也;笪冀平;黄林平;杨猛
因版权原因,仅展示原文概要,查看原文内容请购买。
HPLC在线二阶微分光谱法检测人表皮生长因子的C-端肽张丽华;屠红旻;吴高德;徐来根;夏其昌
【期刊名称】《高技术通讯》
【年(卷),期】1995(005)005
【摘要】Trp(色氨酸)与Tyr(酪氮酸)二阶微分光谱能被用来在线检测RP-HPLC(反相高效液相色谱)中含芳香族氨基酸的肽段,这些特征光谱是通过二极管矩阵检测器(DAD)得到的,用这种方法分析人表皮生长因子(hEGF)的胰蛋白酶酶解图谱,能鉴别出含Trp的C-端肽.
【总页数】4页(P7-10)
【作者】张丽华;屠红旻;吴高德;徐来根;夏其昌
【作者单位】中国科学院上海生物化学研究所,上诲,200031;中国科学院上海生物化学研究所,上诲,200031;中国科学院上海生物化学研究所,上诲,200031;中国科学院上海生物化学研究所,上诲,200031;中国科学院上海生物化学研究所,上
诲,200031
【正文语种】中文
【相关文献】
1.二阶微分火焰光谱法在痕量钠测定中的应用 [J], 钟云泰
2.分子改进后人绒毛膜促性腺激素β链C-末端肽免疫活性的初步观察 [J],
3.二阶微分火焰光谱法与pNa法测量水汽中痕量钠优略性比较 [J], 黄毅婷
4.二阶微分火焰发射光谱法在锅炉蒸汽
钠离子含量测定中的应用 [J], 祁福平;党红娟
5.血清试验检测骨质疏松患者血清Ⅰ型胶原C-末端交联端肽的评价 [J], 杜国有因版权原因,仅展示原文概要,查看原文内容请购买。
人表皮生长因子的纯化及浓度在线检测童望宇1, * , 姚善泾2, *, 朱自强2(1上海市华东理工大学生物反应器工程国家重点实验室 上海市 200237;2浙江省杭州市浙江大学化学工程与生物工程系,杭州 310027)摘要 在分离纯化快速开拓系统(ÄKTA explorer 100)中用凝胶(Sephadex G-50 superfine )纯化人表皮生长因子,并在优化条件下对其纯化过程中的hEGF 进行定量测定。
用标准人表皮生长因子经离子交换柱、蛋白质扫描分析系统及SDS-PAGE 间相互印证,结果表明:在优化条件下,可得到在SDS-PAGE 上与标准样品hEGF 一样清晰的单条带,其产品纯度高于94%,回收率高于36%;其检测的灵敏度可达1μg/ml 。
该法不仅对人表皮生长因子的在线检测行之有效,而且对其它蛋白质纯化的在线检测也具有参考价值。
关键词 人表皮生长因子,层析,检测,纯化中图分类号 TQ0333 Q819引言人表皮生长因子(human epidermal growth factor ,hEGF )是由53个氨基酸残基所组成的多肽生长因子,分子量约为6200D [1]。
人表皮生长因子具有在体内刺激皮肤组织、角膜、肺、气管上皮组织的生长繁殖及抑制胃酸分泌等多种生物学作用,因而可应用于外科伤口的愈合及溃疡病的治疗等医疗领域[2-5]。
自1975年Cohen 等人[1]从尿液中首先分离纯化得到人表皮生长因子以来,有关研究的进展很快,除了继续研究从天然来源中分离纯化以外,基于基因工程菌发酵生产也已问世[6-7],但是不管是从天然资源,还是来自基因工程菌发酵液,hEGF 的浓度总是偏低,需要经过较长时间的分离和纯化流程,才能得到相对较纯的产品。
为了设计一个高效和可控的纯化过程,hEGF 的在线分析和检测就成为非常重要。
目前,hEGF 的定量检测方法主要有放射免疫分析(Radio immuno-assay, RIA )[4]、放射受体分析(Radio receptor assay, RRA) [8]、酶联免疫吸附分析(Enzyme-linked immunosorbent assay, ELISA )[9]、酶免疫分析(Enzyme immunoassay, EIA )[10]、反相HPLC [11]和免疫荧光技术[12]等。
以上各种方法均有其特点和不同的条件局限性,但均难用于过程的在线检测。
我们在使用ÄKTA explorer 100进行蛋白质纯化时发现,该系统通过本身带有的软件,不仅可以与各种层析柱结合进行多种生物质的分离流程研究,而且还可以比较精确地通过出峰面积表示蛋白质量的多少。
利用这种定量关系,就为定量确定生物质含量提供了基础。
以此为依据,对hEGF 这个比较难于定量与分离的多肽,进行了凝胶层析中在线检测与纯化工艺的优化,达到了纯化与在线定量检测的目的。
1 材料与方法1.1 仪器与试剂联系人:童望宇,姚善泾, E-mail: tongwy@ , yaosj@第一作者:童望宇,男,40岁,博士* 国家自然科学基金资助项目(批准号:29736180)_______________________________________________________________________________分离纯化快速开拓系统(ÄKTA explorer 100)、进样柱(Superloop TM 50)、层析柱(XK 16/20)、离子交换预装柱(RESOURCE Q6)、凝胶(Sephadex G-50 superfine)、蛋白质扫描分析系统(Image Master VDS Video Documentation System)购自Amersham Pharmacia Biotech AB. Sweden;电泳仪(Mini VE complete)购自Amersham Pharmacia Biotech Inc., USA;hEGF 标准品购自Pepro Tech EC Ltd, England。
其它试剂均为市售的分析纯试剂。
平衡液:pH 7.0,0.02M的磷酸缓冲液(PBS);洗脱液:pH7.0 PBS+2 M NaCl的磷酸盐缓冲液。
1.2 样品的预处理将含有hEGF的发酵液[13]经冷冻离心机进行离心(8000rpm,10min, 4 0C),收集上清液,取该上清液1000 ml,用1M浓度的盐酸小心调发酵液的pH于4.6左右,缓慢加入210 g硫酸铵(硫酸铵饱和度为:35%),搅拌溶解,4 0C下静置4~24小时,至沉淀彻底,人表皮生长因子进入沉淀中。
虹吸去除700~850 ml上清液,剩余的150~300 ml于4 0C条件下8000 rpm、20 min离心,收集沉淀。
用100 ml 平衡液搅拌溶解沉淀,形成悬浊液,4 0C下静置4~24小时,待溶解充分后,于4 0C下8000 rpm、20 min离心,收集上清液,于4 0C 下保存备用。
1.3 hEGF的定性分析hEGF的定性分析用SDS-PAGE电泳[14]。
1.4 hEGF的定量分析1.4.1 实验原理在蛋白质及多肽分子中,酪氨酸、色氨酸及苯丙氨酸等芳香氨基酸的苯环含有共轭双键,因而具有吸收紫外线的性质,吸收高峰在280nm波长处。
在此波长范围内,蛋白质溶液的光吸收值(A280)与其含量呈正比例关系(m =f ×A,式中m为蛋白质的含量,f 为比例系数,A为峰面积),由此可用作总蛋白质及被纯化蛋白质的定量测定。
1.4.2 实验设计对待测浓度的目标蛋白,可先用标准样品在相同层析条件下确定其保留值,再用其它方法给予验证,为定量分析提供基础。
不同样品的组成各不相同,实验中应尽可能优化层析条件,扩大目标产物与其它组成的保留值差距以提高检测的准确性。
由于ÄKTA explorer 100能够提供相应正确的峰面积与蛋白质定量关系,因此在hEGF的纯化中,将其与凝胶柱结合,并在优化条件下,进行hEGF的纯化与在线检测,然后再配以SDS-PAGE及蛋白质扫描分析系统的进一步印证。
使得分析的可信度大为提高。
2 结果与讨论2.1 hEGF标准曲线的制定为考察ÄKTA explorer 100紫外检测仪的灵敏度及紫外吸收峰面积与蛋白质浓度的关系。
实验选用了RESOURCE Q6强阴离子预装柱,用Unicorn3.0所推荐的模板[15]经空柱(bypass)流程对多种标准蛋白质进行了多浓度水平反复验证,并用牛血清白蛋白标准品共进行了5次μg/ml级重复测定,其标准偏差为0.9948。
在此基础上,采用了浓度为2μg/ml hEGF 的标准hEGF,分别用1.0、2.0、4.0、6.0、8.0和10.0ml的体积进样,测试其峰面积与进样量的关系,结果如图1、2所示。
A r e a (m A U ×m l )Standard hEGF (μg)图 1 标准hEGF 层析图 图 2 hEGF 标准曲线Figure 1 Chromatographic profile of standatrd hEGF Figure 2 Plot of peak area vs standard hEGF由图1可见:随着进样量的增加,出峰明显变宽,峰面积增加,其峰面积的具体数据由ÄKTA explorer 100自动给出,由此作成了由图2所示的峰面积与样品含量关系图,作为标准曲线。
其关系可由下述方程给出:4127.00971.2−=C A (1)式中A 表示峰面积(mAU*ml ),C 表示hEGF 含量(μg )。
该方程的方差R 2为0.9995,表明标准hEGF 样品的峰面积与样品含量呈良好的线性关系。
2.2 人表皮生长因子标准曲线的延伸为进一步检测样品中较高浓度的hEGF 与峰面积的关系,扩大上述方程的使用范围,我们加大了被测样品的量,这里采用了我们自己纯化的hEGF (简称纯化hEGF )样品,使图2的标准曲线得以延伸,结果如图3所示。
A r e a (m A U ×m l )Purified hEGF (μg)图 3 纯化的hEGF 曲线Figure 3 Plot of peak area vs purified hEGF图3结果表明,在hEGF 的浓度放大了10倍以后,hEGF 含量与峰面积的曲线不仅保持了良好的线性关系,而且还很好地与图2相连接。
这种良好的线性就可为在较广的浓度范围内实现在线检测hEGF 提供依据。
相应的回归方程是:6989.10916.2−=C A(2)用上述方程回归,其方差R 2为0.9997,说明hEGF 样品的峰面积与样品含量呈良好的线性关系。
但值得注意的是,方程(2)中的系数与方程(1)的系数稍有差别,主要体现在方程的截距上,也就是说,用方程(2)计算低浓度时,误差会稍大些。
但是用方程(1)外推到浓度较高时,精确度就相对较高。
2.3 人表皮生长因子的纯化及浓度在线检测在实验中,我们发现发酵液中目标产物hEGF的分子量(~6200D)与其它蛋白质的最小分子量(~18000D)相距约10000D以上,故用凝胶Sephadex G-50 superfine进行hEGF的纯化。
优化后的纯化条件为:柱床高度=16 cm,线性流速=6 cm/h,进样量=1 ml。
此条件下的层析结果如图4所示。
图 4 样品纯化过程中的Sephadex G-50凝胶层析图Figure 4 Gel chromatographic profile of the supernatant being purified从图4可见,在两个大峰群中间所夹的一个小峰,其保留体积与我们在相同条件下所测到的标准hEGF样品的保留体积相一致,再用SDS-PAGE分析后,确认该小峰就是hEGF 峰。
与其它杂质峰基本分离。
经ÄKTA explorer 100检测,1 ml样品中总峰面积为11996 mAU*ml,hEGF峰面积为327 mAU*ml,计算得hEGF峰面积比值为2.73%,此即该盐析液中hEGF的含量(%)。
由标准曲线回归方程(1)可得,hEGF的绝对含量为156.13 μg,于是其浓度就为156.13 μg/ml;如果用方程(2)计算,绝对含量为157.15 μg,浓度为157.15 μg/ml。
由此可见,两方程的计算结果基本一致。
故标准曲线可从20μg延伸至200μg不会造成很大误差。
2.4 纯化结果验证上述纯化后的收集液经冷冻干燥后,得到了白色的hEGF粉末。
随后我们对该产品用阴离子交换预装柱(RESOURCE Q6)在其推荐操作条件下进行了分析,得到了如图5-A所示的结果,同时也对标准品进行了检测,以作对比之用,结果如图5-B所示。