亲核取代反应 (SN )
- 格式:ppt
- 大小:449.50 KB
- 文档页数:27


有机化学中的亲核取代反应孙金鱼;赵三虎;赵明根【摘要】亲核取代反应是有机化学中的一类非常重要的反应,可分为四种类型:①饱和碳原子上的亲核取代反应(SN1和SN2);②不饱和碳原子(主要是芳环)上的亲核取代反应;③经苯炔中间体的亲核取代反应;④底物为羧酸衍生物(酰卤、酸酐、酯、酰胺)的亲核取代反应。
这些亲核取代反应在有机合成上有着极其广泛的应用,但因反应机理的差异性较大,学生学买并掌握起来困难较大。
文章拟将上述四种类型的亲核取代反应进行系统分析和比较,找出反应的规律性,以期帮助学生学习之需要。
%As a kind of very important organic chemistry reactions, nucleophilic substitution reactions are generally di- vided into four types:①nucleophilic substitution reactions on the saturated carbon atoms(SN1 and SN2);②nucleophilic substitution reactions on the u nsaturated carbon atoms (mainly aromatic ring); ③nucleophilic substitution reactions through such intermediate as benzyne, ④nucleophilic substitution reactions which substrates are carboxylic derivatives (acyl halides, anhydrides, esters, amides). These nucleophilic substitution reactions have an extremely wide range of ap- plications, but due to the differences of reaction mechanisms, we have found it difficult for students to learn and master these reactions. In this paper, we will analyse and compare the four types of nucleophilic substitution reactions systemati- cally and find out their regularities so as to meet the need of students.【期刊名称】《海南师范大学学报(自然科学版)》【年(卷),期】2012(025)001【总页数】7页(P109-114,118)【关键词】有机化学;亲核取代反应;机理【作者】孙金鱼;赵三虎;赵明根【作者单位】忻州师范学院化学系,山西忻州034000;忻州师范学院化学系,山西忻州034000;忻州师范学院化学系,山西忻州034000【正文语种】中文【中图分类】O621.13在有机化学中,亲核取代反应是一种特别重要的反应,按照其反应机理可以归纳为四种类型.即①饱和碳原子上的亲核取代(SN1和SN2);②不饱和碳原子(主要是芳环)上的亲核取代;③经苯炔中间体的亲核取代;④底物为羧酸衍生物(酰卤、酸酐、酯、酰胺)的亲核取代.这些反应本质上都是亲核取代,但由于反应机理的差异性较大,学生学习并掌握起来困难较大.只有从反应机理上彻底认识并掌握各类亲核取代反应,才是解决问题的根本方法.1.1 一般的饱和碳原子上的亲核取代反应这类反应主要涉及卤代烷烃(RX)、醇(ROH)以及饱和碳原子上连有羟基、卤原子等的其他类型的有机物.从反应机理讲,分为SN1和SN2两种极限历程.SN1为单分子亲核取代历程,中间体为碳正离子,整个反应分两步完成,立体化学为外消旋化.SN2为双分子亲核取代历程,经过渡态一步完成,立体化学为瓦尔登(Walden)翻转,即构型翻转.简要表示其通式[1]如下:①SN1的反应通式为:②SN2的反应通式为:在SN1中,反应的快慢取决于离去基团的性质.离去基团的亲核性弱,则易于离去;反之,则不易离去.离去基团的碱性、中心原子的半径大小等影响着它亲核性的强弱.一般来说,碱性弱则亲核性弱,易于离去;中心原子的半径大则变形性大(强),也易于离去.在SN2中,反应的快慢与底物结构、离去基团、亲核试剂的性质有关,有时还与溶剂的极性有关.底物结构简单、试剂的亲核性强,离去基团的碱性弱(即易于离去),都有利于反应的快速进行;反之,反应则不易进行.对于亲核试剂,碱性强则亲核性强;中心原子的半径大则变形性大,亲核性也强.对于离去基团,则与SN1相同.对于那些碱性特别强的离去基团如羟基(-OH)、氨基(-NH2)等,须在酸催化下才能顺利离去,以实现取代.醇分子间脱水成醚的反应属于亲核取代,反应一般按SN2历程进行.例如[2]:Williamson合成法制醚的反应也属于亲核取代,反应一般按SN2历程进行.反应通式为:RX+NaOR′(或NaOAr)→ROR′(或ROAr)因醇钠或酚钠碱性较强而容易引起脱卤化氢的消除反应,反应中所用卤代烃一般要求是一级卤代烃.醚键断裂的反应是重要的亲核取代反应,特别是环氧乙烷衍生物的开环反应更为重要.醚键断裂反应的通式为:反应中氢卤酸的活性顺序为:HI>HBr>HCl.一般用HI进行反应,偶尔用HBr进行反应,几乎不用HCl,因其反应活性差.对于脂肪族混合醚,醚键优先在较小烃基一边断裂(SN2机理)[2].对于含有叔烃基的脂肪族混合醚,醚键优先在叔烃基一边断裂,因这种断裂可生成稳定的叔碳正离子(SN1机理)[3].对于芳基烷基混合醚与HX反应,醚键总是在脂肪族烃基一边断裂,这是因为芳基碳氧键结合得很牢固(p-π共轭).显然,二芳基醚在HI作用下也不会发生断裂反应.环氧乙烷衍生物的开环反应是一种特殊的亲核取代反应.环氧乙烷衍生物因其具有三元环而能与许多含有活泼氢化合物(如水、醇、胺、酚、氢卤酸等)发生反应,可用酸或碱作催化剂.不对称环氧乙烷衍生物的开环反应有一个方向问题.在碱性条件下开环,亲核试剂优先进攻空间位阻较小的环碳原子(SN2机理).而在酸性条件下开环,亲核试剂优先进攻取代程度高的环碳原子(带有SN1机理性质)[4]:从立体化学上讲,酸性开环和碱性开环反应都属于SN2类型的反应[2],如下列两个例子:1.2 特殊的饱和碳原子上的亲核取代反应1.2.1 邻近基团参与的亲核取代反应邻近基团参与的亲核取代反应简称邻基参与.当能够提供电子的基团处于底物中心碳原子的邻近位置时,它们通过某种环状中间体先于亲核试剂参与亲核取代反应,其结果不仅加快了反应速率,而且使产物保持原构型(但有时也会得到重排产物).其反应分两步进行,先发生分子内亲核取代形成环状结构(此时构型已发生翻转),然后亲核试剂沿着离去基团离去路径反方向进攻,发生取代(此时构型再次发生翻转),两次构型翻转(SN2)等于构型不变,即构型保持.反应通式[2]如下:常见的邻近基团有:COO-、O-、S-、OH、OR、NH2、NR2-、SR、Cl、Br、I、以及苯基、烯基等.列举三例如下:例1 (S)-α-溴代丙酸盐的水解反应例2 β-苯基溴代烷的水解反应例3 β-碘代醇的溴化反应1.2.2烯胺为亲核试剂的亲核取代反应烯胺与活泼卤代烃可进行亲核取代反应.五元环酮或六元环酮形成烯胺后可与活泼卤代烃进行亲核取代,在羰基α-位引入烷基(烃基),生成取代环酮.其反应通式[2]如下:R′X=CH2=CHCH2Cl,BrCH2COOC2H5,RCOCl,CH3I,BrCH2COR等1.2.3 丙二酸二乙酯、乙酰乙酸乙酯中活泼亚甲基为亲核试剂的亲核取代反应丙二酸二乙酯、乙酰乙酸乙酯作为特殊的试剂在有机合成上非常有用,可合成众多有机化合物.它们的反应是在强碱作用下形成碳负离子,并作为亲核试剂进行亲核取代反应,从而引入各种不同的基团,再经酮式或酸式分解,可得到不同结构的酮、酸或二酸等.应该特别指出的是,如果引入两个相同的烃基,丙二酸二乙酯可一次完成,而乙酰乙酸乙酯由于无法形成双钠盐,必须分步进行才能完成.1.2.3.1 丙二酸二乙酯在有机合成上具体应用反应通式:其中R1X或R2X=使用二卤代烃还可合成环状产物:1.2.3.2 乙酰乙酸乙酯在有机合成上具体应用反应通式:2.1 苯环上的亲核取代反应当芳环上连有强拉电子基时可使环上的电子云密度降低,不利于发生亲电取代反应,有利于发生亲核取代反应.亲核试剂首先同芳环加成,然后离去基团离去,重新恢复环的芳香性,反应机理为加成-消除历程[1]:当环上连有拉电子基,尤其是在邻、对位有拉电子基时,会使反应速率加快.因邻对位拉电子基通过共轭效应,使连有离去基团的碳原子上的电子云密度降低,有利于亲核试剂进攻,也有利于碳负离子中间体的稳定.当卤原子的邻对位有拉电子基团存在时,可以发生水解、醇解、氰解、氯解等亲核取代反应.例如[2]:应该指出:①乙酰乙酸乙酯亚甲基上的取代产物可以分别在稀碱或浓碱的作用下发生酮式分解或酸式分解.由于在浓碱的作用下酸式分解时往往伴随有酮式分解,因此,合成羧酸最好使用丙二酸二乙酯.②由于乙酰乙酸乙酯不像丙二酸二乙酯那样能形成双钠盐,因此不能合成三四元环.③如果反应底物为卤代烃、α-卤代酮、α-卤代酸酯等,则机理一般为SN2;如果反应底物为酰卤,则机理为加成-消除历程. 反应活性顺序与脂肪族卤代烃的亲核取代反应活性顺序正好相反,原因在于反应机理为加成-消除机理,与饱和碳原子上的亲核取代反应机理不同.一个典型的例子是氯苯水解时随着环上硝基数目的增多,取代反应越来越易[3,5]:拉电子基主要活化其邻、对位,对间位的活化作用很弱.例如:在制备脂基芳基混合醚(Williamson合成法)时,一般选择酚钠和脂肪族卤代烃进行反应.但在芳环上邻、对位连有拉电子基的卤代芳烃,可以和醇钠作用,生成脂基芳基混合醚.例如:2.2 吡啶环上的亲核取代反应吡啶具有芳香性,属于含氮芳杂环化合物.由于环上氮原子的拉电子作用,在2-位或4-位上容易发生亲核取代反应.例如齐齐巴宾(Chicibabin A E)反应:反应机理:当吡啶的2-位或4-位上有易离去基团(如Cl、Br、NO2等)时能与亲核试剂发生亲核取代反应.例如:反应机理为加成-消除历程:2.3 经苯炔中间体的亲核取代反应苯炔(benzyne)是许多芳族亲核取代反应中的中间体.例如,用强碱(如KNH2)处理不活泼芳卤,在生成正常取代产物的同时,也会得到变位(cine)取代的异构产物.这些反应的机理均为消除-加成历程.一般是未被活化的芳基卤代物在强碱作用下发生消除反应生成苯炔中间体,而后亲核试剂再对苯炔进行加成反应得到产物:当生成的苯炔不对称时,就产生苯炔的生成方向及加成方向问题.以芳卤的氨解反应为例讨论如下.2.3.1 苯炔的生成方向取决于取代基Z的诱导效应上述反应可能生成的苯炔中间体为:式(3)中生成两种苯炔中间体.到底哪一种占优势,取决于碳负离子的稳定性,而碳负离子的稳定性又与取代基的诱导效应有关.当Z为拉电子基时,(1)比(2)要稳定,因为前者负电荷更靠近拉电子基Z,相应的主要生成苯炔(1′).当Z为推电子基时,(2)比(1)要稳定,主要生成苯炔(2′).2.3.2 苯炔的加成方向也取决于取代基Z的诱导效应羧酸衍生物(酰卤、酸酐、酯、酰胺)的结构特点是:分子中都有酰基,而且酰基都直接与带有未共用电子对的原子或基团相连,既存在诱导效应,又存在p-π共轭效应.这类化合物发生亲核取代反应的一般通式为:羧酸衍生物的水解、醇解、氨解均属于这类亲核取代,反应活性次序为:酰氯>酸酐>酯>酰胺.此外,酯缩合反应也属于羧酸衍生物的亲核取代反应,其机理加成-消除历程,并且非常重要.如Claisen酯缩合反应和Dieckmann缩合反应.Claisen酯缩合反应[2]:例1 完成反应(中南大学2007年硕士研究生招生试题)例2 完成反应(上海师大2007年硕士研究生招生试题)例3 完成反应(江苏大学2009年硕士研究生招生试题)Dieckmann缩合反应[2]:反应机理为:例4 完成反应(四川大学2008年、天津大学2007年硕士研究生招生试题)【相关文献】[1]高鸿宾.有机化学[M].北京:高等教育出版社,2005:243,252.[2]王积涛,张宝申,王永梅,等.有机化学[M].2版.天津:南开大学出版社,2003:313,318,332,239,550,507,508.[3]曾昭琼.有机化学(下册)[M].北京:高等教育出版社,2004:299-300,81.[4]王永梅,王桂林.有机化学提要·例题和习题[M].天津:天津大学出版社,1999:125.[5]曾昭琼.有机化学(上册)[M].北京:高等教育出版社,2004:293.。


判断SN、SN2反应SN(亲核取代)反应和SN2(亲核取代双分子)反应都是化学中的重要反应类型。
它们都是亲核取代反应,与其他反应不同,SN和SN2反应所需的反应组成部分非常少,通常只需要一个亲核试剂和一个底物。
在这篇文章中,我将详细介绍SN和SN2反应的基本概念和判断方法。
SN(亲核取代)反应SN反应是指一种亲核试剂(通常是氧、氮、硫或卤素)与一个无电荷或正离子底物发生反应的亲核取代反应。
在SN反应中,亲核试剂的亲核性质使其攻击底物的反应中心,从而形成一个新的化学键,并释放出一个离去基团。
SN反应共有三种可能的机理:SN1、SN2和SNi。
其中SN1和SN2反应是最常见的。
SN1反应:SN1反应通常发生在亲核试剂反应速度比离去基团离开速度慢的底物中。
在SN1反应中,底物通常通过两步反应机理进行。
在第一步中,离去基团离开,并在产生孤电子的中间体的同时,生成一个正离子。
在第二步中,亲核试剂进攻正离子并形成新化学键。
SN1反应机理的主要特点是反应中产生了一个相对稳定的中间体,这种中间体通常通过质子转移过程形成。
在SN2反应中,亲核试剂和底物分子的结合被称为二分子,因为它们同时参与到反应中。
此外,SN2反应的主要特征是反应速度较快,通常在溶解度和温度相适宜的情况下,反应速度高达几个亿分之一秒。
在SN2反应中,亲核试剂进攻底物中心,与离去基团同时形成新化学键。
在SN2反应中,亲核试剂和离去基团同时出现,因此碳中心的手性不会改变。
当发生SN2反应时,负离子进攻底物中心,因此底物通常是一个良好的亲核试剂。
要判断SN和SN2反应的类型,需要考虑以下要素:· 底物的置换机制· 亲核试剂的类型和性质通常情况下,如果亲核试剂是一个良好的亲核试剂,即可以在较低的浓度下进攻底物中心,则会发生SN2反应。
如果亲核试剂比较弱,反应速度较慢,而离去基团在底物中心的亲核目标上形成了中间体,还会发生SN1反应。
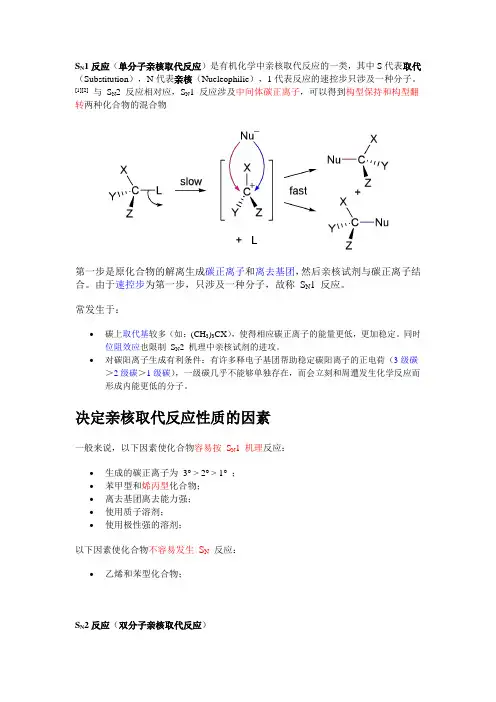
S N1反应(单分子亲核取代反应)是有机化学中亲核取代反应的一类,其中S代表取代(Substitution),N代表亲核(Nucleophilic),1代表反应的速控步只涉及一种分子。
[1][2]与S2 反应相对应,S N1 反应涉及中间体碳正离子,可以得到构型保持和构型翻N转两种化合物的混合物第一步是原化合物的解离生成碳正离子和离去基团,然后亲核试剂与碳正离子结合。
由于速控步为第一步,只涉及一种分子,故称S N1 反应。
常发生于:∙碳上取代基较多(如:(CH3)3CX),使得相应碳正离子的能量更低,更加稳定。
同时位阻效应也限制S N2 机理中亲核试剂的进攻。
∙对碳阳离子生成有利条件:有许多释电子基团帮助稳定碳阳离子的正电荷(3级碳>2级碳>1级碳),一级碳几乎不能够单独存在,而会立刻和周遭发生化学反应而形成内能更低的分子。
决定亲核取代反应性质的因素一般来说,以下因素使化合物容易按S N1 机理反应:∙生成的碳正离子为3° > 2° > 1°;∙苯甲型和烯丙型化合物;∙离去基团离去能力强;∙使用质子溶剂;∙使用极性强的溶剂;以下因素使化合物不容易发生S N反应:∙乙烯和苯型化合物;S N2反应(双分子亲核取代反应)是亲核取代反应的一类,其中S代表取代(Substitution),N代表亲核(Nucleophilic),2代表反应的决速步涉及两种分子。
与S N1反应相对应,S N2反应中,亲核试剂带着一对孤对电子进攻具亲电性的缺电子中心原子,形成过渡态的同时,离去基团离去。
反应中不生成碳正离子,速率控制步骤是上述的协同步骤,反应速率与两种物质的浓度成正比,因此称为双分子亲核取代反应。
无机化学中,常称双分子亲核取代反应类型的反应机理为“交换机理”。
由于亲核试剂是从离去基团的背面进攻,故如果受进攻的原子具有手性,则反应后手性原子的立体化学发生构型翻转,也称“瓦尔登翻转”。


烷烃亲核取代反应sn1机理
本文旨在详细阐述烷烃亲核取代反应SN1机理。
SN1机理是一种重要的有机
反应机理,它通常发生在无官能团的烷烃中。
SN1(SubstitutionNucleophilicUnimolecular)机理是一种立即发生的亲核
取代反应,其特征是反应物的反应速率只和反应物的活性有关。
它以一步发生,
与催化剂和增感剂无关。
SN1机理的反应过程可以概括为:烷烃先离解成氯仿离子和活性基团,活性基
团以不定离子(Leblanc离子)格式临时存在,而该Leblanc离子之后被亲核试剂
H-R捕获,其最终形成有机产物。
另一方面,SN1反应受反应物特性影响很小,烷烃的官能团越来越接近氯仿键,该反应的活化能量越低,反应的活性变得越来越高,也就是反应的速率越来越快。
此外,存在取代剂的烷烃的反应速率要比受不取代的烷烃要高。
最后,SN1机理是有机化学中的一种重要的反应机理,它的特点是活性取决于
原料的活性,具有宽泛的应用前景。
如果我们正确理解SN1机理,并熟练掌握它,就可以为我们工作、科研提供有效的技术支持。




有机化学中的亲核取代反应有机化学是研究碳化合物及其衍生物的科学,涵盖了广泛的知识和反应类型。
在有机化学中,亲核取代反应是一类重要的反应类型,它在有机合成中起着至关重要的作用。
本文将介绍有机化学中的亲核取代反应,包括基本概念、机理和实际应用。
亲核取代反应是一种核酸(亲核试剂)与一个带正电荷或部分正电荷的碳原子相互作用的反应。
亲核试剂指的是具有孤对电子或由共轭体系提供可用孤对电子的分子或离子。
在反应中,亲核试剂攻击带正电荷的碳原子,将其替换为亲核试剂中的原子或基团。
亲核取代反应可以分为以下几种类型:1. SN1反应(亲核取代一型):SN1反应是一种两步反应,首先发生离解步骤,生成一个离子中间体,然后亲核试剂与离子中间体发生反应。
SN1反应的速率仅取决于离解步骤,与亲核试剂无关。
2. SN2反应(亲核取代二型):SN2反应是一种一步反应,亲核试剂直接攻击带正电荷的碳原子,并将其替换。
SN2反应的速率与亲核试剂的浓度成正比。
3. SNi反应(亲核取代离解负离子反应):SNi反应类似于SN1反应,但离解步骤形成负离子中间体。
4. 过渡态化合物的亲核取代反应:过渡态化合物的亲核取代反应是一类特殊的反应,其中反应物形成一个比中间体更稳定的产物。
这种反应常见于环化合物的开环反应。
亲核取代反应在有机合成中有广泛的应用。
例如,通过SN2反应,可以合成含有新碳-亲核试剂键的化合物。
此外,亲核取代反应还可以用于合成酯、醚、胺等有机物。
通过选择适当的亲核试剂和反应条件,可以实现高效的选择性反应。
需要注意的是,亲核取代反应的机理和速率常受到多种因素的影响,包括亲核试剂的性质、反应物的结构和环境条件等。
因此,合理选择反应条件对于实现期望的反应结果非常重要。
总结起来,有机化学中的亲核取代反应是一类重要的反应类型,它在有机合成中具有广泛的应用。
通过理解亲核取代反应的基本概念和机理,我们可以更好地应用这些反应,合成有机化合物,并推动有机化学领域的进一步发展。
亲核取代反应一.亲核取代反应机理。
亲核取代反应是指有机分子中的与碳相连的原子或原子团被作为亲核试剂的某原子或原子团取代的反应。
反应分为SN1型(单分子取代反应),与SN2型双分子取代反应。
1.SN1型(单分子取代反应)第一步是碳原子上正电荷增加,离去基团负点性增加,经过过渡态(1)并最终解离,生成活性中间体碳正离子与离去基团负离子。
由于这一步反应的活化能较高,速率较慢,所以这一步是反应的决速步。
第二步是活性中间体的碳正离子与亲和试剂作用,生成反应产物。
这一步仅需少量能量,速率很快。
反应特点:(1)SN1反应的决速步是中心碳原子与离去基团之间化学键的异裂。
反应速率只取决于一种分子的浓度,因此,它在动力学上是一级反应。
(2)一般是一个两步反应。
第一步生成的碳正离子采取SP2杂化,是平面构型。
故若反应物的中心碳原子是手性碳,反应产物一般是一对等量的对映异构体的混合物——外消旋体。
(3)反应中间体生成的碳正离子导致反应有重排的趋势。
2.SN2型(双分子取代反应)反应中,离去基团离开中心碳原子的同时,亲核试剂与中心碳原子发生部分键合,无中间体生成。
有机反应中,将两种分子参与决速步的亲核取代反应陈伟双分子亲核取代反应。
反应特点:(1)SN2反应是一步反应,只有一个过渡态。
(2)在SN2反应中,亲核试剂进攻中心碳原子是总是从离去基团溴原子的背面沿着碳原子和离去基团连接的中心线方向进攻。
这个过程会使得碳原子与三个未参与反映的键发生翻转,这种翻转称为瓦尔登翻转,又称构型翻转。
二.影响亲核取代反应的因素1.烃基结构的影响。
对SN1反应,主要考虑碳正离子的稳定性。
对SN2反应,主要取决于过渡态形成的难易,也就是空间效应的影响。
2.离去基团的影响。
离去基团的性质对SN1和SN2将产生相似的影响:离去基团的离去能力越强,亲核取代反应越易进行。
对于离去基团:键能越弱,离去基团的稳定性越好,该离去基团的离去能力就越强。
3.亲核试剂的影响仅对SN2有影响。
SN1和SN2反应机制一、SN1反应机制:SN1反应是亲核取代反应中的一个重要机制,SN代表取代反应的类型,其中S代表极性反应,N代表亲核反应。
SN1反应包括三个步骤:离去基团脱离、亲核物种攻击、质子转移。
1.离去基团脱离:在SN1反应中,首先离去基团(通常为卤素)脱离底物,形成一个类似于溴化亚甲基的离子中间体。
此步骤的速率决定了整个反应的速率。
2.亲核物种攻击:离去基团脱离后,生成的离子中间体很不稳定,会很快解离为一个稳定的互变异构体(通常为碳正离子)和一个孤立的正离子。
3.质子转移:亲核物种(通常为一个带负电的离子,例如水、醇等)攻击形成的稳定的碳正离子,形成最终的产物。
SN1反应的特点:1.SN1反应是一个两步反应,中间体稳定性较高,反应速率主要取决于离去基团的离去速率。
2.SN1反应喜欢消耗极性溶剂,反应速率越快。
3.反应底物的立体化学构型变化较小,因为离去基团首先脱离产生的离子中间体是不手性的。
4.SN1反应喜欢在稳定的孤立原子上发生,通常涉及孤立空间轨道的产物形成。
二、SN2反应机制:SN2反应也是亲核取代反应中的一种机制,代表一级亲核取代反应,其中S代表极性反应,N代表亲核反应,2代表反应中存在两个底物。
1.亲核物种攻击:在SN2反应中,亲核物种(例如卤素离子、醇酸等)直接攻击底物分子,取代底物上的一个离去基团。
此时,键的断裂和键的形成是同步进行的。
2.离去基团脱离:在亲核物种攻击时,底物上的离去基团会立即脱离,形成产物。
SN2反应的特点:1.SN2反应是一个一步反应,整个过程的速率由亲核物种的浓度和底物的浓度共同决定。
2.反应速率与底物的立体化学构型有关,反应底物的立体构型由于亲核物种的攻击而发生倒置。
3.SN2反应对于溶剂的要求较宽泛,可以在极性和非极性溶剂中进行。
4.SN2反应喜欢在不稳定的孤立原子上发生,通常对于为手性的底物可以得到相应手性产物。
总结:SN1和SN2反应机制都是有机化学中常见的取代反应机制。
亲核取代反应总结1、反应定义:亲核取代反应(Nucleophilic Substitution Reaction)是指有机分子中与碳相连的某原子或基团被作为亲核试剂的某原子或基团取代的反应。
在反应过程中,取代基团提供形成新键的一对电子,而被取代的基团则带着旧键的一对电子离去。
2、反应意义:这类反应是有机化学中非常重要的一类反应,不论在理论研究中还是在有机合成实际中都是极其有用的一类反应。
3、反应分类:亲核取代反应的主要类型为脂肪族饱和碳上的亲核取代反应,即饱和卤代烃与亲核试剂的取代反应,较特殊结构的有苄基卤代物、烯丙基卤代物亲核反应。
其他类型还包括与酰氯、磺酸酯、磺酰卤、卤代苯等的取代反应。
从电荷类型来分,亲核取代反应只能有四种类型:(1)中性底物和负离子亲核试剂反应(2)中性底物和中性亲核试剂反应(3)正离子底物和负离子亲核试剂反(4) 正离子底物和中性亲核试剂反应亲核试剂包括有机和无机两类分子或离子:无机类亲核试剂:OH -、CN -、X -、H 2O 、NH 3等有机类亲核试剂:ROH 、RO -、PhO -、RS -、RMgX 、RCOO -等4、反应机理类型分类:(1)双分子亲核取代反应(S N 2)有两种分子参与了决定反应速率关键步骤的亲核取代反应称为双分子亲核取代反应。
反应过程中,亲核试剂从反应物离去基团的背面向与它连接的碳原子进攻,先与碳原子形成比较弱的键,同时离去基团与碳原子的键有一定程度的减弱,两者与碳原子成一条直线,碳原子上另外三个键逐渐由伞形转变成平面,这需要消耗能量,即活化能,当反应进行和达到能量最高状态即过渡态后,亲核试剂与碳原子之间的键开始形成,碳原子与离去基团之间的键断裂,碳原子上三个键由平面向另一边偏转,整个过程犹如大风将雨伞由里向外反转一样,这时就要释放能量,形成产物,S N 2反应机理一般式表示为:Nu -+ R X [Nuδ-···R···X δ- ] NuR + X -例如,溴甲烷与OH -的水解反应:(2)单分子亲核取代反应(S N 1)只有一种分子参与了决定反应速率关键步骤的亲核取代反应称为单分子亲核取代反应,反应中,反应物首先解离成碳正离子与带负电荷的离去基团,这个过程需要能量,是控制反应速率的一步,即慢的一部。
亲核取代反应sn1机理
亲核取代反应(SN1)是一种重要的有机化学反应,它涉及一个步骤的离子解离和生成。
SN1反应是一种两步反应,首先是生成一个离子中间体,然后是它被亲核试剂攻击的步骤。
在SN1反应中,亲核试剂通常是一个带有孤对电子的分子或离子,例如水、醇或卤素离子。
SN1反应的机理可以从多个角度来理解。
首先,它涉及亲核试剂攻击离子中间体,这种攻击通常会导致立体化学反应。
其次,SN1反应的速率决定步骤是生成离子中间体,这意味着反应速率只依赖于底物的浓度,而与亲核试剂的浓度无关。
此外,SN1反应通常发生在次级或三级碳中心上,因为这些底物的离子中间体相对稳定。
另一个角度来理解SN1反应是通过考虑反应条件对其影响。
例如,溶剂的选择可以影响SN1反应的速率和产物选择。
极性溶剂通常会促进SN1反应,因为它们有助于离子中间体的形成和稳定。
此外,温度和反应物的结构也会影响SN1反应的速率和产物选择。
从反应动力学的角度来看,SN1反应通常表现出一级反应的特征,其速率与底物的浓度成正比。
这意味着SN1反应是一个较慢的
反应,通常在较高温度下进行以提高反应速率。
总的来说,亲核取代反应(SN1)是一个复杂而重要的有机化学反应,其机理涉及离子中间体的生成和亲核试剂的攻击。
理解SN1反应的机理对于预测其产物和优化反应条件非常重要。