芳香烃亲电取代反应
- 格式:pptx
- 大小:601.28 KB
- 文档页数:19
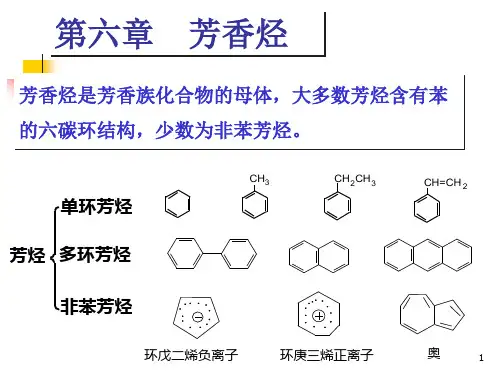

芳烃烷基化反应芳烃烷基化反应是一种常见的有机化学反应,也是合成有机化合物的重要方法之一。
该反应是在芳香烃分子上引入烷基基团,使得分子结构发生改变。
本文将全面介绍芳烃烷基化反应的定义、反应机制、应用以及实验指导,希望对读者有所启发。
芳烃烷基化反应是指将一个烷基基团与芳香烃分子中的氢原子进行置换的化学反应。
在该反应中,常用的烷基基团包括甲基、乙基、丙基等。
芳烃烷基化反应属于亲电取代反应,反应的具体条件和机理因具体反应物而异。
芳烃烷基化反应的机理主要有两种:亲电芳香烃取代机理和自由基芳香烃取代机理。
在亲电芳香烃取代机理中,亲电试剂通过亲电取代进攻芳环上的电子丰富位点,形成中间体后,再通过脱去偶电子对或酸碱中和步骤来得到产物。
自由基芳香烃取代机理是通过氢原子的自由基取代芳香烃分子,其中甲基自由基是最常用的自由基试剂。
芳烃烷基化反应在有机化学合成中具有广泛的应用。
首先,它可以用于合成重要的有机化合物,如药物、染料和香料等。
其次,芳烃烷基化反应可以用于合成具有不同取代基的芳香烃,从而改变化合物的性质和活性。
此外,芳烃烷基化反应还可以用于合成充满活力的材料,如聚合物和液晶等。
进行芳烃烷基化反应的实验前,我们需要准备好实验装置和试剂。
在实验中,应注意遵守安全操作规程,注意个人防护,并确保实验室通风良好。
实验步骤一般包括溶剂的选取和配制、催化剂的选择和添加、控制反应条件等。
反应结束后,应注意正确处理废弃物和清洁实验装置。
总之,芳烃烷基化反应是一种重要的有机合成方法,具有广泛的应用前景。
通过深入了解该反应的定义、机制和实验指导,我们可以更好地应用和掌握该反应,从而为有机化学的研究和应用贡献自己的力量。
希望本文能够为读者提供有益的指导和启发。
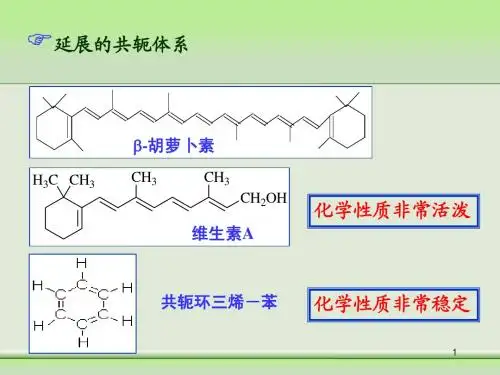


芳香化合物的性质与反应芳香化合物是一类具有独特香味的有机化合物,由苯环及其衍生物组成。
它们具有一些特殊的性质和反应,让我们一起来了解它们吧。
一、芳香化合物的性质1. 香味:芳香化合物得名于其独特的香味,许多香料和芳香精油中的成分属于芳香化合物。
这种香味主要来源于化合物分子中含有的苯环结构。
2. 稳定性:芳香化合物具有较高的稳定性,这是由于苯环中的π电子共轭结构所致。
共轭结构使得芳香化合物在反应中能够更好地保持分子结构的稳定。
3. 不饱和性:尽管芳香化合物看似含有多个双键,但实际上它们是不饱和的。
这是因为在芳香化合物的苯环中存在特殊的π电子共轭结构,使得芳香化合物中的双键呈现出较为稳定的性质。
4. 短程有序:芳香化合物具有较短的分子间相互作用距离,使得它们分子间的排列较为有序。
这种短程有序结构使得芳香化合物在溶解性、熔点等方面表现出独特的性质。
二、芳香化合物的反应1. 亲电取代反应:芳香化合物对电子亲和力较强,容易进行亲电取代反应。
在这类反应中,一个取代基取代苯环上的氢原子。
常见的亲电取代反应包括硝化反应、卤代反应等。
2. 自由基取代反应:在适当的条件下,芳香化合物可以进行自由基取代反应。
这类反应中,自由基基团取代苯环上的氢原子。
自由基取代反应常见的例子是芳香烃对卤原子的取代反应。
3. 加成反应:芳香化合物中的π电子可以与电荷云较集中的亲电试剂进行加成反应。
常见的加成反应有迈克尔加成反应和腈酸的加成反应等。
4. 氧化反应:芳香化合物可以发生氧化反应。
例如,苯能够与浓硝酸反应产生硝基苯,还能够与浓硫酸和高锰酸钾反应产生苯酚。
5. 还原反应:芳香化合物也可以发生还原反应。
例如,硝基苯可以经过还原反应生成苯胺。
总结:芳香化合物具有独特的性质和反应,包括香味、稳定性、不饱和性和短程有序等。
它们在化学反应中表现出亲电取代、自由基取代、加成、氧化和还原等多种反应类型。
深入理解芳香化合物的性质与反应对于有机化学的研究和应用具有重要意义。



有机化学芳香烃习题与答案有机化学是化学的一个重要分支,研究有机物的结构、性质和合成方法。
其中,芳香烃是一类具有特殊结构的有机化合物,其分子中含有苯环或苯环衍生物。
对于有机化学的学习者来说,掌握芳香烃的性质和反应是非常重要的。
下面,我们将介绍一些有机化学芳香烃的习题以及相应的答案,希望对大家的学习有所帮助。
1. 以下哪个化合物是芳香烃?A) 甲烷B) 乙烷C) 苯D) 乙醇答案:C) 苯。
苯是最简单的芳香烃,其分子结构由六个碳原子组成一个六角形环,每个碳原子上都有一个氢原子。
2. 以下哪个化合物不是芳香烃?A) 甲苯B) 苯酚C) 乙烯D) 苯答案:C) 乙烯。
乙烯是一个不饱和烃,它的结构中没有苯环。
3. 下列化合物中,哪一个是苯的同分异构体?A) 乙烯B) 丙烯C) 乙炔D) 环己烷答案:D) 环己烷。
环己烷是一个由六个碳原子组成的环状结构,它的分子结构与苯非常相似,因此是苯的同分异构体。
4. 以下哪个反应是芳香烃的典型反应?A) 羟基取代反应B) 氧化反应C) 加成反应D) 亲电取代反应答案:D) 亲电取代反应。
芳香烃的亲电取代反应是其最常见的反应类型,它通常发生在苯环上的氢原子被亲电试剂取代的过程中。
5. 以下哪个化合物是苯的衍生物?A) 甲醇B) 甲酸C) 甲苯D) 丙酮答案:C) 甲苯。
甲苯是苯的一个衍生物,它的分子结构中,一个氢原子被甲基基团取代。
通过以上习题和答案,我们可以加深对有机化学芳香烃的理解。
芳香烃是有机化学中的重要概念,掌握其性质和反应对于解题和实际应用具有重要意义。
希望大家通过不断学习和练习,能够更好地理解和应用有机化学芳香烃的知识。


