课题1 常见的酸和碱2
- 格式:ppt
- 大小:812.50 KB
- 文档页数:12




课题1 常见的酸和碱(第2课时)[温故知新]2.回忆金属活动顺序表:哪些金属可以与酸发生反应?[我会自学]1.盐酸的主要用途;硫酸的主要用途。
2.因为浓硫酸溶于水时________________,所以在稀释浓硫酸时,一定要把________沿器壁慢慢注入_____里,并不断_______,使产生的热量迅速地扩散,防止液体暴沸,发生危险。
3.酸的化学性质[我会探究]1.硫酸有很强的腐蚀性,如果沾到皮肤或衣服上,应如何处理?2.硫酸为什么可以除去金属制品表面的锈,除锈时能否将金属制品长时间浸没在酸中?为什么?以除铁锈为例描述实验现象,并写出有关化学方程式。
3.为了探究影响金属与酸反应程度的因素,进行了以下实验:因素一:;因素二:;因素三:。
[例题解析]现有失去标签的相同体积的两瓶液体,一瓶是98%的浓硫酸,另一瓶是10%的稀硫酸,请你用学过的物理和化学知识,用两种方法将它们鉴别出来。
物理方法:__________________________________________________化学方法:__________________________________________________[解析] 本题答案不唯一。
回答时需要对浓硫酸和稀硫酸的性质进行比较分析,如浓硫酸的特性有强腐蚀性、吸水性、脱水性等,而稀硫酸则具有酸的通性。
[答案] 物理方法:(1)用天平称质量,体积相同的两种液体中质量大的为浓硫酸;(2)用密度计测密度,密度大的为浓硫酸;(3)倾斜观察,较粘稠的为浓硫酸;4)稀释两种酸,用手摸杯壁,较热的为浓硫酸。
化学方法:(1)用小木条分别蘸取两种酸,变黑的是浓硫酸;(2)用白纸条分别蘸取两种酸,变黑的是浓硫酸;(3)取少量的两种酸于试管中,分别加入铁钉,有气泡产生的是稀硫酸。
[体验收获]1.浓盐酸的下列性质中,属于物理性质的是()A.在空气中形成白雾B.滴在石灰石上有气泡放出C.使紫色石蕊溶液变红 D.除去金属制品表面的锈斑2.氧气、氢气、二氧化碳三种气体都能用浓硫酸做干燥剂,是因为浓硫酸具有()A.酸性 B.脱水性 C.吸水性 D.氧化性3.长期暴露在空气中,溶质成分不变,但溶质质量分数减小且溶液质量增加的是()A.浓硫酸B.浓盐酸C.稀硫酸D.稀盐酸4.下列金属与盐酸反应速度最快的是()A.Zn B.Fe C.Mg D.Al5.实验室欲用质量分数98%、密度 1.84g/cm3浓硫酸酸配制质量分数为19.8%,密度为1.14g/cm3的稀硫酸75ml,请按要求填写空格。

课题1 常见的酸和碱(第二课时) 教学目标1.知识与技能(1)知道几种常见酸和碱的主要性质和用途。
(2)会用酸碱指示剂检验溶液的酸碱性。
(3)认识酸和碱的腐蚀性及使用时的安全注意事项。
(4)能完成简单的探究实验。
2.过程与方法(1)进一步认识和体验科学探究的过程。
(2)运用实验的方法获取信息,运用比较概括等方法对获取的信息进行加工。
(3)增强对化学现象的探究欲,发展善于合作、勤于思考的科学精神。
3.情感态度与价值观进一步增强探究物质的好奇心和求知欲。
教学重点1.运用酸碱指示剂检验溶液的酸碱性。
2.酸碱各自相似的化学性质。
教学难点酸和碱各自具有相似化学性质的原因。
教学方法复习、总结、联系实际、实验探究、巩固练习。
教具准备教师用具:仪器:烧杯、玻璃棒、锥形瓶、双孔塞、分液漏斗、短玻璃导管、镊子、投影仪;药品:浓硫酸、鸡爪、NaOH溶液(20%)。
学生用具:仪器:滴管、研钵、烧杯、纱布、纸、小木棍、布、玻璃片、玻璃棒、点滴板、镊子、表面皿、蒸发皿、溶液导电性实验仪器;药品:食醋、稀盐酸、稀硝酸、稀硫酸、食盐水、石灰水、氢氧化钠溶液、紫色石蕊试液、无色酚酞试液、酒精、花(果实)、浓盐酸、浓硫酸、生锈的铁钉、NaOH固体、生石灰、蒸馏水。
课时安排3课时第一课时:酸和碱溶液与酸碱指示剂的反应。
第二课时:几种常见酸和碱的主要性质和用途。
第三课时:酸和碱各自具有相似化学性质的原因。
教学过程[引入]上节课我们学习了酸碱指示剂,并熟悉了几种酸和碱,这节课我们重点探讨几种酸和碱的性质和用途。
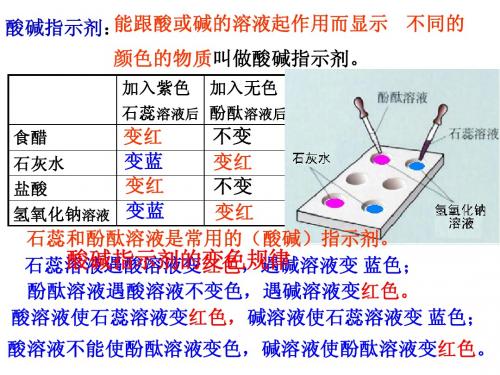
[板书]二、几种常见的酸[活动与探究](投影展示)(1)观察盐酸、硫酸的状态。
(2)分别打开盛有浓盐酸、硫酸的试剂瓶的瓶盖,观察现象并闻气味。
盐酸硫酸颜色、状态打开瓶盖后的现象气味[教师]强调闻气味的方法。
[学生活动][讨论交流][总结]无色液体无色液体瓶口出现白雾无明显现象刺激性气味无味[引导]探究了盐酸、硫酸的一些简单性质,你是否想了解它们的用途呢?[投影]用途盐酸(HCl)重要化工产品。




课题1 常见的酸和碱第2课时常见的酸一、教学目标1.熟悉常见的酸——盐酸和硫酸的物理性质和用途;2.了解浓硫酸的特性,掌握浓硫酸的稀释方法;3.通过活动与探究,掌握酸的化学性质。
二、教学重难点重点:酸的化学性质。
难点:浓硫酸的稀释方法。
三、教学过程【知识回顾】请同学们写出所学过的有酸参与的化学反应的化学方程式。
【总结与交流】①CaCO3+2HCl=CaCl2+H2O+CO2↑②Na2CO3+2HCl=2NaCl+H2O+CO2↑③Zn+H2SO4=ZnSO4+H2↑④Fe+H2SO4=FeSO4+H2↑⑤Mg+2HCl=MgCl2+H2↑……【过渡】反应①是实验室制取二氧化碳的反应原理,反应③是实验室制取氢气的反应原理,所以盐酸和硫酸是我们在实验室中经常用到的酸,另外硝酸和醋酸也是实验室中常见的酸,那么这些酸具有哪些物理性质和化学性质呢?本节课我们一起探究吧!【实验探究】(1)观察盐酸、硫酸的颜色和状态;(2)分别打开盛有盐酸,硫酸的试剂瓶的瓶盖,观察现象并闻气味。
(注意闻气味的正确操作)【实验记录】【交流讨论】打开浓盐酸的瓶盖出现白雾的原因是什么?【总结与交流】浓盐酸具有挥发性,浓盐酸中挥发出的氯化氢气体遇到空气中的水蒸气生成的盐酸小液滴。
【交流讨论】现在有两瓶装着盐酸和硫酸的未贴标签的试剂瓶,根据它们的物理性质,你知道该如何区分它们吗?【总结与交流】轻轻摇晃观察液体是否黏稠、打开瓶盖看其是否出现白雾、闻其是否有刺激性气味等。
【学生活动】根据课本52页表格内容,总结硫酸和盐酸各有什么用途?【总结】生产、生活中很多地方都要用到盐酸和硫酸。
盐酸常用于金属除锈、制造含氯的药物,如生活中的洁厕灵等。
人的胃液中含有盐酸用以帮助消化。
硫酸也可用于金属除锈,还广泛用于生产化肥、农药、火药、冶炼金属、精炼石油等。
浓硫酸具有吸水性,还可以用作实验室里的干燥剂。
【交流讨论】两试剂瓶分别敞口放置的浓盐酸和浓硫酸,过一段时间后,该溶液的溶质质量分数会有什么变化,为什么?【总结与交流】浓盐酸易挥发,溶解的氯化氢气体易扩散到空气中,造成溶液的溶质质量分数变小;浓硫酸具有吸水性,易吸收空气中的水蒸气,造成溶质质量分数也变小。

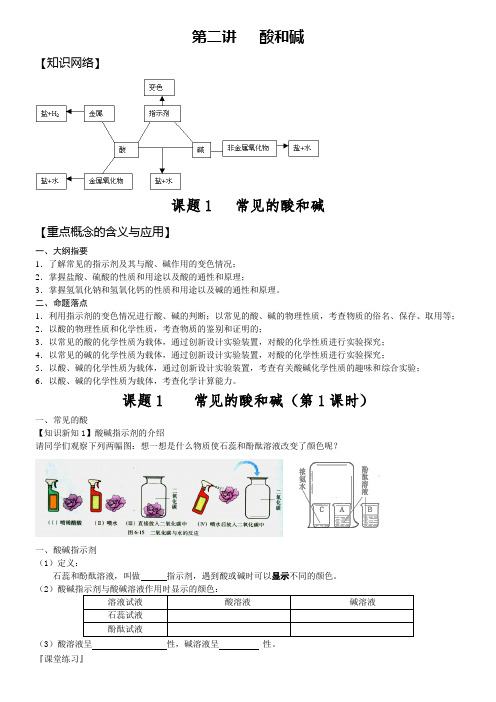
第二讲酸和碱【知识网络】课题1 常见的酸和碱【重点概念的含义与应用】一、大纲指要1.了解常见的指示剂及其与酸、碱作用的变色情况;2.掌握盐酸、硫酸的性质和用途以及酸的通性和原理;3.掌握氢氧化钠和氢氧化钙的性质和用途以及碱的通性和原理。
二、命题落点1.利用指示剂的变色情况进行酸、碱的判断;以常见的酸、碱的物理性质,考查物质的俗名、保存、取用等;2.以酸的物理性质和化学性质,考查物质的鉴别和证明的;3.以常见的酸的化学性质为载体,通过创新设计实验装置,对酸的化学性质进行实验探究;4.以常见的碱的化学性质为载体,通过创新设计实验装置,对酸的化学性质进行实验探究;5.以酸、碱的化学性质为载体,通过创新设计实验装置,考查有关酸碱化学性质的趣味和综合实验;6.以酸、碱的化学性质为载体,考查化学计算能力。
课题1 常见的酸和碱(第1课时)一、常见的酸【知识新知1】酸碱指示剂的介绍请同学们观察下列两幅图:想一想是什么物质使石蕊和酚酞溶液改变了颜色呢?一、酸碱指示剂(1)定义:石蕊和酚酞溶液,叫做指示剂,遇到酸或碱时可以显示不同的颜色。
(2)酸碱指示剂与酸碱溶液作用时显示的颜色:(3)酸溶液呈性,碱溶液呈性。
『课堂练习』1、无色酚酞试液及某些植物的花瓣或果实的酒精浸出液遇到酸或碱溶液,也能显示出不同的颜色。
如下表所示:⑴ 上表列出的五种物质中,不能作为酸碱指示剂的有_____ ___(填名称)⑵ 酒精在其中起的作用是 。
⑶ 小明在厨房中取少量白醋滴入大红花的花汁中,他看到的现象为__________;为什么? 2、能使紫色石蕊试液变成蓝色的溶液,它能使无色酚酞试液( ) A 、变红色 B 、变蓝色 C 、呈无色 D 、变紫色3、小李在学习酸碱指示剂与常见酸、碱溶液作用时,归纳成如右图所示 的关系。
图中A 、B 、C 、D 是两圆相交的部分,分别表示指示剂与酸、 碱溶液作用时所显示出的颜色,则其中表示不正确...的是( ) A .紫色 B .蓝色 C .红色 D .无色 【知识新知2】浓盐酸和浓硫酸的介绍[知识回顾] 通过前面的学习你已经知道哪些酸?(1)浓硫酸和浓盐酸的物理性质和盐酸、硫酸的用途说明:①盐酸是HCl 气体的水溶液,浓盐酸易挥发。




课题一常见的酸和碱(第二课时)【教学目标】1.知道浓硫酸、浓盐酸的物理性质;2.了解浓硫酸的特性;3.初步掌握稀盐酸、稀硫酸的化学性质;【教学重点】稀盐酸、稀硫酸的化学性质。
【教学难点】酸的化学性质。
【教学过程】一、自主学习:认真阅读课本52-54页完成以下问题1、盐酸的用途1、__________2、________________________3__________________2、硫酸的用途1、_________________2、________________3、___________________3、浓硫酸具有______性,在实验室常用作干燥剂。
这是______变化。
4、常见的酸有_________、______、________、______________5、浓硫酸有强烈的______性,它能读取纸张、木材、布料里的水分,生成黑色的炭,这是_____变化。
6、稀释浓硫酸时一定要将______沿烧杯壁慢慢的注入_______中,并用_______不断搅拌。
如果不慎将浓硫酸沾到皮肤或衣服上,应立即用大量的_____ 冲洗,然后涂上3%——5%的________溶液。
7、填写下表8、回忆所学的知识,完成下表我们小组在完成预习学案中遇到的问题是:三、合作探究活动一、感知浓盐酸和浓硫酸典型的物理性质观察演示实验:1、分别向两支试管中倒入少量的浓盐酸和浓硫酸观察现象2、向上述两支试管中分别加一火柴梗。
填写下面表格。
共3页第1页【交流讨论】(1)打开浓盐酸的瓶盖为什么会产生白雾?说明浓盐酸具有什么性质?(2)浓硫酸没有白雾说明浓硫酸具有什么性质?(3)浓盐酸、浓硫酸的敞口放置一段时间后质量以及质量分数如何变化:(4)保存浓盐酸、浓硫酸的时要注意些什么?(5)实验室制二氧化碳时,为什么不用浓盐酸?活动二、认识浓硫酸特性以及使用时的注意点。
认真观察教师的演示实验10-3,填写下表观察实验10-4【交流讨论】(1)如果不慎将浓硫酸溅在皮肤或者衣物上会有什么结果?应该怎么处理?说明浓硫酸具有什么性质?(2)如果将稀硫酸沾到皮肤和衣服上,是否也要象浓硫酸这样处理,为什么?(3)在稀释浓硫酸时应该怎样操作?为什么要这样做?活动三、探究稀盐酸、稀硫酸的化学性质【活动探究】将生锈的铁钉分别放入盛有稀盐酸和稀硫酸的试管里,过一会将铁钉取出后,观察铁钉表面的现象(1)上述反应生成物有什么相同之处?(2)在实验室里如何除去铁钉表面的铁锈?能否将生锈的物质长时间浸泡在酸中?(3)总结酸有哪些共同的化学性质?为什么?四、当堂检测:一课一练P89页2、3、4、6、8五、课堂小结一、浓盐酸、浓硫酸的物理性质、特性及用途:1.浓盐酸和浓硫酸的物理性质共3页第2页3.浓硫酸的特性:⑴脱水性:⑵吸水性⑶强烈的腐蚀性。
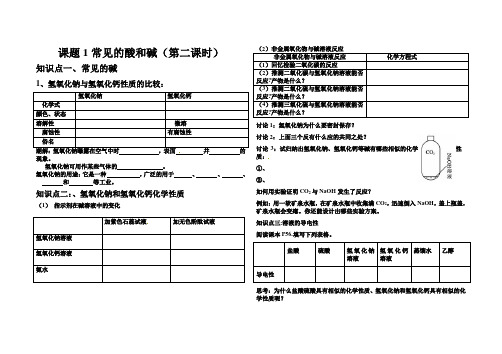
课题1常见的酸和碱(第二课时)知识点一、常见的碱1、氢氧化钠与氢氧化钙性质的比较:氢氧化钠氢氧化钙化学式颜色、状态溶解性微溶腐蚀性有腐蚀性俗名潮解:氢氧化钠曝露在空气中时,表面并的现象。
氢氧化钠可用作某些气体的。
氢氧化钠的用途:它是一种,广泛的用于、、、和等工业。
知识点二:、氢氧化钠和氢氧化钙化学性质(1)指示剂在碱溶液中的变化加紫色石蕊试液加无色酚酞试液氢氧化钠溶液氢氧化钙溶液氨水(2)非金属氧化物与碱溶液反应非金属氧化物与碱溶液反应化学方程式(1)回忆检验二氧化碳的反应(2)推测二氧化碳与氢氧化钠溶液能否反应?产物是什么?(3)推测二氧化硫与氢氧化钠溶液能否反应?产物是什么?(4)推测三氧化硫与氢氧化钠溶液能否反应?产物是什么?讨论1:氢氧化钠为什么要密封保存?讨论2:上面三个反有什么应的共同之处?讨论3:试归纳出氢氧化钠、氢氧化钙等碱有哪些相似的化学性质:①、②、如何用实验证明CO2与NaOH发生了反应?例如:用一软矿泉水瓶,在矿泉水瓶中收集满CO2,迅速倒入NaOH,盖上瓶盖,矿泉水瓶会变瘪。
你还能设计出哪些实验方案。
知识点三:溶液的导电性阅读课本P56.填写下列表格。
盐酸硫酸氢氧化钠溶液氢氧化钙溶液蒸馏水乙醇导电性思考:为什么盐酸硫酸具有相似的化学性质、氢氧化钠和氢氧化钙具有相似的化学性质呢?课堂练习:1、氧化钙俗名_____________,它溶于水后生成熟石灰,化学方程式为__________________________,该反应是_____________(填放热或吸热)反应。
氢氧化钙属于_____________哪类物质?在前面还学过哪些碱_____________、、。
2、氢氧化钠暴露在空气中表面_____________,说明氢氧化钠_____________。
保存氢氧化钠时应__________保存。
它____(“能”或“不能”)做干燥剂。
3.下列各物质的俗名中,属于同种物质的名称是( )A.烧碱、火碱、苛性钠 B.熟石灰、消石灰、生石灰C.金刚石、大理石、石灰石 D.沼气、天然气、水煤气4.下列各项对氢氧化钠的描述正确的是( )①是一种有色晶体,易溶于水,溶解时放出大量的热②固体氢氧化钠置于空气中易潮解③氢氧化钠水溶液使石蕊溶液呈红色④对皮肤、衣服等有强烈的腐蚀性⑤氢氧化钠在空气中不仅吸收水分,还和二氧化碳反应A.①②④⑤B.②④⑤ C.①②④ D.④5.若将潮湿的空气依次通过烧碱溶液、浓硫酸和红热的铜网,将会依次除去空气中的______________、______________、______________,最后剩余的气体主要是______________。