烃的衍生物重要知识点总结
- 格式:doc
- 大小:1.39 MB
- 文档页数:5

烃的衍生物知识点归纳烃是由碳和氢元素组成的有机化合物家族,是天然气、煤油和石油的主要成分。
由于其分子结构简单,烃具有许多重要的应用领域,包括燃料、化学原料和制药等。
本文将整理烃的衍生物知识点,以帮助读者更好地了解烃化合物的特性和应用。
1. 烃的分类烃可以根据碳原子的结构和连接方式进行分类。
最简单的烃是烷烃,由单个碳-碳单键组成。
其他类别包括烯烃(含有碳-碳双键)和炔烃(含有碳-碳三键)。
2. 烃的命名烃的命名方法基于碳原子的数量和连接方式。
烷烃的命名使用前缀和后缀的组合,例如甲烷、乙烷、丙烷等。
烯烃和炔烃的命名使用前缀、中缀和后缀,例如乙烯、丙烯、乙炔等。
3. 烃的物理特性烃的物理特性与其分子结构和分子量有关。
通常,烃具有较低的沸点和熔点,是易燃的液体或气体。
随着分子量的增加,烃的密度和黏度也会增加。
4. 烃的化学性质烃的化学性质主要与有机反应有关。
对于烃基本上是非极性分子,它们通常不会发生直接的化学反应。
然而,通过在化学反应中引入适当的催化剂、温度和压力条件,烃可以被氧化、加成、取代等。
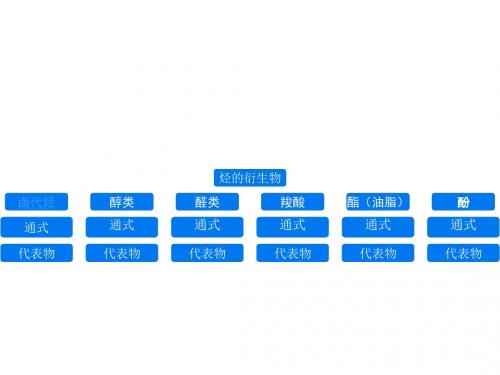
5. 烃的衍生物烃衍生物是通过对烃进行功能化改变而产生的化合物。
主要的烃衍生物包括醇、醚、酮、羧酸、醛、胺、卤代烃等。
6. 烯烃的衍生物烯烃衍生物是通过对烯烃进行不同的反应而形成的。
烯烃的衍生物包括环烯烃、烯烃醇、烯烃醛、烯烃酸等。
7. 炔烃的衍生物炔烃衍生物是通过对炔烃进行不同的反应而形成的。
炔烃的衍生物包括环炔烃、炔烃醇、炔烃醛、炔烃酸等。
8. 烷烃的衍生物烷烃衍生物是通过对烷烃进行不同的反应而形成的。
烷烃的衍生物包括醇、醚、酮、醛、胺、酸等。
9. 烃衍生物的应用烃衍生物广泛应用于多个领域。
醇是重要的溶剂和溶剂中间体,醚常用作溶剂、非极性溶剂和反应中间体,酮可以用作溶剂、溶剂中间体和有机合成中间体,羧酸常用于制备酯类化合物,胺是重要的有机合成试剂等。
10. 烃衍生物的制备方法烃衍生物的制备方法多种多样,包括催化加氢、氧化、取代、加成等。

高中化学烃的衍生物知识点化学是我们生活中广泛应用的学科,也是高中学业中流程科目之一。
其中烃是很重要的一个化学分支,包括一类由碳和氢原子组成的有机化合物。
烃的衍生物非常广泛,有很多在生活中被广泛使用,下面就介绍一下高中化学中关于烃衍生物的知识点。
一、烃的衍生物简介烃的衍生物是由烃分子中的一个或多个氢原子被其他原子或分子所取代的化合物。
根据取代基的不同,烃的衍生物可以分为醇、酚、醛、酮、羧酸、酯、胺、腈、卤代烃、烷基卤化物以及芳族烃等多种。
这些化合物在工业化学及日常生活中应用广泛,如酒精、羧酸类化合物、氨、麻醉剂等。
二、醇醇是烃的一种衍生物,它的分子中含有一个或多个羟基(-OH)。
醇以它的羟基而得名,例如甲醇、乙醇和丙醇等。
醇有许多性质和功能,其中最常见的是作为饮料或用于生产其他有机化合物,比如酯。
三、酚酚是一种由苯环上的一个氢原子被羟基所取代的有机化合物,化学式为C6H5OH。
酚可以作为消毒剂、防腐剂和颜料等方面的原料,同时也可制成不少药品,例如阿司匹林、麻醉剂。
但由于酚具有剧烈的腐蚀性和毒性,过度使用会引起严重的健康问题。
四、醛与酮醛和酮都是由烃分子中的碳氢键被氧原子所取代的化合物。
它们之间的区别是醛分子中有一个羰基(C=O),而酮分子中有两个羰基。
常见的醛包括甲醛和乙醛,可以用于杀菌、熏蒸等方面;酮则包括丙酮、己酮等,可以用于催化反应、制作绝缘材料。
五、羧酸羧酸分子中含有一个羧基(-COOH),能够与醇或胺形成酯或酰胺。
羧酸可以分为饱和脂肪酸和不饱和脂肪酸。
饱和脂肪酸存在于许多生物中,例如麻油、黄油、椰子油等,而不饱和脂肪酸则分布在水生和陆生动物中,例如鱼油、坚果等。
六、酯酯分子中含有一个羧酸和一个醇分子中的氢原子被取代掉了,能够用于制备香料、溶剂等。
酯可以按是否含有羰基分为二元酯和酸酐。
二元酯是指含有一个酸基和一个醇基的酯,例如甲酸乙酯、乙酸丙酯等。
而酸酐是由两个酸分子的羧基进行结合形成的,例如醋酸酐。

可编辑修改精选全文完整版烃的衍生物知识总结一、卤代烃(代表物C 2H 5Br ):烃分子中的氢原子被卤素原子取代后的产物。
(卤素原子) 1、通式: C n H 2n+1X 、 R —X 2、化学性质:(1)、取代反应:C 2H 5Br + H 2O C 2H 5OH + HBr (水解反应)C 2H 5Br + NaOH C 2H 5OH + NaBr(2)、消去反应:C 2H 5Br + NaOH CH 2==CH 2↑+ NaBr +H 2O 3、卤代烃中卤素原子的检验:取少量卤代烃,加NaOH 溶液,加热,一段时间后加HNO 3酸化后再加AgNO 3,如有白色沉淀说明有Cl ¯,如有浅黄色沉淀则有Br ¯,如有黄色沉淀则有I ¯。
二、醇(代表物:CH 3CH 2OH )1、通式:R —OH ,饱和一元醇C n H 2n+1OH2、化学性质:(1)非电解质,中性,不电离出H+; (2)与K 、Ca 、Na 等活泼金属反应放出H 2; 2C 2H 5OH + 2Na 2C 2H 5ONa + H 2↑(3)氧化反应:燃烧:C 2H 5OH +3O 2 2CO 2 +3H 2O 催化氧化:2C 2H 5OH + O 2 2CH 3CHO + H 2O(4)脱水生成乙烯或乙醚。
消去反应: C 2H 5OH CH 2==CH 2↑+ H 2O 取代反应:2C 2H 5OH CH3CH 2OCH 2CH 3+ H 2O(5三、酚(代表物:) 1、化学性质:(1)、弱酸性:酸性: + NaOH + H 2O弱酸性: + H 2O + CO 2 + NaHCO 3(强酸制弱酸)(2)、取代反应: + 3Br 2↓ + 3HBr (3)、显色反应:与Fe 3+反应生成紫色物质 四、醛(代表物:CH 3CHO 、HCHO )1、通式:RCHO ,一元饱和醛:C n H 2n+1CHO ,分子式:C n H 2n O2、化学性质:(1)、加成反应:CH 3CHO + H 2催化剂 △CH 3CH 2OH (还原反应)NaOH △醇 △—OH —OH—ONa—ONa —OH —OH —OH BrBrBr点燃Cu 或Ag △浓硫酸170℃浓硫酸 140℃△(2)、氧化反应:①催化氧化:2CH 3CHO + O 2催化剂 △2CH 3COOH②银镜反应:CH 3CHO +2 Ag (NH 3)2OH△2Ag ↓+ CH 3COONH 4 +3 NH 3 + H 2O③与新制Cu (OH )2反应:CH 3CHO + 2Cu (OH )2△Cu 2O + CH 3COOH + 2H 2O3、制法:(1)乙烯氧化法 (2)乙炔水化法 (3)乙醇氧化法 五、羧酸(代表物: CH 3COOH 、HCOOH )1、通式:R —COOH ,一元饱和酸C n H 2n+1COOH ,分子式C n H 2n O 22、化学性质:(1)具有酸的通性(羧酸盐几乎全溶于水):CH 3COOH + NaOH === CH 3COONa + H 2O2CH 3COOH +2 Na → 2CH 3COONa + H 2↑ CH 3COOH + NaHCO 3→ CH 3COONa + H 2O+CO 2↑ (2)与醇酯化成酯(酸脱羟基醇脱氢): CH 3COOH + CH 3CH 2OH浓硫酸 △CH 3COOCH 2CH 3 + H 2O(3)甲酸、甲酸盐、甲酸形成的酯都具有醛基能发生银镜反应。

第3章烃的衍生物第一节卤代烃一、卤代烃1.定义烃分子中的氢原子被卤素原子取代后生成的化合物称为卤代烃。
官能团是碳卤键,可表示为R—X(X=F、Cl、Br、I)。
2.分类3.物理性质(1)状态:常温下,卤代烃中除个别为气体外,大多为液体或固体。
如一氯甲烷为气体。
(2)溶解性:卤代烃不溶于水,可溶于有机溶剂,某些卤代烃本身就是很好的有机溶剂,如CCl4、氯仿(CHCl3)等。
(3)密度与沸点:①卤代烃的密度和沸点都高于相应的烃;②卤代烃的密度一般随烃基中碳原子数目的增加而减小,如ρ(CH3Cl)>ρ(CH3CH2Cl);③卤代烃的沸点一般随碳原子数目的增加而升高,如沸点CH3Cl<CH3CH2Cl。
4.卤代烃的系统命名——类似于烃的命名方法二、溴乙烷的结构与性质1.溴乙烷的物理性质纯净的溴乙烷是无色液体,沸点是38.4 ℃,密度比水的大,难溶于水,可溶于多种有机溶剂(如乙醇、苯、汽油等)。
2.溴乙烷的分子结构3.溴乙烷的化学性质(1)取代反应——又称水解反应①条件:NaOH水溶液、加热。
②反应方程式:C 2H5—Br+NaOH――→水△C2H5—OH+NaBr。
③反应原理:(2)消去反应——又称为消除反应。
①条件:NaOH的乙醇溶液、加热。
②反应方程式:(以溴乙烷为例)CH3CH2Br+NaOH――→乙醇△CH2===CH2↑+NaBr+H2O。
③反应原理:④定义:有机化合物在一定条件下,从一个分子中脱去一个或几个小分子(如H2O、HX等),而生成含不饱和键的化合物的反应叫做消去反应(消除反应)。
(3)加成和加聚反应含有不饱和键(如)的卤代烃也可以发生加成和加聚反应。
①氯乙烯加聚反应生成聚氯乙烯:。
②四氟乙烯加聚反应生成聚四氟乙烯:。
三、卤代烃破坏臭氧层原理(了解)氟利昂可在强烈的紫外线作用下分解,产生的氯原子自由基会对臭氧层产生长久的破坏作用。
以CCl3F为例,它破坏臭氧层的反应过程可表示为:CCl3F――→紫外线CCl2F·+Cl·卤代烃的主要性质及检验1.卤代烃的消去反应和取代反应的比较消去反应取代反应卤代烃的结构特点与卤素原子相连的碳原子的邻位碳原子上有氢原子一般是1个碳原子上只有1个—X反应实质脱去1个HX分子,形成不饱和键—X被—OH取代反应条件强碱的醇溶液、加热强碱的水溶液、加热化学键变化主要产物烯烃或炔烃醇2.卤代烃消去反应的规律(1)没有邻位碳原子的卤代烃不能发生消去反应。

烃的衍生物知识归纳总结一、溴乙烷与卤代烃溴乙烷1、溴乙烷的分子组成:结构简式:。
注意:(1)乙烷分子为非极性分子,而溴乙烷为极性分子。
(2)溴乙烷的官能团为溴原子。
(3)溴乙烷是非电解质,在水溶液中(实际上不溶于水)或熔化状态下均不电离。
2、溴乙烷的物理性质:纯净的溴乙烷是无色液体,沸点38.4度,密度比水轻不溶于水,易溶于乙醇等多种有机溶剂。
3、溴乙烷的化学性质a 溴乙烷的水解反应:b 溴乙烷的消去反应反应方程式:反应条件:有强碱的醇溶液存在,加热。
反应特点:溴乙烷的反应是从分子中相邻的碳原子上脱去一个溴化氢分子,有机物由饱和变为不饱和。
消去反应的概念:有机化合物在一定条件下,从一个分子中脱去一个小分子生成不饱和化合物的反应叫消去反应。
卤代烃1、卤代烃的概念:烃分子中的氢原子被卤素原子取代后生成的化合物叫卤代烃2、卤代烃的分类:根据卤素原子的不同可以分为氟代烃、氯代烃、溴代烃和碘代烃。
根据卤素原子的个数不同,可以分为一卤代烃和多卤代烃。
根据烃基的种类不同可以分为饱和卤代烃和不饱和卤代烃。
3、卤代烃的物理性质:(1)溶解性:不溶于水可以溶于大多数有机溶剂。
(2)有关卤代烃沸点的总结:1在一系列正某烷的一氯代烃中,随分子里的碳原子数增加(相对分质量逐渐增大),物质的沸点逐渐升高。
2、分子数相同的一氯代烷中,主链长的比主链短的沸点高。
4、卤代烃的化学性质:(1)取代反应(水解反应):所有卤代烃都可以发生水解反应。
(2)消去反应:a 能发生消去反应的氯代烃必须具备两个条件:一是分子中碳原子大于二;二是与卤原子相连的碳原子的邻碳上必须有氢原子。
(3)卤代烃发生消去反应和水解反应的外界条件不同:在碱和醇存在的的条件的条件下发生消去反应,在碱和水存在的条件下发生水解反应。
5、卤代烃中卤素元素的检验:卤代烃不溶于水,也不能电离出卤素原子,分子中的卤素原子检验步骤如下:(1)首先将卤代烃与过量的氢氧化钠溶液混合,充分震荡,加热。
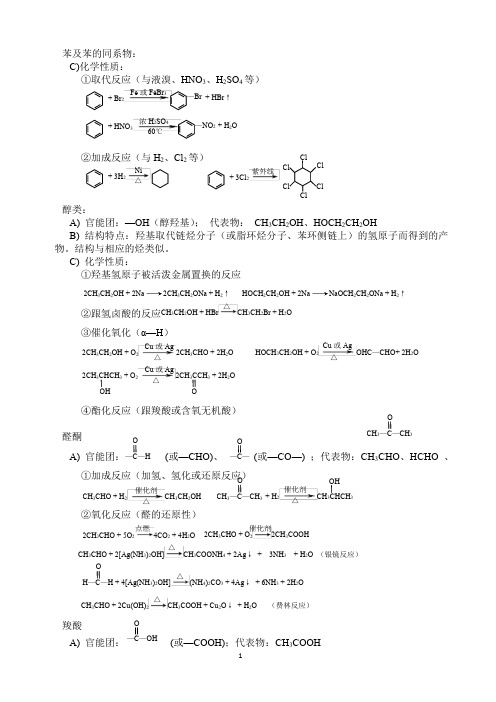
苯及苯的同系物: C)化学性质:①取代反应(与液溴、HNO 3、H 2SO 4等)②加成反应(与H 2、Cl 2等)醇类:A) 官能团:—OH (醇羟基); 代表物: CH 3CH 2OH 、HOCH 2CH 2OHB) 结构特点:羟基取代链烃分子(或脂环烃分子、苯环侧链上)的氢原子而得到的产物。
结构与相应的烃类似。
C) 化学性质:①羟基氢原子被活泼金属置换的反应②跟氢卤酸的反应 ③催化氧化(α—H )④酯化反应(跟羧酸或含氧无机酸) 醛酮A) 官能团:(或—CHO)、 (或—CO —) ;代表物:CH 3CHO 、HCHO 、 ①加成反应(加氢、氢化或还原反应)②氧化反应(醛的还原性)羧酸A) 官能团: (或—COOH);代表物:CH 3COOH2CH 3CH 2OH + 2Na2CH 3CH 2ONa + H 2↑ HOCH 2CH 2OH + 2NaNaOCH 2CH 2ONa + H 2↑CH 3CH 2OH + HBr CH 3CH 2Br + H 2O△2CH 3CH 2OH + O 22CH 3CHO + 2H 2O △ Cu 或AgHOCH 3CH 2OH + O 2OHC —CHO+ 2H 2O△Cu 或Ag 2CH 3CHCH 3 + O 22CH 3CCH 3 + 2H 2OOHO△Cu 或AgO—C —H O—C —O CH 3—C—CH 3CH 3CHO + H 2CH 3CH 2OH△催化剂 + H 2CH 33OH OCH 3—C —CH 3 △催化剂 2CH3CHO + 5O24CO 2 + 4H 2O 点燃CH 3CHO + 2[Ag(NH 3)2OH]CH 3COONH 4 + 2Ag ↓ + 3NH3 + H 2O (银镜反应)△CH 3CHO + 2Cu(OH)2CH 3COOH + Cu 2O ↓ + H 2O (费林反应)△2CH 3CHO + O 22CH 3COOH 催化剂OH —C —H + 4[Ag(NH 3)2OH](NH 4)2CO 3 + 4Ag ↓ + 6NH 3 + 2H 2O△O—C —OH + Br 2+ HBr ↑ Br Fe 或FeBr 3+ HNO 3+ H 2O NO 2 浓H 2SO 460℃ + 3H 2Ni △+ 3Cl 2 紫外线C) 化学性质:①具有无机酸的通性 ②酯化反应 酯类A) 官能团:(或—COOR )(R 为烃基); 代表物: CH 3COOCH 2CH 3 C) 化学性质:水解反应(酸性或碱性条件下)与Na 反应的有机物:含有—OH 、—COOH 的有机物.与NaOH 反应的有机物:常温下,易与含有 酚羟基...、—COOH 的有机物反应加热时,能与卤代烃、酯反应(取代反应)与Na 2CO 3反应的有机物:含有酚.羟基的有机物反应生成酚钠和NaHCO 3;含有—COOH 的有机物反应生成羧酸钠,并放出CO 2气体;与NaHCO 3反应的有机物:含有—COOH 、—SO 3H 的有机物反应生成羧酸钠、磺酸钠并放出等物质的量的CO 2气体。

《烃和烃的衍生物我》知识点整理一、重要的物理性质1.有机物的溶解性(1)难溶于水的有:各类烃、卤代烃、硝基化合物、酯、绝大多数高聚物、高级的(指分子中碳原子数目较多的,下同)醇、醛、羧酸等。
(2)易溶于水的有:低级的[一般指N(C)≤4]醇、(醚)、醛、(酮)、羧酸及盐、氨基酸及盐、单糖、二糖。
(它们都能与水形成氢键)。
(3)具有特殊溶解性的:① 乙醇是一种很好的溶剂,既能溶解许多无机物,又能溶解许多有机物,所以常用乙醇来溶解植物色素或其中的药用成分,也常用乙醇作为反应的溶剂,使参加反应的有机物和无机物均能溶解,增大接触面积,提高反应速率。
例如,在油脂的皂化反应中,加入乙醇既能溶解NaOH,又能溶解油脂,让它们在均相(同一溶剂的溶液)中充分接触,加快反应速率,提高反应限度。
② 苯酚:室温下,在水中的溶解度是9.3g(属可溶),易溶于乙醇等有机溶剂,当温度高于65℃时,能与水混溶,冷却后分层,上层为苯酚的水溶液,下层为水的苯酚溶液,振荡后形成乳浊液。
苯酚易溶于碱溶液和纯碱溶液,这是因为生成了易溶性的钠盐。
③乙酸乙酯在饱和碳酸钠溶液中更加难溶,同时饱和碳酸钠溶液还能通过反应吸收挥发出的乙酸,溶解吸收挥发出的乙醇,便于闻到乙酸乙酯的香味。
④有的淀粉、蛋白质可溶于水形成胶体..。
蛋白质在浓轻金属盐(包括铵盐)溶液中溶解度减小,会析出(即盐析,皂化反应中也有此操作)。
但在稀轻金属盐(包括铵盐)溶液中,蛋白质的溶解度反而增大。
⑤线型和部分支链型高聚物可溶于某些有机溶剂,而体型则难溶于有机溶剂。
⑥氢氧化铜悬浊液可溶于多羟基化合物的溶液中,如甘油、葡萄糖溶液等,形成绛蓝色溶液。
2.有机物的密度(1)小于水的密度,且与水(溶液)分层的有:各类烃、一氯代烃、酯(包括油脂)(2)大于水的密度,且与水(溶液)分层的有:多氯代烃、溴代烃(溴苯等)、碘代烃、硝基苯3.有机物的状态[常温常压(1个大气压、20℃左右)](1)气态:① 烃类:一般N(C)≤4的各类烃注意:新戊烷[C(CH3)4]亦为气态② 衍生物类:一氯甲烷(....-.29.8℃...2.F.2.,沸点为.....)......CH..3.Cl..,.沸点为...-.24.2℃.....)氟里昂(.....CCl氯乙烯(....,沸点为....CH..2.==CHCl...).....HCHO....-.21℃.....)甲醛(......,沸点为....-.13.9℃℃.).一溴甲烷(CH3Br,沸点为3.6℃)氯乙烷(....CH..3.CH..2.C.l.,沸点为........12.3四氟乙烯(CF2==CF2,沸点为-76.3℃)甲醚(CH3OCH3,沸点为-23℃)甲乙醚(CH3OC2H5,沸点为10.8℃)环氧乙烷(,沸点为13.5℃)(2)液态:一般N(C)在5~16的烃及绝大多数低级衍生物。

高中化学烃及其衍生物知识点详解一、烃的概念与分类1. 概念:烃是只含有碳和氢两种元素的有机物。
2. 分类:饱和烃(烷烃):分子中所有的碳原子都形成四个单键,如甲烷(CH₄)、乙烷(C₂H₆)等。
不饱和烃:分子中含有碳碳双键或碳碳三键的烃。
烯烃:分子中含有一个或多个碳碳双键的烃,如乙烯(C₂H₄)、丙烯(C₃H₆)等。
炔烃:分子中含有一个或多个碳碳三键的烃,如乙炔(C₂H₂)、丙炔(C₃H₄)等。
二、烃的物理性质状态:随着碳原子数的增加,烷烃由气态逐渐过渡到液态、固态。
熔沸点:随着碳原子数的增加,熔沸点逐渐升高。
溶解度:烃类都不溶于水,但易溶于有机溶剂。
三、烃的化学性质1. 取代反应:烷烃在光照条件下与卤素单质发生取代反应,生成卤代烃和卤化氢。
例如:CH₄ + Cl₂ →CH₃Cl + HCl2. 加成反应:烯烃和炔烃能与卤素单质、氢气等发生加成反应。
例如:CH₂=CH₂ + Br₂ →CH₂BrCH₂BrCH₂=CH₂ + H₂ →CH₃CH₃3. 氧化反应:烷烃在燃烧时发生氧化反应,生成二氧化碳和水。
烯烃和炔烃也能被高锰酸钾等氧化剂氧化。
例如:2CH₃CH₂CH₂CH₃ + 13O₂ →8CO₂ + 10H₂OCH₂=CH₂ + KMnO₄ →CO₂ + H₂O四、烃的衍生物烃分子中的氢原子被其他原子或原子团所取代而生成的一系列化合物称为烃的衍生物。
常见的烃的衍生物包括卤代烃、醇、酚、醛、酮、羧酸、酯等。
1. 卤代烃:烃分子中的氢原子被卤素原子取代而形成的化合物。
例如:氯乙烷(CH₃CH₂Cl)、溴苯(C₆H₅Br)等。
2. 醇:烃分子中的一个或多个氢原子被羟基(-OH)取代而形成的化合物。
例如:乙醇(C₂H₅OH)、丙三醇(C₃H₈O₃)等。
3. 酚:苯环上的氢原子被羟基取代而形成的化合物。
例如:苯酚(C₆H₅OH)。
4. 醛:烃基与醛基(-CHO)相连而形成的化合物。
例如:甲醛(HCHO)、乙醛(CH₃CHO)等。

烃的衍生物-规律•易混点•易错点I.性质•制法•鉴别一.卤代烃:(以饱和一元卤代烃为代表物.通式:C n H2n+1X)化学性质:1.消去反应:⑴.条件:与NaOH醇溶液共热(无水条件下,醇作溶剂)。
⑵.结果:形成碳碳不饱和键。
⑶.反应举例:⑷.特例:*①.扎依采夫定则:当消去反应有两种可能时,卤素原子主要与其所连碳原子邻旁含氢较少的碳原子上的氢原子发生消去反应。
*②.多元卤代烃的消去反应:一般来说,卤代烃分子中有多少个卤原子,经过完全消去就能形成多少碳碳不饱和键。
⑸.不能发生消去反应的卤代烃:①.分子中只有1个碳原子的卤代烃。
如CH3X、CH2X2、CHX3等。
②.卤素原子所连碳原子邻旁碳原子上不含氢原子的卤代烃。
如R-C(CH3)2CHXC(C2H5)CH3、CR3-CH2X.2.水解反应:⑴.条件:与NaOH水溶液共热。
⑵.结果:发生取代反应,生成含羟基的化合物。
⑶.反应举例:CH3CH2Cl+H2O CH3CH2OH+HCl.⑷.特例:多元卤代烃的水解反应:①.当卤原子连在不同碳原子上时:完全水解时生成多元醇。
②.当卤原子连在相同碳原子上时:i.同一碳原子上连两个卤原子:完全水解时生成醛。
R-CHX2+H2O R-CHO+2HX.ii.同一碳原子上连3个卤原子:完全水解时生成羧酸。
R-CX3+H2O R-COOH+3HX.*③.双键碳原子及苯环碳原子上的卤原子不易发生水解反应。
制法:1.卤代反应:⑴.烷烃卤代:属于链锁反应,制得的产物不纯。
一般不用。
例如:CH4+Cl2CH3Cl+HCl.⑵.醇与卤化氢反应:RCH2OH+HX→RCH2X+H2O.*⑶.烯烃α-氢原子的高温卤代:只生成一元卤代物。
CH3-CH=CH2+Cl2Cl-CH2-CH=CH2+HCl.⑷.醛、羧酸α-氢原子的卤代:CH3-CHO+3Cl2→CCl3-CHO+3HCl. CH3-COOH+3Cl2→CCl3-COOH+3HCl.2.加成反应:⑴.加卤素:生成多元卤代物。

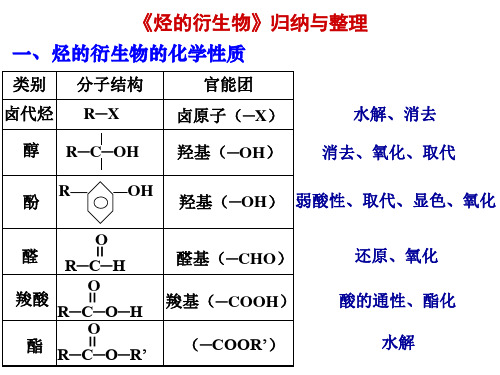


1.烃的衍生物的比较
类别官能团分子结构特点分类主要化学性质卤
代烃卤原子
(-X)
碳-卤键
(C-X)有极性,
易断裂
烃、氯代烃、溴代烃
②一卤代烃和多代卤烃;
③饱和卤代烃、不饱和卤代
烃和芳香卤代烃
①取代反应(水解反应):
R-X+H2O R-OH + HX
②消去反应:
R-CH2-CH2X + NaOH RCH=H2 + NaX + H2O
醇
均为羟基
(-OH)-OH在非苯环碳
原子上
①脂肪醇(包括饱和醇、不饱
和醇);②脂环醇(如环己醇)
③芳香醇(如苯甲醇)
④一元醇与多元醇
(如乙二醇、丙三醇)
①取代反应:a.与Na等活泼金属反应;b.与HX反应;
c.分子间脱水;d.酯化反应。
②氧化反应:2R-CH2OH + O22R-CHO+2H2O
③消去反应,CH3CH2OH CH2=CH2↑+ H2O
酚-OH直接连在苯
环上.酚类中均
含苯的结构
一元酚、二元酚、三元酚等
被空气氧化而变质;②具有弱酸性
③取代反应④显色反应⑤缩聚反应
醛
醛基
(-CHO)分子中含有醛基
的有机物
①脂肪醛(饱和醛和不饱和
醛);②芳香醛;
③一元醛与多元醛
①加成反应:R-CHO+H2R-CH2OH
②氧化反应:a.银镜反应;b.与新制Cu(OH)2反应:c.在
一定条件下,被空气氧化
羧酸
羧基
(-COOH)分子中含有羧基
的有机物
①脂肪酸与芳香酸;
②一元酸与多元酸;
③饱和羧酸与不饱和羧酸;
④低级脂肪酸与高级脂肪酸
①具有酸的通性;
②酯化反应
羧酸酯酯基
(R为烃基或H
原子,R′只能为
烃基)
①饱和一元酯:
C n H2n+1COOC m H2m+1
②高级脂肪酸甘油酯
③聚酯
④环酯
水解反应:
RCOOR′+ H2O RCOOH + R'OH
RCOOR′+ NaOH RCOONa + R'OH
(酯在碱性条件下水解较完全)
2.有机反应的主要类型
反应类型定义举例(反应的化学方程式)
消去反应有机物在一定条件下,从一个分子中脱去一个小分
子(如H2O、HBr等)而生成不饱和(含双键或叁键)
化合物的反应
C2H5OH CH2=CH2↑+ H2O
苯酚的显色反应苯酚与含Fe3+的溶液作用,使溶液呈现紫色的反应
还原反应有机物分子得到氢原子或失去氧原子的反应CH≡CH + H2CH2=CH2 CH2=H2 + H2CH3CH3 R—CHO + H2R-CH2OH
氧化反应燃烧或被空气中
的O2氧化
有机物分子得到氧原子或失去氢原子的反应
2CH3CH2OH + O2 2CH3CHO + 2H2O
2CH3CHO + O2 2CH3COOH
银镜反应CH
3CHO + 2Ag(NH3)2OH CH3COONH4+2Ag↓+ 3NH3↑+ H2O
红色沉淀反应CH
3CHO + 2Cu(OH)2CH3COOH + Cu2O↓+ 2H2O
取代反应卤代烃水解
NaOH水溶液,卤代烃水解,生成醇和卤化氢的反
应
R-CH2X + H2O RCH2OH + HX 酯化反应
酸(无机含氧酸或羧酸)与醇作用,生成酯和水的反
应
RCOOH + R'CH2OH RCOOCH2R′+ H2O 酯的水解反应
在酸或碱存在的条件下,酯与水作用生成醇与酸的
反应
RCOOR′+ H2O RCOOH + R'OH
RCOOR′+ NaOH → RCOONa + R'OH
4.醇、酚、羧酸中羟基的活性比较
羟基种类重要代表物与Na反应
与NaOH反
应
与Na2CO3反应
醇羟基CH3CH2-OH√××
酚羟基
HO
√√√但不放出气体
羧酸羟基
CH3-C-OH
O
√√√放出CO2。