新版大学有机化学知识点整理考试必备-新版.pdf
- 格式:pdf
- 大小:13.68 KB
- 文档页数:6

完整版大学有机化学知识点整理考试必备一、基础概念1. 有机化学的定义2. 同分异构体的定义和分类3. 共价键的构成和性质4. 电子云模型和分子轨道模型5. 共轭体系和杂环化合物的概念6. 化学平衡7. 离子的化学性质8. 酸碱性及其影响因素二、物质分类和性质1. 醇的性质及其与酸反应2. 烷基卤化酯的性质及其合成3. 胺的性质及其与酸碱反应4. 羧酸的性质及其合成5. 酯的性质及其制备、加成和加水反应6. 假脂类的性质及其与酸碱的反应7. 烷基磺酸酯的性质及其合成8. 脂肪族化合物的氧化和还原反应三、化学反应和机理1. 反应速率和速率常数2. 化学反应的平衡常数3. 酸催化和碱催化的化学反应4. 木质素的生物合成和人工合成5. 光化学反应的能量和机理6. 重绝旋化合物的立体化学和合成方法7. 质子转移催化的克鲁森斯基反应和迈克尔加成反应8. 半羧酸的制备和酯化反应四、有机分析和表征1. 元素分析和红外光谱分析2. 液体和气相色谱分析3. 质谱和核磁共振分析4. 过氧化氢值的测定和比色法分析5. 紫外光谱和拉曼光谱分析6. 纯度的测定和晶体衍射分析7. 氢谱和电子自旋共振分析8. 光电子能谱和电子能损谱分析五、应用和前沿1. 医药,例如:阿司匹林的合成和应用2. 食品,例如:食用油的合成和性质3. 环境,例如:污染物的分析和去除4. 原料化工和新能源,例如:糖基化合物的生产和利用5. 生物学和材料科学,例如:合成生物材料和功能化金属氧化物6. 多相催化和光化学反应机理研究7. 有机化学的计算方法和机器学习应用8. 网络化学和人工智能发展对有机化学的影响有机化学知识点非常广泛深奥,以上只是其中一部分,仅供参考。
在学习过程中,建议多数练习和思考,加强理解和记忆。

链烷烃1、新(neo):表示第二位碳原子上带有两个甲基2、命名时,较优基团后列出:甲基、乙基、丙基、丁基、戊基、异戊基、异丁基、新戊基、异丙基、仲丁基、叔丁基3、在支链烷烃中,相对分子质量相同时,对称性好的熔点较高4、相同碳数的烷烃,支链越多,其相对密度越小5、烷基自由基的相对稳定性:甲基最不稳定6、卤化反应:条件——光照决定反应速度的步骤是:夺氢过程卤素反应活性:氟氯溴碘氢反应活性:根据烷基稳定性判断(越稳定越易生成)7、溴化具有很高的选择性环烷烃1、卤代反应:五元环、六元环2、加氢:三元环、四元环、五元环(Ni作催化剂,所需温度逐渐升高)3、加卤素:三元环室温,四元环温热4、加卤化氢:只有三元环5、不对称环丙烷加HX 的规律:①开环位置:在含氢最多与含氢最少的两个碳之间②氢加在含氢较多的碳原子上。
6、O260%HNO3100o C HOOC(CH2)4COOH7、环丙烷不使KMnO4水溶液褪色,可用此区别:环丙烷和不饱和烃8、三键与银氨离子反应有白色沉淀9、键角变形程度越大,张力越大。
张力越大,环的稳定性越低,反应性越大。
环戊烷、环己烷偏转角度最小,也最稳定。
10、椅式是环己烷的最稳定的构象,在各种构象的平衡混合中,椅式占99.9%。
多环烃中,含椅式最多的构象为最稳定的构象。
平伏键(e键),直立键(a键)11、一取代环己烷最稳定构象是取代基在e键上。
多取代环己烷,e取代基最多的构象最稳定。
多取代环己烷,体积较大的取代基为e型的构象最稳定。
取代基体积越大,e取代占的比例越大。
烯烃1、正构(无支链)端烯烃称为α-烯烃,与双键碳直接相连的饱和碳称为α-C,其上的氢称为α-H。
2、在不发生化学反应的情况下,顺式(Z )不可能转变成反式(E )。
3、含两个及以上双键的烯烃称为某二烯、某三烯、某四烯等,用数字详细说明双键的位置。
4、写名称时把双键的Z 或E 构型用“()”标在前面并注明位号。
5、与HX 反应(与X2也是):反应活性——取代烃基多的反应活性大(因为R 有+I 效应,使C 上电子云密度变高,有利于H+作用6、一般热力学稳定性好的烯烃,其亲电加成反应活性也高。

大一有机考试知识点总结有机化学是化学的重要分支之一,也是大学化学课程中的重要内容之一。
下面是大一有机化学考试中的重要知识点总结。
1. 化学键的类型:- 单键:由两个原子共享一对电子而形成的键。
- 双键:由两个原子共享两对电子而形成的键。
- 三键:由两个原子共享三对电子而形成的键。
2. 饱和与不饱和化合物:- 饱和化合物:每个碳原子的化合价都用完,并且没有多余的键。
例如甲烷(CH4)。
- 不饱和化合物:至少存在一对碳原子之间的双键或三键。
例如乙烯(C2H4)。
3. 碳的立体化学:- 手性:一个分子非对称,不能与其镜像重叠的性质。
手性分子具有两个互为镜像的异构体,称为手性体。
- 手性中心:一个碳原子连接着四个不同的基团时,就形成一个手性中心。
手性中心也被称为立体中心。
4. 碳的杂化轨道:- sp3杂化轨道:四个σ键,四个sp3杂化轨道。
例如甲烷的碳原子。
- sp2杂化轨道:三个σ键和一个π键,三个sp2杂化轨道。
例如乙烯的碳原子。
- sp杂化轨道:两个σ键和两个π键,两个sp杂化轨道。
例如乙炔的碳原子。
5. 反应机理:- 亲核取代反应:亲核试剂攻击含有部分正电荷的反应物,将原来的基团替换掉。
- 亲电取代反应:亲电试剂从反应物中吸引电子,形成新的键。
- π加成反应:π电子云中的电子攻击亲电试剂。
6. 重要的反应类型:- 加成反应:两个分子结合形成一个新的分子。
例如烯烃加成反应。
- 消除反应:一个分子分解成两个或多个分子。
例如脱水反应。
- 变位反应:化学键的重新组合而成不同的构型。
例如环化反应。
- 氧化还原反应:涉及电子的转移。
例如醛酮的氧化反应。
- 反应类型与机构的学习与辨认:了解不同反应类型和机构的特点,并能根据反应过程和产物识别反应类型和机构。
这些是大一有机化学考试中的重要知识点总结。
希望对你的学习有所帮助!。

最新大学有机化学复习总结、试剂的分类与试剂的酸碱性 自由(游离)基引发剂 在自由基反应中能够产生自由基的试剂叫自由基引发剂(free radical in itiator),产生自由基的过程叫链引发。
如:hv 或高温… Br 2CI ・ Br 2均裂CI 2、Br 2是自由基引发剂,此外,过氧化氢、过氧化苯甲酰、偶氮二异丁氰、过硫 酸铵等也是常用的自由基引发剂。
少量的自由基引发剂就可引发反应,使反应进行 下去。
2、亲电试剂简单地说,对电子具有亲合力的试剂就叫亲电试剂(electrophilicreage nt )。
亲电试剂一般都是带正电荷的试剂或具有空的 p 轨道或d 轨道,能够接 受电子对的中性分子,女口: H 十、CIS Br +> RCH 2 +> CH 3CO + > NO 2 +> + SO 3H 、SO 3、BF 3、AICI 3等,都是亲电试剂。
在反应过程中,能够接受电子对试剂,就是路易斯酸( Lewis acid ),因此,路易斯酸就是亲电试剂或亲电试剂的催化剂。
3、 亲核试剂 对电子没有亲合力,但对带正电荷或部分正电荷的碳原子具有亲合力的试剂叫亲核试剂(n ucleophilic reage nt )。
亲核试剂一般是带负电荷的试剂或 是带有未共用电子对的中性分子,如:OH 一、HS 一、CN 一、NH 2_、RCH 2_、RO 一、RS _、PhO _、RCOO _、X _、H 2O 、ROH 、ROR 、NH 3、RNH 2等,都是亲核试剂。
在反应过程中,能够给出电子对试剂,就是路易斯碱(Lewis base ),因此,路 易斯碱也是亲核试剂。
4、 试剂的分类标准在离子型反应中,亲电试剂和亲核试剂是一对对立的矛盾。
如: CH 3ONa + CH 3Br -CH 3OCH 3 + NaBr 的反应中,Na 十和+ CH 3是亲电试剂,而CH 3O 和Br _是亲核试 剂。

大学有机化学笔记整理(精选)(一)引言概述:大学有机化学是化学专业中的一门重要课程,涵盖了有机化合物的结构、性质和反应机制等内容。
本文是对大学有机化学课程进行笔记整理,以帮助学生更好地理解和掌握有机化学的基础知识。
正文内容:大点一:有机化合物的基本结构1. 有机化合物的组成元素2. 有机化合物的键的类型及特点3. 有机化合物的立体构型4. 有机化合物的分子式与结构式表示5. 有机化合物的同分异构体大点二:有机化合物的物理性质1. 有机化合物的颜色2. 有机化合物的溶解性3. 有机化合物的沸点和熔点4. 有机化合物的密度和折射率5. 有机化合物的光学活性大点三:有机化合物的反应机制1. 有机化合物的取代反应2. 有机化合物的加成反应3. 有机化合物的消除反应4. 有机化合物的氧化还原反应5. 有机化合物的重排反应大点四:有机化合物的官能团转化1. 烷烃的官能团转化2. 卤代烃的官能团转化3. 醇的官能团转化4. 酮和醛的官能团转化5. 酸和酯的官能团转化大点五:有机合成的基本方法1. 反应的选择与优化2. 反应条件的控制3. 催化剂的作用与选择4. 有机合成的常用试剂5. 实验技术与安全注意事项总结:大学有机化学是一门让人感到挑战和兴趣并存的科目。
通过本文对有机化学的基础知识进行整理,希望能够帮助学生加深对有机化学的理解,提升学习效果。
在学习过程中,不仅要掌握有机化合物的基本结构和物理性质,还要了解有机化合物的反应机制和官能团转化方法,最终能够运用所学知识进行有机合成。

有机化学知识点归纳一、有机物的结构与性质1 、官能团的定义:决定有机化合物主要化学性质的原子、原子团或化学键。
原子: —X官能团 原子团(基): —OH 、—CHO (醛基) 、—COOH (羧基) 、C 6H 5— 等化学键: C=C 、—C≡C—2、常见的各类有机物的官能团,结构特点及主要化学性质(1)烷烃A) 官能团:无 ;通式: C n H 2n+2;代表物: CH 4B) 结构特点:键角为 109°28′,空间正四面体分子。
烷烃分子中的每个 C 原子的四个价键也都如此。
C) 物理性质: 1.常温下,它们的状态由气态、液态到固态,且无论是气体还是液体,均为无色。
一般地, C1~C4 气态, C5~C16 液态, C17 以上固态。
2.它们的熔沸点由低到高。
3.烷烃的密度由小到大,但都小于 1g/cm^3 ,即都小于水的密度。
4.烷烃都不溶于水,易溶于有机溶剂D) 化学性质:①取代反应(与卤素单质、在光照条件下)CH 4 + Cl 2 CH 3Cl + HCl , CH 3Cl + Cl 2 CH 2Cl 2 + HCl ,……。
点燃②燃烧 CH 4 + 2O 2 CO 2 + 2H 2O高温C 16H 34 催化剂C 8H 18 + C 8H 16加热、加压④烃类燃烧通式: C x H t + (x +y )O 2 点———燃 xCO 2 + y H 2O 4 2⑤烃的含氧衍生物燃烧通式 : C x H y O z + (x +y - z )O 2 点———燃 xCO 2 + yH 2O 4 2 2E) 实验室制法:甲烷: CH 3 COONa + NaOHOCH 4 个 +Na 2 CO 3△注: 1.醋酸钠:碱石灰=1: 3 2.固固加热 3.无水(不能用 NaAc 晶体) 4.CaO :吸水、稀释 NaOH 、不是催化剂(2)烯烃:A) 官能团: C=C ;通式: C n H 2n (n≥2);代表物: H 2C=CH 2B) 结构特点:键角为 120° 。

大学有机化学复习总结(全)-大学有机化学大家好,我是你们的有机化学老师,今天我要给大家讲一下大学有机化学的复习总结。
我要告诉大家一个秘密,其实有机化学并不可怕,只要你用心去学,一定会有所收获。
好了,不多说了,让我们开始吧!一、基础知识1.1 烷基和烯基烷基和烯基是有机化学的基础,它们是构成有机分子的基本单元。
烷基是由碳、氢和一个或多个氧原子组成的链状烃基,常见的烷基有甲烷、乙烷、丙烷等。
烯基是由碳、氢和一个氧原子组成的支链状烃基,常见的烯基有乙烯、丙烯等。
1.2 烃的取代反应烃的取代反应是指在烃分子中加入一个或多个原子或原子团的过程。
例如,将一个氢原子加到甲烷分子中,就可以得到甲基甲烷(CH3)。
这个过程可以用下面的方程式表示:CH3 + H2 → CH3CH21.3 羟基和胺的反应羟基和胺的反应是指羟基与胺分子中的氨基反应生成酰胺的过程。
这个反应在医药工业中有广泛的应用,例如制备青霉素等抗生素。
这个过程可以用下面的方程式表示:NH2 + OH -> NH2OHNH2OH + RCOOR' -> RCOOR' + NH3 + H2O二、官能团及其性质2.1 羧酸和酚的性质羧酸和酚都是含有羧基(-COOH)的化合物,它们的性质有很多相似之处。
例如,它们都可以发生酯化反应、酰胺化反应等。
羧酸和酚还可以通过缩合反应形成醚类化合物。
例如,苯酚可以与甲醛缩合生成环氧树脂。
2.2 醛和酮的性质醛和酮都是含有羰基(C=O)的化合物,它们的性质有很多相似之处。
例如,它们都可以发生氧化反应、还原反应等。
醛和酮还可以通过缩合反应形成高分子化合物。
例如,甲醛可以与苯酚缩合生成酚醛树脂。
三、合成路线设计3.1 基本合成路线设计方法合成路线设计是有机化学研究的核心内容之一。
基本的合成路线设计方法包括以下几个步骤:确定目标产物;选择合适的原料;设计反应条件;优化合成路线;进行实验验证。
在设计合成路线时,要充分考虑原料的来源、价格、易得性等因素。

有机化学知识点归纳(一)一、同系物结构相似,在分子组成上相差一个或若干个CH2原子团的物质。
同系物的判断要点:1、通式相同,但通式相同不一定是同系物。
2、组成元素种类必须相同3、结构相似指具有相似的原子连接方式,相同的官能团类别和数目。
结构相似不一定完全相同,如CH3CH2CH3和(CH3)4C,前者无支链,后者有支链仍为同系物。
4、在分子组成上必须相差一个或几个CH2原子团,但通式相同组成上相差一个或几个CH2原子团不一定是同系物,如CH3CH2Br 和CH3CH2CH2Cl都是卤代烃,且组成相差一个CH2原子团,但不是同系物。
5、同分异构体之间不是同系物。
二、同分异构体化合物具有相同的分子式,但具有不同结构的现象叫做同分异构现象。
具有同分异构现象的化合物互称同分异构体。
1、同分异构体的种类:⑴碳链异构:指碳原子之间连接成不同的链状或环状结构而造成的异构。
如C5H12有三种同分异构体,即正戊烷、异戊烷和新戊烷。
⑵位置异构:指官能团或取代基在碳链上的位置不同而造成的异构。
如1—丁烯与2—丁烯、1—丙醇与2—丙醇、邻二甲苯与间二甲苯及对二甲苯。
⑶异类异构:指官能团不同而造成的异构,也叫官能团异构。
如1—丁炔与1,3—丁二烯、丙烯与环丙烷、乙醇与甲醚、丙醛与丙酮、乙酸与甲酸甲酯、葡萄糖与果糖、蔗糖与麦芽糖等。
⑷其他异构方式:如顺反异构、对映异构(也叫做镜像异构或手性异构)等,在中学阶段的信息题中屡有涉及。
各类有机物异构体情况:⑴C n H2n+2:只能是烷烃,而且只有碳链异构。
如CH3(CH2)3CH3、CH 3CH(CH 3)CH 2CH 3、C(CH 3)4⑵ C n H 2n :单烯烃、环烷烃。
如CH 2=CHCH 2CH 3、CH 3CH=CHCH 3、CH 2=C(CH 3)2、 、⑶C n H 2n -2:炔烃、二烯烃。
如:CH ≡CCH 2CH 3、CH 3C ≡CCH 3、CH 2=CHCH=CH 2⑷ C n H 2n -6、⑸ C n H 2n +2O :饱和脂肪醇、醚。

大学有机化学重点总结引言有机化学是化学中的一个重要分支,研究的是含有碳元素的化合物的性质、结构和反应。
大学有机化学作为化学专业中的重要课程,对于学习和了解有机化学的基本原理和应用具有重要意义。
本文将重点总结大学有机化学课程中的重点内容,包括有机化学的基本概念、命名方法、反应机理等。
一、有机化学的基本概念1.1 有机化合物有机化合物是由碳元素和氢元素以及其他元素通过共价键相连而成的化合物。
在有机化学中,碳元素可以通过形成单、双或三键与其他元素形成分子结构多样的化合物,使有机物的种类极为丰富。
1.2 有机化合物的结构有机化合物的结构包括分子式、结构式和构象式。
分子式是用元素符号和下标表示分子中各元素的原子个数,结构式是用键线表示共价键和原子间的连接关系,构象式是描述分子中原子的空间排布情况。
1.3 有机化学中的键有机化学中常见的键有单键、双键和三键。
单键由一个σ 键组成,双键由一个σ 键和一个π 键组成,三键由一个σ 键和两个π 键组成。
键的长度和键的强度会受到原子的电性和大小以及受到共轭和杂化的影响。
二、有机化合物的命名方法2.1 按照直链和支链进行命名直链烷烃的命名是根据碳原子数目的不同来命名的,例如甲烷、乙烷、丙烷等。
当有机化合物中存在支链时,需要按照支链的位置和代表性碳原子数目命名,例如异丙烷、2-甲基丁烷等。
2.2 有机官能团的命名有机官能团是分子中具有一定化学性质的基团,如羟基、羰基、羧基等。
有机官能团的存在会影响有机化合物的性质和反应能力,因此在命名中需要明确官能团的存在和位置。
2.3 代号命名法代号命名法是根据有机化合物的结构、化学性质或有效成分命名的一种方法,如乙醇、苯胺等。
三、有机化合物的反应机理有机化合物的反应机理是研究有机化合物之间发生反应的过程和机理。
常见的有机反应机理有取代反应、加成反应、消除反应和重排反应。
3.1 取代反应取代反应是指有机化合物中的一个官能团发生取代反应,产生另一个官能团。

大一有机化学绪论知识点1.有机化合物的分类:有机化合物是含有碳元素的化合物,按照功能基团可以分为醇、醚、醛、酮、羧酸、酯等。
2.有机化学键:有机化合物中的化学键可以分为共价键和极性键。
共价键是由共用电子对形成的,常见的有单键、双键和三键。
极性键则是由于电负性差异而产生的偏向性。
3.共轭体系:共轭体系是指一个或多个单键和一个或多个共轭双键相互交替排列而形成的一组π键的结构。
共轭体系具有较小的能量差异,因此比较稳定。
4.异构体:异构体是指分子式相同但结构不同的化合物。
包括构造异构体、空间异构体和立体异构体。
构造异构体是指化合物的分子结构不同,如链异构体和环异构体。
空间异构体是指化合物的空间取向不同,如顺反异构体。
立体异构体是指化合物分子中具有手性中心,存在手性异构体。
5.有机反应的基本原理:有机反应是有机化合物发生变化的过程。
常见的有机反应包括加成反应、消除反应、取代反应和重排反应。
加成反应是指两个分子结合而形成一个新的分子,消除反应是指一个分子分解为两个分子,取代反应是指一个原子或基团被另一个原子或基团取代,重排反应是指分子内原子或基团的位置发生变化。
6.极性和溶解性:极性是指分子中正负电荷分布的不均匀性。
极性分子通常具有较强的溶解性,而非极性分子溶解性较差。
极性溶剂通常可以溶解极性物质,非极性溶剂可以溶解非极性物质。
7.共沉淀和分配:共沉淀是指两种或更多种物质在溶液中发生反应而形成沉淀。
分配是指两个相互不相溶的液体中的物质在两相之间分配的过程。
分配系数是用来描述分配过程的指标。
8.杂环化合物:杂环化合物是指含有不同原子的环状化合物。
常见的杂环化合物包括含氧杂环、含氮杂环、含硫杂环等。
杂环化合物具有较强的化学活性和生物活性。
9.光学活性和手性:光学活性是指一些化合物对旋光的作用。
手性是指分子不具有镜面对称性,分为左旋体和右旋体。
手性分子与手性反应物之间发生反应时会产生对映异构体。
10.环加成反应和开链加成反应:环加成反应是指在环状化合物中发生加成反应,如环状醇的开环加成反应。

《有机化学基础》知识点整理一、重要的物理性质1.有机物的溶解性(1)难溶于水的有:各类烃、卤代烃、硝基化合物、酯、绝大多数高聚物、高级的(指分子中碳原子数目较多的 , 下同)醇、醛、羧酸等。
(2)易溶于水的有:低级的 [ 一般指 N(C)≤4] 醇、(醚)、醛、(酮)、羧酸及盐、氨基酸及盐、单糖、二糖。
(它们都能与水形成氢键) 。
(3)具有特殊溶解性的: ① 乙醇是一种很好的溶剂 , 既能溶解许多无机物 , 又能溶解许多有机物 , 所以常用乙醇来溶解植物色素或其中的药用成分 , 也常用乙醇作为反应的溶剂 , 使参加反应的有机物和无机物均能溶解 , 增大接触面积 , 提 高反应速率。
例如 , 在油脂的皂化反应中 , 加入乙醇既能溶解 NaOH,又能溶解油脂 , 让它们在均相 (同一溶剂的溶液) 中充分接触 , 加快反应速率 , 提高反应限度。
② 苯酚:室温下 , 在水中的溶解度是 9.3g (属可溶) , 易溶于乙醇等有 机溶剂 , 当温度高于 65℃时, 能与水混溶 , 冷却后分层 , 上层为苯酚的水溶液 , 下层为水的苯酚溶液 , 振荡后形成乳浊 液。
苯酚易溶于碱溶液和纯碱溶液 , 这是因为生成了易溶性的钠盐。
③ 乙酸乙酯在饱和碳酸钠溶液中更加难溶 , 同 时饱和碳酸钠溶液还能通过反应吸收挥发出的乙酸 , 溶解吸收挥发出的乙醇 , 便于闻到乙酸乙酯的香味。
④ 有的淀 粉、蛋白质可溶于水形成 胶.体.。
蛋白质在浓轻金属盐(包括铵盐)溶液中溶解度减小 , 会析出(即盐析 , 皂化反应 中也有此操作) 。
但在稀轻金属盐(包括铵盐)溶液中 , 蛋白质的溶解度反而增大。
⑤ 线型和部分支链型高聚物可 溶于某些有机溶剂 , 而体型则难溶于有机溶剂。
⑥ 氢氧化铜悬浊液可溶于多羟基化合物的溶液中 , 如甘油、葡萄糖 溶液等 , 形成绛蓝色溶液。
2.有机物的密度(1)小于水的密度 , 且与水(溶液)分层的有:各类烃、一氯代烃、酯(包括油脂)(2)大于水的密度 , 且与水(溶液)分层的有:多氯代烃、溴代烃(溴苯等) 、碘代烃、硝基苯3.有机物的状态 [ 常温常压( 1 个大气压、 20℃左右)](1)气态:① 烃类:一般 N(C)≤4 的各类烃 注意: 新戊烷 [C(CH 3) 4] 亦为气态② 衍生物类:一氯.甲.烷.(.. C . .H .C ..l ,.沸.点.为.-.2..4..2.℃. ). 氟.里.昂.(.C . .C .l .F ..,.沸.点.为.-.2.9...8.℃. ).3 2 2氯.乙.烯.(.C . .H .=..=.C .H .C .,l .沸.点.为.-.1.3...9.℃. ). 甲.醛.(.H ..C .H .O,.沸.点.为.-.2.1.℃. ).2氯.乙.烷.(.C . .H32 3Br, 沸点为3.6 ℃)四氟乙烯( C F 2==CF 2, 沸点为 -76.3 ℃) 甲醚( CH 3OCH 3, 沸点为 -23 ℃) 甲乙醚( CH 3O C 2H 5, 沸点为 10.8 ℃) 环氧乙烷( , 沸点为 13.5 ℃)(2)液态:一般 N(C)在 5~16 的烃及绝大多数低级衍生物。
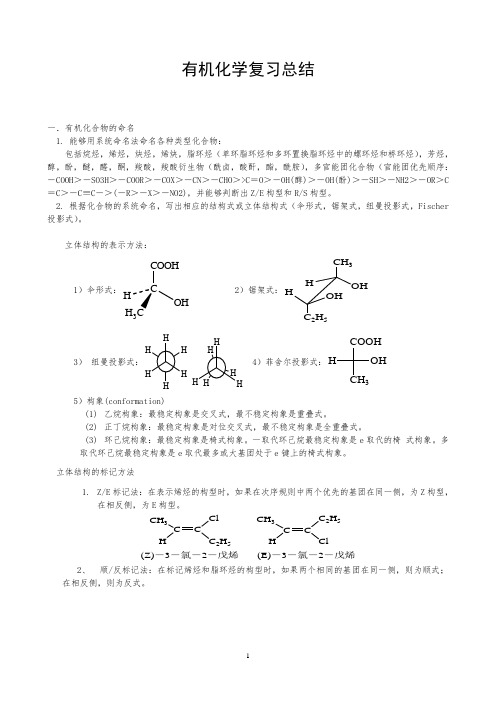
有机化学复习总结一.有机化合物的命名1. 能够用系统命名法命名各种类型化合物:包括烷烃,烯烃,炔烃,烯炔,脂环烃(单环脂环烃和多环置换脂环烃中的螺环烃和桥环烃),芳烃,醇,酚,醚,醛,酮,羧酸,羧酸衍生物(酰卤,酸酐,酯,酰胺),多官能团化合物(官能团优先顺序:-COOH >-SO3H >-COOR >-COX >-CN >-CHO >>C =O >-OH(醇)>-OH(酚)>-SH >-NH2>-OR >C =C >-C ≡C ->(-R >-X >-NO2),并能够判断出Z/E 构型和R/S 构型。
2. 根据化合物的系统命名,写出相应的结构式或立体结构式(伞形式,锯架式,纽曼投影式,Fischer 投影式)。
立体结构的表示方法:1)伞形式:CCOOHOHH 3 2)锯架式:CH 3OH HHOH C 2H 53)纽曼投影式:H H 4)菲舍尔投影式:COOHCH 3OH H5)构象(conformation)(1) 乙烷构象:最稳定构象是交叉式,最不稳定构象是重叠式。
(2) 正丁烷构象:最稳定构象是对位交叉式,最不稳定构象是全重叠式。
(3) 环己烷构象:最稳定构象是椅式构象。
一取代环己烷最稳定构象是e 取代的椅 式构象。
多取代环己烷最稳定构象是e 取代最多或大基团处于e 键上的椅式构象。
立体结构的标记方法1. Z/E 标记法:在表示烯烃的构型时,如果在次序规则中两个优先的基团在同一侧,为Z 构型,在相反侧,为E 构型。
CH 3C H C 2H 5CH 3C CH 2H 5Cl(Z)-3-氯-2-戊烯(E)-3-氯-2-戊烯2、 顺/反标记法:在标记烯烃和脂环烃的构型时,如果两个相同的基团在同一侧,则为顺式;在相反侧,则为反式。
CH 3C CHCH 3HCH 3CCH HCH 3顺-2-丁烯反-2-丁烯333顺-1,4-二甲基环己烷反-1,4-二甲基环己烷3、 R/S 标记法:在标记手性分子时,先把与手性碳相连的四个基团按次序规则排序。

引言概述:有机化学作为化学学科的一个重要分支,研究有机化合物的结构、性质和反应机理,是化学学习的基础。
有机化学基础知识点对于理解和掌握有机化学的原理和应用至关重要。
本文将从五个大点出发,详细阐述有机化学的基础知识点。
一、有机化合物的命名1.醇类的命名:通过识别羟基的位置和数量,采用“字根+ol”的命名法。
2.醛和酮的命名:以醛基和酮基分别作为命名的基础,通常采用“字根+al”的命名法和“字根+one”的命名法。
3.酸类和酯的命名:以羧基和酯基分别作为命名的基础,通常采用“希酸”和“酸酯”的命名法。
4.芳香化合物的命名:根据苯环上的取代基的位置和数量,采用数字和字母的组合进行命名。
5.范德华力、静电干涉和氢键的重要性:通过这些相互作用力的存在,可以解释分子之间的特殊性质和反应。
二、有机化学反应的机理1.加成反应:通过两个或多个分子中部分反应性的化学物质结合形成一个新的化合物。
2.消除反应:通过两个或多个分子中部分反应性的化学物质相互分离形成两个或更多的产物。
3.变位反应:通过化合物中某一部分的结构重新组合形成产物。
4.羰基化合物的还原反应:通过添加一种强还原剂,将羰基物质转化为相应的醇。
5.羟醇的氧化反应:通过添加一种强氧化剂,将醇转化为相应的醛或酮。
三、有机化合物的结构和性质1.共价键与键长:共价键是有机化合物中最常见的键,其长度取决于成键原子的电子云分布。
2.极性共价键:由于成键原子之间电子云密度的不均匀,导致共价键中电子密度分布的不均匀。
3.分子的分散力和溶解性:分子之间的分散力是由于电子云的不均匀分布而引起的吸引力。
4.电子云的亲核性/亲电性:电子云可以表现出亲核性或亲电性,取决于原子内的电子分布和外部原子的电子密度。
5.光学活性:光学活性是指一个有机化合物可以使平面偏振光彻底旋转一定角度。
四、有机化合物的合成方法1.羰基化合物的合成:羰基化合物可以通过醛或酮的氧化获得,也可以通过相应的醇的氧化后进行脱水反应得到。

有机化学基础知识点总结一、常见有机物的性质和应用二、官能团的性质三、官能团得引入(1)官能团的引入(或转化)方法+H2O;R—X+H2O;R—CHO+H2;RCOR′+H2;R—COOR′+H2O;多糖发酵(2)官能团的消除①消除双键:加成反应。
②消除羟基:消去、氧化、酯化反应。
③消除醛基:还原和氧化反应。
四、有机综合推断1.根据反应条件推断反应物或生成物(1)“光照”为烷烃的卤代反应。
(2)“NaOH水溶液、加热”为R—X的水解反应,或酯(CROOR′)的水解反应。
(3)“NaOH醇溶液、加热”为R—X的消去反应。
(4)“HNO3(H2SO4)”为苯环上的硝化反应。
(5)“浓H2SO4、加热”为R—OH的消去或酯化反应。
(6)“浓H2SO4、170 ℃”是乙醇消去反应的条件。
2.根据有机反应的特殊现象推断有机物的官能团(1)使溴水褪色,则表示有机物分子中可能含有碳碳双键、碳碳三键或醛基(注意酚羟基的邻对位取代、液态有机物的萃取等)。
(2)使酸性KMnO4溶液褪色,则该物质中可能含有碳碳双键、碳碳三键、醛基或苯的同系物、醇酚。
(3)遇FeCl3溶液显紫色或加入浓溴水出现白色沉淀,表示该物质分子中含有酚羟基。
(4)加入新制Cu(OH)2悬浊液并加热,有砖红色沉淀生成(或加入银氨溶液并水浴加热有银镜出现),说明该物质中含有—CHO。
(5)加入金属钠,有H2产生,表示该物质分子中可能有—OH 或—COOH。
(6)加入NaHCO3溶液有气体放出,表示该物质分子中含有—COOH。
(7)能与碳酸钠反应,则有酚—OH 或—COOH3.以特征的产物为突破口来推断碳架结构和官能团的位置(1)醇的氧化产物与结构的关系(2)由消去反应的产物可确定“—OH”或“—X”的位置。
(3)由取代产物的种类或氢原子环境可确定碳架结构。
有机物取代产物越少或相同环境的氢原子数越多,说明该有机物结构的对称性越高,因此可由取代产物的种类或氢原子环境联想到该有机物碳架结构的对称性而快速进行解题。


大一有机化学知识点汇总有机化学是化学的一个重要分支,研究有机物的结构、性质和反应。
在大一的学习中,我们首次接触到了有机化学的知识,下面将对大一有机化学的主要知识点进行汇总和总结。
1. 有机化学的基本概念和性质有机化合物是由碳和氢为主要成分,并且常常伴随有氧、氮、硫等元素,以及其他杂原子的化合物。
有机化合物有着多样的性质,包括燃烧、酸碱性、溶解性等。
2. 碳的化合价与杂化四价的碳原子可以通过杂化形成四个等价的sp3杂化轨道,称为sp3杂化。
而其他化合价的碳原子可以通过sp2、sp等杂化形式。
3. 有机化合物的分类和命名有机化合物可以根据其结构特征和性质进行分类,其中包括烷烃、烯烃、炔烃、芳香烃、醇、醚、醛、酮、羧酸等。
有机化合物的命名采用IUPAC命名法,根据其结构和官能团进行命名。
4. 有机化学的反应类型和机理有机化学的反应主要包括取代反应、加成反应、消除反应、重排反应等。
这些反应是通过分子中的化学键的形成和断裂来完成的。
反应机理是指反应步骤、中间体和过渡态的描述。
5. 有机物的官能团转化官能团是有机分子中具有化学性质相似或相容的原子团。
有机化合物的官能团转化是指通过化学反应,将一个官能团转换成另一个官能团。
6. 碳原子的化学键和分子构象碳原子与其他原子形成共价键,其中包括单键、双键和三键。
分子的构象是指分子在空间中的排列方式,包括隐式构象和立体构象。
7. 共轭体系和芳香性共轭体系是指由一系列相邻的具有共轭双键和孤对电子的原子组成的分子。
芳香性是共轭体系的一种特殊表现形式。
8. 有机物的立体化学有机化学中的立体化学研究涉及到手性、对映体、立体异构体等概念。
手性分子是非重合镜像的分子,具有对映体的属性。
9. 有机物的合成和分离有机物的合成是指通过化学反应将简单的有机物转化为复杂的有机物。
而有机物的分离是指从混合物中分离出目标化合物。
10. 有机化学在生物学和药物学中的应用有机化学在生物学和药物学中有着广泛的应用,例如药物的合成、天然产物的研究以及生物活性分子的设计等。

大一有机化学知识点总结pdf 大一有机化学是大学化学专业的重要基础课程之一,也是许多理工科学生的必修课。
学好有机化学对于进一步深入理解化学的基本原理和应用具有重要意义。
为了帮助大家系统地总结和复习大一有机化学的知识点,本文将以PDF形式提供一份大一有机化学知识点总结。
1. 有机化学的基本概念有机化学是研究碳及其化合物的科学,其中碳原子是有机化合物的主要构成元素。
有机化学主要涉及有机化合物的结构、性质和反应等方面内容。
2. 有机化合物的命名有机化合物的命名是有机化学的基础,根据化合物的结构和功能团等特征,可以使用不同的命名方法,如系统命名法、功能团命名法等。
3. 有机化合物的结构有机化合物的结构主要包括分子式、结构式、立体化学和共轭体系等方面。
分子式可以简单表示有机分子的组成元素和原子数目,而结构式可以显示有机分子的空间结构和键的连接方式。
4. 有机反应的基本类型有机反应可以分为加成反应、消去反应、取代反应和重排反应等基本类型。
了解不同类型的有机反应对于预测和理解化学反应机理有重要作用。
5. 有机反应的机理有机反应的机理涉及键的形成和断裂过程,可以通过共价键的极性、反应物的结构和反应条件等方面推导。
了解有机反应的机理可以提高学生对于有机反应的理解和应用能力。
6. 功能团的性质和反应功能团是有机化合物中具有特定功能的官能团,不同的功能团对于化合物的性质和反应具有重要影响。
比如羧酸和醇有明显不同的性质和反应路径。
7. 碳氢化合物的分类和性质碳氢化合物是有机化合物中最简单的一种类别,可以根据碳原子间的连接方式分为烷烃、烯烃和炔烃等不同类别。
不同类型的碳氢化合物具有不同的化学性质和应用。
8. 碳链的分支和环状化合物碳链的分支和环状化合物具有特殊的结构和性质,对于有机化合物的稳定性和反应有一定影响。
了解碳链的分支与环状化合物的特点,可以帮助学生更好地理解有机化学的一些概念。
9. 芳香化合物的特性和反应芳香化合物是具有芳香性质的环状化合物,具有特殊的结构和化学性质。