有机化学课后习题
- 格式:doc
- 大小:2.99 MB
- 文档页数:18

第一章绪论习题参考答案1.什么是有机化合物?它有那些特性?有机化合物是指碳氢化合物及其衍生物。
有机化合物的特性:1、数目众多、结构复杂;2、易燃;3、熔沸点较低3、难溶于水,易溶于有机溶剂;4.反应慢、副反应多。
2.什么是σ键和π键?沿着轨道对称轴方向重叠形成的键叫σ键。
其特点为电子云可以达到最大程度的重叠,所以比较牢固。
另外σ键旋转时不会破坏电子云的重叠,所以σ键可以沿对称轴自由旋转。
P轨道“肩并肩”平行重叠形成的共价键叫π键,其特点为电子云重叠程度小,键能低;电子云分布呈块状分布于σ键所在平面的上下,受核的束缚小,易受极化;成键的两个原子不能沿键轴自由旋转。
3.指出下列化合物所含的官能团名称:(1) (2) (3) (4) (5)NO2CH3CH3H3C CCH3CH3CH2Cl OH苯环、硝基苯环卤代烃酚环烯(6) (7) (8) (9)O CHO NH2OH环酮环醛苯环、胺环、醇4.根据键能的数据,当乙烷分子受热裂解时,那一个共价键首先破裂?为什么?这个过程是吸热还是放热?乙烷分子受热裂解时,分子中的碳碳首先破裂,因为C—C键能为376 KJ·mol-1,而C—H 键能为439 KJ·mol-1。
这个过程是吸热。
5.指出下列各化合物分子中碳原子的杂化状态:(1)(2)(3)H3C CH CHCHO sp3sp2sp2sp2CH3sp3CH CH2sp2sp2苯环上的碳原子是sp2 杂化环己烷上的碳原子是sp3杂化(4)(5)(6)HC CCH2CH CH2sp3sp sp sp2sp2H2C C CHCH3sp2sp sp2sp3H3C COOHsp3sp2第二章烷烃习题参考答案1.解:(1)CH3CH2CHCH2CH2CH2CH3CH2CH3(2)CH32CHCH3CH333(3)CH3CH2CH2CHCHCH2CH2CH3CH3CH2CH3(4)CH3CH2CCHCHCH2CH2CH3CH23CH(CH3)2H3CCH2CH2CH32.解:(不匹配)(1) 2,3-二甲基辛烷(2) 2,7-二甲基-4-乙基壬烷 (3) 3,6-二甲基壬烷 3.解:(1)C CH 3CH 3H 3C CH 3(2) CH 32CH 3CH 3(3)CH 3CH 2CH 2CH 2CH 34.解:(1)CH 3CH 2CH 2CH 2CH(CH 3)2,(CH 3)2CHCH 2CH(CH 3)2,CH 3CH 2CHCHCH 3CH 3CH 3,H 3C C HC CH 3H 3H 3CCH 3(2)CH 3CH 2CH 2CHCH 3CH 3,CH 3CH 2CHCH 2CH 3CH 3(3)H 3C C HC CH 3H 3H 3CCH 35.解:(不匹配)(1)CH 2CH 2CH 3,CH 2CH 2CH 3( 正戊烷绕C 1-C 2σ键旋转产生的交叉式和重叠式构象)(2)C 2H 5H 3C ,C 2H 5CH 3,C 2H 5CH 3,C 2H 5CH 3(正戊烷绕C 2-C 3σ键旋转产生的全重叠式、邻位交叉式、部分重叠式、对位交叉式构象)(3)CH 3C 2H 5,CH 3C 2H 5(异戊烷绕C 1-C 2σ键旋转产生的交叉式和重叠式构象)(4)H 3CCH 3CH 3H 3C CH 3CH 3H 3C CH 3H 3CH 3CCH 3CH 3(异戊烷绕C 2-C 3σ键旋转产生的全重叠式、邻位交叉式、部分重叠式、对位交叉式构象) (5)CH(CH 3)2CH(CH 3)2(异戊烷绕C 3-C 4σ键旋转产生的交叉式和重叠式构象) (6)H 3CCH 3H 3CCH 3CH 3H 3C(新戊烷绕C 1-C 2σ键旋转产生的交叉式和重叠式构象) 6.解:(3)>(2)>(4)>(1) 7.解: 1°H =12;2°H =0;3°H =0 8.解:FF F9.解:310.解: 链引发:Cl 2hvCl ·+Cl ·链增长:Cl ·+CH 3CH 3CH 3CH 2·+HCl Cl 2+CH 3CH 2Cl ·+CH 3CH 2Cl 链终止:Cl ·+Cl ·2 Cl ·+CH 3CH 2·3CH 2Cl CH 3CH 2·+CH 3CH 2CH 3CH 2CH 2CH 3第三章 烯烃 炔烃 二烯烃习题参考答案1.(不匹配) (1)5–甲基–1–己烯 (2)3–甲基–1–丁炔 (3)4–甲基–1,3–戊二烯(4)2,7–二甲基–2,7–壬二烯 (5)3–乙基–4–己烯–1–炔 (6)5–甲基–1,3–环己二烯 (7)( Z )–3–甲基 –3–庚烯 (8)顺,反–2,4–庚二烯(或(2Z,4E )–2,4–庚二烯) 2.CH 3C H CCH(CH 3)2HH 3CH C3)CH 2CH 3CH 3CCl Br C CH 2CH 2CH 3HClHC C C(CH 3)2CH 2CH 2CH 3CH CHH 2C C 2H 5C CH(1)(2)(3)(4)(5)(6)3.(1)(2)(3)(4)(5)(6)(7)(8)CH 3CH 3CH 2CH 2COOH + CO 2CH 3CCH 2CH 2CH 33BrCH 2ClCH 2CF 3CH 3CH CH 33HCH 3CH CH 3COOC 2H 5COOC 2H 5CH 3CH 2CH 2CH 2BrCH 3CH 2CHCCH 3OCuCCCH 34.答案不唯一,只要方法可行都可以。

有机化学课后习题参考答案在有机化学的学习过程中,课后习题是巩固知识、加深理解的重要环节。
以下是对一些常见有机化学课后习题的参考答案,希望能对大家的学习有所帮助。
一、选择题1、下列化合物中,属于饱和烃的是()A 乙烯B 乙炔C 环己烷D 苯答案:C解析:饱和烃是指分子中只含有碳碳单键和碳氢键的烃。
环己烷分子中只含有单键,属于饱和烃;乙烯和乙炔分子中含有碳碳双键和碳碳三键,属于不饱和烃;苯分子中的碳碳键是介于单键和双键之间的独特键,也不是饱和烃。
2、能使高锰酸钾溶液褪色的是()A 甲烷B 乙烷C 乙烯D 苯答案:C解析:乙烯分子中含有碳碳双键,能被高锰酸钾溶液氧化,从而使高锰酸钾溶液褪色;甲烷和乙烷属于饱和烃,性质稳定,不能使高锰酸钾溶液褪色;苯分子中的碳碳键比较稳定,一般也不能使高锰酸钾溶液褪色。
3、下列化合物中,沸点最高的是()A 正丁烷B 异丁烷C 正戊烷D 新戊烷答案:C解析:在同系物中,随着碳原子数的增加,沸点逐渐升高。
对于碳原子数相同的烷烃,支链越多,沸点越低。
正戊烷的碳原子数最多,所以沸点最高;正丁烷和异丁烷的碳原子数相同,但异丁烷有支链,沸点低于正丁烷;新戊烷的支链最多,沸点最低。
4、下列化合物中,酸性最强的是()A 乙醇B 苯酚C 乙酸D 碳酸答案:C解析:羧酸的酸性一般强于酚和醇,碳酸的酸性弱于乙酸。
所以酸性最强的是乙酸。
二、填空题1、烷烃的通式为_____。
答案:CₙH₂ₙ₊₂(n≥1)2、苯的分子式为_____,结构简式为_____。
答案:C₆H₆;3、乙醇在铜作催化剂加热的条件下发生氧化反应的化学方程式为_____。
答案:2CH₃CH₂OH + O₂ 2CH₃CHO + 2H₂O4、酯化反应的化学方程式通式为_____。
答案:RCOOH + R'OH RCOOR' + H₂O三、简答题1、简述烷烃的命名原则。
答:烷烃的命名原则主要包括以下几点:(1)选择最长的碳链作为主链,根据主链所含碳原子的数目称为“某烷”。

第一章绪论习题参考答案1. 某化合物的分子量为60,含碳%、含氮%、含氧%,确定该化合物的分子式;解:①由各元素的百分含量,根据下列计算求得实验式该化合物实验式为:CH2O②由分子量计算出该化合物的分子式该化合物的分子式应为实验式的2倍,即:C2H 4 O22. 在C—H、C—O、O—H、C—Br、C—N等共价键中,极性最强的是哪一个解:由表1-4可以查得上述共价键极性最强的是O—H键;3. 将共价键⑴ C—H ⑵ N—H ⑶ F—H ⑷ O—H按极性由大到小的顺序进行排列;解:根据电负性顺序F > O > N > C,可推知共价键的极性顺序为:F—H > O—H > N—H > C—H4. 化合物CH3Cl、CH4、CHBr3、HCl、CH3OCH3中,哪个是非极性分子解:CH4分子为高度对称的正四面体空间结构,4个C—H的向量之和为零,因此是非极性分子;5. 指出下列化合物所含官能团的名称和该化合物所属类型;碳碳三键,炔烃羟基 ,酚酮基 ,酮羧基 ,羧酸醛基 ,醛羟基 ,醇氨基 ,胺6. 甲醚CH3OCH3分子中,两个O—C键的夹角为°;甲醚是否为极性分子若是,用表示偶极矩的方向;解:氧原子的电负性大于碳原子的电负性,因此O—C键的偶极矩的方向是由碳原子指向氧原子;甲醚分子的偶极矩是其分子中各个共价键偶极矩的向量之和,甲醚分子中的两个O—C键的夹角为°,显然分子是具有极性的,其偶极矩的方向如下图所示;7. 什么叫诱导效应什么叫共轭效应各举一例说明之;研读教材第11~12页有关内容8. 有机化学中的离子型反应与无机化学中的离子反应有何区别解:无机化学中的离子反应是指有离子参加的反应,反应物中必须有离子;而有机化学中的离子型反应是指反应物结构中的共价键在反应过程中发生异裂,反应物本身并非一定是离子;第二章链烃习题参考答案1. 写出分子式为C6H14的化合物的所有碳链异构体的构造式,并按系统命名法命名;解:①所有可能的碳架如下:②所有异构体的构造式及名称:己烷 2—甲基戊烷 3—甲基戊烷2,3—二甲基丁烷 2,2—二甲基丁烷2. 写出下列化合物的结构式或名称,并指出分子中的1°、2°、3°、4°碳原子;3. 将下列化合物的结构式改写成键线式4. 写出分子式为C5H10的所有开链异构体的结构式,并用系统命名法命名;5. 完成下列反应式6. 用化学方法鉴别下列各组化合物1 乙烷、乙烯、乙炔解答:分别将三种气体通入溴水中,不能使溴水褪色的是乙烷;将能使溴水褪色的两种气体分别通入银氨溶液中,能使之产生白色沉淀的气体是乙炔,另一个是乙烯;2 丁烷、1—丁炔、2—丁炔解答:分别将三种待测物分别与高锰酸钾酸性溶液混合,不能使高锰酸钾紫红色褪色的是丁烷;将能使高锰酸钾褪色的两种待测物分别与银氨溶液混合,能使之产生白色沉淀的是1—丁炔,另一个是2—丁炔;3 1,3—丁二烯、1—丁炔解答:分别将两种待测物与氯化亚铜氨溶液混合,能使之产生棕红色色沉淀的是1—丁炔,另一个是1,3—丁二烯;7. 以乙炔、丙炔为原料,合成下列化合物其他试剂任选;1 1,2—二氯乙烷2 异丙醇3 2,2—二氯丙烷4 乙烯基乙炔5 丙酮6 苯7 乙烯基乙醚8. 如何除去乙烷中含有的少量丙烯解答:将含有少量丙烯的乙烷气体通入硫酸溶液中,其中的丙烯杂质因与硫酸发生加成反应而被吸收;9. 丁烷和异丁烷分子中哪个氢原子最容易发生卤代反应为什么解答:异丁烷分子中的叔氢原子最易发生卤代反应;有大量实验结果表明,在取代反应中,各种类型氢原子的反应活性顺序为:3°H > 2°H > 1°H ;10. 用杂化轨道理论简述甲烷、乙烯、乙炔的分子结构;解答:1 甲烷的结构根据杂化轨道理论,甲烷分子中的碳原子采取sp3杂化,4个价电子分别位于4个sp3杂化轨道中;4个sp3杂化电子云在空间呈正四面体排布,各个sp3杂化电子云的大头分别指向四面体的四个顶点;C与H成键时,4个H原子的s电子云沿着4个sp3杂化电子云的大头重叠形成4个s-sp3σ键,因此形成的甲烷分子是正四面体型的,键角为109°28/ ;2乙烯的结构乙烯分子中的碳原子采取sp2杂化,4个价电子中有3个分别位于3个sp2杂化轨道中,1个位于2p轨道中;3个sp2杂化电子云在空间呈平面三角形分布,各sp2杂化电子云的大头指向三角形的3个顶点,2p电子云对称轴垂直穿过3个sp2杂化电子云所在的平面;11. 乙烯和乙炔都能使溴水褪色,两者的反应速度有何区别为什么会有此不°同解答:乙烯使溴水褪色的速度较乙炔的快;乙炔碳碳键长较乙烯碳碳键的键长短,因此乙炔分子中的π键较乙烯的π键稳定,反应活性低、反应速度慢;12. 乙烯既能使高锰酸钾溶液褪色,也能使溴水褪色;这两个实验的本质有无区别解答:这两个实验有着本质的区别,乙烯使高锰酸钾溶液褪色是因为乙烯与高锰酸钾发生了氧化还原反应,乙烯使高锰酸钾还原而褪色;乙烯使溴水褪色是因为乙烯与溴发生了加成反应,生成了无色的溴代烷烃;13. 写出分子式C4H6的开链构造异构体的结构式,并用系统命名法命名;1—丁炔 2—丁炔 1,3—丁二烯 1,2—丁二烯14. A,B 两化合物的分子式都是C 6H 12 ,A 经臭氧化并与锌和酸反应后的乙醛和甲乙酮,B 经高锰酸钾氧化只得丙酸,写出A 和B 的结构式;解答:顺—3—甲基—2—戊烯 反—3—甲基—2—戊烯顺—3—己烯 反—3—己烯15. 化合物A 和B 互为同分异构体,二者都能使溴水褪色,A 能与硝酸银的氨溶液反应而B 不能;A 用酸性高锰酸钾溶液氧化后生成CH 32CHCOOH 和CO 2,B 用酸性高锰酸钾溶液氧化后生成CH 3COCOOH 和CO 2;试推测A 和B 的结构式和名称,并写出有关的反应式;解答:化合物A 的有关反应式: 化合物B 的有关反应式:16. 某化合物分子量为82,每摩尔该化合物可吸收2摩尔氢,不与硝酸银的氨溶液反应,当他吸收1摩尔氢时,生成2,3—二甲基—1—丁烯;试写出该化合物的结构式;解答:A. B. CH 2 C CH CH 2CH 3(CH 3)2CHC CH 3—甲基—1—丁炔2—甲基—1,3—丁二烯 CH 2 C C CH 2CH 3CH 3第三章脂环烃习题参考答案1. 命名下列化合物2. 写出下列化合物的结构1 3—甲基环丁烯2 5—甲基二环2.2.2—2—辛烯 3. 用化学方法鉴别下列各组化合物解答:将上述三种试剂分别通入溴水中,不能使溶液棕红色褪色的是CH3CH2CH3;将能使溴水褪色的两种试剂分别通入高锰酸钾酸性溶液中,能使溶液紫红色褪色的是CH3CH=CH2;2 1,1—二甲基环丙烷和环戊烯解答:将两种试剂与高锰酸钾酸性溶液混合,能使溶液紫红色褪色的是环戊烯,不能使溶液褪色的是1,1—二甲基环丙烷;4. 完成下列反应式5. 完成苯基环丙烷与下列试剂的反应;1 HCl2 Cl2Cl43 Br2FeBr34 H2SO46. 回答下列问题:1 在环丙烷中含有少量杂质丙烯,在提纯环丙烷时如何去除杂质解答:将含有少量丙烯杂质的环丙烷气体通入高锰酸钾溶液,丙烯因为与高锰酸钾反应而被溶液吸收去除,然后用排水集气法收集得到不含丙烯的环丙烷气体;2 解释环丙烷的稳定性解答:环丙烷的3个碳原子在同一平面上,其每一个碳原子的sp3杂化电子云夹角为°;因此,当成键时,两个成键电子云是以弯曲方式重叠,形成“弯曲σ键”;与以“头对头”方式正面重叠形成的一般σ键相比,弯曲σ键重叠程度低,而且具有恢复正常重叠方式的自在趋势力——张力,因此不稳定;环丙烷的3个“弯曲σ键”的不稳定决定了环丙烷分子的不稳定性,它容易发生开环加成反应;7. 有一化合物分子式为C7H14,此化合物发生如下反应:1 可以催化加氢,产物分子式为C7H16;2 在室温下不能使高锰酸钾溶液褪色;3 能与HBr反应得产物2—溴—2,3—二甲基戊烷;写出该化合物的结构;解答:CH3CH3或H3CH3C CH3CH3第四章芳香烃习题参考答案1. 命名下列化合物;对乙基甲苯对异丙基甲苯 4—乙基—2—溴甲苯2—环戊基甲苯对二氯苯三苯甲基游离基6—溴—1—萘磺酸 2,4—二硝基甲苯2. 写出下列化合物的结构;1 间甲乙苯2 β-萘酚3 4-氯-2,3-二硝基甲苯4 环戊二烯负离子5 间二乙烯苯6 邻二异丙苯7 6-氯-1-萘磺酸 8 环丙烯正离子3. 完成下列反应;4. 写出下列反应所需试剂,并完成反应,1 苯→甲苯→氯苄2 甲苯→苯甲酸→邻、对硝基苯甲酸3 硝基苯→间硝基氯苯4 萘→邻苯二甲酸5. 用化学方法鉴别下列各组化合物;1 甲苯、1-甲基环己烯、甲基环己烷解答:取三种待测物少许,分别与溴水混合,能使溴水迅速褪色的是1-甲基环己烯;将不能使溴水褪色的两种待测物分别与高锰酸钾溶液混合加热,能使高锰酸钾紫红色褪色的是甲苯,余者为甲基环己烷;2 苯、1,3-己二烯解答:取两种待测物少许,分别与高锰酸钾酸性溶液混合,能使溶液紫红色褪色的是1,3-己二烯;6. 二甲苯的邻、间、对位三个异构体,在进行硝化时,分别得到一个一硝基产物,二个一硝基产物和三个一硝基产物,写出相对应的二甲苯结构;解答:得一个硝基产物的是对二甲苯:得二个硝基产物的是邻二甲苯:得三个硝基产物的是间二甲苯:7. 按照亲电取代反应活性由强到弱的顺序排列下列化合物;1 甲苯、苯、氯苯、硝基苯、苯酚解答:亲电取代反应活性顺序为苯酚 > 甲苯 > 苯 > 氯苯 > 硝基苯2 溴苯、苯甲酸、间二甲苯、甲苯、间硝基苯甲酸解答:亲电取代反应活性顺序为间二甲苯 > 甲苯 > 溴苯 > 苯甲酸 > 间硝基苯甲酸8. 判断下列化合物有无芳香性;1 环戊二烯解答:环戊二烯分子中没有闭合的共轭大π健结构,故不具有芳香性;2 环戊二烯负离子解答:环戊二烯负离子具有闭合的6电子共轭大π健结构,且π电子数6符合“4n+2”;因此根据休克尔规则,环戊二烯负离子具有芳香性;3 环戊二烯正离子解答:环戊二烯正离子具有闭合的4电子共轭大π健结构,但其π电子数4不符合“4n+2”;因此根据休克尔规则,环戊二烯正离子不具有芳香性;4 1,2,3,4-四氢萘解答:1,2,3,4-四氢萘保留了一个完整的苯环,因此具有芳香性;5 1,3,5,7-环辛四烯解答:1,3,5,7-环辛四烯π电子数8不符合“4n+2”;因此根据休克尔规则,1,3,5,7-环辛四烯不具有芳香性;6 环丙烯正离子解答:环丙烯正离子具有闭合的2电子共轭大π健结构,且π电子数2符合“4n+2”;因此根据休克尔规则,环丙烯正离子具有芳香性;9. 以苯为主要原料合成下列化合物;1 叔丁基苯2 2,4-二硝基苯甲酸3 间硝基苯甲酸4 2-甲基-5-硝基苯磺酸5 环戊基苯10. 某芳烃A分子式为C8H10,被酸性高锰酸钾氧化生成分子式为C8H6O4的B;若将B进一步硝化,只得到一种一元硝化产物而无异构体,推出A、B的结构并写出反应式;解答:A和B的结构分别为:相关反应式如下:第五章芳香烃习题参考答案1. 简述卤代烃的结构特点、分类,并举例说明;参见教材第62页2. 写出分子式为C4H9Br所有异构体及名称,并指出它们分别属于伯、仲、叔卤烃的哪一种解答:所有可能的碳链如下所有异构体如下1-溴丁烷 2-溴丁烷 2-甲基-1-溴丙烷 2-甲基-2-溴丙烷伯卤烃仲卤烃伯卤烃叔卤烃3. 解释下列名词并举例说明:1 亲核试剂2 亲核取代反应3 反应底物4 中心碳原子5 离去基团6 消除反应参见教材4. 叙述卤代烷的单分子亲核取代反应SN 1机理和双分子亲核取代反应SN2机理;参见教材解答:1.单分子亲核取代反应SN1以叔溴丁烷的水解反应为例加以讨论;叔溴丁烷的水解反应的分两步进行;第一步:叔丁基溴的C—Br键发生异裂,生成叔丁基碳正离子和溴负离子,此步反应的速率很慢;第二步:生成的叔丁基碳正离子很快地与进攻试剂结合生成叔丁醇;2. 双分子亲核取代反应SN2实验证明,溴甲烷水解反应的机制为SN2,反应一步完成:该反应的反应速率与溴甲烷和碱的浓度有关,称为双分子亲核取代反应,用SN22代表决定反应速率所涉及的两种分子表示;在该反应过程中,OH-从Br的背面进攻带部分正电荷的α-C,C—O键逐渐形成,C—Br键逐渐变弱形成一个过渡状态;然后C—Br 键迅速断裂,C—O键形成,完成取代;5. 简述卤代烷的消除反应和亲核取代反应及二者之间的关系;参见教材6. 用系统命名法命名下列化合物;(1)(2)(3)CH3C(CH3)2CH2Br CH3CH2CHBrCH2I CH2CHCH2CH3Cl 2,2-二甲基-1-溴丙烷 2-溴-1-碘丁烷 1-苯基-2-氯丁烷 3-甲基-3-碘-1-戊烯 3-氯环己烯 2-甲基-1-溴萘间溴甲苯 1-环戊基-2-溴乙烷7. 写出下列化合物的结构式;1 二碘二溴甲烷2 叔丁基溴3 烯丙基氯4 氟烷5 1-溴-1-丙烯6 2,4-二氯甲苯7 苄基氯8 5-溴-1,3-环己二烯8. 完成下列反应式9. 完成下列转变解答:解答:解答:解答:10. 用化学方法鉴别下列各组化合物;1 氯苯、苄基氯、1-苯基-2-氯丙烷解答:各取待测物少许分别与硝酸银醇溶液混合,室温下立即产生白色沉淀的为苄基氯;加热后产生白色沉淀的为1-苯基-2-氯丙烷,余者为氯苯;2 溴苯、溴乙烯、异丙基溴解答:各取待测物少许分别与硝酸银醇溶液混合加热,产生淡黄色沉淀的为异丙基溴;将剩余2种待测物分别与高锰酸钾酸性溶液混合,能使高锰酸钾紫红色褪色的是溴乙烯,余者为溴苯;3 2-氯丙烯、2-氯丙烷、3-氯丙烯、3-碘环戊烯解答:各取待测物少许分别与硝酸银醇溶液混合,立即产生黄色沉淀的为3-碘环戊烯,立即产生白色沉淀的为3-氯丙烯,加热后产生白色沉淀的为2-氯丙烷,余者为2-氯丙烯;4 4-溴-1-丁炔、2-溴-2-丁烯、3-溴环戊烯解答:各取待测物少许分别与硝酸银醇溶液混合,立即产生淡黄色沉淀的为3-溴环戊烯,立即产生白色沉淀的为4-溴-1-丁炔,余者为2-溴-2-丁烯;11. 下列卤代烃与氢氧化钾醇溶液发生消除反应,按反应速率由大到小排列顺序;2-甲基-1-氯丁烷、2-甲基-2-氯丁烷、2-甲基-3-氯丁烷解答:2-甲基-2-氯丁烷 > 2-甲基-3-氯丁烷 > 2-甲基-1-氯丁烷12. 下列卤代烃与硝酸银醇溶液反应,按生成沉淀的快慢顺序排列; 1-溴环己烯、4-溴环己烯、溴化苄、1-甲基-1-溴环己烷解答:溴化苄 > 1-甲基-1-溴环己烷 > 4-溴环己烯 > 1-溴环己烯1. 写出下列化合物的名称或结构简式2,2-二甲基-3-戊烯-1-醇甲基异丙基醚2. 完成下列反应式3. 用化学方法区别下列化合物1 正丁醇、仲丁醇和叔丁醇解答:各取待测物少许分别与卢卡斯试剂浓盐酸+无水ZnCl2混合,室温下立即出现沉淀的是叔丁醇,过5~10分钟出现沉淀的是仲丁醇,无沉淀的是正丁醇;2 苯甲醇和对甲苯酚解答:各取待测物少许分别与FeCl3混合,出现显着颜色变化的是对甲苯酚;3 1,3-丁二醇和2,3-丁二醇解答:各取待测物少许分别与新制CuOH2混合并振摇,CuOH2溶解并得到深蓝色溶液的是2,3-丁二醇,余者为1,3-丁二醇;4. 苯甲醇和苯酚都含有苯环和羟基,为什么他们性质有很大差别解答:苯酚中的羟基与苯环发生了p-π共轭,而苯甲醇中的羟基与苯环相隔一个碳原子没有共轭发生,因此他们的性质大相径庭;5. 推导结构化合物AC9H12O与NaOH、KMnO4均不反应,遇HI生成B和C,B遇溴水立即变为白色浑浊,C经NaOH水解,与Na2Cr2O7的H2SO4溶液反应生成酮D,试写出A、B、C、D的结构简式与相应反应式;解答:A、B、C、D的结构简式为相关反应式如下:A B CD1. 写出下列化合物的结构式14-甲基-3-戊烯-2-酮 2α,γ-二甲基己醛 3甲基异丁基酮43-硝基苯乙酮 5环己酮腙2. 命名下列化合物2,4-戊二酮对甲氧基苯甲醛 3-环己基丙醛 3-戊烯-2-酮 2,8-二羟基-9,10-蒽醌对苯醌单肟3. 写出苯甲醛和环己酮分别与下列化合物的反应如果有的话所得产物的结构式;1 托伦试剂苯甲醛与托伦试剂作用的产物是:环己酮与托伦试剂不反应;,H+,加热2 KMnO4环己酮一般条件下不易被氧化;3 2,4-二硝基苯肼4 NaHSO35 LiAlH46 浓NaOH苯甲醛与之作用的产物为:环己酮与之不反应;7 乙醇,HCl苯甲醛与之作用的产物为:环己酮与之不反应;8 乙基溴化镁苯甲醛与之作用的产物为:环己酮与之作用的产物为:9 稀NaOH苯甲醛和环己酮与稀碱均不作用;4. 完成下列反应式;5. 按照与HCN反应的活性,由高至低顺序排列下列各组化合物;解答:空间位阻的不同造成上述顺序;解答:硝基的吸电子作用增加了羰基碳原子的正电荷有利于亲和加成反应;甲氧基通过p,π-共轭效应供电子使羰基碳原子的正电荷降低不利于亲核加成反应;解答:空间位阻的不同是造成上述顺序的主要因素;6. 用简单方法区别下列各组化合物;1 苯甲醛、苯乙酮、环己酮解答:分别取上述待测物质少许与托伦试剂混合后水浴加热,出现银镜的为苯甲醛;将剩余两种待测物分别与碘的碱溶液混合,出现黄色沉淀的为苯乙酮,余者为环己酮;2 乙醛、丙醛、丁酮、二乙酮解答:取上述待测物少许分别与托伦试剂混合后水浴加热,出现银镜的是乙醛和丙醛,未有银镜出现的是丁酮和二乙酮;将乙醛和丙醛少许分别与碘的氢氧化钠溶液混合,出现黄色沉淀的乙醛,另一个溶液,出现白色结晶的为丁酮,未为丙醛;将丁酮和二乙酮少许分别滴入饱和NaHSO3有沉淀的是二乙酮;3 甲醛、仲丁醇、丁醛、3-戊酮解答:取上述待测物少许分别与西夫试剂混合,出现紫红色的是甲醛和丁醛,然后加入浓硫酸,紫色不退色的为甲醛,紫色褪去的为丁醛;与西夫试剂混合后未有颜色变化的是仲丁醇和3-戊酮;各取它俩少许分别与2,4-二硝基苯肼混合,出现黄色结晶沉淀的为3-戊酮,余者为仲丁醇;4 2-丁烯醛、异丁醛、3-戊酮、异丁醇解答:各取上述待测物少许,分别与溴水混合,能使溴水棕色褪至无色的是2-丁烯醛;将剩余3待测物少许分别与托伦试剂混合后水浴加热,产生银镜的是异丁醛;将最后2个待测物少许分别与2,4-二硝基苯肼混合,出现黄色结晶沉淀的是3-戊酮;7. 用6个碳以下的直链醛或酮合成下列化合物,无机试剂任选;请写出各步反应式;1 2-辛醇2 3-甲基-3-己醇3 正庚醇4 异己烷解答:1合成2-辛醇的方法首先制得格氏试剂己基溴化镁:然后用己基溴化镁与乙醛反应制得2-辛醇: 2合成3-甲基-3-己醇的方法 首先制得格氏试剂丙基溴化镁:然后用丙基溴化镁与丁酮反应制得3-甲基-3-己醇: 3合成正庚醇的方法首先制得格氏试剂己基溴化镁见前题;然后用己基溴化镁与甲醛作用制得正庚醇:4合成异己烷的方法 首先制得2-甲基-3-戊酮:然后用克莱门森还原法制得异己烷:8. 某化合物化学式为C 5H 12OA,A 氧化后得一产物C 5H 10OB;B 可与亚硫酸氢钠饱和溶液作用,并有碘仿反应;A 经浓硫酸脱水得一烯烃C,C 被氧化可得丙酮;写出A 可能的结构式及有关反应式;解答:A 的结构式为: 有关反应式如下:9. 某化合物AC 6H 10O 2可使溴水褪色,可与2,4-二硝基苯肼产生沉淀,并能与三氯化铁显色,无银镜反应;试写出A 的结构式;解答:A 的结构式为:CH 3CHCH(CH 3)2OH第八章 羧酸及其衍生物习题参考答案1. 命名下列化合物β-甲基丁酸 对苯二甲酸 3-苯基丁酸3,7—壬二烯酸 丙酰氯对甲基苯甲酰氯 乙丙酐 二甲基丙二酸二乙酯 乙酸异丙酯 丙酰胺2. 写出下列化合物的结构式1 2,3-二甲基戊酸2 反-2-甲基-2-丁烯酸当归酸3 α,α-二氯丁酸4 丙二酸甲乙酯5 邻苯二甲酸酐6 丙烯酰氯 3. 比较下列化合物酸性的强弱 1 丙酸 丙二酸 乙二酸 解答:乙二酸 > 丙二酸 > 丙酸2 α-氯丙酸 α,α-二氯丙酸 丙酸 β-氯丙酸 解答:α,α-二氯丙酸 >α-氯丙酸>β-氯丙酸> 丙酸 4. 写出乙酸与下列试剂的反应方程式;1 乙醇2 五氯化磷3 氨4 氢化锂铝5. 用化学方法鉴别下列各组化合物 1 甲酸 乙酸 乙醛解答:取上述待测物少许,分别与石蕊试剂混合,不出现红色的是乙醛;将能使石蕊变红的两个化合物分别与高锰酸钾溶液混合,能使高锰酸钾紫红色褪色的是甲酸,余者为乙酸;解答:取上述待测物少许,分别与2,4-二硝基苯肼混合,能使之出现黄色结晶状沉淀的是对-羟基苯乙酮;将余下两种待测物分别与溴水混合,能使溴水褪色的是乙烯基对苯二酚,余者为对甲基苯甲酸;6. 写出下列反应的主要产物或反应所需的条件7. 完成下列转化+CH 3COOH CH 3CH 2CH 3COOC 2H 5+H 2O +CH 3COOH CH 3COCl +HCl PCl +POCl 3+CH 3COOH CH 3COONH NH 3+CH 3CONH 2H 2O CH 3LiAlH4CH 3CH 2OH1 由异丁烯制备2,2-二甲基丙酸解答: 2 由乙炔制乙酸乙酯解答:3 由丙二酸二乙酯制丁酸 解答:8. 写出分子式为C 5H 6O 4的不饱和二元羧酸的各种异构体的结构式,如有顺反异构,则注明Z 、E 构型;解答:9.有三种化合物的分子式均为C 3H 6O 2,其中A 能与NaHCO 3反应放出CO 2,B 和C 则不能;B 和C 在NaOH 溶液中加热均可发生水解,B 的水溶液蒸馏出的液体能发生碘仿反应,而C 的则不能;试推测A 、B 、C 的结构式;解答:MgCO 2H 2O CH 3C CH 2CH 3HBrCH 3C CH 3CH 3Br(CH 3)3(CH 3)3CCOOH KMnO 4 , H H 2O , Hg 2+HC CH CH 3CH 3COOH +CH 3COOC 2H 51. 命名下列化合物;β-羟基丁酸γ-戊酮酸 3-甲基-4-羟基丁酸 2-氨基-3-4-羟基苯基丙酸α-甲基-γ-戊酮酸 4-甲基-3-氯戊酸2. 写出下列化合物的结构式;3. 完成下列反应式;4. 用简单化学方法鉴别下列每组化合物;解答:各取三种待测物少许分别与FeCl3溶液混合,没有出现显色现象的是乳酸;将与FeCl3溶液显色的2种待测物分别与2,4-二硝基苯肼试剂作用,出现黄色结晶的是乙酰乙酸乙酯,余者为水杨酸;解答:各取2种待测物少许分别与FeCl3溶液混合,出现显色现象的是2,4-戊二酮,另一个就是丙酮;3 丙二酸二乙酯与乙酰乙酸乙酯解答:各取2种待测物少许,分别与2,4-二硝基苯肼试剂作用,出现黄色结晶的是乙酰乙酸乙酯,另一个为丙二酸二乙酯;5. 将下列化合物按其酸性从大到小次序排列;6. 将下列化合物写成酮式与烯醇式的互变平衡体系;7. 用乙酰乙酸乙酯及其他必要的试剂合成下列化合物;解答:解答:解答:解答:8. 化合物AC9H10O3,它不溶于水,稀盐酸及稀碳酸氢钠溶液,但能溶于氢氧化钠溶液;A与稀氢氧化钠共热后,冷却酸化得一沉淀BC7H6O3,B能溶于NaHCO3溶液,并放出气体,B遇FeCl3溶液产生紫色,B的一种衍生物是常用药物APC的成分之一;试写出A、B 的结构式及各步反应式;解答:A、B的结构式为:有关反应式如下:1. 下列化合物中,哪些是旋光性物质哪些是非旋光性物质为什么解答:1是非旋光性物质,因为以其结构中的碳原子和2个氯原子所确定的平面是分子的对称面,具有对称面的分子不具有手性;2、3、4、5和6均是旋光性物质,其中2、3、4分子中均含有多个不同的手性碳原子,属于手性分子;5和6两个化合物的空间结构不含有对称面和对称中心等对称因素,因而属于手性分子;2. 下列各对化合物哪些互为对映异构体哪些互为非对映异构体哪些为同一化合物同一个化合物互为对映体互为对映体互为非对映体3. 写出下列旋光性物质所有的光学异构体的费歇尔投影式,并指出它们之间的关系;解答:1的所有光学异构体的费歇尔投影式如下:Ⅰ与Ⅱ互为对映体;Ⅲ是内消旋体,不具有旋光性;Ⅰ与Ⅲ、Ⅱ与Ⅲ的关系为非对映体;2的所有光学异构体的费歇尔投影式如下:Ⅰ与Ⅱ、Ⅲ与Ⅳ互为对映体;Ⅰ和Ⅱ中的任意一个与Ⅲ和Ⅳ中的任意一个互为非对映体;4. 用R、S构型标示方法标示下列化合物中手性碳原子的构型;R S R2R,3S S5. 写出下列光学活性药物的费歇尔投影式,并指出是赤型还是苏型;1 1R,2S---2-甲氨基-1-苯基-1-丙醇左旋麻黄碱2 1R,2R---1-对硝基苯基-2-二氯乙酰氨基-1,3-丙二醇左旋氯霉素6. 写出下列化合物的费歇尔投影式,用R、S构型标示方法标出手性碳原子的构型;S 2R,3R 2S,3R 1R,2R7. 解释下列名词;略8. 某蔗糖溶液在20℃及2dm长的盛液管中测得旋光度为+°,求该蔗糖溶液的浓度;。

烷烃1.用系统命名法命名下列化合物:1.(CH 3)2CHC(CH 3)2CHCH 3CH 32.CH 3CH 2CH CHCH 2CH 2CH 3CH 3CH(CH 3)23-甲基-4-异丙基庚烷2,3,3,4-四甲基戊烷 2,4-二甲基-3-乙基己烷3.CH 3CH 2C(CH 3)2CH 2CH 34.CH 3CH 3CH 2CHCH 2CH 2CCH 2CH 3CHCH 3CH 3CH 2CH 3123456783,3-二甲基戊烷 2,6-二甲基-3,6-二乙基辛烷5.12345676.2,5-二甲基庚烷 2-甲基-3-乙基己烷7.8.12345672,4,4-三甲基戊烷 2-甲基-3-乙基庚烷2.写出下列各化合物的结构式:1.2,2,3,3-四甲基戊烷 2,2,3-二甲基庚烷CH 3CCCH 2CH 3CH 3CH 3CH 3CH 3CH 3CH 3CHCHCH 2CH 2CH 2CH 3CH 33、 2,2,4-三甲基戊烷4、2,4-二甲基-4-乙基庚烷CH 3C CHCH 3CH 3CH 3CH 3CH 3CHCH 2CCH 2CH 2CH 3CHCH 3CH 3CH 35、 2-甲基-3-乙基己烷6、三乙基甲烷CH 3CH 3CHCHCH 2CH 2CH 3CH 2CH 3CH 3CH 2CHCH 2CH 3CH 2CH 37、甲基乙基异丙基甲烷 8、乙基异丁基叔丁基甲烷CH3CHCH(CH3)2 CH2CH3CH3CH2CH C(CH3)3CH2CHCH3CH33.用不同符号表示下列化合物中伯、仲、叔、季碳原子32CCH32CH3CCH3CH31.0011111122CH342.4313323)334.2.3.4.5.6.1.5.不要查表试将下列烃类化合物按沸点降低的次序排列:(1) 2,3-二甲基戊烷 (2) 正庚烷 (3) 2-甲基庚烷(4) 正戊烷 (5) 2-甲基己烷解:2-甲基庚烷>正庚烷> 2-甲基己烷>2,3-二甲基戊烷> 正戊烷(注:随着烷烃相对分子量的增加,分子间的作用力亦增加,其沸点也相应增加;同数碳原子的构造异构体中,分子的支链愈多,则沸点愈低。

第一章习题(一) 用简单的文字解释下列术语:(1)键能:形成共价鍵的过程中体系释放出的能量,或共价鍵断裂过程中体系所吸收的能量。
(2)构造式:能够反映有机化合物中原子或原子团相互连接顺序的化学式。
(3)sp2杂化:由1 个s轨道和2个p轨道进行线性组合,形成的3个能量介于s轨道和p轨道之间的、能量完全相同的新的原子轨道。
sp2杂化轨道的形状也不同于s轨道或p轨道,而是“一头大,一头小”的形状,这种形状更有利于形成σ键。
(4)相转移催化剂:在非均相反应中能将反应物之一由一相转移到另一相的催化剂。
第二章饱和烃习题(一) 用系统命名法命名下列各化合物,并指出这些化合物中的伯、仲、叔、季碳原子。
(1) 1234567(2)123453-甲基-3-乙基庚烷2,3-二甲基-3-乙基戊烷(3)123456(4) 101234567892,5-二甲基-3,4-二乙基己烷1,1-二甲基-4-异丙基环癸烷(5) (6)1234乙基环丙烷2-环丙基丁烷(7)12345678910(8)123456789CH3 1,7-二甲基-4-异丙基双环[4.4.0]癸烷2-甲基螺[3.5]壬烷(9)1234567(10) (C H3)3C C H25-异丁基螺[2.4]庚烷新戊基(11)H3C (12)C H3C H2C H2C H2C H C H32-甲基环丙基2-己基or (1-甲基)戊基(十) 已知环烷烃的分子式为C5H10,根据氯化反应产物的不同,试推测各环烷烃的构造式。
(1) 一元氯代产物只有一种(2) 一元氯代产物可以有三种解:(1) (2)C H3C H3(十一) 等物质的量的乙烷和新戊烷的混合物与少量的氯反应,得到的乙基氯和新戊基氯的摩尔比是1∶2.3。
试比较乙烷和新戊烷中伯氢的相当活性。
解:设乙烷中伯氢的活性为1,新戊烷中伯氢的活性为x ,则有:x123.261=15.1=x ∴ 新戊烷中伯氢的活性是乙烷中伯氢活性的1.15倍。

有机化学课后习题参考答案在有机化学的学习过程中,课后习题是巩固知识、深化理解的重要途径。
以下是为大家提供的一些常见课后习题的参考答案,希望能对大家的学习有所帮助。
一、选择题1、下列化合物中,属于醇类的是()A 甲醛B 乙醛C 乙醇D 乙酸答案:C解析:醇类是指羟基(OH)与烃基相连的有机化合物。
乙醇(C₂H₅OH)符合醇类的定义,甲醛(HCHO)、乙醛(CH₃CHO)属于醛类,乙酸(CH₃COOH)属于羧酸。
2、能与金属钠反应放出氢气的有机物是()A 苯B 乙醇C 四氯化碳D 乙酸乙酯答案:B解析:乙醇分子中含有羟基,羟基中的氢原子较活泼,能与金属钠反应放出氢气。
苯、四氯化碳和乙酸乙酯都不能与金属钠反应。
3、下列有机物中,能发生加成反应的是()A 甲烷B 乙烷C 乙烯D 乙酸答案:C解析:含有不饱和键(如双键、三键)的有机物能发生加成反应。
乙烯(CH₂=CH₂)含有双键,能发生加成反应。
甲烷(CH₄)和乙烷(C₂H₆)属于饱和烃,乙酸(CH₃COOH)一般不发生加成反应。
二、填空题1、乙醇的结构简式为_____,官能团是_____。
答案:C₂H₅OH;羟基(OH)解析:乙醇的化学式为 C₂H₆O,结构简式为 C₂H₅OH,官能团是羟基(OH)。
2、乙酸与乙醇发生酯化反应的化学方程式为_____。
答案:CH₃COOH + C₂H₅OH ⇌ CH₃COOC₂H₅+ H₂O解析:乙酸(CH₃COOH)和乙醇(C₂H₅OH)在浓硫酸作催化剂、加热的条件下发生酯化反应,生成乙酸乙酯(CH₃COOC₂H₅)和水。
3、写出丙烯(CH₃CH=CH₂)与溴水发生加成反应的化学方程式_____。
答案:CH₃CH=CH₂+ Br₂ → CH₃CHBrCH₂Br解析:丙烯中的双键与溴水发生加成反应,两个溴原子分别加到双键两端的碳原子上。
三、简答题1、简述有机化合物的特点。
答:有机化合物通常具有以下特点:(1)大多数有机化合物易燃,这是因为它们主要由碳、氢等元素组成,燃烧时能释放出大量的能量。

构思新颖,品质一流,适合各个领域,谢谢采纳目录第一章绪论 (1)第二章饱和烃 (2)第三章不饱和烃 (6)第四章环烃 (14)第五章旋光异构 (23)第六章卤代烃 (28)第七章波谱法在有机化学中的应用 (33)第八章醇酚醚 (43)第九章醛、酮、醌 (52)第十章羧酸及其衍生物 (63)第十一章取代酸 (71)第十二章含氮化合物 (78)第十三章含硫和含磷有机化合物 (86)第十四章碳水化合物 (89)第十五章氨基酸、多肽与蛋白质 (100)第十六章类脂化合物 (105)第十七章杂环化合物 (114)Fulin 湛师第一章 绪论1.1扼要归纳典型的以离子键形成的化合物与以共价键形成的化合物的物理性质。
答案:1.2 NaCl 与KBr 各1mol 溶于水中所得的溶液与NaBr 及KCl 各1mol 溶于水中所得溶液是否相同?如将CH 4及CCl 4各1mol 混在一起,与CHCl 3及CH 3Cl 各1mol 的混合物是否相同?为什么? 答案:NaCl 与KBr 各1mol 与NaBr 及KCl 各1mol 溶于水中所得溶液相同。
因为两者溶液中均为Na +,K +,Br -, Cl -离子各1mol 。
C+624H CCH 4中C 中有4个电子与氢成键为SP 3杂化轨道,正四面体结构CH 4SP 3杂化2p y2p z2p x2sH1.4写出下列化合物的Lewis 电子式。
a.C 2H 4b.CH 3Clc.NH 3d.H 2Se.HNO 3f.HCHOg.H 3PO 4h.C 2H 6i.C 2H 2j.H 2SO 4 答案:a.C C H H HHCC HH HH或 b.H C H c.H N Hd.H S He.H O NO f.O C H Hg.OPO O H H Hh.H C C HHH H HO P O O H HH或i.H C C Hj.O S O HH OH H或1.5下列各化合物哪个有偶极矩?画出其方向。

目录第一章绪论 (1)第二章饱和烃 (2)第三章不饱和烃 (6)第四章环烃 (14)第五章旋光异构 (23)第六章卤代烃 (28)第七章波谱法在有机化学中的应用 (33)第八章醇酚醚 (43)第九章醛、酮、醌 (52)第十章羧酸及其衍生物 (63)第十一章取代酸 (71)第十二章含氮化合物 (77)第十三章含硫和含磷有机化合物 (85)第十四章碳水化合物 (88)第十五章氨基酸、多肽与蛋白质 (99)第十六章类脂化合物 (104)第十七章杂环化合物 (113)Fulin 湛师第一章 绪论1.1扼要归纳典型的以离子键形成的化合物与以共价键形成的化合物的物理性质。
答案:1.2 NaCl 与KBr 各1mol 溶于水中所得的溶液与NaBr 及KCl 各1mol 溶于水中所得溶液是否相同?如将CH 4及CCl 4各1mol 混在一起,与CHCl 3及CH 3Cl 各1mol 的混合物是否相同?为什么? 答案:NaCl 与KBr 各1mol 与NaBr 及KCl 各1mol 溶于水中所得溶液相同。
因为两者溶液中均为Na +,K +,Br -, Cl -离子各1mol 。
由于CH 4与CCl 4及CHCl 3与CH 3Cl 在水中是以分子状态存在,所以是两组不同的混合物。
1.3碳原子核外及氢原子核外各有几个电子?它们是怎样分布的?画出它们的轨道形状。
当四个氢原子与一个碳原子结合成甲烷(CH 4)时,碳原子核外有几个电子是用来与氢成键的?画出它们的轨道形状及甲烷分子的形状。
答案:C+624H CCH 4中C 中有4个电子与氢成键为SP 3杂化轨道,正四面体结构CH 4SP 3杂化2p y2p z2p x2sH1.4写出下列化合物的Lewis 电子式。
a.C 2H 4b.CH 3Clc.NH 3d.H 2Se.HNO 3f.HCHOg.H 3PO 4h.C 2H 6i.C 2H 2j.H 2SO 4 答案:a.C C H H HHCC HH HH或 b.H C H c.H N Hd.H S He.H O NO f.O C H Hg.O POO H H Hh.H C C HHH H HO P O O H HH或i.H C C Hj.O S O HH OH H或1.5下列各化合物哪个有偶极矩?画出其方向。
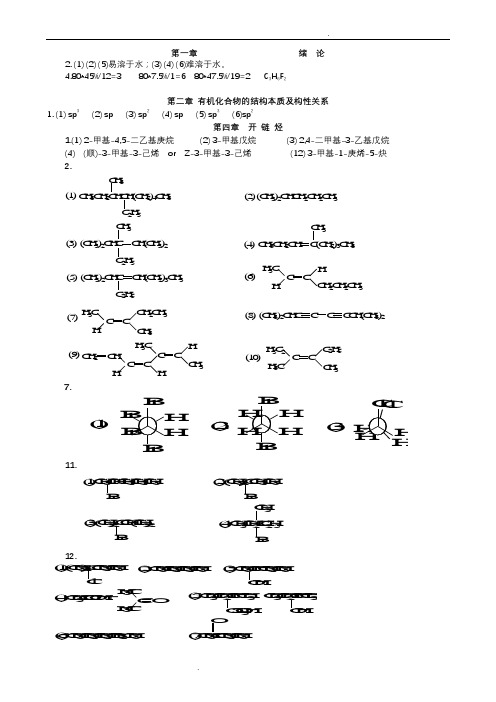
第一章绪论2. (1) (2) (5)易溶于水;(3) (4) (6)难溶于水。
4.80*45%/12=3 80*7.5%/1=6 80*47.5%/19=2 C3H6F2第二章有机化合物的结构本质及构性关系1.(1) sp3(2) sp (3) sp2(4) sp (5) sp3(6)sp2第四章开链烃1.(1) 2-甲基-4,5-二乙基庚烷(2) 3-甲基戊烷(3) 2,4-二甲基-3-乙基戊烷(4) (顺)-3-甲基-3-己烯or Z-3-甲基-3-己烯(12) 3-甲基-1-庚烯-5-炔2.7.11.14. (5) > (3) > (2) >(1) > (4) 即: CH 2=CHC +HCH 3 >(CH3)3C +>CH 3CH 2C +HCH 3 >CH 3CH 2CH 2C +H 2> (CH 3)2CHC +H 216. (1)(2)(3)17.21AB.10.(1)CH 3-CH=CH 2−−−−−→−+H /KMnO 4CH 3COOH(2)CH 3-C ≡CH+HBr (2mol ) CH 3CBr 2CH 3(3)CH 3-C ≡3-C=CH 2−−→−2Br CH 3CBr 2CH 2Br Br第四章 环 烃 2.1-戊烯 1-戊炔 戊 烷Br 2/CCl 4室温,避光√ 溴褪色√ 溴褪色× × √灰白色1-丁炔 2-丁炔 丁 烷Br 2/CCl 4 室温,避光√溴褪色 × Ag(NH 3)2+√灰白色↓ × × 1,3-丁二烯 1-己炔 2,3-二甲基丁烷Br 2/CCl 4√ 溴褪色 √ 溴褪色 × Ag(NH 3)2+×√ 灰白色↓C(CH 3)3CH 3(1)(2)(3)3.(1)反式CH 3Br(3)顺式4.C H 3B rC lC l +C l C lC O O HH 3CO 2N (C H 3)3C C O O H(1)(2)(3)(4)(5)(6)(7) B rC 2H 5C 2H 5B r +C H 3C O C H 3(C H 3)2C C H (C H 3)2B r(8) 1molCl 2 / h , 苯/无水AlCl 3N H C O C H 3N O 2C H 3C H 3S O 3H (9) (10)7. (2)有芳香性 10.第六章 旋光异构6-32. (1)× (2)× (3)× (4)√ (5)√ (6)√7.2.66120678.58.18][20+=⨯÷+=⨯=l c Dαα第七章 卤 代 烃2、C l C lC l (2)4、第八章 醇、酚、醚1. (1) 3-甲基-3-戊烯-1-醇 (2) 2-甲基苯酚 (3) 2,5-庚二醇 (4) 4-苯基-2-戊醇 (5) 2-溴-1-丙醇 (6) 1-苯基乙醇(7) 2-硝基-1-萘酚 (8) 3-甲氧基苯甲 (9) 1,2-二乙氧基乙烷(乙二醇二乙醚)(1)(2)3、4. (1) 甲醇 分子间氢键 (6) 邻硝基苯酚 分子内氢键、分子间氢键 5、(1)CH 2IH 3COOH(5)(6)HOOCH 3H(7)6、AgNO 3/乙醇,室温白↓× ×AgNO 3/乙醇,加热白↓×OH+OHBrBr(1)(2)10、OH O ClA B C D第九章醛、酮、醌一、命名下列化合物。
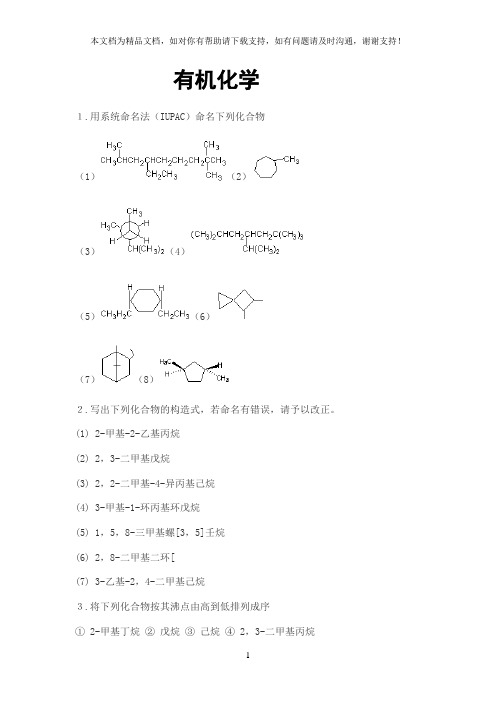
有机化学1.用系统命名法(IUPAC)命名下列化合物(1)(2)(3)(4)(5)(6)(7)(8)2.写出下列化合物的构造式,若命名有错误,请予以改正。
(1) 2-甲基-2-乙基丙烷(2) 2,3-二甲基戊烷(3) 2,2-二甲基-4-异丙基己烷(4) 3-甲基-1-环丙基环戊烷(5) 1,5,8-三甲基螺[3,5]壬烷(6) 2,8-二甲基二环[(7) 3-乙基-2,4-二甲基己烷3.将下列化合物按其沸点由高到低排列成序① 2-甲基丁烷② 戊烷③ 己烷④ 2,3-二甲基丙烷4.将下列自由基按稳定性大小排序① ② ③ ④5.写出由一个异丙基和一个异丁基组成的烷烃的构造式。
6.写出一个含有7个碳原子的烷烃,分子中有3组等性氢,其比值为6∶1∶1。
7.写出下列化合物的优势构象(1) 异丙基环己烷(2) (3) 顺-1-甲基-4-异丙基环己烷8.下列各对化合物是构造异构还是构象异构?(1)与(2)与9.完成下列反应(写主要产物)(1)(2)10.写出相对分子质量为100,并含有伯、叔、季碳原子的烷烃的可能构造式。
11.饱和烃的分子式为C7H14,写出符合下列条件的可能结构:(1)没有伯碳原子;(2)含有一个伯碳原子和一个叔碳原子;(3)含有两个伯碳原子,没有叔碳原子。
12.某烷烃的相对分子质量为72,溴化时,(1)只得一种一溴代产物;(2)得到三种一溴代产物;(3)得到四种一溴代产物。
分别写出相应烷烃的结构。
第三章1.命名下列化合物。
(1)(2) (3)(4) (5) (6)(7)(8)(9)(10)(11)(12)2.写出下列化合物的结构式。
(1) E- 2, 5-二甲基-3-己烯(2) E-3-乙基-4-氯-2-己烯(3) 异戊二烯(4) 2, 2, 5-三甲基-3-己炔(5)(2E, 4Z)-6-甲基-2, 4-庚二烯(6) 1-己烯-5 -炔(7) (Z)-3-乙基-4-丙基-1, 3-己二烯-5-炔3.写出下列反应式。

烷烃1.用系统命名法命名下列化合物:1.(CH 3)2CHC(CH 3)2CHCH 3CH 32.CH 3CH 2CH CHCH 2CH 2CH 3CH 3CH(CH 3)23-甲基-4-异丙基庚烷2,3,3,4-四甲基戊烷 2,4-二甲基-3-乙基己烷3.CH 3CH 2C(CH 3)2CH 2CH 34.CH 3CH 3CH 22CH 2CCH 2CH 3CHCH 3CH 3CH 2CH 3123456783,3-二甲基戊烷 2,6-二甲基-3,6-二乙基辛烷5.12345676.2,5-二甲基庚烷 2-甲基-3-乙基己烷7.8.12345672,4,4-三甲基戊烷 2-甲基-3-乙基庚烷2.写出下列各化合物的结构式:1.2,2,3,3-四甲基戊烷 2,2,3-二甲基庚烷CH 3CCCH 2CH 3CH 3CH 3CH 3CH 3CH 3CH 3CHCHCH 2CH 2CH 2CH 3CH 33、 2,2,4-三甲基戊烷4、2,4-二甲基-4-乙基庚烷CH 3C CHCH 3CH 3CH 3CH 3CH 3CHCH 2CCH 2CH 2CH 33CH 3CH 35、 2-甲基-3-乙基己烷6、三乙基甲烷CH 3CH 3CHCHCH 2CH 2CH 32CH 3CH 3CH 2CHCH 2CH 32CH 37、甲基乙基异丙基甲烷 8、乙基异丁基叔丁基甲烷CH3CHCH(CH3)22CH3CH3CH2CH C(CH3)3CH2CHCH3CH33.用不同符号表示下列化合物中伯、仲、叔、季碳原子32CCH32CH3CCH3CH31.0011111122CH342.4313323)334.2.3.4.5.6.1.5.不要查表试将下列烃类化合物按沸点降低的次序排列:(1) 2,3-二甲基戊烷 (2) 正庚烷 (3) 2-甲基庚烷(4) 正戊烷 (5) 2-甲基己烷解:2-甲基庚烷>正庚烷> 2-甲基己烷>2,3-二甲基戊烷> 正戊烷(注:随着烷烃相对分子量的增加,分子间的作用力亦增加,其沸点也相应增加;同数碳原子的构造异构体中,分子的支链愈多,则沸点愈低。


第一章绪论2. (1) (2) (5) 易溶于水;(3) (4) (6) 难溶于水。
4.80*45%/12=3 80*7.5%/1=6 80*47.5%/19=2 C 3H6F2第二章有机化合物的结构本质及构性关系1. (1) sp 3(2) sp (3) sp 2 (4) sp (5) sp 3 (6)sp2第四章开链烃1. (1) 2- 甲基-4,5- 二乙基庚烷(2) 3- 甲基戊烷(3) 2,4- 二甲基-3- 乙基戊烷(4) ( 顺)-3- 甲基-3- 己烯or Z-3- 甲基-3- 己烯(12) 3- 甲基-1- 庚烯-5- 炔2.CH3(1)CH3CH2CH C H (CH2)4CH3 (2) (CH3)2CHCH2CH2CH3C2H5CH3C H3(3) (CH3)2CHC CH(CH3)2 (4) CH3CH2CH C(CH2)3CH3C2H5 (5) (CH3)2CHC CH(CH2)3CH3C2H5H3C(6) C CHHCH2CH2CH3H3C CH2CH3(7) (8) (CH3)2CHC C C CCH(CH3)2C CH CH3(9)H3CC CCH2 CHC CH HHCH3H5C2 C2H5(1 0) C CH3CCH37.(1)Br BrBr H HCl Cl H(2) (3)HBrH H H HH HBrBr11.(1) CH3CHCH2CH2CH3 (2) (CH3)2CCH2CH3Br BrCH3(3) (CH3)2CCH( C H3)2(4) C H3CH2CC2H5BrBr 12.(1) (2) CH3CH2CH2CH3 (3) CH3CHCH2CH3(CH3)2CCH2CH3ClOHH3C (4) CH3COOH + C OH3C (5) C H3CH2CHCH3OSO3HOC H3CH2CHCH3OH(6) CH3CH2CH2CBr2C H3 (7)C H3CCH2CH3Br(8) ( C H3)2CCH CH2 + (CH3)2C CH C H2BrCH CH2CHO (9) ( CH2C CH C H2 ) n (10)+ ( CH2 C ) nClCl14. (5) >(3) >(2) >(1) >(4) 即:+HCH + CH2=CHC 3 >(CH3) 3C+HCH +H +H>CH3CH2C 3 >CH3CH2CH2C 2>(CH3) 2CHC216. (1)1-戊烯√溴褪色+ ×Ag(NH 3)21-戊炔B r 2/CCl 4室温,避光√溴褪色√灰白色戊烷×(2)1-丁炔+Ag(NH 3)2√灰白色↓√溴褪色Br2/CCl 42-丁炔×室温,避光×丁烷×(3)1,3-丁二烯√溴褪色+ ×Ag(NH 3)2Br2/CCl 4 1-己炔√溴褪色√灰白色↓2,3-二甲基丁烷×17.(2)H2OCH CH [CH2 CHOH]H2SO4,H g SO4C H3CHO21 A B.10.(1)CH3-CH=CH2KMnO / H4 CH3COOH(2)CH3- C≡CH+HB(r 2mol)CH 3CBr2CH3HBr (1mol )(3)CH3- C≡CH CH3-C=CH2 Br2 CH3CBr2CH2BrBr第四章环烃2.C(CH 3 )3(1) (2) (3)CH 33.(1)(3)C H 3Br反式顺式4.Br ClCl +Cl(1)(2)(3)( C H 3)2CCH (CH 3)2 O 2NC H 3BrClB r(4)(5)H 3CCOOHC 2H 5+ Br C 2H 5(6) (CH 3)3CCOOH(7) CH 3COCH 3(8) 1molCl2/ h, 苯/ 无水 AlCl 3CH 3N H COCH 3NO 2(9) (10)SO 3HC H 37. (2) 有芳香性 10.第六章 旋光异构6-32. (1) × (2) × (3) × (4) √ (5) √ (6) √7. [ ] 20 Dc l18.85.678 20 166.2第七章卤代烃2、Cl白↓ClAgNO 3/乙醇,室温(2)×白↓AgNO 3/乙醇,加热××Cl4、第八章醇、酚、醚1. (1) 3- 甲基-3- 戊烯-1- 醇(2) 2- 甲基苯酚(3) 2,5- 庚二醇(4) 4- 苯基-2- 戊醇(5) 2-溴-1- 丙醇(6) 1- 苯基乙醇(7) 2- 硝基-1- 萘酚(8) 3- 甲氧基苯甲(9) 1,2- 二乙氧基乙烷(乙二醇二乙醚)3、(2)(1)4. (1) 甲醇分子间氢键(6) 邻硝基苯酚分子内氢键、分子间氢键5、(1)H3 CO OH(5) (6) (7)H OHCH2I OCH 36、(1)OH+O,△浓硫酸,△H 3OHBr(2)浓硫酸,△Br2/CCl4OHBrKOH/EtOH△10、OH O ClA B C D第九章醛、酮、醌一、命名下列化合物。

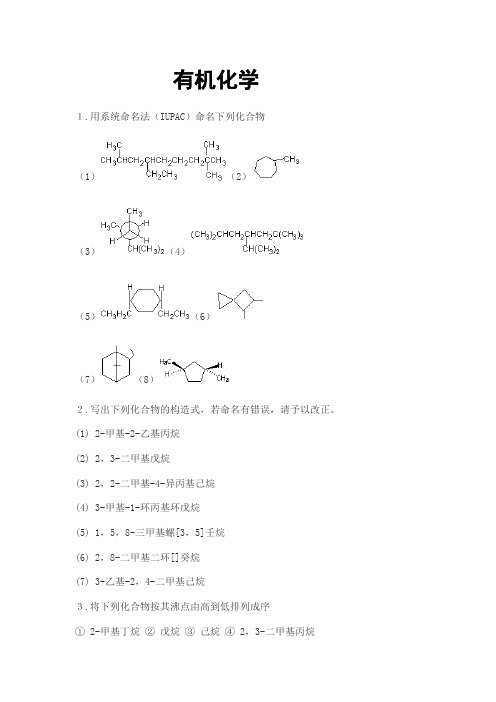
有机化学1.用系统命名法(IUPAC)命名下列化合物(1)(2)(3)(4)(5)(6)(7)(8)2.写出下列化合物的构造式,若命名有错误,请予以改正。
(1) 2-甲基-2-乙基丙烷(2) 2,3-二甲基戊烷(3) 2,2-二甲基-4-异丙基己烷(4) 3-甲基-1-环丙基环戊烷(5) 1,5,8-三甲基螺[3,5]壬烷(6) 2,8-二甲基二环[]癸烷(7) 3-乙基-2,4-二甲基己烷3.将下列化合物按其沸点由高到低排列成序① 2-甲基丁烷② 戊烷③ 己烷④ 2,3-二甲基丙烷4.将下列自由基按稳定性大小排序① ② ③ ④5.写出由一个异丙基和一个异丁基组成的烷烃的构造式。
6.写出一个含有7个碳原子的烷烃,分子中有3组等性氢,其比值为6∶1∶1。
7.写出下列化合物的优势构象(1) 异丙基环己烷(2) (3) 顺-1-甲基-4-异丙基环己烷8.下列各对化合物是构造异构还是构象异构?(1)与(2)与9.完成下列反应(写主要产物)(1)(2)10.写出相对分子质量为100,并含有伯、叔、季碳原子的烷烃的可能构造式。
11.饱和烃的分子式为C7H14,写出符合下列条件的可能结构:(1)没有伯碳原子;(2)含有一个伯碳原子和一个叔碳原子;(3)含有两个伯碳原子,没有叔碳原子。
12.某烷烃的相对分子质量为72,溴化时,(1)只得一种一溴代产物;(2)得到三种一溴代产物;(3)得到四种一溴代产物。
分别写出相应烷烃的结构。
第三章1.命名下列化合物。
(1)(2) (3)(4) (5) (6)(7)(8)(9)(10)(11)(12)2.写出下列化合物的结构式。
(1) E- 2, 5-二甲基-3-己烯(2) E-3-乙基-4-氯-2-己烯(3) 异戊二烯(4) 2, 2, 5-三甲基-3-己炔(5)(2E, 4Z)-6-甲基-2, 4-庚二烯(6) 1-己烯-5 -炔(7) (Z)-3-乙基-4-丙基-1, 3-己二烯-5-炔3.写出下列反应式。
1-3 写出下列化合物短线构造式。
如有孤对电子对,请用黑点标明。
÷C C CC C CNHHH H HC CH HHC O H HHHC H C H ONOH C HOC H HHHOHC HCO OCC H H HHC HCCHH C HNOOHC H C HOH(1)(2)(3)(4)(5)(6)(7)(8)(9)1-5 判断下列画线原子的杂货状态 (1)sp 2,(2)sp ,(3)sp ,(4)sp 3,(5)sp ,(6)sp 。
1-6哪些分子中含有极性键?哪些是极性分子?试以“”标明极性分子中偶极矩方向。
答:除(2)外分子中都含有极性键。
(2)和(3)是非极性分子,其余都是极性分子。
分子中偶极矩方向见下图所示,其中绿色箭头所示的为各分子偶极矩方向。
HH 33H 3I I(1)(2)(3)(5)(6)(7)(8)1-7 解释下列现象。
(1)CO 2分子中C 为sp 杂化,该分子为直线型分子,两个C=O 键矩相互抵消,分子偶极矩为零,是非极性分子;而SO2分子中S 为sp2杂化,分子为折线型,两个S —O 键矩不能抵消,是极性分子。
(2)在NH 3中,三个N —H 键的偶极朝向N ,与电子对的作用相加;而NF 3中三个N —F 键的偶极朝向F ,与N 上的未成对电子的作用相反并有抵消的趋势。
(3)Cl和F为一同主族元素,原子共价半径是Cl比F大,而电负性是F比Cl大。
键的偶极矩等于μ=qd,q为正电荷中心或负电荷中心上的电荷量,d为正负电荷中心的距离。
HCl 键长虽比HF的长,但F-中心上的电荷量大大于Cl-上的电荷量,总的结果导致HF的偶极矩大于HCl。
所以键长是H—Cl较长,偶极矩是H—F较大。
1-8 将下列各组化合物中指定键的键长由长到短排列并说明理由。
答:(1)从乙烷,乙烯到乙炔,碳原子杂化态由sp3到sp2至sp,s成份提高,拉电子能力增强,虽同属于碳氢键但键长缩短。
(2)键长顺序为C—I>C—Br>C—Cl>C—F。
因为卤素原子核外电子层数为I>Br>Cl >F,即其范德华半径为I>Br>Cl>F,则其原子共价半径I>Br>Cl>F。
(3)碳碳键键长为乙烷>乙烯>乙炔。
因为碳原子杂化态由sp3到sp2至sp,其共价键分别为单键、双键和叁键,碳碳原子间的作用力是乙烷<乙烯<乙炔,作用力越强,则两原子被拉得越紧,键长越短。
1-9 将下列各组化合物按酸性由强到弱排列。
(1)D>A>C>B;(2)A>B>D>C1-10 下列物种哪些是:(1)亲核试剂,(2)亲电试剂,(3)既是亲核试剂又是亲电试剂?答;(1)亲核试剂:Cl-,H2O,CH3OH,CH2=CH2,HCHO,CH3CN,-CH3;(2)亲电试剂:H+,AlCl3,Br+,Fe3+,+NO2,HCHO,CH3CN,+CH3,ZnCl2,Ag+,BF3;(3)既是亲核试剂又是亲电试剂:HCHO,CH3CN;(4)两者都不是的:CH4。
1-11 按质子酸碱理论,下列化合物哪些是酸?哪些是碱?哪些既是酸又是碱?答:酸:NH3,HS-,HBr,H2O,NH4+,HCO3-;碱:NH3,CN-,HS-,H2O,HCO3-;既是酸又是碱:NH3,HS-,H2O,HCO3-。
1-12 按Lewis酸碱理论,在下列反应中,哪个反应物为酸?哪个反应物为碱?答:(1)H2O 为酸,CN-为碱;(2)BF3为酸,HCHO为碱;(3)H2O 为酸,CH3NH2为碱;(4)Cu2+为酸,NH3为碱;(5)AlCl3为酸,COCl2为碱;(6)I2为酸,I-为碱。
1-13 指出下列哪些属于极性质子溶剂?哪些属于极性非质子溶剂?哪些属于非极性溶剂?答:极性质子溶剂:(5)(6);极性非质子溶剂:(1)(4)(7)(8);非极性溶剂:(2)(3)。
1-14 矿物油(相对分子质量较大饱和烃的混合物)不溶于水或乙醇中,但可以溶于正已烷。
答:矿物油为非极性分子,根据“相似相溶”原则,它可溶于非极性的正已烷,而不能溶于有极性的水或乙醇(水或乙醇醇间能形成氢键,分子间的引力非常强,故矿物油分子不能克服这种氢键与乙醇或水相互渗透而溶解)。
1-18 下列物质是否含有共轭酸和共轭碱?如有,请分别写出。
答:(1)即有共轭酸也有共轭碱,共轭酸是CH3NH3+,共轭碱是CH3NH2-;(2)共轭酸是CH3OH;(3)即有共轭酸也有共轭碱,共轭酸是CH3CH2OH2+,共轭碱是CH3CH2O-;(4)共轭酸是H2;(5)共轭酸是CH4;(6)共轭碱酸是CH3CH2+,共轭碱是CH2=CH-。
1-19 将下列物种按碱性,由强至弱排列成序。
答:参照书中表1-9排出,CH3CH2->H2N->HC≡C->CH3O->OH-。
1-20 下列极限式中,哪个式子是错误的,为什么?答:(1)中C是错的,因为此式中原子核的相对位置改变了;(2)中C是错的,因为此式中的单电子数改变了(A、B式中单电子数为1,C中为3);(3)中C和D是错的,因为C式2个N原子外层价电子数不是8(而是6和10),D式中间N原子外层价电子数也不符合八隅体要求。
2-1 用系统命名法命名下列烷烃。
(1)2,2,5-三甲基已烷;(2)3,6-二甲基-4-正丙基辛烷;(3)4-甲基-5-异丙基辛烷;(4)2-甲基-3-异丙基庚烷;(5)5-正丙基-6-异丙基十二烷;(6)3,3-二甲基-4-乙基-5-(1,2-二甲基丙基)壬烷;(7)4-异丙基-5-正丁基癸烷;(8)3,6,6-三甲基-4-正丙基壬烷。
2-2 用系统命名法命名下列不饱和烃。
(1)4-甲基-2-戊炔;(2)2,3-二甲基-1-戊烯-4-炔;(3)1-已烯-5-炔;(4)3-异丁基-4-己烯-1-炔;(5)3-甲基-2,4-庚二烯;(6)2,3-已二烯;(7)2-甲基-2,4,6-辛三烯;(8)4-甲基-1-已烯-5-炔;(9)亚甲基环戊烷;(10)2,4-二甲基-1-戊烯;(11)3-甲基-4-(2-甲基环已基)-1-丁烯。
2-3 用系统命名法命名下列化合物。
(1)3-甲基环戊烯;(2)环丙基乙烯;(3)4,4-二氯-1,1-二溴螺[2.4]庚烷;(4)3-烯丙基环戊烯;(5)1-甲基-3-环丙基环戊烷;(6)3,5-二甲基环已烯;(7)螺[4.5]-1,6-癸二烯;(8)1-甲基螺[3.5]-5-壬烯;(9)2-甲基-1-环丁基戊烷;(10)2,2-二甲基-1-环丁基二环[2.2.2]辛烷;(11)5,7,7-三甲基二环[2.2.1]-2-庚烯;(12)二环[4.2.0]-7-辛烯;(13)1-甲基-4-乙基二环[3.1.0]已烷。
2-4 写出下列化合物的构造式。
(1) 3-甲基环己烯(2) 3,5,5-三甲基环己烯(3) 二环[2.2.1]庚烷(4) 二环[4.1.0]庚烷(5) 二环[2.2.1]-2-庚烯(6)二环[3.2.0]-2-庚烯(7) 螺[3.4]辛烷(8) 螺[4.5]-6癸烯(9) 2-甲基二环[3.2.1]-6-辛烯(10) 7,7-二甲基二环[2.2.1]-2,5-庚二烯33 H33H3H3(1)(2)(3)(4)(5)(6)(7)(8)(9)(10)2-5 用系统命名法命名下列化合物。
(1)3,3-二甲基-2-苯基戊烷;(2)1,3,5-三甲基-2-异丙基苯(或2,4,6-三甲基异丙苯);(3)1-苯(基)丙烯;(4)二苯(基)乙炔;(5)1-甲基蒽;(6)2-环丙基萘(7)1,2-二苯基苯;(8)1,4-二甲基萘。
(1)3-甲基-1-溴丁烷; (2)2-甲基-3-氯丁烷; (3)1,1,3,3-四氟-1-氯丙烷; (4)二氟一氯甲烷;(5)氯甲基苯(或苯甲基氯,或氯化苄,或苄基氯,或苯一氯甲烷); (6)2-甲基-1,2-二碘丁烷; (7)(2-氯苯基)乙烯 ;(8)1-溴-1-丁烯-3炔; (9)3-甲基-6-溴环已烯; (10)4-甲基-5-氯 -2-戊炔。
2-7 写出下列化合物的构造式。
(1) 2,4-二硝基氟苯 (2) 六氯化苯 (3) 六溴代苯 (4) 氯化苄 (5) 2-甲基-2,3-二碘丁烷 (6) 2-氯-2-丁烯 (7)3-苯基-1-溴-2-丁烯 (8) 叔氯丁烷 (9) 仲丁基溴(1)(2)(3)(4)(5)(6)(7)(8)(9)FNO 22ClClClClCl Br BrBrBrBrBr CH 2Cl CH 3CCHCH3I CH 3IH 3CCCHCH 3CH 2CHCCH 3Br (CH 3)3CClCH 3CH 2CHCH 32-8用系统命名法命名下列化合物。
(1)4-甲基-2-戊醇; (2)3-甲氧-2-戊醇; (3)5-溴-1-已炔-3-醇; (4)3-苯基-1,2-戊二醇; (5)1-甲基环已醇; (6)5-甲基-1,3-苯二酚; (7)2-丁硫醇; (8)4-甲基-2-戊硫醇; (9)1-苯基-2-丙烯-1-醇; (10)4-甲基-4’-乙基二苯甲醇; (11)4-环戊烯-1,3-二醇; (12)4-(3,3-二甲基丁基)-6-苯基-5-已烯-3-醇 (13)1,4-丁二醇。
2-9 写出下列化合物的构造式。
(1) 仲丁醇 (2) 2,3-二甲基-2,3-丁二醇 (3) 二苯甲醇 (4) 新戊醇 (5) 1,3-丙二醇甲乙醚 (6) 乙硫醇 (7) 1-苯基-2-丙醇 (8 ) 间溴苯酚 (9) 异丁醇 (10) 叔丁醇 (11)对苯二酚 (12) 丙三醇 (13) β,β′-二甲氧基乙醚(1)(2)(3)(4)(5)(6)(7)(8)(9)(10)CH 3CHCH 2CH 3OHH 3CCCCH 33OH 3OHCH OHCH 32OHCH 3CH 3CH 2CH 2CH 232H 5CH 3CH 2SHCH 23OHOHBr(CH 3)2CHCH 2OH(CH 3)3COHOHHO(11)(12)(13)CH 2CHCH 2(CH 3OCH 2CH 2)2O(1)4-戊烯-2-酮; (2)3-甲基-2-丁烯醛; (3)3-羟基丁醛; (4)1,3-二苯基-2-丙烯酮; (5)3-苯基-2-丙烯醛(或β-苯基丙烯醛); (6)4-甲基环己基甲醛; (7)3-甲酰基己二醛; (8)3,3-二甲基-5-乙基-6-庚烯-2,4-二酮; (9)2,4-戊二酮; (10)3-甲酰基环戊酮(3-环戊酮甲醛); (11)螺[2.4]-5-庚酮; (12)4-溴已醛; (13)3-甲基-2,6-萘醌。
2-11写出下列化合物的构造式。
(1)(2)(3)(4)(5)(6)(7)OCOOH CHOHOOCHOOCCH 2CHCH 2CH 2CH 3NO 2COOHHOOCC CCH 3COOHCH 3HCOOCHCH 3CH 3CH 32CH 22CH 2CHCH 33ClO2-12 命名下列化合物。