【答案】C
2.医疗上颇为流行的“理疗特效热”,就是利用铁缓慢氧化放出 均匀、稳定的热,使患处保持温热状态。若 56 g 铁粉完全氧化成 氧化铁,需要消耗氧气的质量为( )。 A.24 g B.32 g C.21 g D.16 g
【解析】1 mol Fe 生成 mol Fe2O3,消耗氧气 mol,质量为 24 g。 【答案】A
【答案】0.1 mol。(本题可以用差量法计算,1 mol 锌完全反 应生成 1 mol H2,溶液质量增加 63 g,现在溶液质量增加 6.3 g, 则反应的锌的物质的量为 0.1 mol)
在反应 3Cl2+8NH3 6NH4Cl+N2 中,标准状况下有 33.6 L 的氯 气参加反应,求: (1)参加反应的氨的质量。 (2)产生氮气的分子数目。 (3)被氧化的 NH3 的物质的量。
n1=0.2 mol,12 .1 g ×100%=46.3%。 m(Zn)=6.5 g,n2=0.2 mol, 消耗 HCl 的物质的量为 n1+n2=0.42)0.4 mol
活动探究 物质的量在化学方程式计算中的应用
1.将 6.5 g 锌放入足量的盐酸中充分反应,生成标准状况下 氢气的体积是多少?
1.掌握物质的量与其他物理量(质量、 气体体积、 微粒个数、 浓度等)的换算关系。 2.掌握物质的量在化学方程式计算中的应用。 3.了解化学计算中的常用方法。
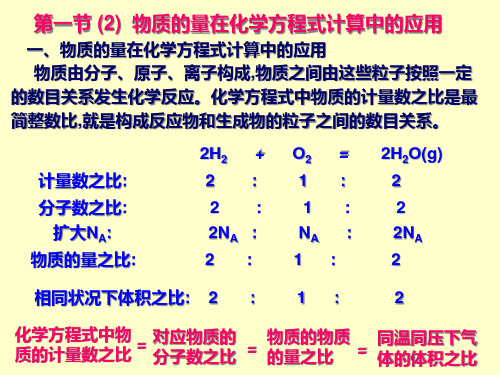
1.化学计量数与化学计量间的关系 2Na + 2H2O 2NaOH+H2↑ 质量之比 46 g∶ 36 g ∶ 80 g ∶ 2 g 化学计量数之比 2 ∶ 2 ∶ 2 ∶ 1 扩大 NA 倍 2NA ∶ 2NA ∶ 2NA ∶ NA 物质的量之比 2 mol∶ 2 mol ∶ 2 mol ∶ 1 mol 结论:化学方程式中各物质的化学计量数之比等于 ① ,也等于② 对于有气体参加的反应还等于③ 。