辅料检验SOP:硬脂酸镁
- 格式:doc
- 大小:33.50 KB
- 文档页数:4

1 目的确定硬脂酸镁检验的操作程序和方法,确保合格的硬脂酸镁投入生产。
2 范围适用于本厂质监科化验室对本厂进厂的辅料硬脂酸镁的检验。
3 责任检验员有责任按照本操作规程对生产过程中所需用的硬脂酸镁进行检验、判定,并对检验结果负责。
4 内容4.1性状本品为白色轻松无砂性的细粉;微有特臭;与皮肤接触有滑腻感。
本品在水、乙醇或乙醚中不溶。
4.2鉴别4.2.1试液的配制4.2.1.1稀硫酸:取硫酸57 ml,加水稀释至1000ml,摇匀。
4.2.1.2氨试液:取浓氨溶液400ml,加水稀释至1000ml ,摇匀。
4.2.1.3氯化铵试液:取氯化铵10.5g,加水使溶解成100ml,摇匀。
4.2.1.4磷酸氢二钠试液:取磷酸氢二钠结晶12g,加水使溶解成100ml,摇匀。
4.2.1.5氢氧化钠试液:取氢氧化钠4.3g,加水使溶解成100ml,摇匀。
4.2.1.6碘试液:取碘13.0g,加碘化钾36g与水50ml溶解后,加盐酸3滴与水适量使成1000ml,摇匀,用垂熔玻璃滤器滤过。
4.2.2操作4.2.2.1供试品的制备:取本品约10g,加稀硫酸25ml与热水100ml,加热并时时搅拌,使脂肪酸成油层分出,保留水层,取油层用沸水洗涤至洗液不显硫酸盐的反应,放冷,分去水层,加热使油层熔化,趁热滤过,在105℃干燥后,第2页/共2页测定凝点。
4.2.2.2凝点的测定仪器装置见中国药典2000年版附录VI D取上述供试品,置内管中,使迅速冷却,并测定供试品的近似凝点,再将内管置较近似凝点约高5—10℃的水浴中,使凝结物仅剩极度微量未熔融。
将仪器按仪器装置装妥,烧杯中加入较供试品近似凝点约低5℃的水或其他适宜的冷却液,用搅拌器不断搅拌供试品,每隔30秒钟观察温度一次,至温度计的汞柱在一点能停留约1分钟不变,或微上升至最高温度后停留约1分钟不变,即将该温度作为供试品的凝点。
测定结果凝点应≥54℃。
4.2.2.3取上述遗留的水层溶液,加氨试液,即生成白色沉淀;滴加氯化铵试液,沉淀溶解;再加磷酸氢二钠试液1滴,振摇,即生成白色沉淀,沉淀在氨试液中不溶。


硬脂酸镁是一种常用的辅料,广泛应用于制药、化妆品和食品工业中。
它具有良好的稳定性和润滑性能,被广泛用作药物制剂的包衣剂、润滑剂和溶剂。
硬脂酸镁的质量控制非常重要,因此药典标准对其进行了详细的规定。
下面将为您介绍硬脂酸镁辅料药典标准,以保证制药行业的安全和质量。
一、名称和性质:硬脂酸镁(Magnesium Stearate),分子式为Mg(C18H35O2)2,相对分子质量为591.27。
它是一种白色或类白色结晶粉末,无臭、无味。
在常温下稳定,不溶于水,微溶于乙醇和乙醚。
二、标准要求:1. 外观:硬脂酸镁应为白色或类白色结晶粉末,不得有异物。
2. 纯度:硬脂酸镁的纯度应不低于99.0%。
3. 重金属:重金属含量不得超过0.001%。
4. 水分:水分含量不得超过1.0%。
5. 酸值:酸值应不大于2.0mg KOH/g。
6. 碱度:碱度应不大于0.5ml 0.1N HCl。
7. 氯化物:氯化物含量不得超过0.35%。
8. 硫酸盐:硫酸盐含量不得超过0.6%。
9. 油脂:油脂含量不得超过1.0%。
三、检测方法:1. 外观检查:取适量样品,目测外观是否为白色或类白色结晶粉末,观察是否有异物。
2. 纯度检验:采用高效液相色谱法(HPLC)进行检测,以评估硬脂酸镁的纯度。
3. 重金属检测:采用原子吸收光谱法(AAS)进行检测,判断重金属含量是否符合标准。
4. 水分测定:采用干燥法进行测定,确定水分含量是否在规定范围内。
5. 酸值测定:采用酸碱滴定法,以测定硬脂酸镁中的酸值。
6. 碱度测定:采用酸碱滴定法,以测定硬脂酸镁中的碱度。
7. 氯化物测定:采用氯离子选择电极法,检测硬脂酸镁中的氯化物含量。
8. 硫酸盐测定:采用重银滴定法,测定硬脂酸镁中的硫酸盐含量。
9. 油脂测定:采用重量法,测定硬脂酸镁中的油脂含量。
四、包装和储存:硬脂酸镁应储存在干燥、通风、阴凉的地方,避免阳光直射。
包装应符合相关规定,常见的包装方式有塑料袋、纸板桶等。

1.范围:本标准规定了硬脂酸镁的检测方法和操作要求;适用于本公司硬脂酸镁的质量检验。
2.引用标准:《中华人民共和国药典》(2010年版二部1234页)3.性状:本品为白色轻松无砂性的细粉:微有特臭;与皮肤接触有滑腻感。
本品在水、乙醇或乙醚中不溶。
4.鉴别:4.1仪器与试剂:天平、量筒、恒温干燥箱、高温炉、凝点测定仪、稀硫酸4.2操作步骤与结果:4.2.1取本品约5.0g,置圆底烧瓶中,加无过氧化物乙醚50ml、稀硝酸20ml与水20ml,加热回流至完全溶解,放冷,移至分液漏斗中,振摇,放置分层,将水层移入另一分液漏斗中,用水提取乙醚层2次,每次4ml,合并水层,用无过氧化物乙醚15ml清洗水层,将水层移至50ml量瓶中,加水稀至刻度,摇匀,作为供试品溶液,应显镁盐的鉴别反应(附录Ⅲ)。
4.2.2 在硬脂酸与棕榈酸相对含量检查项下记录的色谱图中,供试品溶液两主峰的保留时间应分别与对照品溶液两主峰的保留时间一致。
5.检查:5.1酸碱度5.1.1仪器与试剂:天平、量筒、水浴锅、蒸发皿、烧杯、漏斗、溴麝香草酚蓝指示液、盐酸滴定液(0.1mol/L)、氢氧化钠滴定液(0.1 mol/L)5.1.2操作步骤与结果:取本品1.0g,加新沸过的冷水20ml,水浴上加热1分钟并时时振摇,放冷,滤过,取续滤液10ml,加溴麝香草酚蓝指示液0.05ml,用盐酸滴定液(0.1mol/L)或氢氧化钠滴定液(0.1 mol/L)滴至溶液颜色发生变化,滴定液用量不得过0.05ml。
5.2氯化物:5.2.1仪器与试剂:天平、量筒、烧杯、漏斗、高温炉、硝酸、标准氯化钠溶液5.2.2操作步骤与结果:量取鉴别(1)项下的供试品溶液1.0ml,依法检查(附录Ⅷ A),与标准氯化钠溶液10.0ml制成的对照液比较,不得更浓(0.10%)。
5.3硫酸盐:5.3.1仪器与试剂:天平、量筒、烧杯、高温炉、漏斗、盐酸、标准硫酸钾溶液5.3.2操作步骤与结果:量取鉴别(1)项下的供试品溶液1.0ml,依法检查(附录Ⅷ A),依法检查(附录Ⅶ A),与标准硫酸钾溶液6.0ml制面的对照液比较,不得更浓(0.6%)。


硬脂酸镁检验标准操作规程目 的:规范硬脂酸镁检验的操作。
适用范围:硬脂酸镁的检验。
责 任:检验室检验人员按本规程操作,检验室任对本规程的有效实施承担监督检查责任。
规 程:本品为以硬脂酸镁(C 36H 70MgO 4)与棕榈酸镁(C 32H 62MgO 4)为主要成分的混合物。
按干燥品计算,含MgO 应为%~%。
1.性状:本品为白色轻松无砂性的细粉;微有特臭,与皮肤接触有滑腻感。
本品在水、乙醇或乙醚中不溶。
2.鉴别仪器及用具:架盘天平、电炉、干燥箱、烧杯、硅油、温度计、垂熔漏斗、试管、量筒等。
试剂及试液:纯化水、稀硫酸、氨试液、氯化铵试液、磷酸氢二钠试液、氢氧化钠试液、碘试液。
测定法取本品约10g ,加稀硫酸25ml 与热水100ml ,加热并时时搅拌,使脂肪酸成油层分出,保留水层,取油层用沸水洗涤至洗液不显硫酸盐的反应,放冷,分去水层,加热使油层熔化,趁热滤过,在105℃干燥后,依《凝点测定法标准操作规程》测定,应不低于54℃。
上述遗留的水层显镁盐的鉴别反应。
(1) 取供试品溶液,加氨试液,即生成白色沉淀,滴加氯化铵试液,沉淀溶解,再加磷酸氢二钠试液1滴,振摇,即生成白色沉淀,沉淀在氨试液中不溶。
(2)取供试品溶液,加氢氧化钠试液,即生成白色沉淀,分离,沉淀分成两份,一份中加过量的氢氧化钠试液,沉淀不溶,另一份加碘试液,沉淀转成红棕色。
3.检查仪器及用具:万分之一天平、电炉、干燥箱、马弗炉、纳氏比色管、刻度吸管、试管、量筒、漏斗、滤纸、锥形瓶等。
试剂及试液:纯化水、硝酸、稀硝酸、硝酸银试液、标准氯化钠溶液、盐酸溶液(9→100)、标准硫酸钾溶液、稀盐酸、过硫酸铵、醋酸盐缓冲液、标准铁溶液、硝酸银、25%氯化钡溶液、30%硫氰酸铵溶液、硫代乙酰胺试液、标准铅溶液。
测定法氯化物 取本品,加硝酸1ml 与水24ml ,加热煮沸后,放冷,俟油层凝固,滤过,滤液加水稀释使成50ml ;分取滤液5ml ,按《氯化物检查法标准操作规程》(SOP-QC-089-00)检查,与标准氯化钠溶液制成的对照溶液比较,不得更浓%)。

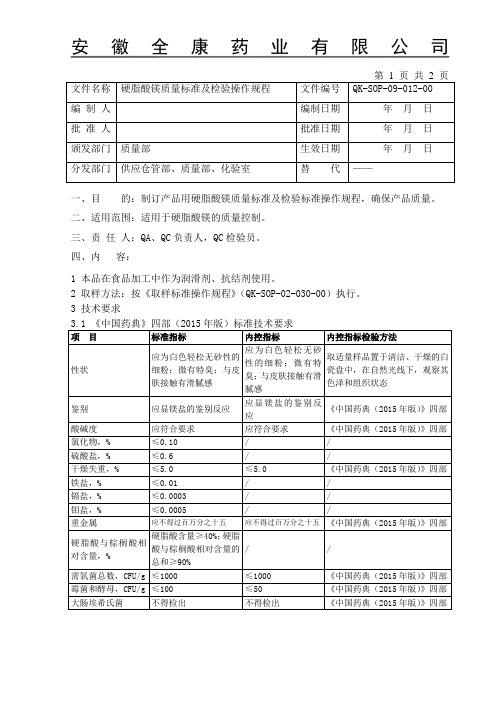
一、目的:制订产品用硬脂酸镁质量标准及检验标准操作规程,确保产品质量。
二、适用范围:适用于硬脂酸镁的质量控制。
三、责任人:QA、QC负责人,QC检验员。
四、内容:
1 本品在食品加工中作为润滑剂、抗结剂使用。
2 取样方法:按《取样标准操作规程》(QK-SOP-02-030-00)执行。
3 技术要求
3.2 3.2 卫生部2011年第8号公告指定标准-10(硬脂酸镁)技术要求
4.1 《中国药典》四部(2015年版)。
4.2 卫生部2011年第8号公告指定标准-10(硬脂酸镁)。
4.3 《食品安全国家标准食品中水分的测定》(GB 5009.3-2010)。
4.4 《食品安全国家标准食品中铅的测定》(GB 5009.12-2010)。
4.5 《食品安全国家标准食品微生物学检验菌落总数测定》(GB 4789.2-2010)。
4.6 《食品安全国家标准食品微生物学检验大肠菌群计数》(GB 4789.3-2010)。
4.7 《食品安全国家标准食品微生物学检验霉菌和酵母计数》(GB 4789.15-2010)。

硬脂酸镁本篇所述内容与欧洲药典和美国药典一致,文中标记为(◆◆)部分与上述两药典不同。
硬脂酸镁是由镁和固体脂肪酸混合而成的化合物,主要由变化比例的硬脂酸镁和从植物与动物来源的棕榈酸镁组成。
按照干燥品计算,本品含镁(Mg:24.31)不少于4.0%且不多于5.0%。
◆性状硬脂酸镁为白色,发亮的松散粉末。
本品触摸光滑,与皮肤接触有粘性。
无味或有微弱的特征性气味。
本品几乎不溶于水和乙醇(99.5)。
◆鉴别取5.0g的硬脂酸镁和50mL无过氧化物乙醚置于圆底烧瓶中混合,然后加20mL的稀硝酸和20mL的水,在回流冷凝器中加热至完全溶解。
放凉后,将烧瓶中的内容物转移至分液漏斗,振摇,放置分层,然后将水层转移至烧瓶中。
用2个4mL的水提取乙醚层,合并提取物至水层。
用15mL的无过氧化物乙醚清洗水层后,将水层转移至50mL的量瓶中,加水至刻度线,将此溶液做为样品溶液。
取1mL的样品溶液加1mL的氨水试液:产生白色沉淀,加1mL的氯化铵试液,白色沉淀溶解。
然后再加入1mL的十二水合磷酸氢二钠溶液(4→25),产生白色水晶沉淀。
纯度(1)酸碱度―取1.0g的硬脂酸镁加入20mL新煮沸放凉的水,水浴加热1min并振摇,放凉后过滤。
取10mL滤液加入0.05mL的溴麝香草酚蓝试液:用0.1mol/L的盐酸滴定液或0.1mol/L的氢氧化钠滴定液至溶液颜色发生变化,所用上述滴定液的量不超过0.05mL。
(2)氯化物<1.03>―取鉴别项下的样品溶液10.0mL进行试验。
使用1.4mL浓度为0.02mol/L的盐酸滴定液做为对照溶液(不多于1.0%)。
(3)硫酸盐<1.14>―取鉴别项下的样品溶液6.0mL进行试验。
使用3.0m L浓度为0.02mol/L的硫酸滴定液做为对照溶液(不多于1.0%)。
◆(4)重金属<1.07>―取1.0g的硬脂酸镁加热变软,以500±25℃温度灼烧成灰烬。

硬脂酸镁辅料药典标准硬脂酸镁是一种常用的辅料药典标准。
硬脂酸镁是一种镁盐,化学式为Mg(C17H35COO)2,分子量为591.27。
它是一种白色结晶粉末,无臭,味微苦。
硬脂酸镁具有良好的溶解性和稳定性,在药物制剂中起着重要的作用。
硬脂酸镁在药物制剂中常用作乳化剂、稳定剂和润滑剂。
它可以增加药物的溶解度,提高药物的生物利用度。
此外,硬脂酸镁还可以改善药物的质地,使药物更易于制剂和使用。
硬脂酸镁在制备乳剂时起到乳化稳定剂的作用。
乳剂是一种由液态药物分散在水相或油相中形成的均匀分散体系。
硬脂酸镁可以使油相和水相之间形成稳定的乳化体系,使乳剂具有良好的稳定性和均匀性。
硬脂酸镁还常用作制备软膏、霜剂和栓剂等外用制剂的基础。
它可以增加制剂的黏度和粘附性,使制剂更易于附着在皮肤或黏膜表面。
同时,硬脂酸镁还可以增加制剂的柔软度和延展性,使制剂更易于涂抹和吸收。
硬脂酸镁还可以用作口服制剂的润滑剂。
口服制剂是指通过口腔进入体内的药物制剂,如片剂、胶囊等。
硬脂酸镁可以减少制剂与口腔黏膜的摩擦,降低患者服用药物时的不适感,并提高药物的可接受性和依从性。
硬脂酸镁作为一种常用的辅料药典标准,在药物制剂中具有广泛的应用。
根据药典标准,硬脂酸镁的质量应符合一定的要求。
例如,硬脂酸镁的含量应在98.0%~102.0%之间,水分含量应小于2.0%,重金属含量应小于0.001%等。
总之,硬脂酸镁是一种重要的辅料药典标准,具有良好的溶解性和稳定性,在药物制剂中起着重要的作用。
它可以作为乳化剂、稳定剂和润滑剂使用,并且符合药典标准的质量要求。
随着药物研究的不断发展,硬脂酸镁在药物制剂中的应用将会越来越广泛。

食品添加剂指定标准食品添加剂硬脂酸镁1、食品添加剂硬脂酸镁 1 范围本标准适用于由氧化镁与食用级固体混合脂肪酸〔以硬脂酸为主〕化合后精制而得的食品添加剂硬脂酸镁。
产品为白色松散粉末,细腻,无沙粒感。
由硬脂酸镁和棕榈酸镁按不定比例组合的混合体。
产品不溶于水,溶于乙醇和乙醚。
2 技术要求应符合表1的规定。
项目指标检验方法硬脂酸镁含量〔以MgO计〕,w/%6.8~8.3附录A中A.3枯燥减量,w/%≤4.0GB5009.3直接枯燥法a铅〔Pb〕/〔mg/kg〕≤5GB5009.12a枯燥温度为105℃,枯燥时间为2h。
表11n附录A检验方法A.1 一2、般规定除非另有说明,在分析中仅使用确认为分析纯的试剂和GB/T6682-2021中规定的水。
分析中所用标准滴定溶液、杂质测定用标准溶液、制剂及制品,在没有注明其他要求时,均按GB/T601、GB/T602、GB/T603的规定制备。
本试验所用溶液在未注明用何种溶剂配制时,均指水溶液。
A.2 鉴别试验A.2.1 取试样1g,混入水25mL和盐酸5mL,加热,脂肪酸被释出,使油状层浮出液体外表。
用水层进行镁试验,应呈阳性反应。
A.2.2 取试样25g,混入热水200mL,再加1mol/L硫酸溶液60mL,加热并不3、断搅拌至脂肪酸析出并呈透亮状清液。
用沸水洗涤脂肪酸,至硫酸盐除尽为止,收集于小烧杯中,于蒸气浴上温热至脂肪酸与水层完全分别,并透亮。
冷却,弃去水层,将脂肪酸熔融后滤入一枯燥烧杯中,在105℃下枯燥20min。
该精制脂肪酸的凝固点应不低于54℃。
凝固点按常规方法测定。
该精制脂肪酸的凝固点应不低于54℃。
凝固点按常规方法测定。
A.3 硬脂酸镁含量的测定精确称取约1g试样,加入50mL浓度为0.1mol/L盐酸溶液,煮沸约30min,或至脂肪酸层澄清,必要时可加水以保持原体积。
冷却,过滤,用水彻底洗涤滤液和烧瓶,至4、最终的洗液对石蕊不再呈酸性。
滤液用1mol/L氢氧化钠试液中和至石蕊呈中性。

目的:建立一个硬脂酸镁检验操作规程。
范围:硬脂酸镁检验。
责任:检验员、质检科长、QA监控员、质保科长、质量总监。
内容:[性状]本品为白色轻松无砂性的细粉,微有特臭;与皮肤接触有滑腻感。
本品在水、乙醇、乙醚中不溶。
[鉴别]1仪器设备:药物分析天平、移液管、量筒、漏斗、电热恒温干燥箱。
2试剂溶液:稀硫酸、氨试液、氯化铵试液、磷酸氢二钠试液、氢氧化钠试液、碘试液。
3操作方法:3.1取本品约10g,加稀硫酸25ml与热水100ml,加热并时时搅拌,使脂肪酸成油层分出,保留水层,取油层用沸水洗涤至洗液不显硫酸盐的反应,放冷,分去水层,加热使油层熔化,趁热滤过,在105℃干燥后,检查方法见凝点测定法操作规程,应不低于54℃。
3.2上述遗留的水层显镁盐的鉴别反应。
3.2.1取供试品溶液,加氨试液,即生成白色沉淀;滴加氯化铵试液;沉淀溶解,再加磷酸氢二钠试液1滴,振摇,即生成白色沉淀,沉淀在氨试液中不溶。
3.2.2取供试品溶液,加氢氧化钠试液,即生成白色沉淀。
分离,沉淀分成两份,一份中加过量的氢氧化钠试液,沉淀不溶;另一份中加碘试液,沉淀转成红棕色。
[检查]1氯化物:取本品0.20g,加硝酸1ml与水24ml,加热煮沸后,放冷,俟油层凝固,滤过,滤液加水稀释使成50ml,检查方法见“氯化物检查法操作规程”,与标准氯化钠溶液3.0ml 制成的对照液比较,不得更浓(0.15%)。
2硫酸盐:取本品0.10g,加水20ml与盐酸溶液(9→100)1ml,加热煮沸后,放冷,俟油层凝固,滤过,油层用水洗涤4-5次,合并滤液与洗液,加水使成40ml,检查方法见硫酸盐检查法操作规程,与标准硫酸钾溶液6.0ml制成的对照液比较,不得更浓(0.6%)。
3干燥失重:取本品,在80℃干燥至恒重,减失重量不得过5.0%。
检查方法见“干燥失重测定法操作规程”。
W2-W0公式:――――×100%W1-W0W0:空瓶恒重的重量W1:空瓶和供试品的总重量。

标准操作规程目的:建立一个硬脂酸镁原料检验标准操作规程。
范围:适用于硬脂酸镁原料。
责任者:QC化验员、QC主任。
规程:1。
本品以硬脂酸镁 C36H70MgO4与(C32H62MgO4为主要成分的混合物2. 检验依椐:硬脂酸镁质量标准QS-016-01。
3. 性状3.1. 本品为白色轻松无砂性的细粉,微有特臭,与皮肤接触有滑腻感。
3。
2。
本品在水、乙醚或乙醇中不溶。
4. 鉴别4。
4。
1。
仪器:天平、三角烧杯、干燥箱(105℃)凝点测定装置等。
4.4。
2。
试剂:稀硫酸、氨解液、氯化铵试液、磷酸氢二钠试液、氢氧化钠试液、碘试液等均照《中国药典》附录中方法配制。
4.4.3. 操作方法4。
3。
1。
取本品约10g,加稀硫酸2.5ml与热水100ml,加热并时时搅拌,使硬脂酸成油层分出,保留水层,取油层用沸水洗涤至洗液不显硫酸盐的反应放冷,分去水层,加热使油层熔化,趁热滤过,在105℃干燥后,照《中国药典》凝点测定法检查,应不低于54℃。
4。
3.2. 取上述剩余溶液,加氨试液,即生成白色沉淀,滴加氯化铵试液,沉液溶解,再加磷酸氢二钠试液滴,振摇,即生成白色沉淀,沉淀在氨试液中不溶。
4。
3。
3。
取上述剩余溶液,加氢氧化钠试液,即生成白色沉淀,分离,沉淀分成两份,一份中加过量的氢氧化钠试液,沉淀不溶,另一份中加碘试液,沉淀转成红棕色.5. 检查标准操作规程5.1。
氯化物5.1。
1. 仪器:万分之一分析天平、三角烧瓶、电炉、漏斗、纳氏比色管。
5.1.2. 试剂:硝酸、硝酸银溶液、标准氯化钠溶液等。
5。
1。
3. 原理:氯化物在硝酸酸性溶液中与硝酸银作用,生成氯化银混浊液,与定量的标准氯化物溶液在同样操作条件下生成的氯化银混浊液比较,检查供试品中氯化物的限量.5。
1.4。
操作方法取本品0.20g ,置三角烧瓶中,加硝酸1ml,水24ml ,加热煮沸后放冷,俟油层凝固,滤过,滤液加水稀释使成50ml ,分取滤液5ml,照SOP-QC-047—01检查,与同时同法取标准氯化钠溶液3。

硬脂酸镁2020药典标准-概述说明以及解释1.引言1.1 概述硬脂酸镁是一种常用的药物成分,被广泛应用于制药、医疗和化妆品等领域。
硬脂酸镁具有稳定性高、生物相容性好的特点,因此在药物制剂中被广泛使用。
它是由硬脂酸和镁离子通过化学反应生成的化合物。
硬脂酸镁的制备方法主要有两种:直接反应法和中盐法。
直接反应法是将硬脂酸和镁盐通过化学反应生成硬脂酸镁,而中盐法则是先形成硬脂酸镁的中间体,再通过酸溶解、碱沉淀等步骤制得。
硬脂酸镁的药典标准对其质量进行了严格规定,包括其外观、溶解性、纯度、含量测定等方面的指标。
这些标准对于确保药物质量的一致性和稳定性具有重要意义。
随着科技的不断进步和人们对高品质药物的需求增加,对硬脂酸镁的药典标准也在不断完善和更新。
未来,我们可以期待更加精确和全面的标准,以满足药物制剂的不断发展和创新需求。
总之,硬脂酸镁作为一种重要的药物成分,在医药领域具有广泛的应用前景。
药典标准的制定对于保障药物的质量和安全至关重要,并将持续更新以适应行业的发展趋势。
未来的发展方向则是更加精确和全面的标准,以提高药物制剂的质量水平。
1.2 文章结构文章结构是指文章整体的组织和分布,它关乎着读者对文章内容的理解和吸收。
对于本篇文章来说,它包括以下几个部分:1. 引言:简要介绍硬脂酸镁及其在医药领域的应用背景,引出本文的研究目的和重要性。
2. 正文:2.1 硬脂酸镁的定义:详细介绍硬脂酸镁的化学性质、物理性质和药理作用等方面的内容,使读者对硬脂酸镁有一个全面的了解。
2.2 硬脂酸镁的制备方法:介绍硬脂酸镁的几种主要制备方法,包括传统的化学合成方法和现代的生物技术合成方法,并对比它们的优缺点和应用范围。
3. 结论:3.1 硬脂酸镁的药典标准总结:总结国内外硬脂酸镁的药典标准,包括质量要求、检测方法、用途范围等方面的内容。
3.2 未来发展方向:展望硬脂酸镁的研究和应用前景,提出未来发展的方向和重点,为相关领域的研究者提供参考。
Shandong Liaocheng Ehua Medicine CO., LTD 页码:1/31. 目的本程序是为硬脂酸镁的化学及微生物检验而制定。
2. 范围本程序规定了硬脂酸镁产品的质量标准、检验操作法。
3.引用标准《中国药典》2005年版二部;《美国药典》现行版 4 质量标准和检验操作法4.1[性状] 本品为白色轻松无砂性的细粉,微有特臭;与皮肤接触有滑腻感。
本品在水、乙醇或乙醚中不溶。
4.2[鉴别]1)取5.0g 样品,加50ml 无过氧化物的乙醚,20ml 稀硝酸,20ml 水,加热回流使完全溶解,冷却,转移到分液漏斗,振摇,分出水层。
用水洗涤醚层二次,每次4ml ,合并水层。
用15ml 无过氧化物的乙醚洗涤水层,将水层转移至50ml 容量瓶中,用水稀释至刻度,混匀。
此为氯化物和硫酸盐测试溶液。
此溶液显镁盐的鉴别反应(中国药典2005年版二部附录Ⅲ)2)硬脂酸和棕榈酸相对含量项下,测试溶液中硬脂酸和棕榈酸峰的保留时间与系统适应性溶液相一致。
4.3[检查]4.3.1酸 碱 度:取本品1.0g ,加新沸过的冷水20ml ,振摇煮沸1分钟,冷却,过滤,取滤液10ml ,加0.05ml 溴百里香酚兰指示液;如显黄气,加氢氧化钠滴定液(0.1mol/L )0.05ml ,应变为蓝色,如显蓝色,加盐酸滴定液(0.1mol/L)0.05ml ,应变为黄色。
4.3.2 氯 化 物:取鉴别1)项下的水溶液10.0ml 置于50 ml 比色管中,依法检查(中Shandong Liaocheng Ehua Medicine CO., LTD 页码:2/3 国药典2005年版二部附录ⅧA),与1.4ml0.020mol/L的盐酸制成的对照液比较,不得更浓(0.10%)。
4.3.3硫酸盐:取鉴别1)项下的水溶液3.0ml置于50 ml比色管中,依法检查(中国药典2005年版二部附录ⅧB),与3.0ml0.020mol/L的硫酸制成的对照液比较,不得更浓(1.0%)。

硬脂酸镁本品是将硬脂酸以20倍的热水溶解,加热至90℃左右加入烧碱,制得稀皂液,再加硫酸镁溶液进行复分解反应,得硬脂酸镁沉淀,用水洗涤,离心脱水,在100℃左右干燥制得:系以硬脂酸镁(C 36H 70MgO 4)与棕榈酸镁(C 32H 62MgO 4)为主要成分的混合物,按干燥品计算,含Mg 应为4.0%~5.0%【性状】本品为白色轻松无砂性的细粉;微有特臭;与皮肤接触有滑腻感。
本品在水、乙醇或乙醚中不溶。
【鉴别】(1)取本品5.0g ,置圆底烧瓶中,加无过氧化物乙醚50ml 、稀硝酸20ml 与水20ml ,加热回流至完全溶解,放冷,移至分液漏斗中,振摇,放置分层,浆水层移入另一分液漏斗中,用水提取乙醚层2次,每次4ml ,合并水层,用无过氧化物乙醚15ml 清洗水层,将水层移至50ml 量瓶中,加水稀至刻度,摇匀,作为供试品溶液,应显镁盐的鉴别反应(附录Ⅲ)(2)在硬脂酸与棕榈酸相对含量检查项下记录的色谱图中,供试品溶液两主峰的保留时间应分别与对照品溶液两主峰的保留时间一致。
【检查】酸碱度 取本品1.0g ,加新沸过的冷水20ml ,水浴上加热1分钟并时时振摇,放冷,滤过,取续滤液10ml ,加溴麝香草酚蓝指示液0.05ml ,用盐酸滴定液(0.1mol/L )或氢氧化钠滴定液(0.1mol/L )滴至溶液颜色发生变化,滴定液用量不得过0.05ml 。
氯化物 量取鉴别(1)项下的供试品溶液1.0ml ,依法检查(附录ⅧA ),与标准氯化钠溶液10.0ml 制成的对照液比较,不得更浓(0.10%)硫酸盐 量取鉴别(1)项下的供试品溶液1.0ml ,依法检查(附录Ⅷ B ),与标准硫酸钾溶液6.0ml 制成的对照液比较,不得更深(0.6%)干燥失重 取本品,在80℃干燥至恒重,减失重量不得过5.0%(附录Ⅷ L )。
铁盐 取本品0.50g ,炽灼灰化后,加稀盐酸5ml 与水10ml ,煮沸,放冷,滤过,滤液加过硫酸铵50mg ,用水稀释成35ml ,依法检查(附录ⅧG ),与标准贴溶液5.0ml 用同一方法制成的对照液比较,不得更深(0.01%)重金属 取本品2.0g ,缓缓炽灼至完全炭化,放冷,加硫酸0.5~1.0ml ,使恰润湿,低温加热至硫酸除尽,加硝酸0.5ml ,蒸干,至氧化氮蒸气除尽后,放冷,在500~600℃炽灼,稀醋酸2ml ,加热溶解后,放冷,加醋酸盐缓冲液(pH3.5)2ml 与水适量使成25ml ,依法检查(附录Ⅷ H 第二法),含重金属不得过百分之十五。

药用辅料硬脂酸镁MS用途润滑剂药用辅料硬脂酸镁MS用途润滑剂硬脂酸镁(Magnesium Stearate)是一种有机化合物,由硬脂酸和镁构成,它是一种无色粉末,具有良好的抗粘性和抗结块性,是药物制剂中常用的辅料。
硬脂酸镁具有抗粘性、抗结块性、降低表面张力、加添润滑性等优点,因此被广泛应用于制药、化妆品、食品、农药等行业。
硬脂酸镁为药品(片剂)的辅料,为疏水性润滑剂,易与颗粒混匀,压片后片面干净美观。
本品有良好附着性,与颗粒混合后不易分别,本品润滑性强,但抗粘性较差,若与其它润滑剂合用,润滑性更好。
一般用量为0.25~1%。
因其具有疏水性,用量过多可延迟片剂中功能成分的溶出。
与淀粉混合使用,可使压片顺当,并能在穿定程度上改善其疏水性而降低对片剂崩解及功能成分溶出的影响[CH3(CH2)16COO]2Mg C36H70MgO4[1]又称十八(碳)酸镁、Dolomol。
白色轻质粉末或块状。
有芳香气。
有滑腻感。
相对分子质量519.27、相对密度1.028、熔点86~88℃。
不溶于水、冷乙醇和乙。
硬脂酸镁白色疏松细粉。
熔点108—115℃,相对密度1.07、在室温水中溶解度77—79mg/L,溶于热的乙醇。
遇酸分解为硬脂酸和相应的镁盐。
微有特臭,有滑腻感。
硬脂酸镁的制备由硬脂酸加氢氧化钠皂化得硬酸钠,再与硫酸镁复分解得硬脂酸镁。
将硬脂酸和水加入反应锅内,加热至85℃,搅拌溶解后,缓缓加入预热至75℃的氢氧化钠溶液。
皂化反应完成后,将温度掌控在72℃,搅拌下缓缓加入预热至55℃的硫酸镁溶液。
复分解后离心甩水,滤饼用水洗涤至硫酸根符合要求为止,然后甩干,气流干燥,过筛,得产品。
硬脂酸镁的用途用作聚氯乙烯热稳定剂,以及化妆品、润肤油膏和医药片剂原料子(赋形药、润滑药);用于校木粉中使之润滑光亮透亮;油漆工业作透亮平光剂等。
交联聚维酮河南产(药用辅料2023药典)有货苯扎溴铵四川产(药用辅料2023药典)有货苯扎氯铵江西产(药用辅料2023药典)有货泊洛沙姆188 407 德国巴斯夫进口(药用辅料2023药典有货羟苯乙酯广州产(药用辅料2023药典)有货乳膏基质有货混合脂肪酸甘油酯山东产(药用辅料2023药典)有货聚乙烯醇低中高江西产(药用辅料2023药典)有货硬脂酸湖南产(药用辅料2023药典)有货羟丙甲倍他环糊精山东产(药用辅料2023药典)有货羟苯丁酯湖北产有货苯甲酸苄酯上海产有货甜菊糖苷山东产(药用辅料2023药典)有货聚山梨酯20 江苏产(药用辅料2023药典)有货甘露醇广西产(药用辅料2023药典)有货油酸乙酯湖北产(药用辅料2023药典)有货氯化钠河北产(药用辅料2023药典)有货。

硬脂酸镁检验操作规程1. 目的建立硬脂酸镁检验标准操作规程,使硬脂酸镁检验操作规范化。
2. 范围适用于硬脂酸镁的质量检验。
3. 术语或定义N/A4. 职责质量控制部对本规程的实施负责。
5. 程序5.1 检验依据5.1.1 《中国药典》2020年版第四部(第766页)。
5.1.2 硬脂酸镁质量标准(质量标准编号:)。
5.1.3 《中国药典》2020年版四部。
5.2 性状:本品为白色轻松无砂性的细粉;微有特臭。
本品在水、乙醇或乙醚中不溶。
5.3 鉴别5.3.1 在硬脂酸与棕榈酸相对含量检查项下记录的色谱图中,供试品溶液色谱中两主峰的保留时间应分别与对照品溶液两主峰的保留时间一致。
5.3.2 镁盐鉴别反应仪器与试剂:电子天平、乙醚、稀硝酸、氨试液、氯化铵试液、磷酸氢二钠试液、氢氧化钠试液、碘试液。
供试品溶液的制备:取本品5.0g,置分液漏斗中,加入乙醚50ml,摇匀,加入稀硝酸20ml 与水20ml,振摇至溶液完全溶解,放置分层,将水层移入另一分液漏斗中,用水提取乙醚层2次,每次4ml,合并水层,用乙醚15ml清洗水层,将水层移至50ml量瓶中,加水稀释至刻度,摇匀,作为供试品溶液,做如下镁盐鉴别试验及氯化物、硫酸盐检查项目。
5.3.2.1 取供试品溶液,加氨试液,即生成白色沉淀;滴加氯化铵试液,沉淀溶解;再加磷酸氢二钠试液1滴,振摇,即生成白色沉淀。
分离,沉淀在氨试液中不溶解。
5.3.2.2 取供试品溶液,加氢氧化钠试液,即生成白色沉淀,分离,沉淀分为2份,一份中加过量的氢氧化钠试液,沉淀不溶解;另一份中加碘试液,沉淀转成红棕色。
5.4 检查5.4.1 酸碱度仪器与试剂:电子天平、无水乙醇、溴麝香草酚蓝指示液、盐酸滴定液(0.1mol/l)、氢氧化钠滴定液(0.1mol/l)。
取本品2.0g,加无水乙醇6.0ml,搅拌使分散均匀,再加水使成40.0ml,摇匀,滤过,取续滤液10.0ml,加溴麝香草酚蓝指示液0.05ml,用盐酸滴定液(0.1mol/l)或氢氧化钠滴定液(0.1mol/l)滴至溶液颜色发生变化,滴定液用量不得过0.05ml。

硬脂酸镁检验标准操作规程适用围:适用于硬脂酸镁的检验。
责任者:质量管理部经理、质检检验中心主任、质量检验员。
容1品名:硬脂酸镁2 取样:照辅料取样标准操作规程(SOP-QC-ZJ-6074)取样。
3检验依据:硬脂酸镁控质量标准操作规程(STP-QS-ZJ-4005)。
4性状4.1仪器与用具:小烧杯4.2试剂:乙醇、乙醚。
4.3操作方法4.3.1从取样样品中取本品5g,置洁净的白色背景上,在明亮处用肉眼观察,本品为白色轻松无砂性的细粉;鼻嗅微有特臭,手指搓捏与皮肤接触有滑腻感。
4.3.2从取样样品中取本品0.1g,置1000ml锥形瓶中,加入水1000ml,每隔 5 分钟强力振摇 30 秒钟,在明亮处用肉眼观察30 分钟的溶解情况,有可见不溶的硬脂酸镁。
4.3.3从取样样品中取本品0.1g,置1000ml锥形瓶中,加入乙醇1000ml,每隔 5 分钟强力振摇 30 秒钟,在明亮处用肉眼观察30 分钟的溶解情况,有可见不溶的硬脂酸镁。
5鉴别5.1镁盐的鉴别反应5.1.1仪器与用具:架盘天平、凝点测定仪、鼓风电热恒温干燥箱。
5.1.2试液无过氧化物乙醚:在空气中长期存放乙醚时,醚中的碳氢键由于生成过氧键而形成有机过氧化聚合物,聚合物不稳定,受热易分解,会引起爆炸等危险事故。
因而必须检验是否有过氧化物。
过氧化物检验方法:将少量的醚用湿润的淀粉碘化钾试纸检验,试纸变蓝,说明有过氧化物生成。
乙醚过氧化物的去除:除去过氧化物可用新配制的硫酸亚铁稀溶液(配制方法是Fe SO4.6H2O 60g,100mL水和6mL浓硫酸)。
将100ml乙醚和10ml新配制的硫酸亚铁溶液放在分液漏斗中洗数次,至无过氧化物为止。
稀硝酸:取硝酸105mL,加水稀释至1000ml,即得。
氢氧化钠试液:取氢氧化钠4.3g,加水使溶解成100ml,即得。
5.1.3操作方法:从取样样品中称取5.0g,置磨口圆底烧瓶中,加无过氧化物乙醚50ml,稀硝酸20ml与水20ml,连接水浴加热回流装置,加热回流至完全溶解,放冷,移至分液漏斗中,振摇,放置分层,将水层移入另一分液漏斗中。
1.主题内容:建立硬脂酸镁检验操作规程以保证其质量。
2.适用范围:本标准适用于牡丹江耀德堂制药有限公司所购进的辅料硬脂酸镁的检验。
3.引用标准:《中国药典》2010年版二部第1234页。
4.责任:质量部、QC。
5. 用途:化验室。
6.内容:
6.1酸碱度:取本品1.0 g,加新沸过的冷水20ml,水浴上加热1分钟并时时振摇,放冷,滤过,取续滤液10ml,加溴麝香草酚蓝指示液0.05ml,用盐酸滴定液(0.1mol/L)滴至溶液颜色发生变化,滴定液用量不得过0.05ml
6.2氯化物量:取鉴别(1)项下的供试品溶液1.0ml,依法检查(附录ⅧA),与标准氯化钠溶液10.0ml制成的对照液比较,不得更浓(0.10%)。
6.3硫酸盐量:取鉴别(1)项下的供试品溶液1.0ml,依法检查(附录ⅧB),与标准硫酸钾溶液6.0ml制成的对照液比较,不得更浓。